| dc.contributor.author | Iovanna, Juan L. | - |
| dc.date.accessioned | 2018-09-27T09:50:04Z | |
| dc.date.available | 2018-09-27T09:50:04Z | |
| dc.date.issued | 2017 | |
| dc.identifier.citation | Iovanna, Juan L. ; L’autophagie contribue à l’initiation du cancer pancréatique, Med Sci (Paris), , Vol. 33, N° 3 ; p. 335-339 ; DOI : 10.1051/medsci/20173303022 | |
| dc.identifier.issn | 1958-5381 | |
| dc.identifier.uri | http://hdl.handle.net/10608/9147 | |
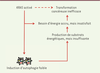
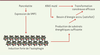
| dc.description.abstract | L’initiation de l’adénocarcinome pancréatique résulte de l’interaction d’événements génétiques combinés à de multiples facteurs moins bien caractérisés. Parmi les altérations génétiques qui contribuent à la pathogenèse de ce cancer, la mutation de l’oncogène KRAS (Kirsten rat sarcoma virus) est importante mais ne suffit pas à le déclencher. La pancréatite, une maladie inflammatoire, facilite et accélère la transformation des cellules pancréatiques si l’oncogène KRAS est muté. Toutefois, le répertoire des médiateurs moléculaires de la pancréatite impliqués dans l’initiation de la transformation reposant sur KRAS n’est pas totalement élucidé. L’autophagie a été proposée comme l’un des mécanismes cellulaires contribuant à la cancérogenèse pancréatique, en particulier dans les étapes initiales dans lesquelles l’oncogène KRAS semble jouer son principal rôle. L’autophagie est fortement induite durant la pancréatite. Bien que certains aspects de l’autophagie dans le développement de l’adénocarcinome pancréatique ne soient pas clairement établis, la surexpression de VMP1 (vacuole membrane protein 1), un inducteur de l’autophagie activé durant la pancréatite, stimule le développement des lésions précancéreuses pancréatiques si l’oncogène KRAS est muté. De plus, l’inhibition du flux autophagique par la chloroquine inhibe l’effet pro-tumoral de KRAS dans le pancréas. En conclusion, l’activation de l’expression de VMP1 favorise le rôle pro-tumoral de KRAS. | fr |
| dc.description.abstract | The pancreatic adenocarcinoma initiation results from the interaction of genetic events combined with multiple other factors. Among the genetic alterations that contribute to the pathogenesis of this disease, the mutation of the KRAS oncogene is required but not sufficient to trigger this cancer. Pancreatitis, an inflammatory disease, facilitates and accelerates the transformation of pancreatic cells when the KRAS oncogene is mutated. Of note, the repertoire of molecular mediators of pancreatitis which are responsible of the promotion of KRAS-mediated transformation is not completely defined. Importantly, autophagy has been proposed as one of the cellular mechanisms contributing to pancreatic carcinogenesis, especially in the initial phases, in which the oncogene KRAS appears to play its leading role. In addition, autophagy is strongly induced during pancreatitis. Although some aspects of autophagy in pancreatic cancer development are not completely established, we can affirm that overexpression of VMP1, an inducer of autophagy which is specifically activated in pancreas during pancreatitis, improves the development of pancreatic precancerous lesions PanINs when the oncogene KRAS is mutated. In addition, inhibition of the autophagic flux with chloroquine inhibits the KRAS pro-tumor effect in the pancreas. In conclusion, activation of expression of VMP1 improves the pro-tumor role of KRAS in pancreas. | en |
| dc.language.iso | fr | |
| dc.publisher | Éditions EDK, Groupe EDP Sciences | |
| dc.relation.ispartof | M/S Revues | |
| dc.rights | Article en libre accès | fr |
| dc.rights | Médecine/Sciences - Inserm - SRMS | fr |
| dc.source | M/S. Médecine sciences [ISSN papier : 0767-0974 ; ISSN numérique : 1958-5381], , Vol. 33, N° 3; p. 335-339 | |
| dc.subject.mesh | Animaux | fr |
| dc.subject.mesh | Autophagie | fr |
| dc.subject.mesh | Transformation cellulaire néoplasique | fr |
| dc.subject.mesh | Humains | fr |
| dc.subject.mesh | Souris | fr |
| dc.subject.mesh | Tumeurs du pancréas | fr |
| dc.subject.mesh | Transduction du signal | fr |
| dc.subject.mesh | physiologie | fr |
| dc.subject.mesh | anatomopathologie | fr |
| dc.title | L’autophagie contribue à l’initiation du cancer pancréatique | fr |
| dc.title.alternative | Autophagy contributes to the initiation of pancreatic cancer | en |
| dc.type | Article | |
| dc.contributor.affiliation | Centre de recherche en cancérologie de Marseille (CRCM), Inserm U1068, CNRS UMR 7258, Aix-Marseille Université et Institut Paoli-Calmettes, Parc scientifique et technologique de Luminy, 163, avenue de Luminy, 13288 Marseille, France | |
| dc.identifier.doi | 10.1051/medsci/20173303022 | |
| dc.identifier.pmid | 28367822 | |