| dc.contributor.author | Martin, Stéphane | - |
| dc.date.accessioned | 2015-04-29T08:17:35Z | |
| dc.date.available | 2015-04-29T08:17:35Z | |
| dc.date.issued | 2009 | fr_FR |
| dc.identifier.citation | Martin, Stéphane ; Nouvelles fonctions extranucléaires de la sumoylation des protéines dans le système nerveux central, Med Sci (Paris), 2009, Vol. 25, N° 8-9; p. 693-698 ; DOI : 10.1051/medsci/2009258-9693 | fr_FR |
| dc.identifier.issn | 1958-5381 | fr_FR |
| dc.identifier.uri | http://hdl.handle.net/10608/6789 | |
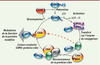
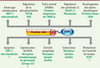
| dc.description.abstract | Les modifications post-traductionnelles de protéines sont essentielles à la régulation de leur fonction et, par conséquent, au maintien de l’intégrité cellulaire. Ces modifications interviennent à tous les niveaux de la communication entre les neurones du système nerveux central. La sumoylation est une modification post- traductionnelle qui crée une liaison covalente entre une lysine de la protéine cible et une petite protéine appelée SUMO. C’est un processus réversible qui fait intervenir des enzymes spécifiques. La sumoylation est un processus régulateur fonctionnel bien connu de l’activité nucléaire et il est maintenant clairement établi que dans les neurones, il assure également un rôle majeur pour de nombreux processus extranucléaires. De plus, la sumoylation intervient dans la transmission synaptique et a été impliquée récemment dans plusieurs désordres neurologiques. | fr |
| dc.description.abstract | Post-translational protein modifications play essential roles in many aspects of cellular functions and therefore in the maintenance of cell integrity. These protein modifications are involved at all stages of neuronal communication within the central nervous system. Sumoylation is a reversible post-translational protein modification that consists in the covalent labelling of a small protein called SUMO to lysine residues of selected target proteins. Sumoylation is a well characterized regulator of nuclear functions and has recently emerged as a key factor for numerous extranuclear processes. Furthermore, sumoylation has recently been shown to modulate synaptic transmission and is also implicated in a wide range of neurodegenerative diseases. | en |
| dc.language.iso | fr | fr_FR |
| dc.publisher | EDK | fr_FR |
| dc.relation.ispartof | M/S revues : Synthèse | fr_FR |
| dc.rights | Article en libre accès | fr |
| dc.rights | Médecine/Sciences - Inserm - SRMS | fr |
| dc.source | M/S. Médecine sciences [ISSN papier : 0767-0974 ; ISSN numérique : 1958-5381], 2009, Vol. 25, N° 8-9; p. 693-698 | fr_FR |
| dc.subject.mesh | Maladie d'Alzheimer | fr |
| dc.subject.mesh | Mort cellulaire | fr |
| dc.subject.mesh | Noyau de la cellule | fr |
| dc.subject.mesh | Système nerveux central | fr |
| dc.subject.mesh | Protéines G | fr |
| dc.subject.mesh | Humains | fr |
| dc.subject.mesh | Lysine | fr |
| dc.subject.mesh | Mitochondries | fr |
| dc.subject.mesh | Protéines tissu nerveux | fr |
| dc.subject.mesh | Maladie de Parkinson | fr |
| dc.subject.mesh | Maturation post-traductionnelle des protéines | fr |
| dc.subject.mesh | Synapses | fr |
| dc.subject.mesh | Ubiquitine | fr |
| dc.title | Nouvelles fonctions extranucléaires de la sumoylation des protéines dans le système nerveux central | fr |
| dc.title.alternative | Extranuclear functions of protein sumoylation in the central nervous system | en |
| dc.type | Article | fr_FR |
| dc.contributor.affiliation | Institut de neuromédecine moléculaire, Institut de pharmacologie moléculaire et cellulaire, Centre national de la recherche scientifique, UMR 6097, Université de Nice Sophia-Antipolis, 660, route des Lucioles, Sophia-Antipolis, 06560 Valbonne, France | fr_FR |
| dc.identifier.doi | 10.1051/medsci/2009258-9693 | fr_FR |
| dc.identifier.pmid | 19765382 | fr_FR |