| dc.contributor.author | Londoño-Vallejo, Arturo | - |
| dc.contributor.author | Lenain, Christelle | - |
| dc.contributor.author | Gilson, Eric | - |
| dc.date.accessioned | 2014-08-13T07:19:37Z | |
| dc.date.available | 2014-08-13T07:19:37Z | |
| dc.date.issued | 2008 | fr_FR |
| dc.identifier.citation | Londoño-Vallejo, Arturo ; Lenain, Christelle ; Gilson, Eric ; Cibler les télomères pour forcer les cellules cancéreuses à rentrer en sénescence, Med Sci (Paris), 2008, Vol. 24, N° 4; p. 383-389 ; DOI : 10.1051/medsci/2008244383 | fr_FR |
| dc.identifier.issn | 1958-5381 | fr_FR |
| dc.identifier.uri | http://hdl.handle.net/10608/6427 | |
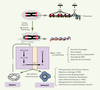
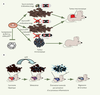
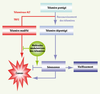
| dc.description.abstract | Dans les cellules somatiques humaines, les télomères raccourcissent au rythme des divisions cellulaires, jusqu’à l’apparition de télomères dysfonctionnels qui induisent la sénescence ou l’apoptose selon le type cellulaire. Deux études viennent d’être publiées montrant qu’un dysfonctionnement télomérique chez la souris supprime la formation de cancers en déclenchant la sénescence. Ces résultats renforcent la notion que la sénescence est un mécanisme qui limite la prolifération tumorale et suggèrent de nouvelles stratégies thérapeutiques ciblant sélectivement certaines fonctions télomériques. Toutefois, une question importante reste sans réponse : est-ce que l’érosion des télomères limite la formation des cancers chez l’homme ? | fr |
| dc.description.abstract | The telomeres protect the end of chromosomes from being recognized and processed as an accidental double stranded break. In human somatic cells, telomeres shorten progressively with every round of DNA replication, leading to dysfunctional telomeres that trigger cellular senescence or apoptosis depending on the cell type. This telomere erosion appears to play a role in cell renewal, ageing and cancer. Two recent studies demonstrated in mouse that eroded telomeres in cancer cells blocked for apoptosis limit cancer formation by triggering senescence. These results suggest that provoking senescence may provide a way to cure cancer and point to new therapeutical strategies targeting specific telomeric functions. Nevertheless, an important question remains unanswered: does replicative senescence limit tumor formation in human ? | en |
| dc.language.iso | fr | fr_FR |
| dc.publisher | EDK | fr_FR |
| dc.relation.ispartof | M/S revues | fr_FR |
| dc.rights | Article en libre accès | fr |
| dc.rights | Médecine/Sciences - Inserm - SRMS | fr |
| dc.source | M/S. Médecine sciences [ISSN papier : 0767-0974 ; ISSN numérique : 1958-5381], 2008, Vol. 24, N° 4; p. 383-389 | fr_FR |
| dc.subject.mesh | Vieillissement de la cellule | fr |
| dc.subject.mesh | Homéostasie | fr |
| dc.subject.mesh | Humains | fr |
| dc.subject.mesh | Modèles biologiques | fr |
| dc.subject.mesh | Tumeurs | fr |
| dc.subject.mesh | Télomère | fr |
| dc.title | Cibler les télomères pour forcer les cellules cancéreuses à rentrer en sénescence | fr |
| dc.title.alternative | Targeting telomeres to enforce cancer cells to senesce | en |
| dc.type | Article | fr_FR |
| dc.contributor.affiliation | Laboratoire Télomères et Cancer, UMR7147, Institut Curie-CNRS-UPMC, 26, rue d’Ulm, 75248 Paris, France | fr_FR |
| dc.contributor.affiliation | Laboratoire de Biologie Moléculaire de la Cellule, CNRS UMR5239, IFR128, École Normale Supérieure de Lyon, Faculté de Médecine Lyon-Sud, 165, Chemin du Grand Revoyet, 69495 Pierre Bénite, France | fr_FR |
| dc.identifier.doi | 10.1051/medsci/2008244383 | fr_FR |
| dc.identifier.pmid | 18405637 | fr_FR |