| dc.contributor.author | Buée, Luc | - |
| dc.contributor.author | Delacourte, André | - |
| dc.date.accessioned | 2014-02-14T13:19:14Z | |
| dc.date.available | 2014-02-14T13:19:14Z | |
| dc.date.issued | 2002 | fr_FR |
| dc.identifier.citation | Buée, Luc ; Delacourte, André ; La maladie d’Alzheimer : une tauopathie parmi d’autres ?, Med Sci (Paris), 2002, Vol. 18, N° 6-7; p. 727-736 ; DOI : 10.1051/medsci/20021867727 | fr_FR |
| dc.identifier.issn | 1958-5381 | fr_FR |
| dc.identifier.uri | http://hdl.handle.net/10608/5000 | |
| dc.description.abstract | La dégénérescence neurofibrillaire - agrégation intraneuronale de protéines tau anormalement phosphorylées - est un processus dégénératif qui affecte la région hippocampique des personnes âgées. Dans la maladie d’Alzheimer, la dégénérescence neurofibrillaire peut progresser vers les régions corticales associatives, selon un schéma établi, séquentiel et hiérarchique. À ce stade, les dépôts amyloïdes sont importants. Pour comprendre la maladie, il faut être capable de différencier la cause de la conséquence. Les formes familiales de la maladie d’Alzheimer ont mis en lumière le rôle majeur joué par le peptide β-amyloïde. Cependant, au cours des dernières années, une pièce maîtresse est venue modifier notre compréhension globale : un grand nombre de maladies neurodégénératives sont dues à des altérations directe ou indirecte du métabolisme de la protéine tau. Nous montrons ici que la maladie d’Alzheimer est une véritable « tauopathie », qui ne peut toutefois se développer qu’en présence d’un dysfonctionnement de l’APP, précurseur du peptide β-amyloïde. | fr |
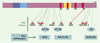
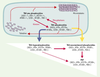
| dc.description.abstract | Tau proteins belong to the family of microtubule-associated proteins. They are mainly expressed in neurons where they play an important role in the assembly of tubulin monomers into microtubules to constitute the neuronal microtubule network. Tau proteins are translated from a single gene located on chromosome 17. Their expression is developmentally regulated by an alternative splicing mechanism and six different isoforms exist in the human adult brain. Tau proteins are the major constituents of fibrillar lesions described in Alzheimer’s disease and numerous neurodegenerative disorders referred to as « tauopathies ». Molecular analysis has revealed that an abnormal phosphorylation might be one of the important events in the process leading to their aggregation. Moreover, a specific set of pathological tau proteins exhibiting a typical biochemical pattern, and a different regional and laminar distribution could characterize each of these disorders. Finally, the recent discovery of tau gene mutations in fron-totemporal dementia with parkinsonism linked to chromosome 17 has reinforced the direct role attributed to tau proteins in the pathogenesis of neurodegenerative disorders, and underlined the fact that distinct sets of tau isoforms expressed in different neuronal populations could lead to different pathologies. Based on these findings, new animal and cell models are developed and should allow for a better understanding of neurofibrillary degeneration. ◊ | en |
| dc.language.iso | fr | fr_FR |
| dc.publisher | EDK | fr_FR |
| dc.relation.ispartof | M/S Revues : Articles de Synthèse | fr_FR |
| dc.rights | Article en libre accès | fr |
| dc.rights | Médecine/Sciences - Inserm - SRMS | fr |
| dc.source | M/S. Médecine sciences [ISSN papier : 0767-0974 ; ISSN numérique : 1958-5381], 2002, Vol. 18, N° 6-7; p. 727-736 | fr_FR |
| dc.title | La maladie d’Alzheimer : une tauopathie parmi d’autres ? | fr |
| dc.type | Article | fr_FR |
| dc.contributor.affiliation | Inserm U.422, nstitut de Médecine Prédictive et Recherche Thérapeutique, place de Verdun, 59045 Lille Cedex, France | fr_FR |
| dc.identifier.doi | 10.1051/medsci/20021867727 | fr_FR |