Protéger et sévir : p53, métabolisme et suppression tumorale
Résumé
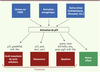
Le gène p53 joue un rôle fondamental dans la suppression tumorale. Ce rôle est généralement expliqué par les trois réponses (le triumvirat)- arrêt transitoire du cycle cellulaire, sénescence ou apoptose - induites par p53 dans les cellules exposées à un stress génotoxique ou oncogénique. Cependant, des résultats récents indiquent que ce triumvirat n’est pas toujours nécessaire à la suppression tumorale. Ils suggèrent, en revanche, que la régulation du métabolisme énergétique par p53, plus précisément sa capacité à diminuer la glycolyse et à stimuler la phosphorylation oxydative, c’est-à-dire à inhiber l’effet Warburg, est un mécanisme important de la suppression tumorale. Une analyse de ces données suggère que les fonctions « conservatrices » de p53, en particulier l’inhibition de l’effet Warburg et l’activité anti-oxydante, mécanistiquement reliées et plutôt associées à une faible expression de p53, préviennent « quotidiennement » la transformation tumorale des cellules normales. Quand cette première barrière est franchie, les fonctions « destructrices » de p53, déclenchées par son expression plus élevée et conduisant à la sénescence ou à l’apoptose, permettent la suppression tumorale vis-à-vis des cellules partiellement ou complètement transformées. The p53 gene is essential for tumor suppression, but how it does so remains unclear. Upon genotoxic or oncogenic stresses, increased p53 activity induces transient cell cycle arrest, senescence or apoptosis, the three cornerstones of the so-called triumvirate. Accordingly, it has long been thought that p53 suppresses tumorigenesis by somehow counteracting cell proliferation or survival. However, several recently described genetically modified mice indicate that p53 can suppress tumorigenesis without triggering these three responses. Rather, as an important mechanism for tumor suppression, these mutant mice point to the ability of p53 to prevent the Warburg effect, that is to dampen glycolysis and foster mitochondrial respiration. Interestingly, these metabolic functions of p53 rely, in part, on its “unstressed” (basal) expression, a feature shared by its mechanistically linked anti-oxydant function. Together, these “conservative” activities of p53 may prevent tumor initiation by promoting and maintaining a normal oxidative metabolism and hence underly the “daily” tumor suppression by p53 in most cells. Conversely, destructive activities elicited by high p53 levels and leading to senescence or apoptosis provide a shield against partially or overtly transformed cells. This last situation, although relatively infrequent throughout life, is usual in experimental settings, which could explain the disproportionally high number of data implicating the triumvirate in tumor suppression by p53.
Pour citer ce document
Albagli, Olivier ; Protéger et sévir : p53, métabolisme et suppression tumorale, Med Sci (Paris), 2015, Vol. 31, N° 10 ; p. 869-880 ; DOI : 10.1051/medsci/20153110013