2021
→ Aller vers ANALYSE→ Aller vers SYNTHESE
| Communications |
Études épidémiologiques dans les populations de travailleurs de l’industrie nucléaire :
apports pour la caractérisation des effets d’expositions chroniques aux rayonnements ionisants
Olivier Laurent
Institut de Radioprotection et de Sûreté Nucléaire (IRSN),
Laboratoire d’épidémiologie des rayonnements ionisants (LEPID)
Institut de Radioprotection et de Sûreté Nucléaire (IRSN),
Laboratoire d’épidémiologie des rayonnements ionisants (LEPID)
Les connaissances sur les effets sanitaires des rayonnements ionisants, issues du suivi épidémiologique des survivants japonais des bombardements atomiques d’Hiroshima et Nagasaki (Shimizu et coll., 2010 ; Ozasa et coll., 2012
; Ozasa et coll., 2012 ; Grant et coll., 2017
; Grant et coll., 2017 ), mais aussi d’autres études, épidémiologiques et expérimentales (UNSCEAR, 2008
), mais aussi d’autres études, épidémiologiques et expérimentales (UNSCEAR, 2008 ; McLean et coll., 2017
; McLean et coll., 2017 ), ont mené à l’élaboration par la Commission Internationale de Protection Radiologique d’un système de radioprotection visant notamment à prévenir les risques de cancers et d’effets héréditaires radio-induits chez les travailleurs et en population générale (ICRP, 2007
), ont mené à l’élaboration par la Commission Internationale de Protection Radiologique d’un système de radioprotection visant notamment à prévenir les risques de cancers et d’effets héréditaires radio-induits chez les travailleurs et en population générale (ICRP, 2007 ). Si ces normes de radioprotection et les réglementations nationales en ayant résulté sont primordiales, certains questionnements sur les effets des rayonnements ionisants à des doses dites faibles (typiquement, inférieures à 100 milliGray (mGy)) suscitent toujours des débats dans la communauté scientifique (HLEG, 2009
). Si ces normes de radioprotection et les réglementations nationales en ayant résulté sont primordiales, certains questionnements sur les effets des rayonnements ionisants à des doses dites faibles (typiquement, inférieures à 100 milliGray (mGy)) suscitent toujours des débats dans la communauté scientifique (HLEG, 2009 ; UNSCEAR, 2015
; UNSCEAR, 2015 ; ICRP, 2017
; ICRP, 2017 ; Kreuzer et coll., 2018
; Kreuzer et coll., 2018 ; NCRP, 2018
; NCRP, 2018 ). Parmi ces questionnements, figurent notamment :
). Parmi ces questionnements, figurent notamment :
 ; Ozasa et coll., 2012
; Ozasa et coll., 2012 ; Grant et coll., 2017
; Grant et coll., 2017 ), mais aussi d’autres études, épidémiologiques et expérimentales (UNSCEAR, 2008
), mais aussi d’autres études, épidémiologiques et expérimentales (UNSCEAR, 2008 ; McLean et coll., 2017
; McLean et coll., 2017 ), ont mené à l’élaboration par la Commission Internationale de Protection Radiologique d’un système de radioprotection visant notamment à prévenir les risques de cancers et d’effets héréditaires radio-induits chez les travailleurs et en population générale (ICRP, 2007
), ont mené à l’élaboration par la Commission Internationale de Protection Radiologique d’un système de radioprotection visant notamment à prévenir les risques de cancers et d’effets héréditaires radio-induits chez les travailleurs et en population générale (ICRP, 2007 ). Si ces normes de radioprotection et les réglementations nationales en ayant résulté sont primordiales, certains questionnements sur les effets des rayonnements ionisants à des doses dites faibles (typiquement, inférieures à 100 milliGray (mGy)) suscitent toujours des débats dans la communauté scientifique (HLEG, 2009
). Si ces normes de radioprotection et les réglementations nationales en ayant résulté sont primordiales, certains questionnements sur les effets des rayonnements ionisants à des doses dites faibles (typiquement, inférieures à 100 milliGray (mGy)) suscitent toujours des débats dans la communauté scientifique (HLEG, 2009 ; UNSCEAR, 2015
; UNSCEAR, 2015 ; ICRP, 2017
; ICRP, 2017 ; Kreuzer et coll., 2018
; Kreuzer et coll., 2018 ; NCRP, 2018
; NCRP, 2018 ). Parmi ces questionnements, figurent notamment :
). Parmi ces questionnements, figurent notamment :
• les effets des expositions chroniques (par comparaison aux expositions très brèves, à haut débit de dose, telles que celles subies par les survivants d’Hiroshima et Nagasaki) ;
• les effets des différentes natures de rayonnements (photons, particules alpha, neutrons) ;
• la forme de la relation dose-risque aux faibles doses, qui est susceptible de varier en fonction des pathologies considérées (NCRP, 2018 ).
).
 ).
).Les études épidémiologiques réalisées dans des populations de travailleurs de l’industrie nucléaire, au-delà de leur intérêt direct pour la santé au travail, visent à apporter des éléments de réponse à plusieurs questionnements de recherche en radioprotection, parmi ceux évoqués ci-dessus. De par les conditions d’exposition des travailleurs et leurs modalités de suivi dosimétrique, ces études permettent de documenter les effets sanitaires d’expositions chroniques à des doses généralement faibles de rayonnements ionisants, qu’il s’agisse d’expositions externes (Leuraud et coll., 2015 ; Richardson et coll., 2015
; Richardson et coll., 2015 ) ou internes par différents radionucléides (Laurier et coll., 2012
) ou internes par différents radionucléides (Laurier et coll., 2012 ).
).
 ; Richardson et coll., 2015
; Richardson et coll., 2015 ) ou internes par différents radionucléides (Laurier et coll., 2012
) ou internes par différents radionucléides (Laurier et coll., 2012 ).
).De nombreuses études de cohortes de travailleurs du nucléaire ont donc été mises en place à travers le monde (Cardis et coll., 2007 ). Les modalités de suivi sanitaire employées dans la plupart d’entre elles correspondent à un croisement avec des registres locaux ou nationaux de pathologies ou de mortalité. Dans de nombreux pays disposant d’une industrie nucléaire développée, aucun registre national rétrospectif d’incidence de pathologies n’est disponible pour les populations adultes. C’est pourquoi la plupart des études de travailleurs du nucléaire ont étudié la mortalité par cancers ou par autres pathologies (Cardis et coll., 2007
). Les modalités de suivi sanitaire employées dans la plupart d’entre elles correspondent à un croisement avec des registres locaux ou nationaux de pathologies ou de mortalité. Dans de nombreux pays disposant d’une industrie nucléaire développée, aucun registre national rétrospectif d’incidence de pathologies n’est disponible pour les populations adultes. C’est pourquoi la plupart des études de travailleurs du nucléaire ont étudié la mortalité par cancers ou par autres pathologies (Cardis et coll., 2007 ; Vrijheid et coll., 2007
; Vrijheid et coll., 2007 ). Dans certains pays cependant, des études d’incidence ont été rendues possibles par l’existence de registres nationaux d’incidence de cancers comme au Royaume-Uni (constituant une exception dans ce domaine) (Haylock et coll., 2018
). Dans certains pays cependant, des études d’incidence ont été rendues possibles par l’existence de registres nationaux d’incidence de cancers comme au Royaume-Uni (constituant une exception dans ce domaine) (Haylock et coll., 2018 ) ou grâce à d’autres efforts spécifiques plus localisés d’identification de cas incidents (par ex. : via la mise en place de systèmes de suivi médical spécifiques aux salariés et ex-salariés de certains sites nucléaires) (Azizova et coll., 2008
) ou grâce à d’autres efforts spécifiques plus localisés d’identification de cas incidents (par ex. : via la mise en place de systèmes de suivi médical spécifiques aux salariés et ex-salariés de certains sites nucléaires) (Azizova et coll., 2008 ).
).
 ). Les modalités de suivi sanitaire employées dans la plupart d’entre elles correspondent à un croisement avec des registres locaux ou nationaux de pathologies ou de mortalité. Dans de nombreux pays disposant d’une industrie nucléaire développée, aucun registre national rétrospectif d’incidence de pathologies n’est disponible pour les populations adultes. C’est pourquoi la plupart des études de travailleurs du nucléaire ont étudié la mortalité par cancers ou par autres pathologies (Cardis et coll., 2007
). Les modalités de suivi sanitaire employées dans la plupart d’entre elles correspondent à un croisement avec des registres locaux ou nationaux de pathologies ou de mortalité. Dans de nombreux pays disposant d’une industrie nucléaire développée, aucun registre national rétrospectif d’incidence de pathologies n’est disponible pour les populations adultes. C’est pourquoi la plupart des études de travailleurs du nucléaire ont étudié la mortalité par cancers ou par autres pathologies (Cardis et coll., 2007 ; Vrijheid et coll., 2007
; Vrijheid et coll., 2007 ). Dans certains pays cependant, des études d’incidence ont été rendues possibles par l’existence de registres nationaux d’incidence de cancers comme au Royaume-Uni (constituant une exception dans ce domaine) (Haylock et coll., 2018
). Dans certains pays cependant, des études d’incidence ont été rendues possibles par l’existence de registres nationaux d’incidence de cancers comme au Royaume-Uni (constituant une exception dans ce domaine) (Haylock et coll., 2018 ) ou grâce à d’autres efforts spécifiques plus localisés d’identification de cas incidents (par ex. : via la mise en place de systèmes de suivi médical spécifiques aux salariés et ex-salariés de certains sites nucléaires) (Azizova et coll., 2008
) ou grâce à d’autres efforts spécifiques plus localisés d’identification de cas incidents (par ex. : via la mise en place de systèmes de suivi médical spécifiques aux salariés et ex-salariés de certains sites nucléaires) (Azizova et coll., 2008 ).
).Disposer de cohortes de larges tailles (typiquement, de plusieurs milliers à centaines de milliers d’individus) est indispensable pour disposer de la puissance statistique nécessaire pour pouvoir mettre en évidence de faibles accroissements de risque associés à de faibles niveaux d’expositions, lorsqu’ils existent (Bouyer et coll., 1992 ; Richardson et coll., 2015
; Richardson et coll., 2015 ). Plus les doses reçues sont faibles et plus les niveaux d’exposition au sein de la cohorte sont homogènes, plus ce constat prévaut (UNSCEAR, 2008
). Plus les doses reçues sont faibles et plus les niveaux d’exposition au sein de la cohorte sont homogènes, plus ce constat prévaut (UNSCEAR, 2008 ). Par ailleurs, des durées de suivi de plusieurs décennies sont également nécessaires pour que des études puissent être informatives vis-à-vis des effets tardifs d’expositions chroniques, se cumulant lentement au cours du temps (Leuraud et coll., 2015
). Par ailleurs, des durées de suivi de plusieurs décennies sont également nécessaires pour que des études puissent être informatives vis-à-vis des effets tardifs d’expositions chroniques, se cumulant lentement au cours du temps (Leuraud et coll., 2015 ; Richardson et coll., 2015
; Richardson et coll., 2015 ).
).
 ; Richardson et coll., 2015
; Richardson et coll., 2015 ). Plus les doses reçues sont faibles et plus les niveaux d’exposition au sein de la cohorte sont homogènes, plus ce constat prévaut (UNSCEAR, 2008
). Plus les doses reçues sont faibles et plus les niveaux d’exposition au sein de la cohorte sont homogènes, plus ce constat prévaut (UNSCEAR, 2008 ). Par ailleurs, des durées de suivi de plusieurs décennies sont également nécessaires pour que des études puissent être informatives vis-à-vis des effets tardifs d’expositions chroniques, se cumulant lentement au cours du temps (Leuraud et coll., 2015
). Par ailleurs, des durées de suivi de plusieurs décennies sont également nécessaires pour que des études puissent être informatives vis-à-vis des effets tardifs d’expositions chroniques, se cumulant lentement au cours du temps (Leuraud et coll., 2015 ; Richardson et coll., 2015
; Richardson et coll., 2015 ).
).Des cohortes de travailleurs surveillés pour exposition aux rayonnements ionisants ont été mises en place depuis les années 1960. La maturité atteinte par plusieurs de ces cohortes leur permet à présent de fournir des informations pertinentes sur les effets sanitaires d’expositions chroniques aux rayonnements ionisants, que ce soit par voie externe ou par contamination interne. Ces deux aspects seront abordés séparément ci-dessous.
Effets des expositions chroniques aux rayonnements ionisants par voie externe
De nombreuses cohortes ont été mises en place chez les travailleurs de l’industrie électronucléaire surveillés pour une exposition externe aux rayonnements ionisants via le port de dosimètres individuels (Cardis et coll., 2007 ). La plupart des analyses réalisées dans des pays isolés, sauf exception (Haylock et coll., 2018
). La plupart des analyses réalisées dans des pays isolés, sauf exception (Haylock et coll., 2018 ), ne disposent pas de la puissance statistique nécessaire à la caractérisation d’associations entre exposition externe aux rayonnements ionisants à faibles doses et causes de décès, hormis pour quelques causes de décès fortement associées à ces expositions comme par exemple les leucémies (Leuraud et coll., 2017
), ne disposent pas de la puissance statistique nécessaire à la caractérisation d’associations entre exposition externe aux rayonnements ionisants à faibles doses et causes de décès, hormis pour quelques causes de décès fortement associées à ces expositions comme par exemple les leucémies (Leuraud et coll., 2017 ). Seule la réalisation d’analyses conjointes de grande ampleur, notamment au niveau international, peut alors fournir les effectifs nécessaires à ce type d’analyses.
). Seule la réalisation d’analyses conjointes de grande ampleur, notamment au niveau international, peut alors fournir les effectifs nécessaires à ce type d’analyses.
 ). La plupart des analyses réalisées dans des pays isolés, sauf exception (Haylock et coll., 2018
). La plupart des analyses réalisées dans des pays isolés, sauf exception (Haylock et coll., 2018 ), ne disposent pas de la puissance statistique nécessaire à la caractérisation d’associations entre exposition externe aux rayonnements ionisants à faibles doses et causes de décès, hormis pour quelques causes de décès fortement associées à ces expositions comme par exemple les leucémies (Leuraud et coll., 2017
), ne disposent pas de la puissance statistique nécessaire à la caractérisation d’associations entre exposition externe aux rayonnements ionisants à faibles doses et causes de décès, hormis pour quelques causes de décès fortement associées à ces expositions comme par exemple les leucémies (Leuraud et coll., 2017 ). Seule la réalisation d’analyses conjointes de grande ampleur, notamment au niveau international, peut alors fournir les effectifs nécessaires à ce type d’analyses.
). Seule la réalisation d’analyses conjointes de grande ampleur, notamment au niveau international, peut alors fournir les effectifs nécessaires à ce type d’analyses.Des analyses internationales de cette nature ont donc été réalisées à plusieurs reprises. Ainsi, une analyse conjointe de cohortes de travailleurs du nucléaire de 15 pays coordonnée par le Centre International de Recherche sur le Cancer (CIRC) a été réalisée et publiée dans les années 2000 (Cardis et coll., 2007 ). Cette analyse, intégrant plus de 400 000 travailleurs parmi lesquels 24 158 étaient décédés à la fin du suivi, a rapporté une association statistiquement significative entre expositions à des rayonnements ionisants à faibles doses et risques de cancers solides ; toutefois ces résultats ont été très discutés en raison notamment de la jeunesse de la population en fin de suivi (46 ans en moyenne), limitant fortement sa capacité à observer l’expression des risques chroniques en lien avec des doses se cumulant lentement au fil des années (la durée moyenne de suivi n’était que de 13 ans) et de questionnements sur la qualité de la reconstruction dosimétrique dans un pays participant, à savoir le Canada (Wakeford, 2014
). Cette analyse, intégrant plus de 400 000 travailleurs parmi lesquels 24 158 étaient décédés à la fin du suivi, a rapporté une association statistiquement significative entre expositions à des rayonnements ionisants à faibles doses et risques de cancers solides ; toutefois ces résultats ont été très discutés en raison notamment de la jeunesse de la population en fin de suivi (46 ans en moyenne), limitant fortement sa capacité à observer l’expression des risques chroniques en lien avec des doses se cumulant lentement au fil des années (la durée moyenne de suivi n’était que de 13 ans) et de questionnements sur la qualité de la reconstruction dosimétrique dans un pays participant, à savoir le Canada (Wakeford, 2014 ).
).
 ). Cette analyse, intégrant plus de 400 000 travailleurs parmi lesquels 24 158 étaient décédés à la fin du suivi, a rapporté une association statistiquement significative entre expositions à des rayonnements ionisants à faibles doses et risques de cancers solides ; toutefois ces résultats ont été très discutés en raison notamment de la jeunesse de la population en fin de suivi (46 ans en moyenne), limitant fortement sa capacité à observer l’expression des risques chroniques en lien avec des doses se cumulant lentement au fil des années (la durée moyenne de suivi n’était que de 13 ans) et de questionnements sur la qualité de la reconstruction dosimétrique dans un pays participant, à savoir le Canada (Wakeford, 2014
). Cette analyse, intégrant plus de 400 000 travailleurs parmi lesquels 24 158 étaient décédés à la fin du suivi, a rapporté une association statistiquement significative entre expositions à des rayonnements ionisants à faibles doses et risques de cancers solides ; toutefois ces résultats ont été très discutés en raison notamment de la jeunesse de la population en fin de suivi (46 ans en moyenne), limitant fortement sa capacité à observer l’expression des risques chroniques en lien avec des doses se cumulant lentement au fil des années (la durée moyenne de suivi n’était que de 13 ans) et de questionnements sur la qualité de la reconstruction dosimétrique dans un pays participant, à savoir le Canada (Wakeford, 2014 ).
).Plus récemment, afin de pallier ces limites, l’étude internationale INWORKS (International Nuclear Workers Study) rassemblant les travailleurs du nucléaire de trois pays (France, Royaume-Uni et États-Unis) avec une durée de suivi étendue jusqu’au milieu des années 2000 a été mise en place, là encore sous la coordination du CIRC (Hamra et coll., 2016 ). La population étudiée dans INWORKS inclut plus de 300 000 travailleurs, hommes (87 %) et femmes (13 %) employés dans l’industrie nucléaire (préparation du combustible, recherche, production d’électricité, retraitement des combustibles irradiés) à partir du milieu des années 1940.
). La population étudiée dans INWORKS inclut plus de 300 000 travailleurs, hommes (87 %) et femmes (13 %) employés dans l’industrie nucléaire (préparation du combustible, recherche, production d’électricité, retraitement des combustibles irradiés) à partir du milieu des années 1940.
 ). La population étudiée dans INWORKS inclut plus de 300 000 travailleurs, hommes (87 %) et femmes (13 %) employés dans l’industrie nucléaire (préparation du combustible, recherche, production d’électricité, retraitement des combustibles irradiés) à partir du milieu des années 1940.
). La population étudiée dans INWORKS inclut plus de 300 000 travailleurs, hommes (87 %) et femmes (13 %) employés dans l’industrie nucléaire (préparation du combustible, recherche, production d’électricité, retraitement des combustibles irradiés) à partir du milieu des années 1940.La robustesse de cette étude résulte du protocole mis en place, qui repose sur la combinaison des cohortes de travailleurs les plus importantes au monde, une longue durée de suivi, la standardisation des critères d’inclusion entre cohortes, la vérification de l’homogénéité et de la qualité des données et la vérification de la stabilité des résultats par la réalisation d’analyses de sensibilité1
. Les travailleurs inclus dans l’étude INWORKS ont fait l’objet d’un suivi épidémiologique en moyenne pendant 27 ans. La dose moyenne reçue par les travailleurs est de 25 milliSieverts (mSv) cumulés sur la durée de l’activité professionnelle, dont la moyenne est de 15 ans. Plus de 94 % des individus de cette cohorte ont reçu des doses cumulées inférieures à 100 mSv. Parmi les 6 % d’individus dont la dose cumulée a dépassé 100 mSv, 75 % ont été embauchés avant les années 1970. Au total, plus de 66 600 décès ont été enregistrés dans la cohorte. Plusieurs séries d’analyses statistiques ont été réalisées, en considérant différents groupes de causes de décès.
Analyse des risques de mortalité par cancers lympho-hématopoïétiques dans INWORKS
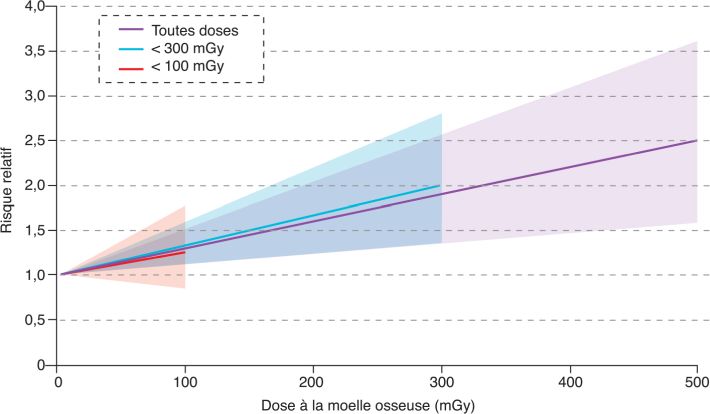
Les premières analyses ont porté sur 531 décès par leucémie (hors leucémie lymphoïde chronique), 814 par lymphome et 293 par myélome multiple (Leuraud et coll., 2015 ). Les résultats montrent que le risque de leucémie (hors leucémie lymphoïde chronique) est multiplié par un facteur d’environ 4 pour une augmentation de la dose reçue à la moelle osseuse de 1 Gy ; l’excès de risque relatif (ERR) par Gy étant de 2,96 (intervalle de confiance à 90 % : IC 90 % [1,17-5,21]), en considérant un délai de latence minimal de deux ans entre exposition et expression du risque. Cette relation reste statistiquement significative pour les travailleurs ayant reçu des doses à la moelle osseuse inférieures à 300 mGy. Lorsque l’analyse est restreinte à des gammes de doses plus faibles, les estimations d’excès de risque relatif sont moins précises et ne sont plus statistiquement significatives ; toutefois les valeurs des pentes estimées (valeur centrale de l’ERR par Gy) demeurent très proches de celles estimées sur l’ensemble de la gamme de doses observées (figure 1
). Les résultats montrent que le risque de leucémie (hors leucémie lymphoïde chronique) est multiplié par un facteur d’environ 4 pour une augmentation de la dose reçue à la moelle osseuse de 1 Gy ; l’excès de risque relatif (ERR) par Gy étant de 2,96 (intervalle de confiance à 90 % : IC 90 % [1,17-5,21]), en considérant un délai de latence minimal de deux ans entre exposition et expression du risque. Cette relation reste statistiquement significative pour les travailleurs ayant reçu des doses à la moelle osseuse inférieures à 300 mGy. Lorsque l’analyse est restreinte à des gammes de doses plus faibles, les estimations d’excès de risque relatif sont moins précises et ne sont plus statistiquement significatives ; toutefois les valeurs des pentes estimées (valeur centrale de l’ERR par Gy) demeurent très proches de celles estimées sur l’ensemble de la gamme de doses observées (figure 1 ). Pour les lymphomes et les myélomes multiples, l’étude ne montre pas d’augmentation statistiquement significative du risque de mortalité avec la dose (Leuraud et coll., 2015
). Pour les lymphomes et les myélomes multiples, l’étude ne montre pas d’augmentation statistiquement significative du risque de mortalité avec la dose (Leuraud et coll., 2015 ).
).
 ). Les résultats montrent que le risque de leucémie (hors leucémie lymphoïde chronique) est multiplié par un facteur d’environ 4 pour une augmentation de la dose reçue à la moelle osseuse de 1 Gy ; l’excès de risque relatif (ERR) par Gy étant de 2,96 (intervalle de confiance à 90 % : IC 90 % [1,17-5,21]), en considérant un délai de latence minimal de deux ans entre exposition et expression du risque. Cette relation reste statistiquement significative pour les travailleurs ayant reçu des doses à la moelle osseuse inférieures à 300 mGy. Lorsque l’analyse est restreinte à des gammes de doses plus faibles, les estimations d’excès de risque relatif sont moins précises et ne sont plus statistiquement significatives ; toutefois les valeurs des pentes estimées (valeur centrale de l’ERR par Gy) demeurent très proches de celles estimées sur l’ensemble de la gamme de doses observées (figure 1
). Les résultats montrent que le risque de leucémie (hors leucémie lymphoïde chronique) est multiplié par un facteur d’environ 4 pour une augmentation de la dose reçue à la moelle osseuse de 1 Gy ; l’excès de risque relatif (ERR) par Gy étant de 2,96 (intervalle de confiance à 90 % : IC 90 % [1,17-5,21]), en considérant un délai de latence minimal de deux ans entre exposition et expression du risque. Cette relation reste statistiquement significative pour les travailleurs ayant reçu des doses à la moelle osseuse inférieures à 300 mGy. Lorsque l’analyse est restreinte à des gammes de doses plus faibles, les estimations d’excès de risque relatif sont moins précises et ne sont plus statistiquement significatives ; toutefois les valeurs des pentes estimées (valeur centrale de l’ERR par Gy) demeurent très proches de celles estimées sur l’ensemble de la gamme de doses observées (figure 1 ). Pour les lymphomes et les myélomes multiples, l’étude ne montre pas d’augmentation statistiquement significative du risque de mortalité avec la dose (Leuraud et coll., 2015
). Pour les lymphomes et les myélomes multiples, l’étude ne montre pas d’augmentation statistiquement significative du risque de mortalité avec la dose (Leuraud et coll., 2015 ).
).Analyse des risques de mortalité par cancers solides dans INWORKS
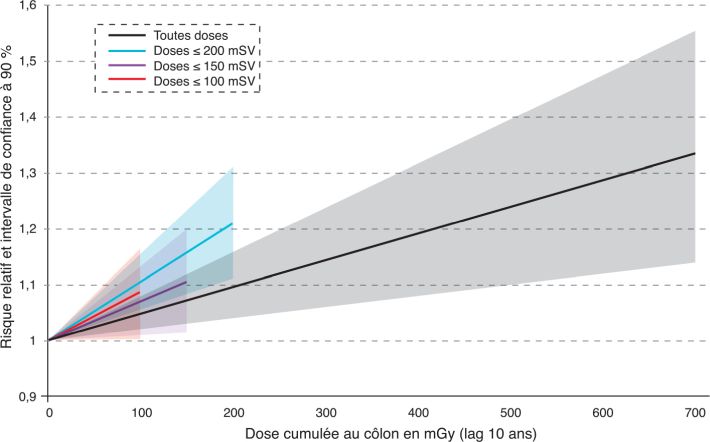
Les résultats de l’analyse de la mortalité par cancers solides (incluant 17 957 cas observés) montrent que l’ERR par Gy reçu au côlon est de 0,47 (IC 90 % [0,18-0,79]) en considérant un délai de latence minimal de dix ans entre exposition et expression du risque (Richardson et coll., 2015 ). Les résultats sont similaires lorsque la mortalité par tous cancers autres que leucémies (19 064 cas observés) est analysée : l’ERR par Gy est alors de 0,48 (IC 90 % [0,20-0,79]). En dessous de 100 mGy, l’estimation est moins précise et la relation n’est plus statistiquement significative. Toutefois la pente estimée reste compatible avec celle estimée en considérant l’ensemble de la gamme de doses (figure 2
). Les résultats sont similaires lorsque la mortalité par tous cancers autres que leucémies (19 064 cas observés) est analysée : l’ERR par Gy est alors de 0,48 (IC 90 % [0,20-0,79]). En dessous de 100 mGy, l’estimation est moins précise et la relation n’est plus statistiquement significative. Toutefois la pente estimée reste compatible avec celle estimée en considérant l’ensemble de la gamme de doses (figure 2 ).
).
 ). Les résultats sont similaires lorsque la mortalité par tous cancers autres que leucémies (19 064 cas observés) est analysée : l’ERR par Gy est alors de 0,48 (IC 90 % [0,20-0,79]). En dessous de 100 mGy, l’estimation est moins précise et la relation n’est plus statistiquement significative. Toutefois la pente estimée reste compatible avec celle estimée en considérant l’ensemble de la gamme de doses (figure 2
). Les résultats sont similaires lorsque la mortalité par tous cancers autres que leucémies (19 064 cas observés) est analysée : l’ERR par Gy est alors de 0,48 (IC 90 % [0,20-0,79]). En dessous de 100 mGy, l’estimation est moins précise et la relation n’est plus statistiquement significative. Toutefois la pente estimée reste compatible avec celle estimée en considérant l’ensemble de la gamme de doses (figure 2 ).
).La relation observée est stable. Elle présente peu d’hétérogénéité entre pays, et seules des variations de faible ampleur ont été observées dans les analyses de sensibilité considérant par exemple différents délais de latence minimale entre exposition et expression du risque (5 ou 15 ans), le test de différentes formes de relation dose-risque (linéaire, quadratique, linéaire-quadratique), ou encore l’exclusion des individus susceptibles d’avoir reçu des expositions radiologiques substantielles via des neutrons ou des contaminations internes (Richardson et coll., 2015 ). Pour évaluer l’existence d’un biais potentiel qu’aurait pu induire sur les résultats le tabagisme (non mesuré dans l’étude), les cancers du poumon ont été exclus dans le cadre d’une analyse de sensibilité ; cette exclusion a eu peu d’impact sur l’estimation du risque (l’ERR/Gy étant alors de 0,46 (IC 90 % [0,11-0,85]) en considérant un délai de latence minimal de dix ans entre exposition et expression du risque). Ce résultat n’aurait pas été observé en présence d’un biais important dû au tabagisme.
). Pour évaluer l’existence d’un biais potentiel qu’aurait pu induire sur les résultats le tabagisme (non mesuré dans l’étude), les cancers du poumon ont été exclus dans le cadre d’une analyse de sensibilité ; cette exclusion a eu peu d’impact sur l’estimation du risque (l’ERR/Gy étant alors de 0,46 (IC 90 % [0,11-0,85]) en considérant un délai de latence minimal de dix ans entre exposition et expression du risque). Ce résultat n’aurait pas été observé en présence d’un biais important dû au tabagisme.
 ). Pour évaluer l’existence d’un biais potentiel qu’aurait pu induire sur les résultats le tabagisme (non mesuré dans l’étude), les cancers du poumon ont été exclus dans le cadre d’une analyse de sensibilité ; cette exclusion a eu peu d’impact sur l’estimation du risque (l’ERR/Gy étant alors de 0,46 (IC 90 % [0,11-0,85]) en considérant un délai de latence minimal de dix ans entre exposition et expression du risque). Ce résultat n’aurait pas été observé en présence d’un biais important dû au tabagisme.
). Pour évaluer l’existence d’un biais potentiel qu’aurait pu induire sur les résultats le tabagisme (non mesuré dans l’étude), les cancers du poumon ont été exclus dans le cadre d’une analyse de sensibilité ; cette exclusion a eu peu d’impact sur l’estimation du risque (l’ERR/Gy étant alors de 0,46 (IC 90 % [0,11-0,85]) en considérant un délai de latence minimal de dix ans entre exposition et expression du risque). Ce résultat n’aurait pas été observé en présence d’un biais important dû au tabagisme.Plus récemment, une analyse sur la mortalité par sites spécifiques de cancers solides a été publiée (Richardson et coll., 2018 ). Parmi les 17 957 décès par cancers solides observés dans INWORKS, les localisations tumorales les plus fréquentes étaient le poumon (5 802 décès), la prostate (1 685 décès) et le côlon (1 570 décès). Même pour ces cancers les plus fréquents, les effectifs demeurent limités pour permettre une quantification précise des associations avec de faibles doses de rayonnements ionisants par site de cancer spécifique : globalement, les estimations obtenues demeurent très imprécises. Pour la mortalité par cancer du poumon, des estimations de risque similaires ont été obtenues en utilisant deux méthodes d’analyse (respectivement, pour une régression de Poisson basée sur la méthode du maximum de vraisemblance : ERR/Gy = 0,51 ; IC 90 % [0-1,09] ; et pour une régression de Poisson hiérarchique utilisant une méthode de Monte Carlo par chaîne de Markov : ERR/Gy = 0,56 ; IC 90 % [0,08-1,02]). Pour les cancers moins fréquents, les estimations pouvaient différer notablement selon la méthode utilisée. Ces résultats suggèrent qu’une augmentation du suivi des cohortes incluses sera nécessaire pour qu’elles puissent exprimer tout leur potentiel d’information et notamment pour caractériser les associations entre expositions aux rayonnements ionisants et risques de cancers solides par sites spécifiques.
). Parmi les 17 957 décès par cancers solides observés dans INWORKS, les localisations tumorales les plus fréquentes étaient le poumon (5 802 décès), la prostate (1 685 décès) et le côlon (1 570 décès). Même pour ces cancers les plus fréquents, les effectifs demeurent limités pour permettre une quantification précise des associations avec de faibles doses de rayonnements ionisants par site de cancer spécifique : globalement, les estimations obtenues demeurent très imprécises. Pour la mortalité par cancer du poumon, des estimations de risque similaires ont été obtenues en utilisant deux méthodes d’analyse (respectivement, pour une régression de Poisson basée sur la méthode du maximum de vraisemblance : ERR/Gy = 0,51 ; IC 90 % [0-1,09] ; et pour une régression de Poisson hiérarchique utilisant une méthode de Monte Carlo par chaîne de Markov : ERR/Gy = 0,56 ; IC 90 % [0,08-1,02]). Pour les cancers moins fréquents, les estimations pouvaient différer notablement selon la méthode utilisée. Ces résultats suggèrent qu’une augmentation du suivi des cohortes incluses sera nécessaire pour qu’elles puissent exprimer tout leur potentiel d’information et notamment pour caractériser les associations entre expositions aux rayonnements ionisants et risques de cancers solides par sites spécifiques.
 ). Parmi les 17 957 décès par cancers solides observés dans INWORKS, les localisations tumorales les plus fréquentes étaient le poumon (5 802 décès), la prostate (1 685 décès) et le côlon (1 570 décès). Même pour ces cancers les plus fréquents, les effectifs demeurent limités pour permettre une quantification précise des associations avec de faibles doses de rayonnements ionisants par site de cancer spécifique : globalement, les estimations obtenues demeurent très imprécises. Pour la mortalité par cancer du poumon, des estimations de risque similaires ont été obtenues en utilisant deux méthodes d’analyse (respectivement, pour une régression de Poisson basée sur la méthode du maximum de vraisemblance : ERR/Gy = 0,51 ; IC 90 % [0-1,09] ; et pour une régression de Poisson hiérarchique utilisant une méthode de Monte Carlo par chaîne de Markov : ERR/Gy = 0,56 ; IC 90 % [0,08-1,02]). Pour les cancers moins fréquents, les estimations pouvaient différer notablement selon la méthode utilisée. Ces résultats suggèrent qu’une augmentation du suivi des cohortes incluses sera nécessaire pour qu’elles puissent exprimer tout leur potentiel d’information et notamment pour caractériser les associations entre expositions aux rayonnements ionisants et risques de cancers solides par sites spécifiques.
). Parmi les 17 957 décès par cancers solides observés dans INWORKS, les localisations tumorales les plus fréquentes étaient le poumon (5 802 décès), la prostate (1 685 décès) et le côlon (1 570 décès). Même pour ces cancers les plus fréquents, les effectifs demeurent limités pour permettre une quantification précise des associations avec de faibles doses de rayonnements ionisants par site de cancer spécifique : globalement, les estimations obtenues demeurent très imprécises. Pour la mortalité par cancer du poumon, des estimations de risque similaires ont été obtenues en utilisant deux méthodes d’analyse (respectivement, pour une régression de Poisson basée sur la méthode du maximum de vraisemblance : ERR/Gy = 0,51 ; IC 90 % [0-1,09] ; et pour une régression de Poisson hiérarchique utilisant une méthode de Monte Carlo par chaîne de Markov : ERR/Gy = 0,56 ; IC 90 % [0,08-1,02]). Pour les cancers moins fréquents, les estimations pouvaient différer notablement selon la méthode utilisée. Ces résultats suggèrent qu’une augmentation du suivi des cohortes incluses sera nécessaire pour qu’elles puissent exprimer tout leur potentiel d’information et notamment pour caractériser les associations entre expositions aux rayonnements ionisants et risques de cancers solides par sites spécifiques.En résumé, pour les cancers solides considérés conjointement et pour les leucémies, sur l’ensemble de la population d’INWORKS, la relation dose-réponse suite à une exposition externe chronique aux rayonnements ionisants est statistiquement significative. Aux très faibles doses, c’est-à-dire en dessous de quelques dizaines de mSv, l’incertitude statistique devient importante, et la relation dose-réponse n’est plus statistiquement significative, sans que l’on puisse écarter l’existence d’une association. Les associations doses-risques observées dans l’étude INWORKS sont cohérentes avec celles observées dans d’autres études, en particulier chez les survivants des bombardements atomiques d’Hiroshima et Nagasaki, exposés à des forts débits de doses. Les résultats d’INWORKS montrent ainsi que la relation entre le risque de décès par cancers solides ou par leucémie et une exposition chronique à de faibles doses de rayonnements ionisants est similaire à celle déjà connue pour des doses délivrées à fort débit. Ces résultats sont compatibles avec l’une des hypothèses sous-jacentes au système de radioprotection actuel qui est la transposition du modèle dérivé des survivants des bombardement d’Hiroshima et Nagasaki aux populations exposées de façon répétée à de faibles doses (ICRP, 2007 ).
).
 ).
).À partir des relations dose-risque estimées, sous l’hypothèse que les relations observées sont causales, il apparaît que la proportion de décès attribuable à l’exposition externe aux rayonnements au sein de la population d’INWORKS est de l’ordre de :
• 1 % de l’ensemble des 19 064 décès par cancer hors leucémie observés ;
• 5 % de l’ensemble des 531 décès par leucémie observés.
Analyse des risques de mortalité par pathologies non cancéreuses
dans INWORKS
Parmi les 46 029 décès survenus pour d’autres causes que le cancer, une analyse spécifique a été réalisée sur les risques de pathologies non cancéreuses (Gillies et coll., 2017b ). Une association positive, statistiquement significative, a été observée entre la dose externe cumulée et le risque de décès par maladies du système circulatoire (27 848 cas observés), l’ERR/ Sv étant de 0,22 (IC 90 % [0,08-0,37]). Cette association est principalement due à une augmentation du risque de décès par infarctus du myocarde (ERR/Sv = 0,26 (IC 90 % [0,03-0,51]) et par pathologies cérébrovasculaires (ERR/Sv = 0,50 (IC 90 % [0,12-0,94]). L’association avec les décès par pathologies du système circulatoire reste statistiquement significative lorsqu’elle est estimée sur une gamme de doses restreinte à moins de 300 mSv (ERR/Sv = 0,28 ; IC 90 % [0,03-0,53]). Cependant lorsque la relation est étudiée sur une gamme de doses restreinte à moins de 200 mSv, l’association n’est plus statistiquement significative. Pour la mortalité par cardiopathie ischémique, l’ERR par Sv estimé à des doses inférieures à 300 mSv n’est pas statistiquement significatif mais est très proche de celui estimé pour l’ensemble de la gamme de doses observées. Pour la mortalité par pathologies cérébrovasculaires, la relation dose-réponse est non linéaire, avec un risque qui augmente avec la dose pour des doses inférieures à 200 mSv, puis demeure stable à des doses plus élevées. L’association est positive et statistiquement significative pour des doses inférieures à 100 mSv (ERR/Sv = 2,07 (IC 90 % [0,43-3,80]).
). Une association positive, statistiquement significative, a été observée entre la dose externe cumulée et le risque de décès par maladies du système circulatoire (27 848 cas observés), l’ERR/ Sv étant de 0,22 (IC 90 % [0,08-0,37]). Cette association est principalement due à une augmentation du risque de décès par infarctus du myocarde (ERR/Sv = 0,26 (IC 90 % [0,03-0,51]) et par pathologies cérébrovasculaires (ERR/Sv = 0,50 (IC 90 % [0,12-0,94]). L’association avec les décès par pathologies du système circulatoire reste statistiquement significative lorsqu’elle est estimée sur une gamme de doses restreinte à moins de 300 mSv (ERR/Sv = 0,28 ; IC 90 % [0,03-0,53]). Cependant lorsque la relation est étudiée sur une gamme de doses restreinte à moins de 200 mSv, l’association n’est plus statistiquement significative. Pour la mortalité par cardiopathie ischémique, l’ERR par Sv estimé à des doses inférieures à 300 mSv n’est pas statistiquement significatif mais est très proche de celui estimé pour l’ensemble de la gamme de doses observées. Pour la mortalité par pathologies cérébrovasculaires, la relation dose-réponse est non linéaire, avec un risque qui augmente avec la dose pour des doses inférieures à 200 mSv, puis demeure stable à des doses plus élevées. L’association est positive et statistiquement significative pour des doses inférieures à 100 mSv (ERR/Sv = 2,07 (IC 90 % [0,43-3,80]).
 ). Une association positive, statistiquement significative, a été observée entre la dose externe cumulée et le risque de décès par maladies du système circulatoire (27 848 cas observés), l’ERR/ Sv étant de 0,22 (IC 90 % [0,08-0,37]). Cette association est principalement due à une augmentation du risque de décès par infarctus du myocarde (ERR/Sv = 0,26 (IC 90 % [0,03-0,51]) et par pathologies cérébrovasculaires (ERR/Sv = 0,50 (IC 90 % [0,12-0,94]). L’association avec les décès par pathologies du système circulatoire reste statistiquement significative lorsqu’elle est estimée sur une gamme de doses restreinte à moins de 300 mSv (ERR/Sv = 0,28 ; IC 90 % [0,03-0,53]). Cependant lorsque la relation est étudiée sur une gamme de doses restreinte à moins de 200 mSv, l’association n’est plus statistiquement significative. Pour la mortalité par cardiopathie ischémique, l’ERR par Sv estimé à des doses inférieures à 300 mSv n’est pas statistiquement significatif mais est très proche de celui estimé pour l’ensemble de la gamme de doses observées. Pour la mortalité par pathologies cérébrovasculaires, la relation dose-réponse est non linéaire, avec un risque qui augmente avec la dose pour des doses inférieures à 200 mSv, puis demeure stable à des doses plus élevées. L’association est positive et statistiquement significative pour des doses inférieures à 100 mSv (ERR/Sv = 2,07 (IC 90 % [0,43-3,80]).
). Une association positive, statistiquement significative, a été observée entre la dose externe cumulée et le risque de décès par maladies du système circulatoire (27 848 cas observés), l’ERR/ Sv étant de 0,22 (IC 90 % [0,08-0,37]). Cette association est principalement due à une augmentation du risque de décès par infarctus du myocarde (ERR/Sv = 0,26 (IC 90 % [0,03-0,51]) et par pathologies cérébrovasculaires (ERR/Sv = 0,50 (IC 90 % [0,12-0,94]). L’association avec les décès par pathologies du système circulatoire reste statistiquement significative lorsqu’elle est estimée sur une gamme de doses restreinte à moins de 300 mSv (ERR/Sv = 0,28 ; IC 90 % [0,03-0,53]). Cependant lorsque la relation est étudiée sur une gamme de doses restreinte à moins de 200 mSv, l’association n’est plus statistiquement significative. Pour la mortalité par cardiopathie ischémique, l’ERR par Sv estimé à des doses inférieures à 300 mSv n’est pas statistiquement significatif mais est très proche de celui estimé pour l’ensemble de la gamme de doses observées. Pour la mortalité par pathologies cérébrovasculaires, la relation dose-réponse est non linéaire, avec un risque qui augmente avec la dose pour des doses inférieures à 200 mSv, puis demeure stable à des doses plus élevées. L’association est positive et statistiquement significative pour des doses inférieures à 100 mSv (ERR/Sv = 2,07 (IC 90 % [0,43-3,80]).Parmi les autres causes de décès étudiées, une association significative est observée entre la dose cumulée et le risque de décès par pathologies mentales (ERR/Sv = 1,30 (IC 90 % [0,23-2,72]), sur la base de 705 décès principalement par démence). Des associations positives, mais non statistiquement significatives, sont également rapportées pour les décès par pathologies respiratoires (ERR/Sv = 0,13 (IC 90 % [-0,17-0,47]) et digestives (ERR/Sv = 0,11 (IC 90 % [-0,36-0,69]).
Concernant le risque de décès par bronchopneumopathie chronique obstructive (BPCO, une pathologie très fortement associée au tabagisme), aucune association avec la dose de rayonnements ionisants n’est observée (ERR/Sv = -0,07 (IC 90 % [-0,45-0,38]), suggérant à nouveau que le tabagisme, bien que non directement pris en compte par ajustement statistique dans le cadre de l’étude en raison d’un manque de données individuelles, ne peut fortement biaiser les résultats de la relation entre exposition aux rayonnements et autres pathologies (cancers, maladies de l’appareil circulatoire). Les autres facteurs de risque individuels (également non mesurés, par exemple : obésité, diabète) pourraient néanmoins potentiellement impacter les résultats observés pour les pathologies du système circulatoire. Par ailleurs, les auteurs soulignent que les résultats observés dans INWORKS pour les pathologies de l’appareil circulatoire sont moins robustes que ceux observés pour les cancers. En effet, pour les pathologies de l’appareil circulatoire, on observe une hétérogénéité des estimations de risque entre les différents pays et sites industriels (Gillies et coll., 2017b ). Ils appellent par conséquent à la prudence quant à la conclusion de liens de causalité pour les pathologies non cancéreuses dans INWORKS.
). Ils appellent par conséquent à la prudence quant à la conclusion de liens de causalité pour les pathologies non cancéreuses dans INWORKS.
 ). Ils appellent par conséquent à la prudence quant à la conclusion de liens de causalité pour les pathologies non cancéreuses dans INWORKS.
). Ils appellent par conséquent à la prudence quant à la conclusion de liens de causalité pour les pathologies non cancéreuses dans INWORKS.Autres études récentes
Très récemment, une analyse de mortalité et d’incidence de cancers au Royaume-Uni a été publiée, sur la base d’une mise à jour jusqu’à la fin de l’année 2011 d’une cohorte de 167 003 travailleurs surveillés pour exposition aux rayonnements ionisants, avec un suivi sur une moyenne de 32 années, à l’aide d’un registre national dédié, le National Registry of Radiation Workers (NRRW) (Haylock et coll., 2018 ). Une large proportion des travailleurs de cette cohorte a également été incluse dans INWORKS (avec une durée de suivi qui était alors moins longue). Les résultats de l’analyse de mortalité montrent une bonne cohérence avec ceux de l’étude INWORKS et de l’étude des survivants d’Hiroshima et Nagasaki. Par ailleurs, une comparaison des estimations de risque observées pour la mortalité par cancers (toutes localisations confondues) à l’exception des leucémies, et l’incidence des cancers montre des estimations de risques très proches : ERR/Sv pour la mortalité = 0,28 (IC 90 % [0,06-0,53]) ; ERR/Sv pour l’incidence = 0,28 (IC 90 % [0,10-0,48]) (Haylock et coll., 2018
). Une large proportion des travailleurs de cette cohorte a également été incluse dans INWORKS (avec une durée de suivi qui était alors moins longue). Les résultats de l’analyse de mortalité montrent une bonne cohérence avec ceux de l’étude INWORKS et de l’étude des survivants d’Hiroshima et Nagasaki. Par ailleurs, une comparaison des estimations de risque observées pour la mortalité par cancers (toutes localisations confondues) à l’exception des leucémies, et l’incidence des cancers montre des estimations de risques très proches : ERR/Sv pour la mortalité = 0,28 (IC 90 % [0,06-0,53]) ; ERR/Sv pour l’incidence = 0,28 (IC 90 % [0,10-0,48]) (Haylock et coll., 2018 ).
).
 ). Une large proportion des travailleurs de cette cohorte a également été incluse dans INWORKS (avec une durée de suivi qui était alors moins longue). Les résultats de l’analyse de mortalité montrent une bonne cohérence avec ceux de l’étude INWORKS et de l’étude des survivants d’Hiroshima et Nagasaki. Par ailleurs, une comparaison des estimations de risque observées pour la mortalité par cancers (toutes localisations confondues) à l’exception des leucémies, et l’incidence des cancers montre des estimations de risques très proches : ERR/Sv pour la mortalité = 0,28 (IC 90 % [0,06-0,53]) ; ERR/Sv pour l’incidence = 0,28 (IC 90 % [0,10-0,48]) (Haylock et coll., 2018
). Une large proportion des travailleurs de cette cohorte a également été incluse dans INWORKS (avec une durée de suivi qui était alors moins longue). Les résultats de l’analyse de mortalité montrent une bonne cohérence avec ceux de l’étude INWORKS et de l’étude des survivants d’Hiroshima et Nagasaki. Par ailleurs, une comparaison des estimations de risque observées pour la mortalité par cancers (toutes localisations confondues) à l’exception des leucémies, et l’incidence des cancers montre des estimations de risques très proches : ERR/Sv pour la mortalité = 0,28 (IC 90 % [0,06-0,53]) ; ERR/Sv pour l’incidence = 0,28 (IC 90 % [0,10-0,48]) (Haylock et coll., 2018 ).
).De nombreuses analyses ont également été menées dans la cohorte des travailleurs du complexe militaro-industriel de Mayak (Russie) dédié à la production de plutonium (Mayak Production Association). Cette cohorte présente une taille moins importante que celles précédemment évoquées puisqu’elle inclut environ 20 000 travailleurs, mais ceux-ci ont été exposés à une très large gamme de doses et à des niveaux en moyenne plus élevés que dans les autres cohortes de travailleurs du nucléaire (en particulier durant les années 1948 à 1958, en raison notamment d’un manque d’expérience vis-à-vis des opérations réalisées ; Azizova et coll., 2017 ) : la dose moyenne externe cumulée était ainsi de 0,54 Sv pour les hommes et de 0,44 Sv pour les femmes (Azizova et coll., 2018a
) : la dose moyenne externe cumulée était ainsi de 0,54 Sv pour les hommes et de 0,44 Sv pour les femmes (Azizova et coll., 2018a ). Si les contaminations internes par le plutonium constituent également un aspect important de l’exposition dans cette cohorte (ces aspects seront détaillés dans une autre section ci-dessous), de nombreuses analyses portant plus spécifiquement sur les effets de l’exposition externe aux rayonnements ionisants y ont été réalisées.
). Si les contaminations internes par le plutonium constituent également un aspect important de l’exposition dans cette cohorte (ces aspects seront détaillés dans une autre section ci-dessous), de nombreuses analyses portant plus spécifiquement sur les effets de l’exposition externe aux rayonnements ionisants y ont été réalisées.
 ) : la dose moyenne externe cumulée était ainsi de 0,54 Sv pour les hommes et de 0,44 Sv pour les femmes (Azizova et coll., 2018a
) : la dose moyenne externe cumulée était ainsi de 0,54 Sv pour les hommes et de 0,44 Sv pour les femmes (Azizova et coll., 2018a ). Si les contaminations internes par le plutonium constituent également un aspect important de l’exposition dans cette cohorte (ces aspects seront détaillés dans une autre section ci-dessous), de nombreuses analyses portant plus spécifiquement sur les effets de l’exposition externe aux rayonnements ionisants y ont été réalisées.
). Si les contaminations internes par le plutonium constituent également un aspect important de l’exposition dans cette cohorte (ces aspects seront détaillés dans une autre section ci-dessous), de nombreuses analyses portant plus spécifiquement sur les effets de l’exposition externe aux rayonnements ionisants y ont été réalisées.À Mayak, sur la base d’un suivi de population sur la période 1948-2004, l’association entre dose externe reçue à la moelle osseuse et incidence de leucémies (hors leucémie lymphoïde chronique) était statistiquement significative, y compris après ajustement sur les doses internes dues au plutonium (ERR/Gy = 3,57 (IC 90 % [1,55-8,22]) (Kuznetsova et coll., 2016 ). D’autres analyses menées dans cette cohorte sur la période 1948-2008 ont également mis en évidence des associations entre dose externe et mortalité par cancers solides (Sokolnikov et coll., 2015
). D’autres analyses menées dans cette cohorte sur la période 1948-2008 ont également mis en évidence des associations entre dose externe et mortalité par cancers solides (Sokolnikov et coll., 2015 ). Les cancers du poumon, du foie et de l’os ont toutefois été exclus de cette analyse en raison de fortes associations entre ces cancers et les expositions internes au plutonium (voir paragraphe dédié plus loin). Après ajustement sur les expositions au plutonium, l’ERR par Gy (dose externe reçue au côlon) était de 0,12 (IC 95 % [0,03-0,21]) (Sokolnikov et coll., 2015
). Les cancers du poumon, du foie et de l’os ont toutefois été exclus de cette analyse en raison de fortes associations entre ces cancers et les expositions internes au plutonium (voir paragraphe dédié plus loin). Après ajustement sur les expositions au plutonium, l’ERR par Gy (dose externe reçue au côlon) était de 0,12 (IC 95 % [0,03-0,21]) (Sokolnikov et coll., 2015 ). Lorsque cette analyse était restreinte aux travailleurs non exposés au plutonium par voie interne, l’ERR par Gy était de 0,19 (IC 95 % [0,02-0,39]) (Sokolnikov et coll., 2017
). Lorsque cette analyse était restreinte aux travailleurs non exposés au plutonium par voie interne, l’ERR par Gy était de 0,19 (IC 95 % [0,02-0,39]) (Sokolnikov et coll., 2017 ).
).
 ). D’autres analyses menées dans cette cohorte sur la période 1948-2008 ont également mis en évidence des associations entre dose externe et mortalité par cancers solides (Sokolnikov et coll., 2015
). D’autres analyses menées dans cette cohorte sur la période 1948-2008 ont également mis en évidence des associations entre dose externe et mortalité par cancers solides (Sokolnikov et coll., 2015 ). Les cancers du poumon, du foie et de l’os ont toutefois été exclus de cette analyse en raison de fortes associations entre ces cancers et les expositions internes au plutonium (voir paragraphe dédié plus loin). Après ajustement sur les expositions au plutonium, l’ERR par Gy (dose externe reçue au côlon) était de 0,12 (IC 95 % [0,03-0,21]) (Sokolnikov et coll., 2015
). Les cancers du poumon, du foie et de l’os ont toutefois été exclus de cette analyse en raison de fortes associations entre ces cancers et les expositions internes au plutonium (voir paragraphe dédié plus loin). Après ajustement sur les expositions au plutonium, l’ERR par Gy (dose externe reçue au côlon) était de 0,12 (IC 95 % [0,03-0,21]) (Sokolnikov et coll., 2015 ). Lorsque cette analyse était restreinte aux travailleurs non exposés au plutonium par voie interne, l’ERR par Gy était de 0,19 (IC 95 % [0,02-0,39]) (Sokolnikov et coll., 2017
). Lorsque cette analyse était restreinte aux travailleurs non exposés au plutonium par voie interne, l’ERR par Gy était de 0,19 (IC 95 % [0,02-0,39]) (Sokolnikov et coll., 2017 ).
).Une étude d’incidence utilisant le même regroupement de cancers (tous cancers solides sauf poumon, foie et os), basée sur un suivi jusqu’en 2004, a rapporté une association avec les rayonnements externes plus faible (ERR/Gy = 0,07 ; IC 95 % [0,01-0,15]), devenue non significative après ajustement sur les expositions internes au plutonium (Hunter et coll., 2013 ). Une association significative a toutefois été mise en évidence avec le cancer de la lèvre (ERR/Gy = 1,74 ; IC 95 % [0,37-6,71]). Plus récemment, une analyse basée sur un suivi jusqu’à la fin de l’année 2013 a mis en évidence des associations entre l’exposition externe aux rayonnements ionisants et l’incidence de cancers de la peau, à l’exclusion des mélanomes (Azizova et coll., 2018a
). Une association significative a toutefois été mise en évidence avec le cancer de la lèvre (ERR/Gy = 1,74 ; IC 95 % [0,37-6,71]). Plus récemment, une analyse basée sur un suivi jusqu’à la fin de l’année 2013 a mis en évidence des associations entre l’exposition externe aux rayonnements ionisants et l’incidence de cancers de la peau, à l’exclusion des mélanomes (Azizova et coll., 2018a ). L’ERR/Sv correspondant était de 0,51 (IC 95 % [0,22-0,93]).
). L’ERR/Sv correspondant était de 0,51 (IC 95 % [0,22-0,93]).
 ). Une association significative a toutefois été mise en évidence avec le cancer de la lèvre (ERR/Gy = 1,74 ; IC 95 % [0,37-6,71]). Plus récemment, une analyse basée sur un suivi jusqu’à la fin de l’année 2013 a mis en évidence des associations entre l’exposition externe aux rayonnements ionisants et l’incidence de cancers de la peau, à l’exclusion des mélanomes (Azizova et coll., 2018a
). Une association significative a toutefois été mise en évidence avec le cancer de la lèvre (ERR/Gy = 1,74 ; IC 95 % [0,37-6,71]). Plus récemment, une analyse basée sur un suivi jusqu’à la fin de l’année 2013 a mis en évidence des associations entre l’exposition externe aux rayonnements ionisants et l’incidence de cancers de la peau, à l’exclusion des mélanomes (Azizova et coll., 2018a ). L’ERR/Sv correspondant était de 0,51 (IC 95 % [0,22-0,93]).
). L’ERR/Sv correspondant était de 0,51 (IC 95 % [0,22-0,93]).Pour ce qui concerne les pathologies de l’appareil circulatoire chez les travailleurs de Mayak, sur la base d’un suivi jusqu’à la fin de l’année 2008, une association entre dose externe et mortalité par pathologies de l’appareil circulatoire a été observée, y compris après ajustement sur les doses internes au foie dues aux expositions au plutonium (ERR/Gy = 0,10 ; IC 95 % [0,02-0,21]) (Azizova et coll., 2015a ). Des analyses plus détaillées de ces résultats par sous-groupe de pathologies circulatoires font apparaître des résultats complexes. Ainsi, l’association avec la dose externe n’est pas statistiquement significative pour la mortalité par maladies cardiaques ischémiques (ERR/Gy = 0,06 (IC 95 % [< 0-0,15]) (Azizova et coll., 2015b
). Des analyses plus détaillées de ces résultats par sous-groupe de pathologies circulatoires font apparaître des résultats complexes. Ainsi, l’association avec la dose externe n’est pas statistiquement significative pour la mortalité par maladies cardiaques ischémiques (ERR/Gy = 0,06 (IC 95 % [< 0-0,15]) (Azizova et coll., 2015b ) ou par maladies cérébrovasculaires (ERR/Gy = 0,05 (IC 95 % [-0,03-0,16]) (Azizova et coll., 2014
) ou par maladies cérébrovasculaires (ERR/Gy = 0,05 (IC 95 % [-0,03-0,16]) (Azizova et coll., 2014 ). En revanche, des associations statistiquement significatives sont observées entre exposition externe aux radiations et incidence de ces pathologies (maladies cardiaques ischémiques ERR/Gy = 0,10 (IC 95 % [0,04-0,17]) (Azizova et coll., 2015b
). En revanche, des associations statistiquement significatives sont observées entre exposition externe aux radiations et incidence de ces pathologies (maladies cardiaques ischémiques ERR/Gy = 0,10 (IC 95 % [0,04-0,17]) (Azizova et coll., 2015b ) et maladies cérébrovasculaires ERR/Gy = 0,49 (IC 95 % [0,39-0,60]) (Azizova et coll., 2014
) et maladies cérébrovasculaires ERR/Gy = 0,49 (IC 95 % [0,39-0,60]) (Azizova et coll., 2014 ). Récemment, une analyse portant sur l’incidence de maladies artérielles périphériques des membres inférieurs a mis en évidence une association avec l’exposition externe aux rayonnements ionisants (Azizova et coll., 2016
). Récemment, une analyse portant sur l’incidence de maladies artérielles périphériques des membres inférieurs a mis en évidence une association avec l’exposition externe aux rayonnements ionisants (Azizova et coll., 2016 ) après ajustement sur les doses dues aux contaminations internes par le plutonium (ERR/Gy = 0,19 (IC 95 % [0,05-0,39]).
) après ajustement sur les doses dues aux contaminations internes par le plutonium (ERR/Gy = 0,19 (IC 95 % [0,05-0,39]).
 ). Des analyses plus détaillées de ces résultats par sous-groupe de pathologies circulatoires font apparaître des résultats complexes. Ainsi, l’association avec la dose externe n’est pas statistiquement significative pour la mortalité par maladies cardiaques ischémiques (ERR/Gy = 0,06 (IC 95 % [< 0-0,15]) (Azizova et coll., 2015b
). Des analyses plus détaillées de ces résultats par sous-groupe de pathologies circulatoires font apparaître des résultats complexes. Ainsi, l’association avec la dose externe n’est pas statistiquement significative pour la mortalité par maladies cardiaques ischémiques (ERR/Gy = 0,06 (IC 95 % [< 0-0,15]) (Azizova et coll., 2015b ) ou par maladies cérébrovasculaires (ERR/Gy = 0,05 (IC 95 % [-0,03-0,16]) (Azizova et coll., 2014
) ou par maladies cérébrovasculaires (ERR/Gy = 0,05 (IC 95 % [-0,03-0,16]) (Azizova et coll., 2014 ). En revanche, des associations statistiquement significatives sont observées entre exposition externe aux radiations et incidence de ces pathologies (maladies cardiaques ischémiques ERR/Gy = 0,10 (IC 95 % [0,04-0,17]) (Azizova et coll., 2015b
). En revanche, des associations statistiquement significatives sont observées entre exposition externe aux radiations et incidence de ces pathologies (maladies cardiaques ischémiques ERR/Gy = 0,10 (IC 95 % [0,04-0,17]) (Azizova et coll., 2015b ) et maladies cérébrovasculaires ERR/Gy = 0,49 (IC 95 % [0,39-0,60]) (Azizova et coll., 2014
) et maladies cérébrovasculaires ERR/Gy = 0,49 (IC 95 % [0,39-0,60]) (Azizova et coll., 2014 ). Récemment, une analyse portant sur l’incidence de maladies artérielles périphériques des membres inférieurs a mis en évidence une association avec l’exposition externe aux rayonnements ionisants (Azizova et coll., 2016
). Récemment, une analyse portant sur l’incidence de maladies artérielles périphériques des membres inférieurs a mis en évidence une association avec l’exposition externe aux rayonnements ionisants (Azizova et coll., 2016 ) après ajustement sur les doses dues aux contaminations internes par le plutonium (ERR/Gy = 0,19 (IC 95 % [0,05-0,39]).
) après ajustement sur les doses dues aux contaminations internes par le plutonium (ERR/Gy = 0,19 (IC 95 % [0,05-0,39]).Dans le cadre d’une analyse conjointe des cohortes de travailleurs de Mayak et de Sellafield (site situé au Royaume-Uni et également inclus dans l’étude INWORKS), l’analyse de la relation entre la dose externe et la mortalité par maladies de l’appareil circulatoire a mis en évidence une forte hétérogénéité des associations observées dans les deux cohortes, l’association observée à Sellafield étant plus forte que celle observée à Mayak. Cette hétérogénéité, dont les raisons demeurent difficiles à identifier, était toutefois moins marquée lorsque l’analyse a été restreinte aux périodes les plus récentes (Azizova et coll., 2018b ).
).
 ).
).Récemment, une étude réalisée chez les travailleurs de Mayak a mis en évidence des associations entre exposition chronique externe aux rayonnements ionisants et des augmentations de risques de cataractes sous-capsulaires postérieures (ERR/Sv = 0,91 (IC 95 % [0,67-1,20]), corticales (ERR/Sv = 0,63 (IC 95 % [0,49-0,76]) et nucléaires (ERR/Sv = 0,47 (IC 95 % [0,35-0,60]) (Azizova et coll., 2018c ). Une autre étude réalisée à Mayak a également mis en évidence une association entre dose externe reçue au poumon et incidence de bronchites chroniques (après ajustement notamment sur le tabagisme et sur les expositions internes au plutonium) ERR/Gy = 0,14 (IC 95 % [0,02-0,28]). Cependant, à ce jour, ce résultat apparaît isolé dans la littérature (Azizova et coll., 2017
). Une autre étude réalisée à Mayak a également mis en évidence une association entre dose externe reçue au poumon et incidence de bronchites chroniques (après ajustement notamment sur le tabagisme et sur les expositions internes au plutonium) ERR/Gy = 0,14 (IC 95 % [0,02-0,28]). Cependant, à ce jour, ce résultat apparaît isolé dans la littérature (Azizova et coll., 2017 ).
).
 ). Une autre étude réalisée à Mayak a également mis en évidence une association entre dose externe reçue au poumon et incidence de bronchites chroniques (après ajustement notamment sur le tabagisme et sur les expositions internes au plutonium) ERR/Gy = 0,14 (IC 95 % [0,02-0,28]). Cependant, à ce jour, ce résultat apparaît isolé dans la littérature (Azizova et coll., 2017
). Une autre étude réalisée à Mayak a également mis en évidence une association entre dose externe reçue au poumon et incidence de bronchites chroniques (après ajustement notamment sur le tabagisme et sur les expositions internes au plutonium) ERR/Gy = 0,14 (IC 95 % [0,02-0,28]). Cependant, à ce jour, ce résultat apparaît isolé dans la littérature (Azizova et coll., 2017 ).
).En résumé, la cohorte des travailleurs de Mayak apporte également une grande richesse d’information sur les effets d’expositions externes aux rayonnements, notamment grâce au suivi de l’incidence de nombreuses pathologies. Cependant, les niveaux de doses externes rencontrés dans cette cohorte pouvant être très élevés (en moyenne 20 fois plus élevés que ceux rencontrés dans INWORKS), d’importantes incertitudes existent quant à la transposabilité des résultats issus de cette cohorte (ex. : valeurs des ERR/Gy ou ERR/Sv) à des populations exposées à des niveaux de doses faibles.
Études sur les risques de cancer chez les descendants de travailleurs
du nucléaire
Plusieurs études ont porté sur l’incidence de cancers chez les enfants de travailleurs du nucléaire, notamment en lien avec les expositions professionnelles des pères aux rayonnements ionisants préalablement à la conception. En 1990, une étude cas-témoins menée chez des enfants et jeunes adultes âgés de 0 à 25 ans dans l’ouest du comté de Cumbria (Royaume-Uni), où se situe le site de Sellafield, a rapporté des associations entre risques de leucémies (n = 52) ou regroupement de leucémies et lymphomes non hodgkiniens (LNH, n = 22) et doses de rayonnements externes reçues par les pères préalablement à la conception dans le cadre de leur activité professionnelle (Gardner et coll., 1990a et b
et b , 1992
, 1992 ). L’interprétation de ces résultats a fait l’objet de controverses scientifiques, sur la base d’arguments biologiques, mais aussi en raison d’un manque de cohérence de ces résultats avec ceux d’autres études épidémiologiques (Kinlen, 1993
). L’interprétation de ces résultats a fait l’objet de controverses scientifiques, sur la base d’arguments biologiques, mais aussi en raison d’un manque de cohérence de ces résultats avec ceux d’autres études épidémiologiques (Kinlen, 1993 ; Doll et coll., 1994
; Doll et coll., 1994 ; Little et coll., 1994
; Little et coll., 1994 ). Ainsi dans l’Ontario (Canada), une autre étude cas-témoins n’a pas mis en évidence d’association entre leucémies chez des enfants et jeunes adultes âgés de 0 à 25 ans (n = 112 cas) et expositions professionnelles des pères avant la conception (McLaughlin et coll., 1993
). Ainsi dans l’Ontario (Canada), une autre étude cas-témoins n’a pas mis en évidence d’association entre leucémies chez des enfants et jeunes adultes âgés de 0 à 25 ans (n = 112 cas) et expositions professionnelles des pères avant la conception (McLaughlin et coll., 1993 ). De même en Ecosse, une autre étude cas-témoins incluant 1 024 cas de leucémies et 237 cas de LNH chez des enfants et jeunes adultes âgés de 0 à 25 ans n’a pas rapporté d’association (Kinlen et coll., 1993
). De même en Ecosse, une autre étude cas-témoins incluant 1 024 cas de leucémies et 237 cas de LNH chez des enfants et jeunes adultes âgés de 0 à 25 ans n’a pas rapporté d’association (Kinlen et coll., 1993 ). Le manque de cohérence des résultats de ces études entre elles, mais aussi avec les résultats de l’étude des survivants d’Hiroshima et Nagasaki, a conduit certains auteurs (Doll et coll., 1994
). Le manque de cohérence des résultats de ces études entre elles, mais aussi avec les résultats de l’étude des survivants d’Hiroshima et Nagasaki, a conduit certains auteurs (Doll et coll., 1994 ; Little et coll., 1994
; Little et coll., 1994 ) à écarter un jugement de causalité concernant les associations observées avec l’exposition professionnelle des pères dans l’ouest du comté de Cumbria (Gardner et coll., 1990a
) à écarter un jugement de causalité concernant les associations observées avec l’exposition professionnelle des pères dans l’ouest du comté de Cumbria (Gardner et coll., 1990a et b
et b , 1992
, 1992 ). Par la suite, dans une étude de cohorte incluant 266 710 enfants et jeunes adultes nés à Cumbria et suivis jusqu’à l’âge de 25 ans entre 1950 à 1991, aucune association n’a été observée entre risques de cancers solides (n = 18 cas) et exposition professionnelle des pères aux rayonnements externes (Dickinson et coll., 2002
). Par la suite, dans une étude de cohorte incluant 266 710 enfants et jeunes adultes nés à Cumbria et suivis jusqu’à l’âge de 25 ans entre 1950 à 1991, aucune association n’a été observée entre risques de cancers solides (n = 18 cas) et exposition professionnelle des pères aux rayonnements externes (Dickinson et coll., 2002 ).
).
 et b
et b , 1992
, 1992 ). L’interprétation de ces résultats a fait l’objet de controverses scientifiques, sur la base d’arguments biologiques, mais aussi en raison d’un manque de cohérence de ces résultats avec ceux d’autres études épidémiologiques (Kinlen, 1993
). L’interprétation de ces résultats a fait l’objet de controverses scientifiques, sur la base d’arguments biologiques, mais aussi en raison d’un manque de cohérence de ces résultats avec ceux d’autres études épidémiologiques (Kinlen, 1993 ; Doll et coll., 1994
; Doll et coll., 1994 ; Little et coll., 1994
; Little et coll., 1994 ). Ainsi dans l’Ontario (Canada), une autre étude cas-témoins n’a pas mis en évidence d’association entre leucémies chez des enfants et jeunes adultes âgés de 0 à 25 ans (n = 112 cas) et expositions professionnelles des pères avant la conception (McLaughlin et coll., 1993
). Ainsi dans l’Ontario (Canada), une autre étude cas-témoins n’a pas mis en évidence d’association entre leucémies chez des enfants et jeunes adultes âgés de 0 à 25 ans (n = 112 cas) et expositions professionnelles des pères avant la conception (McLaughlin et coll., 1993 ). De même en Ecosse, une autre étude cas-témoins incluant 1 024 cas de leucémies et 237 cas de LNH chez des enfants et jeunes adultes âgés de 0 à 25 ans n’a pas rapporté d’association (Kinlen et coll., 1993
). De même en Ecosse, une autre étude cas-témoins incluant 1 024 cas de leucémies et 237 cas de LNH chez des enfants et jeunes adultes âgés de 0 à 25 ans n’a pas rapporté d’association (Kinlen et coll., 1993 ). Le manque de cohérence des résultats de ces études entre elles, mais aussi avec les résultats de l’étude des survivants d’Hiroshima et Nagasaki, a conduit certains auteurs (Doll et coll., 1994
). Le manque de cohérence des résultats de ces études entre elles, mais aussi avec les résultats de l’étude des survivants d’Hiroshima et Nagasaki, a conduit certains auteurs (Doll et coll., 1994 ; Little et coll., 1994
; Little et coll., 1994 ) à écarter un jugement de causalité concernant les associations observées avec l’exposition professionnelle des pères dans l’ouest du comté de Cumbria (Gardner et coll., 1990a
) à écarter un jugement de causalité concernant les associations observées avec l’exposition professionnelle des pères dans l’ouest du comté de Cumbria (Gardner et coll., 1990a et b
et b , 1992
, 1992 ). Par la suite, dans une étude de cohorte incluant 266 710 enfants et jeunes adultes nés à Cumbria et suivis jusqu’à l’âge de 25 ans entre 1950 à 1991, aucune association n’a été observée entre risques de cancers solides (n = 18 cas) et exposition professionnelle des pères aux rayonnements externes (Dickinson et coll., 2002
). Par la suite, dans une étude de cohorte incluant 266 710 enfants et jeunes adultes nés à Cumbria et suivis jusqu’à l’âge de 25 ans entre 1950 à 1991, aucune association n’a été observée entre risques de cancers solides (n = 18 cas) et exposition professionnelle des pères aux rayonnements externes (Dickinson et coll., 2002 ).
).En 1999, une enquête portant sur 39 557 enfants et jeunes adultes (âgés de 0 à 25 ans) dont les pères ont été employés dans trois entreprises de l’industrie nucléaire britannique (Atomic Energy Authority, Atomic Weapons Establishment et British Nuclear Fuels) a montré que les taux de tous cancers (n = 111 cas, identifiés par déclarations des parents) et de leucémies (n = 28 cas) chez ces enfants étaient similaires à ceux observés dans la population générale de même âge. Un risque plus élevé de leucémies a été estimé chez les enfants de pères exposés à plus de 100 mSv avant la conception (RR = 5,8 (IC 95 % [1,3-24,8]). Cette estimation était basée sur 3 cas observés chez les enfants de pères exposés à des niveaux de dose supérieurs à 100 mSv. Des augmentations de risques de cancers ont également été observées chez les enfants de pères ayant reçu des doses supérieures à 10 mSv durant les 6 mois précédant la conception (RR = 2,5 (IC 95 % [1-5,5]), estimation basée sur 5 cas). Cette association était principalement influencée par une association avec les leucémies (RR = 7,7 (IC 95 % [1,9-31]), estimation basée sur 3 cas) mais non significative pour les cancers hors leucémies et lymphomes. Cependant, lorsque l’ensemble de la gamme de doses reçues par les pères (que ce soit durant les 6 mois ou durant toute la période professionnelle précédant la conception) a été considérée, aucune tendance significative n’a été mise en évidence (Roman et coll., 1999 ).
).
 ).
).En 2003, une analyse basée sur l’étude United Kingdom Childhood Cancer Study (3 838 cas de cancers de l’enfant et 7 629 témoins, âgés de 0 à 14 ans), considérant tous types d’expositions professionnelles, n’a mis en évidence aucune association entre cancers chez les enfants (quel qu’en soit le type) et statut d’exposition professionnelle des pères aux rayonnements ionisants durant l’année précédant la naissance (McKinney et coll., 2003 ).
).
 ).
).Une étude basée sur un croisement entre le registre britannique NRRW (mentionné plus haut) et le Registre national des cancers de l’enfant (n = 35 949 cas, diagnostiqués entre 0 et 15 ans), a en revanche montré que sur la période 1950-1985, les pères d’enfants atteints de leucémies ou de LNH (mais pas d’autres cancers) étaient plus fréquemment surveillés pour exposition professionnelle aux rayonnements ionisants que les pères des témoins (RR = 1,77 (IC 95 % [1,05-3,03]). Cependant, aucune association entre le risque et la dose reçue par les pères préalablement à la conception n’a été observée (Draper et coll., 1997 ; Sorahan et coll., 2003
; Sorahan et coll., 2003 ).
).
 ; Sorahan et coll., 2003
; Sorahan et coll., 2003 ).
).Pour ce qui concerne l’exposition des mères, dans la première étude basée sur le NRRW sur la période 1950-1985 (Draper et coll., 1997 ), le statut de surveillance pour exposition aux radiations de celles-ci était significativement associé au risque de cancer de l’enfant (RR = 5 (IC 95 % [1,42-26,94]) ; l’estimation était basée sur 15 cas et 3 témoins). Cependant, aucune association significative n’a été observée avec la dose reçue ni avant ni pendant la grossesse (Draper et coll., 1997
), le statut de surveillance pour exposition aux radiations de celles-ci était significativement associé au risque de cancer de l’enfant (RR = 5 (IC 95 % [1,42-26,94]) ; l’estimation était basée sur 15 cas et 3 témoins). Cependant, aucune association significative n’a été observée avec la dose reçue ni avant ni pendant la grossesse (Draper et coll., 1997 ). La réplication de cette étude sur la période 1987-1999 (inclusion de 16 964 nouveaux cas et autant de nouveaux témoins) n’a pas permis de mettre en évidence d’association sur cette période plus récente (Bunch et coll., 2009
). La réplication de cette étude sur la période 1987-1999 (inclusion de 16 964 nouveaux cas et autant de nouveaux témoins) n’a pas permis de mettre en évidence d’association sur cette période plus récente (Bunch et coll., 2009 ). Sur la période totale 1950-1999, une association positive mais non statistiquement significative a été observée entre le risque de cancer et le statut de surveillance pour exposition aux radiations des mères durant la grossesse, et aucune association significative n’a été observée avec la dose reçue, que ce soit avant la conception ou in utero. Cependant, les effectifs étaient probablement trop limités pour pouvoir mettre en évidence une possible association (Bunch et coll., 2009
). Sur la période totale 1950-1999, une association positive mais non statistiquement significative a été observée entre le risque de cancer et le statut de surveillance pour exposition aux radiations des mères durant la grossesse, et aucune association significative n’a été observée avec la dose reçue, que ce soit avant la conception ou in utero. Cependant, les effectifs étaient probablement trop limités pour pouvoir mettre en évidence une possible association (Bunch et coll., 2009 ).
).
 ), le statut de surveillance pour exposition aux radiations de celles-ci était significativement associé au risque de cancer de l’enfant (RR = 5 (IC 95 % [1,42-26,94]) ; l’estimation était basée sur 15 cas et 3 témoins). Cependant, aucune association significative n’a été observée avec la dose reçue ni avant ni pendant la grossesse (Draper et coll., 1997
), le statut de surveillance pour exposition aux radiations de celles-ci était significativement associé au risque de cancer de l’enfant (RR = 5 (IC 95 % [1,42-26,94]) ; l’estimation était basée sur 15 cas et 3 témoins). Cependant, aucune association significative n’a été observée avec la dose reçue ni avant ni pendant la grossesse (Draper et coll., 1997 ). La réplication de cette étude sur la période 1987-1999 (inclusion de 16 964 nouveaux cas et autant de nouveaux témoins) n’a pas permis de mettre en évidence d’association sur cette période plus récente (Bunch et coll., 2009
). La réplication de cette étude sur la période 1987-1999 (inclusion de 16 964 nouveaux cas et autant de nouveaux témoins) n’a pas permis de mettre en évidence d’association sur cette période plus récente (Bunch et coll., 2009 ). Sur la période totale 1950-1999, une association positive mais non statistiquement significative a été observée entre le risque de cancer et le statut de surveillance pour exposition aux radiations des mères durant la grossesse, et aucune association significative n’a été observée avec la dose reçue, que ce soit avant la conception ou in utero. Cependant, les effectifs étaient probablement trop limités pour pouvoir mettre en évidence une possible association (Bunch et coll., 2009
). Sur la période totale 1950-1999, une association positive mais non statistiquement significative a été observée entre le risque de cancer et le statut de surveillance pour exposition aux radiations des mères durant la grossesse, et aucune association significative n’a été observée avec la dose reçue, que ce soit avant la conception ou in utero. Cependant, les effectifs étaient probablement trop limités pour pouvoir mettre en évidence une possible association (Bunch et coll., 2009 ).
).L’analyse basée sur l’étude United Kingdom Childhood Cancer Study n’a pas montré d’association entre cancer de l’enfant et statut d’exposition professionnelle des mères aux rayonnements ionisants, même si là encore les effectifs demeuraient très limités (McKinney et coll., 2003 ).
).
 ).
).Deux études chez les enfants des travailleuses de Mayak ont porté respectivement sur la mortalité par cancer (Schonfeld et coll., 2012 ) et l’incidence de cancers (Tsareva et coll., 2016
) et l’incidence de cancers (Tsareva et coll., 2016 ) et n’ont pas mis en en évidence d’associations avec la dose externe cumulée reçue in utero. Une étude récente portant conjointement sur 19 536 enfants de travailleuses de Mayak et de résidentes riveraines de la rivière Techa (en aval du site de Mayak) a rapporté une augmentation de l’incidence de cancers hématologiques (n = 58 cas incidents) pour des expositions in utero (ERR pour 100 mGy = 0,77 (IC 95 % [0,02-2,56]). Aucune association n’a cependant été observée pour la mortalité (Schuz et coll., 2017
) et n’ont pas mis en en évidence d’associations avec la dose externe cumulée reçue in utero. Une étude récente portant conjointement sur 19 536 enfants de travailleuses de Mayak et de résidentes riveraines de la rivière Techa (en aval du site de Mayak) a rapporté une augmentation de l’incidence de cancers hématologiques (n = 58 cas incidents) pour des expositions in utero (ERR pour 100 mGy = 0,77 (IC 95 % [0,02-2,56]). Aucune association n’a cependant été observée pour la mortalité (Schuz et coll., 2017 ). Aucune association entre exposition in utero et cancers solides n’a été observée à ce jour dans cette cohorte (Akleyev et coll., 2016
). Aucune association entre exposition in utero et cancers solides n’a été observée à ce jour dans cette cohorte (Akleyev et coll., 2016 ). Il est à noter que si la contribution des expositions internes à la dose in utero dans la cohorte des travailleuses de Mayak est estimée comme étant très minoritaire par rapport celle des expositions externes (Tsareva et coll., 2016
). Il est à noter que si la contribution des expositions internes à la dose in utero dans la cohorte des travailleuses de Mayak est estimée comme étant très minoritaire par rapport celle des expositions externes (Tsareva et coll., 2016 ), ce n’est pas nécessairement le cas pour la population générale concernant les riveraines de la rivière Techa (Krestinina et coll., 2017
), ce n’est pas nécessairement le cas pour la population générale concernant les riveraines de la rivière Techa (Krestinina et coll., 2017 ). Par ailleurs, cette étude ayant considéré une population mixée (travailleurs et population générale), elle ne porte qu’en partie sur les effets d’expositions professionnelles (Akleyev et coll., 2016
). Par ailleurs, cette étude ayant considéré une population mixée (travailleurs et population générale), elle ne porte qu’en partie sur les effets d’expositions professionnelles (Akleyev et coll., 2016 ; Schuz et coll., 2017
; Schuz et coll., 2017 ).
).
 ) et l’incidence de cancers (Tsareva et coll., 2016
) et l’incidence de cancers (Tsareva et coll., 2016 ) et n’ont pas mis en en évidence d’associations avec la dose externe cumulée reçue in utero. Une étude récente portant conjointement sur 19 536 enfants de travailleuses de Mayak et de résidentes riveraines de la rivière Techa (en aval du site de Mayak) a rapporté une augmentation de l’incidence de cancers hématologiques (n = 58 cas incidents) pour des expositions in utero (ERR pour 100 mGy = 0,77 (IC 95 % [0,02-2,56]). Aucune association n’a cependant été observée pour la mortalité (Schuz et coll., 2017
) et n’ont pas mis en en évidence d’associations avec la dose externe cumulée reçue in utero. Une étude récente portant conjointement sur 19 536 enfants de travailleuses de Mayak et de résidentes riveraines de la rivière Techa (en aval du site de Mayak) a rapporté une augmentation de l’incidence de cancers hématologiques (n = 58 cas incidents) pour des expositions in utero (ERR pour 100 mGy = 0,77 (IC 95 % [0,02-2,56]). Aucune association n’a cependant été observée pour la mortalité (Schuz et coll., 2017 ). Aucune association entre exposition in utero et cancers solides n’a été observée à ce jour dans cette cohorte (Akleyev et coll., 2016
). Aucune association entre exposition in utero et cancers solides n’a été observée à ce jour dans cette cohorte (Akleyev et coll., 2016 ). Il est à noter que si la contribution des expositions internes à la dose in utero dans la cohorte des travailleuses de Mayak est estimée comme étant très minoritaire par rapport celle des expositions externes (Tsareva et coll., 2016
). Il est à noter que si la contribution des expositions internes à la dose in utero dans la cohorte des travailleuses de Mayak est estimée comme étant très minoritaire par rapport celle des expositions externes (Tsareva et coll., 2016 ), ce n’est pas nécessairement le cas pour la population générale concernant les riveraines de la rivière Techa (Krestinina et coll., 2017
), ce n’est pas nécessairement le cas pour la population générale concernant les riveraines de la rivière Techa (Krestinina et coll., 2017 ). Par ailleurs, cette étude ayant considéré une population mixée (travailleurs et population générale), elle ne porte qu’en partie sur les effets d’expositions professionnelles (Akleyev et coll., 2016
). Par ailleurs, cette étude ayant considéré une population mixée (travailleurs et population générale), elle ne porte qu’en partie sur les effets d’expositions professionnelles (Akleyev et coll., 2016 ; Schuz et coll., 2017
; Schuz et coll., 2017 ).
).Effets des expositions aux rayonnements ionisants
par contaminations internes
Les études épidémiologiques chez les travailleurs du nucléaire permettent également de documenter les effets d’expositions internes par différents radionucléides. Parmi ceux pouvant être émis lors d’essais nucléaires (Renaud, 2008 ) et pouvant également être rencontrés dans des situations d’exposition impliquant des travailleurs de l’industrie nucléaire, figurent le plutonium et le tritium. Si d’autres radioéléments pouvant se retrouver dans l’environnement suite à des essais nucléaires ont pu entraîner des expositions professionnelles dans certains contextes (ex. : strontium, césium, iode) (UNSCEAR, 2000
) et pouvant également être rencontrés dans des situations d’exposition impliquant des travailleurs de l’industrie nucléaire, figurent le plutonium et le tritium. Si d’autres radioéléments pouvant se retrouver dans l’environnement suite à des essais nucléaires ont pu entraîner des expositions professionnelles dans certains contextes (ex. : strontium, césium, iode) (UNSCEAR, 2000 ), la quantification des doses associées dans les études épidémiologiques en milieu professionnel est relativement rare (Boice et coll., 2011
), la quantification des doses associées dans les études épidémiologiques en milieu professionnel est relativement rare (Boice et coll., 2011 ). Pour ces radionucléides, des études réalisées en population générale seront plus informatives. Des reconstitutions de doses internes dues à ces radionucléides ont en effet été effectuées pour de larges populations exposées suite notamment à des accidents (Cardis et coll., 2005
). Pour ces radionucléides, des études réalisées en population générale seront plus informatives. Des reconstitutions de doses internes dues à ces radionucléides ont en effet été effectuées pour de larges populations exposées suite notamment à des accidents (Cardis et coll., 2005 ; Davis et coll., 2015
; Davis et coll., 2015 ).
).
 ) et pouvant également être rencontrés dans des situations d’exposition impliquant des travailleurs de l’industrie nucléaire, figurent le plutonium et le tritium. Si d’autres radioéléments pouvant se retrouver dans l’environnement suite à des essais nucléaires ont pu entraîner des expositions professionnelles dans certains contextes (ex. : strontium, césium, iode) (UNSCEAR, 2000
) et pouvant également être rencontrés dans des situations d’exposition impliquant des travailleurs de l’industrie nucléaire, figurent le plutonium et le tritium. Si d’autres radioéléments pouvant se retrouver dans l’environnement suite à des essais nucléaires ont pu entraîner des expositions professionnelles dans certains contextes (ex. : strontium, césium, iode) (UNSCEAR, 2000 ), la quantification des doses associées dans les études épidémiologiques en milieu professionnel est relativement rare (Boice et coll., 2011
), la quantification des doses associées dans les études épidémiologiques en milieu professionnel est relativement rare (Boice et coll., 2011 ). Pour ces radionucléides, des études réalisées en population générale seront plus informatives. Des reconstitutions de doses internes dues à ces radionucléides ont en effet été effectuées pour de larges populations exposées suite notamment à des accidents (Cardis et coll., 2005
). Pour ces radionucléides, des études réalisées en population générale seront plus informatives. Des reconstitutions de doses internes dues à ces radionucléides ont en effet été effectuées pour de larges populations exposées suite notamment à des accidents (Cardis et coll., 2005 ; Davis et coll., 2015
; Davis et coll., 2015 ).
).Plutonium
Les deux principales études de travailleurs de l’industrie nucléaire fournissant des éléments sur les effets sanitaires d’exposition au plutonium sont celles de Mayak et de Sellafield (Gilbert et coll., 2013 ; Gillies et coll., 2017a
; Gillies et coll., 2017a ). La cohorte des travailleurs de Mayak couvre une très large gamme de niveaux d’expositions au plutonium (doses internes cumulées jusqu’à plusieurs Grays). En particulier, des doses plus élevées que celles observées dans le cadre d’opérations de même nature (à savoir, la production de plutonium) réalisées dans d’autres pays ont été reçues à Mayak. Au sein de cette cohorte, une association a été montrée entre les doses internes au poumon dues à l’inhalation de plutonium et le risque de cancer du poumon (pour les hommes à un âge moyen de 60 ans, l’ERR par Gy est de 7,4 (IC 95 % [5-11]) alors que pour les femmes il est de 24 (IC 95 % [11-56]), après ajustement sur le statut tabagique et l’exposition externe aux rayonnements ionisants. Ces estimations sont basées sur 486 cas de cancer du poumon observés dans cette population. Les résultats demeurent similaires lorsque les analyses sont restreintes à des doses dues au plutonium inférieures à 0,2 Gy (Gilbert et coll., 2013
). La cohorte des travailleurs de Mayak couvre une très large gamme de niveaux d’expositions au plutonium (doses internes cumulées jusqu’à plusieurs Grays). En particulier, des doses plus élevées que celles observées dans le cadre d’opérations de même nature (à savoir, la production de plutonium) réalisées dans d’autres pays ont été reçues à Mayak. Au sein de cette cohorte, une association a été montrée entre les doses internes au poumon dues à l’inhalation de plutonium et le risque de cancer du poumon (pour les hommes à un âge moyen de 60 ans, l’ERR par Gy est de 7,4 (IC 95 % [5-11]) alors que pour les femmes il est de 24 (IC 95 % [11-56]), après ajustement sur le statut tabagique et l’exposition externe aux rayonnements ionisants. Ces estimations sont basées sur 486 cas de cancer du poumon observés dans cette population. Les résultats demeurent similaires lorsque les analyses sont restreintes à des doses dues au plutonium inférieures à 0,2 Gy (Gilbert et coll., 2013 ). Des associations ont également été observées entre l’exposition interne au plutonium et la mortalité par cancer du foie, sur la base de 40 cas observés (ERR/Gy au foie de 2,6 (IC 95 % [0,6-6,9]) pour les hommes et de 29 (IC 95 % [9,8-95]) pour les femmes) et de l’os (ERR/Gy de 0,76 (IC 95 % [< 0-5,2]) pour les hommes et de 3,4 (IC 95 % [0,4-20]) pour les femmes (Sokolnikov et coll., 2008
). Des associations ont également été observées entre l’exposition interne au plutonium et la mortalité par cancer du foie, sur la base de 40 cas observés (ERR/Gy au foie de 2,6 (IC 95 % [0,6-6,9]) pour les hommes et de 29 (IC 95 % [9,8-95]) pour les femmes) et de l’os (ERR/Gy de 0,76 (IC 95 % [< 0-5,2]) pour les hommes et de 3,4 (IC 95 % [0,4-20]) pour les femmes (Sokolnikov et coll., 2008 ). Cependant, ces associations ne sont à ce jour observées que pour des doses très élevées (> 3 Gy pour les cancers du foie, > 10 Gy pour les cancers de l’os). Pour la mortalité par les autres cancers, aucune preuve d’association avec l’exposition au plutonium n’a pu être mise en évidence (Sokolnikov et coll., 2015
). Cependant, ces associations ne sont à ce jour observées que pour des doses très élevées (> 3 Gy pour les cancers du foie, > 10 Gy pour les cancers de l’os). Pour la mortalité par les autres cancers, aucune preuve d’association avec l’exposition au plutonium n’a pu être mise en évidence (Sokolnikov et coll., 2015 ). Une étude portant sur l’incidence de cancers a en revanche rapporté une association significative entre cancer du pancréas et exposition au plutonium (ERR/Gy = 1,58 (IC 95 % [0,17-4,77]) (Hunter et coll., 2013
). Une étude portant sur l’incidence de cancers a en revanche rapporté une association significative entre cancer du pancréas et exposition au plutonium (ERR/Gy = 1,58 (IC 95 % [0,17-4,77]) (Hunter et coll., 2013 ).
).
 ; Gillies et coll., 2017a
; Gillies et coll., 2017a ). La cohorte des travailleurs de Mayak couvre une très large gamme de niveaux d’expositions au plutonium (doses internes cumulées jusqu’à plusieurs Grays). En particulier, des doses plus élevées que celles observées dans le cadre d’opérations de même nature (à savoir, la production de plutonium) réalisées dans d’autres pays ont été reçues à Mayak. Au sein de cette cohorte, une association a été montrée entre les doses internes au poumon dues à l’inhalation de plutonium et le risque de cancer du poumon (pour les hommes à un âge moyen de 60 ans, l’ERR par Gy est de 7,4 (IC 95 % [5-11]) alors que pour les femmes il est de 24 (IC 95 % [11-56]), après ajustement sur le statut tabagique et l’exposition externe aux rayonnements ionisants. Ces estimations sont basées sur 486 cas de cancer du poumon observés dans cette population. Les résultats demeurent similaires lorsque les analyses sont restreintes à des doses dues au plutonium inférieures à 0,2 Gy (Gilbert et coll., 2013
). La cohorte des travailleurs de Mayak couvre une très large gamme de niveaux d’expositions au plutonium (doses internes cumulées jusqu’à plusieurs Grays). En particulier, des doses plus élevées que celles observées dans le cadre d’opérations de même nature (à savoir, la production de plutonium) réalisées dans d’autres pays ont été reçues à Mayak. Au sein de cette cohorte, une association a été montrée entre les doses internes au poumon dues à l’inhalation de plutonium et le risque de cancer du poumon (pour les hommes à un âge moyen de 60 ans, l’ERR par Gy est de 7,4 (IC 95 % [5-11]) alors que pour les femmes il est de 24 (IC 95 % [11-56]), après ajustement sur le statut tabagique et l’exposition externe aux rayonnements ionisants. Ces estimations sont basées sur 486 cas de cancer du poumon observés dans cette population. Les résultats demeurent similaires lorsque les analyses sont restreintes à des doses dues au plutonium inférieures à 0,2 Gy (Gilbert et coll., 2013 ). Des associations ont également été observées entre l’exposition interne au plutonium et la mortalité par cancer du foie, sur la base de 40 cas observés (ERR/Gy au foie de 2,6 (IC 95 % [0,6-6,9]) pour les hommes et de 29 (IC 95 % [9,8-95]) pour les femmes) et de l’os (ERR/Gy de 0,76 (IC 95 % [< 0-5,2]) pour les hommes et de 3,4 (IC 95 % [0,4-20]) pour les femmes (Sokolnikov et coll., 2008
). Des associations ont également été observées entre l’exposition interne au plutonium et la mortalité par cancer du foie, sur la base de 40 cas observés (ERR/Gy au foie de 2,6 (IC 95 % [0,6-6,9]) pour les hommes et de 29 (IC 95 % [9,8-95]) pour les femmes) et de l’os (ERR/Gy de 0,76 (IC 95 % [< 0-5,2]) pour les hommes et de 3,4 (IC 95 % [0,4-20]) pour les femmes (Sokolnikov et coll., 2008 ). Cependant, ces associations ne sont à ce jour observées que pour des doses très élevées (> 3 Gy pour les cancers du foie, > 10 Gy pour les cancers de l’os). Pour la mortalité par les autres cancers, aucune preuve d’association avec l’exposition au plutonium n’a pu être mise en évidence (Sokolnikov et coll., 2015
). Cependant, ces associations ne sont à ce jour observées que pour des doses très élevées (> 3 Gy pour les cancers du foie, > 10 Gy pour les cancers de l’os). Pour la mortalité par les autres cancers, aucune preuve d’association avec l’exposition au plutonium n’a pu être mise en évidence (Sokolnikov et coll., 2015 ). Une étude portant sur l’incidence de cancers a en revanche rapporté une association significative entre cancer du pancréas et exposition au plutonium (ERR/Gy = 1,58 (IC 95 % [0,17-4,77]) (Hunter et coll., 2013
). Une étude portant sur l’incidence de cancers a en revanche rapporté une association significative entre cancer du pancréas et exposition au plutonium (ERR/Gy = 1,58 (IC 95 % [0,17-4,77]) (Hunter et coll., 2013 ).
).Les doses cumulées rencontrées chez les travailleurs de Mayak pouvant être particulièrement élevées, d’autres études au sein de populations plus faiblement exposées étaient nécessaires afin d’évaluer la persistance ou non d’associations à plus faibles doses. Des études de ce type ont été menées aux États-Unis (Brown et coll., 2004 ; Wing et Richardson, 2005
; Wing et Richardson, 2005 ; Schubauer-Berigan et coll., 2007
; Schubauer-Berigan et coll., 2007 ), au Royaume-Uni (Atkinson et coll., 2004
), au Royaume-Uni (Atkinson et coll., 2004 ; Gillies et Haylock, 2014
; Gillies et Haylock, 2014 ) (Gillies et coll., 2017a
) (Gillies et coll., 2017a ) ainsi que dans 3 pays européens (Royaume-Uni, Belgique et France) (Grellier et coll., 2017
) ainsi que dans 3 pays européens (Royaume-Uni, Belgique et France) (Grellier et coll., 2017 ). Parmi toutes ces études, la plus informative sur les faibles niveaux de dose demeure une analyse combinée réalisée conjointement chez 45 817 travailleurs des cohortes de Sellafield et de Mayak (Gillies et coll., 2017a
). Parmi toutes ces études, la plus informative sur les faibles niveaux de dose demeure une analyse combinée réalisée conjointement chez 45 817 travailleurs des cohortes de Sellafield et de Mayak (Gillies et coll., 2017a ). Celle-ci a mis en évidence une relation linéaire entre dose due au plutonium et risque de cancer du poumon (que la mortalité ou l’incidence de la pathologie soit considérée) y compris, pour l’incidence de cancer du poumon, à des niveaux de doses inférieurs à 0,1 Gy (Gillies et coll., 2017a
). Celle-ci a mis en évidence une relation linéaire entre dose due au plutonium et risque de cancer du poumon (que la mortalité ou l’incidence de la pathologie soit considérée) y compris, pour l’incidence de cancer du poumon, à des niveaux de doses inférieurs à 0,1 Gy (Gillies et coll., 2017a ).
).
 ; Wing et Richardson, 2005
; Wing et Richardson, 2005 ; Schubauer-Berigan et coll., 2007
; Schubauer-Berigan et coll., 2007 ), au Royaume-Uni (Atkinson et coll., 2004
), au Royaume-Uni (Atkinson et coll., 2004 ; Gillies et Haylock, 2014
; Gillies et Haylock, 2014 ) (Gillies et coll., 2017a
) (Gillies et coll., 2017a ) ainsi que dans 3 pays européens (Royaume-Uni, Belgique et France) (Grellier et coll., 2017
) ainsi que dans 3 pays européens (Royaume-Uni, Belgique et France) (Grellier et coll., 2017 ). Parmi toutes ces études, la plus informative sur les faibles niveaux de dose demeure une analyse combinée réalisée conjointement chez 45 817 travailleurs des cohortes de Sellafield et de Mayak (Gillies et coll., 2017a
). Parmi toutes ces études, la plus informative sur les faibles niveaux de dose demeure une analyse combinée réalisée conjointement chez 45 817 travailleurs des cohortes de Sellafield et de Mayak (Gillies et coll., 2017a ). Celle-ci a mis en évidence une relation linéaire entre dose due au plutonium et risque de cancer du poumon (que la mortalité ou l’incidence de la pathologie soit considérée) y compris, pour l’incidence de cancer du poumon, à des niveaux de doses inférieurs à 0,1 Gy (Gillies et coll., 2017a
). Celle-ci a mis en évidence une relation linéaire entre dose due au plutonium et risque de cancer du poumon (que la mortalité ou l’incidence de la pathologie soit considérée) y compris, pour l’incidence de cancer du poumon, à des niveaux de doses inférieurs à 0,1 Gy (Gillies et coll., 2017a ).
).Une étude cas-témoins sur la mortalité par cancer du poumon menée chez des travailleurs de 3 pays européens (Royaume-Uni, Belgique et France) incluant 553 cas et 1 333 témoins (Grellier et coll., 2017 ), a permis d’estimer un « Excess Odds Ratio » (constituant une bonne approximation d’un ERR) par Gy au poumon résultant d’expositions au plutonium à 50 (IC 90 % [17-106]), après ajustement sur le statut tabagique, la catégorie socioprofessionnelle et l’exposition externe aux rayonnements ionisants.
), a permis d’estimer un « Excess Odds Ratio » (constituant une bonne approximation d’un ERR) par Gy au poumon résultant d’expositions au plutonium à 50 (IC 90 % [17-106]), après ajustement sur le statut tabagique, la catégorie socioprofessionnelle et l’exposition externe aux rayonnements ionisants.
 ), a permis d’estimer un « Excess Odds Ratio » (constituant une bonne approximation d’un ERR) par Gy au poumon résultant d’expositions au plutonium à 50 (IC 90 % [17-106]), après ajustement sur le statut tabagique, la catégorie socioprofessionnelle et l’exposition externe aux rayonnements ionisants.
), a permis d’estimer un « Excess Odds Ratio » (constituant une bonne approximation d’un ERR) par Gy au poumon résultant d’expositions au plutonium à 50 (IC 90 % [17-106]), après ajustement sur le statut tabagique, la catégorie socioprofessionnelle et l’exposition externe aux rayonnements ionisants.Pour ce qui concerne les pathologies non cancéreuses, sur la base d’un suivi de population jusqu’à la fin de l’année 2008 dans la cohorte de Mayak, une association a été mise en évidence entre la dose interne au poumon due à l’inhalation de plutonium et la survenue d’une bronchite chronique, après ajustement notamment sur le tabagisme et l’exposition externe aux rayonnements ionisants (ERR/Gy = 1,19 (IC 95 % [0,32-2,53]) (Azizova et coll., 2017 ). Il n’a pas été observé d’association significative entre dose absorbée au foie résultant d’expositions internes par le plutonium et mortalité par toutes maladies de l’appareil circulatoire confondues, après prise en compte de l’exposition externe (Azizova et coll., 2015a
). Il n’a pas été observé d’association significative entre dose absorbée au foie résultant d’expositions internes par le plutonium et mortalité par toutes maladies de l’appareil circulatoire confondues, après prise en compte de l’exposition externe (Azizova et coll., 2015a ). Toutefois, une tendance significative à l’augmentation de la mortalité par maladies cérébrovasculaires en fonction de la dose interne au foie a été observée, uniquement dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (ERR/Gy = 0,84 (IC 95 % [0,09-1,92]). Pour l’incidence de maladies cérébrovasculaires, une association significative a été observée dans la cohorte entière (ERR/Gy = 0,28 (IC 95 % [0,16-0,42]), et dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (ERR/Gy = 0,90 (IC 95 % [0,56-1,28]), mais la tendance n’apparaît pas clairement comme linéaire (Azizova et coll., 2014
). Toutefois, une tendance significative à l’augmentation de la mortalité par maladies cérébrovasculaires en fonction de la dose interne au foie a été observée, uniquement dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (ERR/Gy = 0,84 (IC 95 % [0,09-1,92]). Pour l’incidence de maladies cérébrovasculaires, une association significative a été observée dans la cohorte entière (ERR/Gy = 0,28 (IC 95 % [0,16-0,42]), et dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (ERR/Gy = 0,90 (IC 95 % [0,56-1,28]), mais la tendance n’apparaît pas clairement comme linéaire (Azizova et coll., 2014 ). La mortalité par maladies cardiaques ischémiques présente une tendance linéaire en fonction de la dose absorbée au foie résultant d’expositions internes par le plutonium, dans la cohorte entière (ERR/Gy = 0,21 (IC 95 % [0,01-0,58]) ainsi que dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (RR/Gy = 1,08 (IC 95 % [0,34-2,15]). Enfin, en ce qui concerne l’incidence de ces pathologies, une tendance significative n’a été observée que dans le groupe exposé à des doses inférieures à 1 Gy (ERR/Gy = 0,44 (IC 95 % [0,09-0,85]) (Azizova et coll., 2015b
). La mortalité par maladies cardiaques ischémiques présente une tendance linéaire en fonction de la dose absorbée au foie résultant d’expositions internes par le plutonium, dans la cohorte entière (ERR/Gy = 0,21 (IC 95 % [0,01-0,58]) ainsi que dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (RR/Gy = 1,08 (IC 95 % [0,34-2,15]). Enfin, en ce qui concerne l’incidence de ces pathologies, une tendance significative n’a été observée que dans le groupe exposé à des doses inférieures à 1 Gy (ERR/Gy = 0,44 (IC 95 % [0,09-0,85]) (Azizova et coll., 2015b ). Toutefois, la dernière analyse réalisée conjointement dans les cohortes de Sellafield et de Mayak n’a pas montré d’association cohérente entre doses dues aux expositions internes par le plutonium et mortalité par pathologies de l’appareil circulatoire (Azizova et coll., 2018b
). Toutefois, la dernière analyse réalisée conjointement dans les cohortes de Sellafield et de Mayak n’a pas montré d’association cohérente entre doses dues aux expositions internes par le plutonium et mortalité par pathologies de l’appareil circulatoire (Azizova et coll., 2018b ).
).
 ). Il n’a pas été observé d’association significative entre dose absorbée au foie résultant d’expositions internes par le plutonium et mortalité par toutes maladies de l’appareil circulatoire confondues, après prise en compte de l’exposition externe (Azizova et coll., 2015a
). Il n’a pas été observé d’association significative entre dose absorbée au foie résultant d’expositions internes par le plutonium et mortalité par toutes maladies de l’appareil circulatoire confondues, après prise en compte de l’exposition externe (Azizova et coll., 2015a ). Toutefois, une tendance significative à l’augmentation de la mortalité par maladies cérébrovasculaires en fonction de la dose interne au foie a été observée, uniquement dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (ERR/Gy = 0,84 (IC 95 % [0,09-1,92]). Pour l’incidence de maladies cérébrovasculaires, une association significative a été observée dans la cohorte entière (ERR/Gy = 0,28 (IC 95 % [0,16-0,42]), et dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (ERR/Gy = 0,90 (IC 95 % [0,56-1,28]), mais la tendance n’apparaît pas clairement comme linéaire (Azizova et coll., 2014
). Toutefois, une tendance significative à l’augmentation de la mortalité par maladies cérébrovasculaires en fonction de la dose interne au foie a été observée, uniquement dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (ERR/Gy = 0,84 (IC 95 % [0,09-1,92]). Pour l’incidence de maladies cérébrovasculaires, une association significative a été observée dans la cohorte entière (ERR/Gy = 0,28 (IC 95 % [0,16-0,42]), et dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (ERR/Gy = 0,90 (IC 95 % [0,56-1,28]), mais la tendance n’apparaît pas clairement comme linéaire (Azizova et coll., 2014 ). La mortalité par maladies cardiaques ischémiques présente une tendance linéaire en fonction de la dose absorbée au foie résultant d’expositions internes par le plutonium, dans la cohorte entière (ERR/Gy = 0,21 (IC 95 % [0,01-0,58]) ainsi que dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (RR/Gy = 1,08 (IC 95 % [0,34-2,15]). Enfin, en ce qui concerne l’incidence de ces pathologies, une tendance significative n’a été observée que dans le groupe exposé à des doses inférieures à 1 Gy (ERR/Gy = 0,44 (IC 95 % [0,09-0,85]) (Azizova et coll., 2015b
). La mortalité par maladies cardiaques ischémiques présente une tendance linéaire en fonction de la dose absorbée au foie résultant d’expositions internes par le plutonium, dans la cohorte entière (ERR/Gy = 0,21 (IC 95 % [0,01-0,58]) ainsi que dans la sous-cohorte de travailleurs exposés à des doses inférieures à 1 Gy (RR/Gy = 1,08 (IC 95 % [0,34-2,15]). Enfin, en ce qui concerne l’incidence de ces pathologies, une tendance significative n’a été observée que dans le groupe exposé à des doses inférieures à 1 Gy (ERR/Gy = 0,44 (IC 95 % [0,09-0,85]) (Azizova et coll., 2015b ). Toutefois, la dernière analyse réalisée conjointement dans les cohortes de Sellafield et de Mayak n’a pas montré d’association cohérente entre doses dues aux expositions internes par le plutonium et mortalité par pathologies de l’appareil circulatoire (Azizova et coll., 2018b
). Toutefois, la dernière analyse réalisée conjointement dans les cohortes de Sellafield et de Mayak n’a pas montré d’association cohérente entre doses dues aux expositions internes par le plutonium et mortalité par pathologies de l’appareil circulatoire (Azizova et coll., 2018b ).
).Tritium
Les études épidémiologiques réalisées chez des travailleurs exposés au tritium demeurent rares à ce jour (Beral et coll., 1985 ; Beral et coll., 1988
; Beral et coll., 1988 ; Fraser et coll., 1993
; Fraser et coll., 1993 ; McLaughlin et coll., 1993
; McLaughlin et coll., 1993 ; Carpenter et coll., 1994
; Carpenter et coll., 1994 ; Hamra et coll., 2013
; Hamra et coll., 2013 ; Zablotska et coll., 2014
; Zablotska et coll., 2014 ). Ces études sont peu informatives sur les effets sanitaires d’expositions au tritium, que ce soit en raison d’un manque de dosimétrie spécifique dans la plupart d’entre elles, ou en raison de leurs tailles modestes (UNSCEAR, 2016
). Ces études sont peu informatives sur les effets sanitaires d’expositions au tritium, que ce soit en raison d’un manque de dosimétrie spécifique dans la plupart d’entre elles, ou en raison de leurs tailles modestes (UNSCEAR, 2016 ).
).
 ; Beral et coll., 1988
; Beral et coll., 1988 ; Fraser et coll., 1993
; Fraser et coll., 1993 ; McLaughlin et coll., 1993
; McLaughlin et coll., 1993 ; Carpenter et coll., 1994
; Carpenter et coll., 1994 ; Hamra et coll., 2013
; Hamra et coll., 2013 ; Zablotska et coll., 2014
; Zablotska et coll., 2014 ). Ces études sont peu informatives sur les effets sanitaires d’expositions au tritium, que ce soit en raison d’un manque de dosimétrie spécifique dans la plupart d’entre elles, ou en raison de leurs tailles modestes (UNSCEAR, 2016
). Ces études sont peu informatives sur les effets sanitaires d’expositions au tritium, que ce soit en raison d’un manque de dosimétrie spécifique dans la plupart d’entre elles, ou en raison de leurs tailles modestes (UNSCEAR, 2016 ).
).Conclusion
Jusqu’à présent, les études épidémiologiques réalisées dans des populations de travailleurs de l’industrie nucléaire ont été particulièrement informatives pour caractériser les risques associés à des expositions chroniques externes aux rayonnements ionisants et à des contaminations internes par le plutonium. Elles sont susceptibles d’apporter dans les années à venir des éléments sur les risques associés à d’autres catégories d’expositions, notamment des contaminations internes par d’autres types de radionucléides. Par ailleurs, ces études au long cours deviennent de plus en plus informatives sur les effets à long terme des expositions aux rayonnements ionisants, au fur et à mesure de l’augmentation de leur durée de suivi.
Ces études présentent toutefois un certain nombre de limites. Les reconstitutions rétrospectives de doses sur plusieurs décennies, réalisées à partir de données initialement collectées à des fins de surveillance dosimétrique opérationnelle ou réglementaire plutôt que d’études épidémiologiques, peuvent dans certains cas être soumises à des incertitudes non négligeables. Par ailleurs, ces études ne documentent que les effets d’expositions survenues à l’âge adulte. Enfin, pour certains radionucléides émis lors d’essais nucléaires (ex. : strontium, césium, iode), les études de cohortes de travailleurs du nucléaire disponibles ne disposent pas de suffisamment d’information pour permettre des caractérisations spécifiques de relations doses-effets. Les éléments les plus informatifs sur les effets sanitaires de ces radionucléides viendront alors d’études épidémiologiques réalisées en population générale.
Références
[1] Akleyev A, Deltour I, Krestinina L, et al . Incidence and mortality of solid cancers in people exposed in utero to ionizing radiation: pooled analyses of two cohorts from the Southern Urals, Russia.
PLoS One. 2016;
11: e0160372p. 

[2] Atkinson WD, Law DV, Bromley KJ, et al . Mortality of employees of the United Kingdom atomic energy authority, 1946-97.
Occup Environ Med. 2004;
61:577- 85

[3] Azizova TV, Day RD, Wald N, et al . The “clinic” medical-dosimetric database of Mayak production association workers: structure, characteristics and prospects of utilization.
Health Phys. 2008;
94:449- 58

[4] Azizova TV, Haylock RG, Moseeva MB, et al . Cerebrovascular diseases incidence and mortality in an extended mayak worker cohort 1948-1982.
Radiat Res. 2014;
182:529- 44

[5] Azizova TV, Grigorieva ES, Hunter N, et al . Risk of mortality from circulatory diseases in Mayak workers cohort following occupational radiation exposure.
J Radiol Protect. 2015a;
35:517- 38

[6] Azizova TV, Grigoryeva ES, Haylock RG, et al . Ischaemic heart disease incidence and mortality in an extended cohort of Mayak workers first employed in 1948-1982.
Br J Radiol. 2015b;
88:20150169. 

[7] Azizova TV, Bannikova MV, Grigorieva ES, et al . Risk of lower extremity arterial disease in a cohort of workers occupationally exposed to ionizing radiation over a prolonged period.
Radiat Environ Biophys. 2016;
55:147- 59

[8] Azizova TV, Zhuntova GV, Haylock R, et al . Chronic bronchitis incidence in the extended cohort of Mayak workers first employed during 1948-1982.
Occup Environ Med. 2017;
74:105- 13

[9] Azizova TV, Bannikova MV, Grigoryeva ES, et al . Risk of malignant skin neoplasms in a cohort of workers occupationally exposed to ionizing radiation at low dose rates.
PLoS One. 2018a;
13: e0205060p. 

[10] Azizova TV, Batistatou E, Grigorieva ES, et al . An assessment of radiation-associated risks of mortality from circulatory disease in the cohorts of Mayak and Sellafield nuclear workers.
Radiat Res. 2018b;
184:371- 88

[11] Azizova TV, Hamada N, Grigoryeva ES, et al . Risk of various types of cataracts in a cohort of Mayak workers following chronic occupational exposure to ionizing radiation.
Eur J Epidemiol. 2018c;
33:1193- 204

[12] Beral V, Inskip H, Fraser P, et al . Mortality of employees of the United Kingdom atomic energy authority, 1946-1979.
Br Med J (Clin Res Ed). 1985;
291:440- 7

[13] Beral V, Fraser P, Carpenter L, et al . Mortality of employees of the Atomic weapons establishment, 1951-82.
BMJ. 1988;
297:757- 70

[14] Boice JD, Jr., Cohen SS, Mumma MT, et al . Updated mortality analysis of radiation workers at Rocketdyne (Atomics International), 1948-2008.
Radiat Res. 2011;
176:244- 58

[15] Bouyer J, Hémon D, Cordier S, et al . Epidémiologie : principes et méthodes quantitatives.
Paris:Inserm, Lavoisier/Tec Doc;
1992;


[16] Brown SC, Schonbeck MF, McClure D, et al . Lung cancer and internal lung doses among plutonium workers at the Rocky flats plant: a case-control study.
Am J Epidemiol. 2004;
160:163- 72

[17] Bunch KJ, Muirhead CR, Draper GJ, et al . Cancer in the offspring of female radiation workers: a record linkage study.
Br J Cancer. 2009;
100:213- 8

[18] Cardis E, Kesminiene A, Ivanov V, et al . Risk of thyroid cancer after exposure to 131I in childhood.
J Natl Cancer Inst. 2005;
97:724- 32

[19] Cardis E, Vrijheid M, Blettner M, et al . The 15-Country collaborative study of cancer risk among radiation workers in the nuclear industry: estimates of radiation-related cancer risks.
Radiat Res. 2007;
167:396- 416

[20] Carpenter L, Higgins C, Douglas A, et al . Combined analysis of mortality in three United Kingdom nuclear industry workforces, 1946-1988.
Radiat Res. 1994;
138:224- 38

[21] Davis FG, Yu KL, Preston D, et al . Solid Cancer incidence in the Techa river incidence cohort: 1956-2007.
Radiat Res. 2015;
184:56- 65

[22] Dickinson HO, Parker L, Salotti J, et al . Paternal preconceptional irradiation, population mixing and solid tumors in the children of radiation workers (England).
Cancer Causes Control. 2002;
13:183- 9

[24] Draper GJ, Little MP, Sorahan T, et al . Cancer in the offspring of radiation workers: a record linkage study.
BMJ. 1997;
315:1181- 8

[25] Fraser P, Carpenter L, Maconochie N, et al . Cancer mortality and morbidity in employees of the United Kingdom atomic energy authority, 1946-86.
Br J Cancer. 1993;
67:615- 24

[27] Gardner MJ, Hall AJ, Snee MP, et al . Methods and basic data of case-control study of leukaemia and lymphoma among young people near Sellafield nuclear plant in West Cumbria.
BMJ. 1990a;
300:429- 34

[28] Gardner MJ, Snee MP, Hall AJ, et al . Results of case-control study of leukaemia and lymphoma among young people near Sellafield nuclear plant in West Cumbria.
BMJ. 1990b;
300:423- 9

[29] Gilbert ES, Sokolnikov ME, Preston DL, et al . Lung cancer risks from plutonium: an updated analysis of data from the Mayak worker cohort.
Radiat Res. 2013;
179:332- 42

[30] Gillies M, Haylock R. The cancer mortality and incidence experience of workers at British Nuclear Fuels plc, 1946-2005.
J Radiol Protect. 2014;
34:595- 623

[31] Gillies M, Kuznetsova I, Sokolnikov M, et al . Lung cancer risk from plutonium: a pooled analysis of the Mayak and Sellafield worker cohorts.
Radiat Res. 2017a;
188:645- 60

[32] Gillies M, Richardson DB, Cardis E, et al . Mortality from circulatory diseases and other non-cancer outcomes among nuclear workers in France, the United Kingdom and the United States (INWORKS).
Radiat Res. 2017b;
188:276- 90

[33] Grant EJ, Brenner A, Sugiyama H, et al . Solid cancer incidence among the Life Span study of atomic bomb survivors: 1958-2009.
Radiat Res. 2017;
187:513- 37

[34] Grellier J, Atkinson W, Berard P, et al . Risk of lung cancer mortality in nuclear workers from internal exposure to alpha particle-emitting radionuclides.
Epidemiology. 2017;
28:675- 84

[35] Hamra G, Richardson D, Maclehose R, et al . Integrating informative priors from experimental research with Bayesian methods: an example from radiation epidemiology.
Epidemiology. 2013;
24:90- 5

[36] Hamra GB, Richardson DB, Cardis E, et al . Cohort profile: the international nuclear workers study (INWORKS).
Int J Epidemiol. 2016;
45:693- 9

[37] Haylock RGE, Gillies M, Hunter N, et al . Cancer mortality and incidence following external occupational radiation exposure: an update of the 3rd analysis of the UK national registry for radiation workers.
Br J Cancer. 2018;
119:631- 7

[38]HLEG. HLEG Report on European low dose risk research.
EUR 23884. Luxembourg, UK:Office for Official Publications of the European Communities;
2009;


[39] Hunter N, Kuznetsova IS, Labutina EV, et al . Solid cancer incidence other than lung, liver and bone in Mayak workers: 1948-2004.
Br J Cancer. 2013;
109:1989- 96

[40]ICRP. The 2007 Recommendations of the International commission on radiological protection. ICRP Publication 103.
Ann ICRP. 2007;
37p. 

[41]ICRP. Areas of research to support the system of radiological protection.
ICRP ref 4832-9526-9446. 2017;


[42] Kinlen LJ. Can paternal preconceptional radiation account for the increase of leukaemia and non-Hodgkin’s lymphoma in Seascale?.
BMJ. 1993;
306:1718- 21

[43] Kinlen LJ, Clarke K, Balkwill A. Paternal preconceptional radiation exposure in the nuclear industry and leukaemia and non-Hodgkin’s lymphoma in young people in Scotland.
BMJ. 1993;
306:1153- 8

[44] Krestinina LY, Kharyuzov YE, Epiphanova SB, et al . Cancer incidence after in utero exposure to ionizing radiation in Techa river residents.
Radiat Res. 2017;
188:314- 24

[45] Kreuzer M, Auvinen A, Cardis E, et al . Low-dose ionising radiation and cardiovascular diseases: strategies for molecular epidemiological studies in Europe.
Mutat Res Rev. 2015;
764:90- 100

[46] Kreuzer M, Auvinen A, Cardis E, et al . Multidisciplinary European low dose initiative (MELODI): strategic research agenda for low dose radiation risk research.
Radiat Environ Biophys. 2018;
57:5- 15

[47] Kuznetsova IS, Labutina EV, Hunter N. Radiation risks of leukemia, lymphoma and multiple myeloma incidence in the Mayak cohort: 1948-2004.
PLoS One. 2016;
11: e0162710p. 

[48] Laurier D, Guseva Canu I, Baatout S, et al . DoReMi workshop on multidisciplinary approaches to evaluating cancer risks associated with low-dose internal contamination.
Radioprotection. 2012;
47:119- 48

[49] Leuraud K, Richardson DB, Cardis E, et al . Ionising radiation and risk of death from leukaemia and lymphoma in radiation-monitored workers (INWORKS): an international cohort study.
Lancet Haematol. 2015;
2:e276- 81

[50] Leuraud K, Fournier L, Samson E, et al. . Mortality in the French cohort of nuclear workers.
Radioprotection. 2017;
52:199- 210

[51] Little MP, Wakeford R, Charles MW. A comparison of the risks of leukaemia in the offspring of the Sellafield workforce born in Seascale and those born elsewhere in West Cumbria with the risks in the offspring of the Ontario and Scottish workforces and the Japanese bomb survivors.
J Radiol Protect. 1994;
14:187- 201

[52] McKinney PA, Fear NT, Stockton D. Parental occupation at periconception: findings from the United Kingdom childhood cancer study.
Occup Environ Med. 2003;
60:901- 9

[53] McLaughlin JR, King WD, Anderson TW, et al . Paternal radiation exposure and leukaemia in offspring: the Ontario case-control study.
BMJ. 1993;
307:959- 66

[54] McLean AR, Adlen EK, Cardis E, et al . A restatement of the natural science evidence base concerning the health effects of low-level ionizing radiation.
Proc Biol Sci. 2017;
284p. 

[55]NCRP. NCRP commentary No. 27. Implications of recent epidemiologic studies for the linear-non threshold model and radiation protection.
Bethesda, USA:NCRP;
2018;


[56] Ozasa K, Shimizu Y, Suyama A, et al . Studies of the mortality of atomic bomb survivors. Report 14, 1950-2003: an overview of cancer and noncancer diseases.
Radiat Res. 2012;
177:229- 43

[57] Renaud P.IRSN. Les essais atmosphériques d’armes nucléaires : des retombées radioactives à l’échelle planétaire.
Fiche information de l’IRSN. DCOM/Direction de l’environnement et de l’intervention. 2008;


[58] Richardson DB, Cardis E, Daniels RD, et al . Risk of cancer from occupational exposure to ionising radiation : retrospective cohort study of workers in France, the United Kingdom, and the United States (INWORKS).
BMJ. 2015;
351: h5359p. 

[59] Richardson DB, Cardis E, Daniels RD, et al . Site-specific solid cancer mortality after exposure to ionizing radiation: a cohort study of workers (INWORKS).
Epidemiology. 2018;
29:31- 40

[60] Roman E, Doyle P, Maconochie N, et al . Cancer in children of nuclear industry employees: report on children aged under 25 years from nuclear industry family study.
BMJ. 1999;
318:1443- 50

[61] Schonfeld SJ, Tsareva YV, Preston DL, et al . Cancer mortality following in utero exposure among offspring of female Mayak worker cohort members.
Radiat Res. 2012;
178:160- 5

[62] Schubauer-Berigan MK, Daniels RD, Fleming DA, et al . Risk of chronic myeloid and acute leukemia mortality after exposure to ionizing radiation among workers at four U.S. nuclear weapons facilities and a nuclear naval shipyard.
Radiat Res. 2007;
167:222- 32

[63] Schuz J, Deltour I, Krestinina LY, et al . In utero exposure to radiation and haematological malignancies: pooled analysis of Southern Urals cohorts.
Br J Cancer. 2017;
116:126- 33

[64] Shimizu Y, Kodama K, Nishi N, et al . Radiation exposure and circulatory disease risk: Hiroshima and Nagasaki atomic bomb survivor data, 1950-2003.
BMJ. 2010;
340: b5349p. 

[65] Sokolnikov ME, Gilbert ES, Preston DL, et al . Lung, liver and bone cancer mortality in Mayak workers.
Int J Cancer. 2008;
123:905- 11

[66] Sokolnikov M, Preston D, Gilbert E, et al . Radiation effects on mortality from solid cancers other than lung, liver, and bone cancer in the mayak worker cohort: 1948-2008.
PLoS One. 2015;
10: e0117784p. 

[67] Sokolnikov M, Preston D, Stram DO. Mortality from solid cancers other than lung, liver, and bone in relation to external dose among plutonium and non-plutonium workers in the Mayak worker cohort.
Radiat Environ Biophys. 2017;
56:121- 5

[68] Sorahan T, Haylock RG, Muirhead CR, et al . Cancer in the offspring of radiation workers: an investigation of employment timing and a reanalysis using updated dose information.
Br J Cancer. 2003;
89:1215- 20

[69] Tsareva Y, Deltour I, Sokolnikov M, et al . Risk of solid cancer in the offspring of female workers of the Mayak nuclear facility in the Southern Urals, Russian Federation.
Radiat Environ Biophys. 2016;
55:291- 7

[70]UNSCEAR (United Nations scientific committee on the effects of atomic radiation). UNSCEAR 2000 Report to the general assembly with scientific annexes. Sources of ionizing radiation. Annex C: exposures to the public from man-made sources of radiation.
New York : United Nations:2000;


[71]UNSCEAR (United Nations scientific committee on the effects of atomic radiation). UNSCEAR 2006 Report to the general assembly with scientific annexes. Effects of ionizing radiation. Vol. 1: report and annexes A and B.
New York : United Nations:2008;


[72]UNSCEAR (United Nations scientific committee on the effects of atomic radiation). Sources, effects and risks of ionizing radiation. UNSCEAR 2012 Report to the general assembly. Scientific annexes A and B. Annex B. Uncertainties in risk estimates for radiation-induced cancer.
New York, NY : United Nations:2012;


[73]UNSCEAR (United Nations scientific committee on the effects of atomic radiation). Unscear 2012 Report to the general assembly with scientific annexes, sources and effects of ionizing radiation. Vol. 2: scientific annex A. Attributing health effects to ionizing radiation exposure and inferring risks.
New York : United Nations:2015;


[74]UNSCEAR (United Nations scientific committee on the effects of atomic radiation). Sources, effects and risks of ionizing radiation. Annex C. Biological effects of selected internal emitters – tritium.
New York : United Nations:2016;


[75] Vrijheid M, Cardis E, Ashmore P, et al . Mortality from diseases other than cancer following low doses of ionizing radiation: results from the 15-country study of nuclear industry workers.
Int J Epidemiol. 2007;
36:1126- 35

[77] Wing S, Richardson DB. Age at exposure to ionising radiation and cancer mortality among Hanford workers: follow up through 1994.
Occup Environ Med. 2005;
62:465- 72

[78] Zablotska LB, Lane RS, Thompson PA. A reanalysis of cancer mortality in Canadian nuclear workers (1956-1994) based on revised exposure and cohort data.
Br J Cancer. 2014;
110:214- 23