| |
| Med Sci (Paris). 34(12): 1092–1099. doi: 10.1051/medsci/2018294.Cellules souches mésenchymateuses et médecine régénératrice Quel avenir pour l’arthrose ? Marie Maumus,1 Yves-Marie Pers,1,2 Maxime Ruiz,1 Christian Jorgensen,1,2 and Danièle Noël1,2* 1IRMB, université de Montpellier, Inserm U1183, 80, avenue Augustin Fliche, 34295Montpellier, France 2Unité d’immunologie clinique et de thérapeutique des maladies ostéoarticulaires, département de rhumatologie, hôpital Lapeyronie, 34000Montpellier, France |
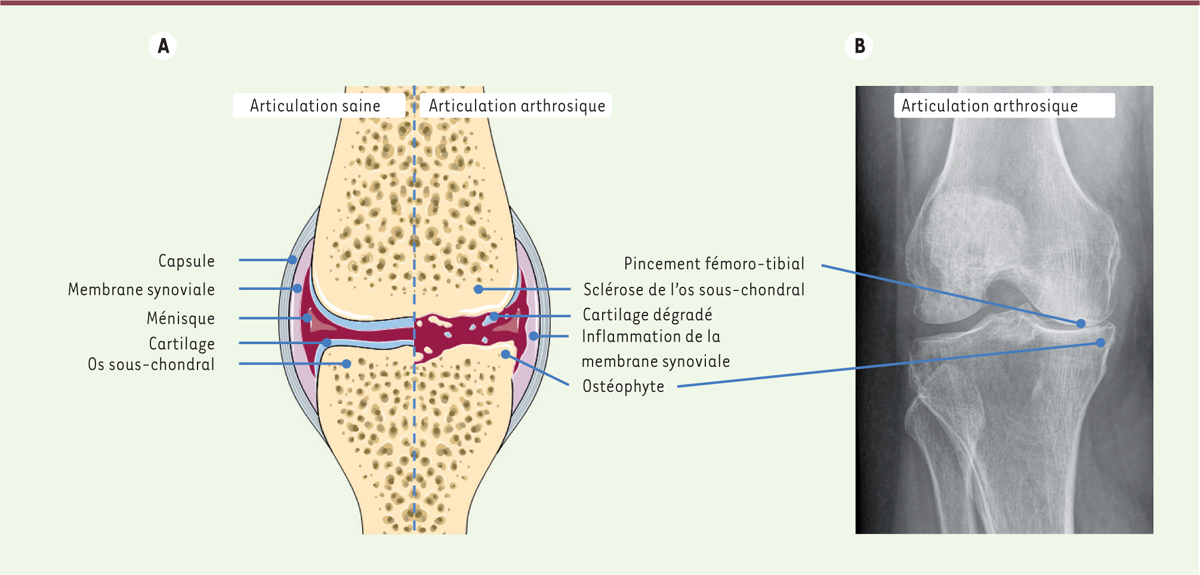
L’arthrose est la plus fréquente des maladies ostéoarticulaires dont la prévalence ne cesse d’augmenter avec le vieillissement de la population. Outre l’âge, les facteurs prédisposants sont le genre, les traumatismes articulaires, les malformations squelettiques, les facteurs génétiques, l’obésité et le syndrome métabolique. Cette pathologie touche tous les tissus de l’articulation : cartilage, os sous-chondral, membrane synoviale et ligaments (Figure 1). Un des mécanismes importants dans la physiopathologie de cette maladie est l’inflammation chronique, de bas grade, liée à l’activation du métabolisme du chondrocyte. L’activation du chondrocyte, unique cellule différenciée constituant le cartilage et impliquée dans l’homéostasie du tissu, entraîne la sécrétion de cytokines, telles que l’IL(interleukine)-1 et l’IL-6, de médiateurs lipidiques, dont la prostaglandine E2 (PGE2), et d’espèces réactives de l’oxygène et de l’azote (ROS, pour reactive oxygen species et RNS, reactive nitrogen species), comme le NO (nitric oxide). Cette inflammation chondrocytaire est activée par les cellules des tissus environnants, notamment les macrophages de la membrane synoviale et l’os sous-chondral. Les traitements actuels sont essentiellement palliatifs et symptomatiques et se limitent à des antalgiques et des anti-inflammatoires. La chirurgie est la dernière alternative avec la pose de prothèses. Parmi les innovations thérapeutiques en cours d’évaluation [35] (→) la médecine régénératrice fondée sur l’utilisation des CSM (cellules souches/stromales mésenchymateuses) est une approche très prometteuse. (→) Voir la Synthèse de Y. Tachikart et al., m/s n° 6-7, juin-juillet 2018, page 547 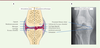 | Figure 1. Diagnostic de l’arthrose du genou. A. Schéma représentatif d’une articulation de genou comportant les différents tissus composant une articulation. B. Radiographie montrant un pincement fémoro-tibial médial avec présence d’ostéophytes. |
|
Les cellules souches mésenchymateuses Caractéristiques des cellules souches mésenchymateuses Les CSM constituent une population hétérogène de cellules multipotentes caractérisées par leurs capacités clonogéniques et leur potentiel de différenciation. Elles sont définies par la Société internationale de thérapie cellulaire (ISCT) selon trois critères : leur propriété d’adhérence au plastique ; leur phénotype : CD73 +/CD90 +/CD105 + et CD45 -/CD34 -/CD14 - ou CD11b -/CD19 - ou CD79a -/HLA-DR - ; et leur potentiel de différenciation en ostéoblastes, chondrocytes et adipocytes [ 1]. Origine des cellules souches mésenchymateuses Les CSM peuvent être identifiées dans tous les tissus, mais elles sont isolées principalement à partir de la moelle osseuse (MO), du tissu adipeux (TA), du placenta ou du cordon ombilical. D’un point de vue qualitatif, toutes les CSM, quelle que soit leur origine, partagent les mêmes propriétés fonctionnelles, mais d’un point de vue quantitatif, des variations ont été mises en évidence. L’un des enjeux en médecine régénératrice est donc de déterminer la meilleure source tissulaire selon la maladie ciblée. Les variations entre CSM issues de sources différentes ont été décrites aux niveaux transcriptionnel et protéomique et pour leurs capacités de différenciation [ 2, 3]. Ainsi, les CSM isolées de la MO ont un potentiel de différenciation chondrogénique plus élevé que celles isolées du TA. De même, la fonction de support des cellules souches hématopoïétiques (CSH) est une caractéristique essentielle des CSM de la MO, qui n’est pas partagée par les autres CSM. Les CSM du TA possèdent, quant à elle, une activité angiogénique supérieure aux autres types de CSM, grâce à leur capacité de sécréter des quantités élevées de facteurs participant à l’angiogenèse. Des différences d’activité immunosuppressive entre les CSM adultes et fœtales et de potentiels de prolifération selon l’âge du donneur ont également été décrites. Rôle physiologique Les CSM ont été initialement identifiées dans la moelle osseuse où elles jouent un rôle de maintien et de régulation des cellules souches hématopoïétiques (CSH) ; la déplétion des CSM périvasculaires réduit en effet la fréquence des CSH médullaires [ 4]. Il existe plusieurs sous-populations de CSM qui, bien qu’identifiées par des marqueurs de surface différents (nestine, CXCL12 [pour les cellules CAR – CXCL12-abundant reticular], récepteur de la leptine) 1, possèdent des fonctions qui se chevauchent. En dehors de celles de la niche hématopoïétique, les CSM d’autres tissus, tels que l’intestin ou la peau, participent également à l’homéostasie tissulaire [ 5]. Le rôle des CSM dans la régénération tissulaire est certainement le plus connu : par leur potentiel de différenciation en cellules spécialisées, elles assurent le renouvellement des cellules vieillissantes. Elles participent également au maintien de l’homéostasie immunitaire par des fonctions qu’elles partagent avec d’autres cellules immunosuppressives, comme les lymphocytes T régulateurs (Treg), en agissant sur l’ensemble des cellules de l’immunité innée ou adaptative. Cependant, cette fonction, qui a été démontrée in vitro, est difficile à étudier in vivo en l’absence de marqueurs spécifiques. Rôle thérapeutique in vitro La capacité des CSM à régénérer les tissus lésés est étroitement liée à leurs propriétés anti-inflammatoires. Les CSM agissent en effet localement au travers d’interactions cellules-cellules reposant sur des liaisons récepteurs-ligands, ou par l’intermédiaire de nanotubes qui transfèrent des molécules et des organelles. Elles interviennent cependant principalement au niveau systémique, en sécrétant des facteurs trophiques qui peuvent être transportés par des vésicules extracellulaires [ 6, 36] ( →). (→) Voir la Nouvelle de S. Le Lay et al., m/s n° 2, février 2017, page 114 Elles peuvent ainsi favoriser la viabilité et la prolifération cellulaires, ou l’angiogenèse par la production de facteurs de croissance (bFGF, PDGF, VEGF, etc.). Elles stimulent également le recrutement de cellules souches endogènes en sécrétant des chimiokines, telles que CCL5 ou CXCL12 et réduisent la fibrose par la production de MMP-2, MMP-9, bFGF, HGF et KGF [7]. Elles interviennent dans la régulation de l’apoptose, via la production de HGF, bFGF, IGF1, et du stress oxydatif, via la libération d’HO-1 ou d’EPO. Enfin, elles possèdent une activité anti-inflammatoire via la libération d’IDO, d’HLAG5, de PGE2, de TSG6, d’IL-6, d’IL-1RA, etc. La sécrétion de l’ensemble de ces facteurs confère ainsi à ces cellules une activité trophique exceptionnelle. |
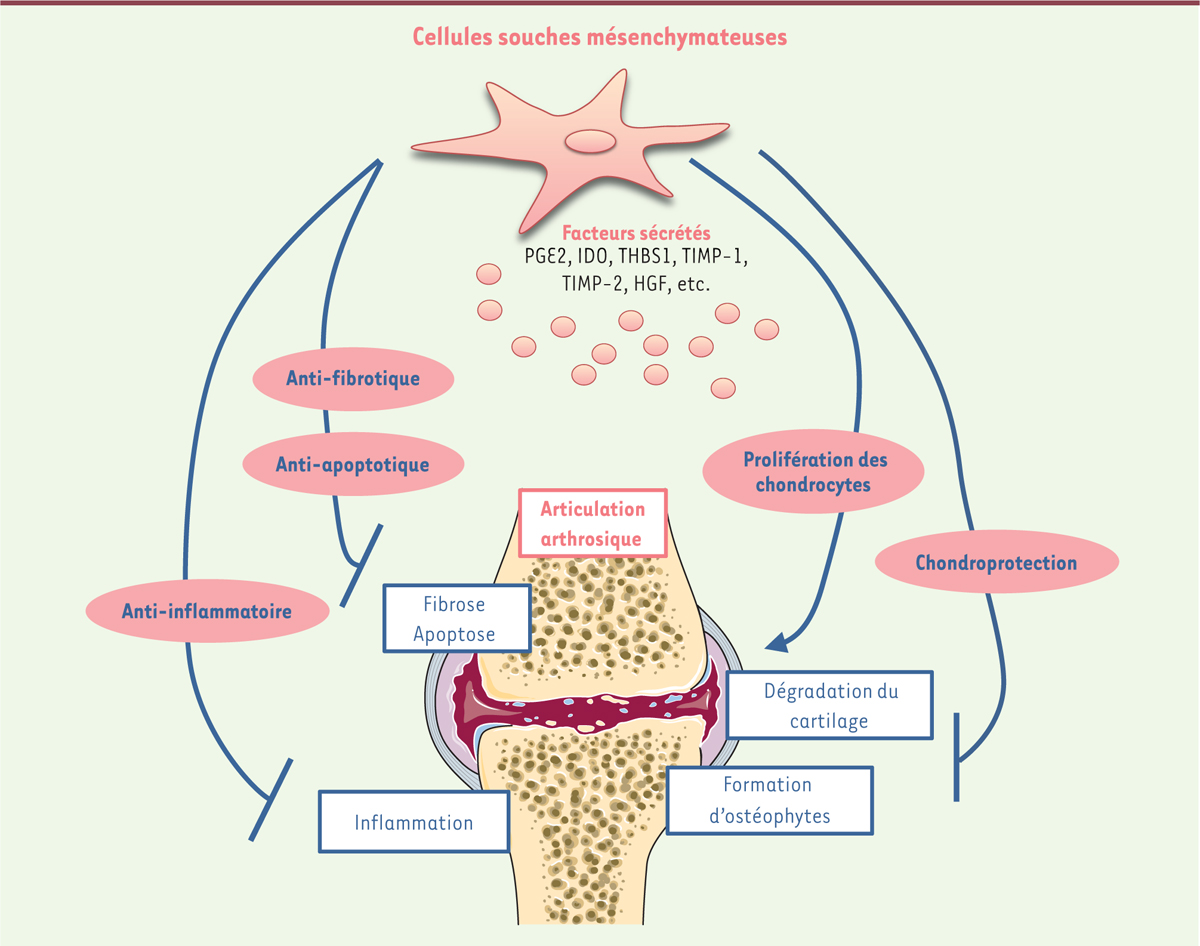
Mécanismes d’action in vitro des cellules souches mésenchymateuses dans l’arthrose Dans l’arthrose, les CSM sont utilisées en pratique comme source de cellules régénératrices afin de stimuler la réparation du cartilage endogène lésé et diminuer l’inflammation locale. In vitro, les études indiquent qu’elles peuvent agir favorablement sur le phénotype pathologique des chondrocytes arthrosiques, mais également sur les autres cellules constitutives de l’articulation. In vivo, certaines études ont identifié les mécanismes biologiques impliqués dans les processus de réparation auxquels participent les CSM, leur conférant un potentiel thérapeutique après implantation (Figure 2). 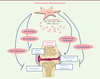 | Figure 2. Intérêt des cellules souches mésenchymateuses dans l’arthrose. Les cellules souches mésenchymateuses possèdent des propriétés fonctionnelles ayant un intérêt thérapeutique dans l’arthrose. Via la production d’un panel de facteurs sécrétés (voir glossaire), ces cellules exercent des effets anti-apoptotiques, anti-fibrotiques, anti-inflammatoires et chondroprotecteurs qui peuvent contrecarrer/améliorer les symptômes de la pathologie. |
Différenciation chondrocytaire et réparation du cartilage La différenciation des CSM en chondrocytes requiert la combinaison de facteurs de croissance exogènes, comme le TGF-β, la BMP, l’IGF, le bFGF, le FSTL1, ou l’IL-6 et d’un support tridimensionnel [ 8]. Plusieurs biomatériaux naturels et synthétiques sont développés pour reproduire la complexité structurelle du cartilage articulaire : des microsphères de collagène ou de PLGA, des hydrogels, des polymères biodégradables [ 9] ( →). (→) Voir le numéro thématique Biomatériaux, m/s n° 1 janvier 2017 Les approches d’ingénierie tissulaire s’appliquent essentiellement à des lésions ostéochondrales résultant d’un traumatisme. Bien qu’elles puissent, à priori, retarder la survenue de la pathologie, elles restent difficilement envisageables pour le traitement de lésions plus étendues comme celles observées dans le cas d’arthroses sévères. La sécrétion d’un grand nombre de médiateurs par les CSM présente un intérêt dans l’arthrose afin de prévenir la dégradation du cartilage et stimuler sa réparation endogène (Figure 2). En coculture in vitro, les CSM augmentent la prolifération des chondrocytes et leur capacité de synthèse de protéines de la matrice extracellulaire [10] en produisant, entre autres, du THBS1 ou du FGF1 [11] Réduction de l’inflammation locale L’arthrose est une maladie pauci-inflammatoire 2 où les médiateurs pro-inflammatoires produits par les chondrocytes et les synoviocytes participent aux altérations des tissus articulaires, surtout lors de la phase précoce de la maladie. La sécrétion d’IGF1 par les CSM réduit la production des cytokines pro-inflammatoires par les chondrocytes, prévenant ainsi leur activité inflammatoire [ 12]. Ceci pourrait être lié à l’inhibition par l’IGF1 de la voie de signalisation menant à l’activation de NF-κB dans les chondrocytes arthrosiques stimulés par l’IL-1β. En sécrétant de l’HGF et de la PGE2, les CSM ont également la capacité de convertir des synoviocytes de type macrophage 3 d’un phénotype M1 (inflammatoire) vers un phénotype M2 (remodelant) [ 13], contribuant ainsi à la diminution de l’inflammation locale. |
Au cours de l’arthrose, la dégénérescence du cartilage aboutit à la formation d’un tissu de type fibrocartilage. Afin de compenser cette transformation, les chondrocytes accélèrent leur différenciation, formant alors un tissu hypertrophique, ou ostéophyte (une excroissance osseuse) (Figure 2). In vitro, en coculture avec des chondrocytes arthrosiques, les CSM, par l’HGF qu’elles produisent, diminuent de façon significative les marqueurs fibrotiques et hypertrophiques liés à l’arthrose, notamment les collagènes de type I, III, VI, la vimentine, et la MMP13 [14, 15]. |
Diminution de la sénescence des chondrocytes Au cours de la progression de l’arthrose, l’inflammation chronique produite peut contribuer à la sénescence des chondrocytes et à la dégénérescence du cartilage. Les chondrocytes arthrosiques présentent en effet des marqueurs de sénescence, comme une activité β-galactosidase associée à la sénescence (SA-βGal), un raccourcissement des télomères et une accumulation de la protéine p16INK4a 4. L’effet bénéfique sur la sénescence des chondrocytes d’un milieu conditionné obtenu par culture de CSM a été récemment mis en évidence, avec une réduction de l’expression de la SA-βGal et des médiateurs du stress oxydatif [16]. Cette inhibition de la SA-βGal est due à l’action des vésicules extracellulaires issues des CSM qui réduisent également l’accumulation de γH2AX, la forme phosphorylée de l’histone H2AX, un marqueur de réponse aux dommages à l’ADN. Cet effet serait lié à la réduction de la sécrétion d’IL-6 et de PGE2 par les chondrocytes [17]. Les CSM jouent donc un rôle régulateur de différentes activités des chondrocytes qui sont modifiées dans l’arthrose. Les cellules cultivées in vitro puis injectées par voie systémique ne survivent néanmoins que peu après leur implantation. Les effets anti-inflammatoires qu’elles produisent persistent pourtant à long terme, après que les cellules immunitaires endogènes aient été engagées vers un phénotype régulateur. Ce sont ces cellules régulatrices qui permettront de maintenir l’effet des CSM [18]. |
Efficacité thérapeutique des cellules souches mésenchymateuses dans l’arthrose Modèles précliniques L’effet thérapeutique des CSM après injection dans une articulation arthrosique est principalement associé à leurs propriétés trophiques, et non à leur capacité à se différencier en chondrocytes et à générer du cartilage. Dès 2003, dans un modèle d’arthrose du genou chez la chèvre, les effets bénéfiques de l’injection de CSM retardant la destruction du cartilage avaient été montrés [ 19]. Pourtant aucune CSM n’avait été identifiée dans le cartilage, indiquant l’absence ou le faible pourcentage de différenciation de ces cellules en chondrocytes après injection. Depuis, plusieurs modèles d’arthrose ont permis de montrer que l’injection intra-articulaire de CSM permettait de réduire le score arthrosique, cet effet étant plus efficace avec une faible quantité de cellules [ 20, 21]. L’ensemble de ces études a donc révélé l’efficacité thérapeutique de l’injection de CSM dans l’arthrose. Cependant, l’impact de ces cellules exogènes sur la stimulation de la réparation endogène et/ou de la protection/réparation du cartilage reste difficile à évaluer. Données cliniques chez l’homme Les premières études cliniques portant sur l’utilisation de CSM au niveau articulaire ont été décrites en chirurgie réparatrice pour le traitement de lésions focales (c’est-à-dire localisées) du cartilage. Les résultats obtenus ont montré la formation, après injection des CSM au niveau de la lésion, d’un tissu de réparation de type cartilage hyalin 5. Les essais réalisés sur des patients présentant une arthrose sont plus récents. On distingue deux stratégies thérapeutiques : la première technique utilise la fraction stromale vasculaire (SVF) du tissu adipeux obtenue après sa digestion enzymatique et la déplétion des adipocytes. La SVF contient entre 1 et 10 % de CSM. Elle présente l’avantage de permettre une injection de cellules non purifiées, dans un seul temps opératoire. Elle conduit à une amélioration globale des scores de douleurs et présente un bon profil de tolérance [ 22]. Aucune étude contrôlée n’a cependant été menée pour évaluer cette procédure dans l’arthrose. La seconde stratégie consiste à isoler et purifier les CSM lors d’une première intervention, selon des conditions de recueil et de culture strictes et contrôlées en conformité avec les bonnes pratiques de fabrication (BPF). Plusieurs équipes ont mené des essais de phase I/II qui ont confirmé l’efficacité de l’injection de ces CSM ainsi purifiées sur la douleur et la fonction articulaires des patients présentant une gonarthrose 6 [ 23]. Ils n’ont révélé aucun problème de tolérance malgré une alloréactivité faible et transitoire développée par certains receveurs contre les CSM du donneur. Dans ces essais, l’effet immunomodulateur de l’injection a été associé à une augmentation du nombre de lymphocytes Treg et une diminution des monocytes inflammatoires 7. Des essais contrôlés prospectifs sont actuellement en cours (en particulier l’essai clinique de phase II ADIPOA2) afin de déterminer la place et le niveau de preuve de cette thérapie cellulaire par CSM dans l’arthrose. |
Limites et perspectives de la thérapie cellulaire ostéo-articulaire L’intérêt des CSM a été démontré dans plusieurs modèles précliniques de l’arthrose et leur sécurité après administration chez l’homme n’est plus un sujet de débat. Néanmoins, leur efficacité thérapeutique reste à démontrer par des essais incluant de larges cohortes de patients et permettant d’envisager des pistes afin d’améliorer les fonctions effectrices des CSM. L’utilisation des vésicules extracellulaires de CSM Les vésicules extracellulaires sont des structures produites par tous les types cellulaires. Elles participent à la communication entre cellules en transportant et délivrant différentes molécules (protéines, lipides, ARN messagers, microARN) ou en intéragissant directement avec les cellules cibles via la liaison à la membrane de celles-ci de molécules qu’elles présentent à leur surface. On distingue trois types de vésicules : (1) les exosomes, de 50 à 150 nm de diamètre, produits dans le compartiment endosomal ; (2) les microparticules ou microvésicules, de 150 à 500 nm, libérées par bourgeonnement de la membrane plasmique ; et (3) les corps apoptotiques mesurant plus de 1 µm et provenant de la lyse des cellules apoptotiques [ 37] ( →). (→) Voir la Synthèse de S. Le Lay et al., m/s n° 11, novembre 2018, page 936 Les vésicules extracellulaires reproduisent la majorité des effets fonctionnels des cellules dont elles sont issues et, désormais, il est admis que la majorité des fonctions que présentent les CSM sont transmises par les vésicules qu’elles produisent. Un intérêt thérapeutique des vésicules extracellulaires produites par les CSM a été montré dans le traitement des rhumatismes [6]. Dans l’arthrose, ces vésicules présentent un effet chondroprotecteur dans des modèles précliniques [24, 25]. In vitro, elles augmentent la production de facteurs anaboliques par les chondrocytes arthrosiques et diminuent leur production de facteurs cataboliques et inflammatoires, notamment la MMP-13, et l’activité de l’iNOS (NO-synthase inductible) [24, 26]. Elles sont également capables de diminuer le nombre de chondrocytes apoptotiques et l’activation des macrophages [24]. Il reste cependant important d’identifier les mécanismes moléculaires à l’origine de ces effets. Il est également nécessaire d’optimiser et de standardiser la production de ces vésicules extracellulaires (aux normes BPF) afin de conduire les essais cliniques qui évalueront l’efficacité des traitements dans les rhumatismes dégénératifs et inflammatoires et, plus largement, dans les maladies où l’inflammation est prépondérante. L’encapsulation de facteurs de croissance chondrogéniques au sein d’échafaudages et leur libération contrôlée reste un enjeu thérapeutique. L’objectif premier est de maîtriser les gradients de concentration optimaux pour un contrôle spatio-temporel de la libération de ces facteurs sans qu’il n’y ait d’effets secondaires ou de toxicité des biomatériaux [27]. L’utilisation des vésicules extracellulaires comme vecteurs naturels de facteurs de croissance pourrait représenter une solution à ces problématiques. Pré-activation des CSM L’activation des CSM avant leur implantation pourrait permettre de stimuler leur effet thérapeutique, en particulier leurs activités anti-inflammatoires. L’IFNγ (interféron gamma) permet d’activer les CSM en induisant l’expression d’IDO ( indoleamine 2,3-dioxygenase), augmentant ainsi leur effet dans l’arthrose [ 28]. L’activation des CSM permet également d’améliorer leur survie après implantation. Ainsi, un pré-conditionnement des cellules par une culture en hypoxie avant injection induit l’expression de facteurs anti-oxydants, notamment HO-1, et une meilleure adaptation au stress de l’environnement pathologique [ 29]. Enfin, un pré-traitement des CSM peut améliorer leur adressage et leur recrutement aux sites lésionnels. Ainsi, différents médiateurs, tels que l’IL-3, l’IL-6, l’HGF ou le SDF-1 stimulent in vitro l’expression de CXCR4 ( C-X-C motif chemokine receptor 4) par les cellules, augmentant ainsi leur implantation in vivo [ 30]. Ces pistes d’amélioration devront bien sûr être validées après vérification que la pré-activation des CSM n’altère pas leurs propriétés fonctionnelles et améliore leur efficacité thérapeutique in vivo. Développement de tests fonctionnels prédictifs d’efficacité À l’heure actuelle, le contrôle des lots de CSM destinés à être utilisés en clinique repose sur l’analyse du phénotype des cellules et l’évaluation de la sécurité du procédé de fabrication. En l’absence de tests pertinents, l’activité biologique des cellules ne peut être mesurée. L’évaluation de la fonctionnalité des lots de CSM est donc un réel enjeu. Le test utilisé doit en effet permettre de révéler la fonction thérapeutique in vivo qui est revendiquée. Une revue récente décrit les tests fonctionnels qui sont en développement pour les immunothérapies et leurs limites [ 31] ; par manque de reproductibilité, ils ne peuvent être utilisés pour valider la mise en circulation des lots cliniques. En parallèle, la quantification de l’expression par les cellules de certains marqueurs a été proposée comme critère de validité : le VEGF pour l’effet angiogénique, ou le TSG-6, pour l’effet anti-inflammatoire [ 32, 33]. D’autres marqueurs « universels » de l’effet immunosuppresseur des CSM pourraient être également utilisés [ 34]. |
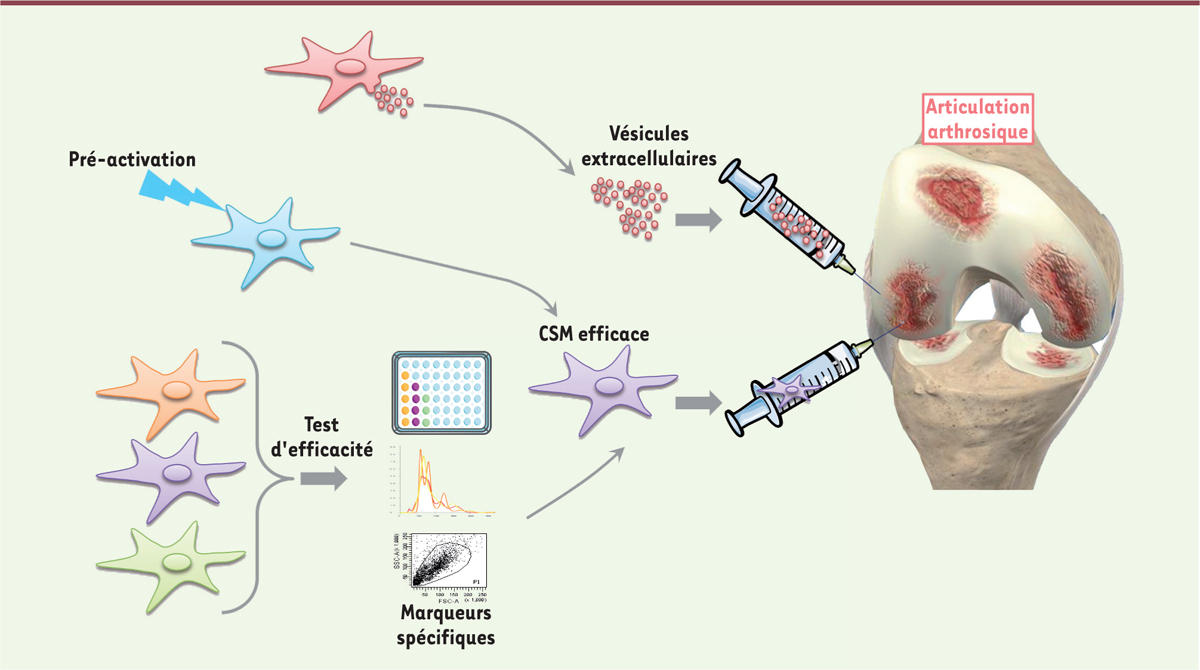
La preuve de concept que les CSM diminuent l’inflammation et préviennent la dégradation du cartilage a été apportée dans les modèles pré-cliniques. Elle est en cours d’évaluation en clinique humaine. La sécurité de l’injection de CSM a été prouvée dans de nombreux essais mais la preuve d’efficacité, en comparaison avec les traitements proposés actuellement, reste à démontrer. Néanmoins, il est possible de proposer d’ores et déjà des pistes de développement pour optimiser les procédés d’obtention des CSM et améliorer leur efficacité. Outre une meilleure standardisation des procédés, le développement de tests fonctionnels, l’identification de marqueurs prédictifs d’efficacité, ou des stratégies de pré-activation des CSM sont à l’étude (Figure 3). Enfin, une alternative d’avenir pourrait reposer sur l’utilisation des vésicules extracellulaires produites par les CSM et dont elles reproduisent la majorité des activités. 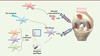 | Figure 3. Perspectives pour une médecine régénératrice optimisée. Afin d’optimiser/améliorer l’efficacité des cellules souches mésenchymateuses, plusieurs pistes sont à l’étude : le développement de tests fonctionnels d’efficacité, l’identification de marqueurs prédictifs d’efficacité, la préactivation des cellules et l’utilisation des vésicules extracellulaires purifiées à partir du surnageant de ces cellules. |
|
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article. |
Ce travail est financé par l’Inserm, l’université de Montpellier, le programme H2020 de l’Union Européenne (ADIPOA2, n° 643809), la Fondation Arthritis R&D (programme ROAD), la fondation FOREUM (projet SEN-OA) et l’ANR (infrastructure Nationale ECELLFRANCE, n°ANR-11-INSB-005). Les figures ont été réalisées grâce à Servier Graphical Art.
|
|
bFGF |
facteur de croissance fibroblastique basique |
|
BMP |
protéines de la morphogénèse osseuse |
|
EPO |
érythropoïétine |
|
FSTL1 |
protéine de type follistatine 1 |
|
HO-1 |
hème oxydase 1 |
|
HGF |
facteur de croissance des hépatocytes |
|
HLAG5 |
antigène du complexe majeur d’histocompatibilité G5 |
|
IGF1 |
insuline facteur de croissance 1 |
|
IDO |
indoléamine 2, 3-dioxygénase |
|
IL1RA |
récepteur antagoniste de l’IL1 |
|
iNOS |
oxyde nitrique synthase inductible |
|
IFNγ |
interféron γ |
|
KGF |
facteur de croissance des kératinocytes |
|
MMP |
métalloprotéase |
|
PDGF |
facteur de croissance dérivé des plaquettes |
|
PGE2 |
prostaglandine E2 |
|
PLGA |
acide poly (lactique-co-glycolique) |
|
ROS |
espèces réactives de l’oxygène |
|
SA-βGal |
β-galactosidase associée à la sénescence |
|
SDF-1 |
facteur dérivé des cellules stromales de type 1 |
|
SVF |
fraction stromale vasculaire |
|
TGF-β |
facteur de croissance transformant β |
|
THBS1 |
thrombospondine 1 |
|
TSG6 |
protéine 6 induite par le facteur de nécrose tumorale |
| VEGF |
facteur de croissance de l’endothélium vasculaire |
|
Footnotes |
1.
Dominici M, Le Blanc K, Mueller I, et al. Minimal criteria for defining multipotent mesenchymal stromal cells. The International Society for Cellular Therapy position statement . Cytotherapy. 2006; ; 8 : :315.–317. 2.
Noel D, Caton D, Roche S, et al. Cell specific differences between human adipose-derived and mesenchymal-stromal cells despite similar differentiation potentials . Exp Cell Res. 2008; ; 314 : :1575.–1584. 3.
Skalnikova H, Motlik J, Gadher SJ, Kovarova H. Mapping of the secretome of primary isolates of mammalian cells, stem cells and derived cell lines . Proteomics. 2011; ; 11 : :691.–708. 4.
Morrison SJ, Scadden DT. The bone marrow niche for haematopoietic stem cells . Nature. 2014; ; 505 : :327.–334. 5.
Hsu YC, Li L, Fuchs E. Emerging interactions between skin stem cells and their niches . Nat Med. 2014; ; 20 : :847.–856. 6.
Cosenza S, Ruiz M, Maumus M, et al. Pathogenic or therapeutic extracellular vesicles in rheumatic diseases: Role of mesenchymal stem cell-derived vesicles . Int J Mol Sci. 2017 ; :18.. 7.
Maumus M, Jorgensen C, Noel D. Mesenchymal stem cells in regenerative medicine applied to rheumatic diseases: role of secretome and exosomes . Biochimie. 2013; ; 95 : :2229.–2234. 8.
Correa D, Somoza RA, Lin P, et al. Sequential exposure to fibroblast growth factors (FGF) 2, 9 and 18 enhances hMSC chondrogenic differentiation . Osteoarthritis Cartilage. 2015; ; 23 : :443.–453. 9.
Rai V, Dilisio MF, Dietz NE, Agrawal DK. Recent strategies in cartilage repair: A systemic review of the scaffold development and tissue engineering . J Biomed Mater Res A. 2017; ; 105 : :2343.–2354. 10.
Wu L, Leijten JC, Georgi N, et al. Trophic effects of mesenchymal stem cells increase chondrocyte proliferation and matrix formation . Tissue Eng Part A. 2011; ; 17 : :1425.–1436. 11.
Maumus M, Manferdini C, Toupet K, et al. Thrombospondin-1 partly mediates the cartilage protective effect of adipose-derived mesenchymal stem cells in osteoarthritis . Front Immunol. 2017; ; 8 : :1638.. 12.
Manferdini C, Maumus M, Gabusi E, et al. Adipose-derived mesenchymal stem cells exert antiinflammatory effects on chondrocytes and synoviocytes from osteoarthritis patients through prostaglandin e2 . Arthritis Rheum. 2013; ; 65 : :1271.–1281. 13.
Manferdini C, Paolella F, Gabusi E, et al. Adipose stromal cells mediated switching of the pro-inflammatory profile of M1-like macrophages is facilitated by PGE2: in vitro evaluation . Osteoarthritis Cartilage. 2017; ; 25 : :1161.–1171. 14.
Maumus M, Manferdini C, Toupet K, et al. Adipose mesenchymal stem cells protect chondrocytes from degeneration associated with osteoarthritis . Stem Cell Res. 2013; ; 11 : :834.–844. 15.
Wang H, Yan X, Jiang Y, et al. The human umbilical cord stem cells improve the viability of OA degenerated chondrocytes . Mol Med Rep. 2018; ; 17 : :4474.–4482. 16.
Platas J, Guillen MI, Perez Del Caz MD, et al. Paracrine effects of human adipose-derived mesenchymal stem cells in inflammatory stress-induced senescence features of osteoarthritic chondrocytes . Aging (Albany NY). 2016; ; 8 : :1703.–1717. 17.
Tofino-Vian M, Guillen MI, Perez Del Caz MD, et al. Extracellular vesicles from adipose-derived mesenchymal stem cells downregulate senescence features in osteoarthritic osteoblasts . Oxid Med Cell Longev. 2017; :7197598.. 18.
Eggenhofer E, Luk F, Dahlke MH, Hoogduijn MJ. The life and fate of mesenchymal stem cells . Front Immunol. 2014; ; 5 : :148.. 19.
Murphy JM, Fink DJ, Hunziker EB, Barry FP. Stem cell therapy in a caprine model of osteoarthritis . Arthritis Rheum. 2003; ; 48 : :3464.–3474. 20.
Ter Huurne M, Schelbergen R, Blattes R, et al. Antiinflammatory and chondroprotective effects of intraarticular injection of adipose-derived stem cells in experimental osteoarthritis . Arthritis Rheum. 2012; ; 64 : :3604.–3613. 21.
Diekman BO, Wu CL, Louer CR, et al. Intra-articular delivery of purified mesenchymal stem cells from C57BL/6 or MRL/MpJ superhealer mice prevents posttraumatic arthritis . Cell Transplant. 2013; ; 22 : :1395.–1408. 22.
Pak J, Lee JH, Park KS, et al. Current use of autologous adipose tissue-derived stromal vascular fraction cells for orthopedic applications . J Biomed Sci. 2017; ; 24 : :9.. 23.
Pers YM, Ruiz M, Noel D, Jorgensen C. Mesenchymal stem cells for the management of inflammation in osteoarthritis: state of the art and perspectives . Osteoarthritis Cartilage. 2015; ; 23 : :2027.–2035. 24.
Cosenza S, Ruiz M, Toupet K, et al. Mesenchymal stem cells derived exosomes and microparticles protect cartilage and bone from degradation in osteoarthritis . Sci Rep. 2017; ; 7 : :16214.. 25.
Tao SC, Yuan T, Zhang YL, et al. Exosomes derived from miR-140-5p-overexpressing human synovial mesenchymal stem cells enhance cartilage tissue regeneration and prevent osteoarthritis of the knee in a rat model . Theranostics. 2017; ; 7 : :180.–195. 26.
Wang L, Gu Z, Zhao X, et al. Extracellular vesicles released from human umbilical cord-derived mesenchymal stromal cells prevent life-threatening acute graft-versus-host disease in a mouse model of allogeneic hematopoietic stem cell transplantation . Stem Cells Dev. 2016; ; 25 : :1874.–1883. 27.
Wang Z, Wang Z, Lu W, et al. Novel biomaterial strategies for controlled growth factor delivery for biomedical applications . NPG Asia Materials. 2017; ; 9 : :e435.. 28.
Maumus M, Roussignol G, Toupet K, et al. Utility of a mouse model of osteoarthritis to demonstrate cartilage protection by IFNgamma-primed equine mesenchymal stem cells . Front Immunol. 2016; ; 7 : :392.. 29.
Mastri M, Lin H, Lee T. Enhancing the efficacy of mesenchymal stem cell therapy . World J Stem Cells. 2014; ; 6 : :82.–93. 30.
Hung SC, Pochampally RR, Hsu SC, et al. Short-term exposure of multipotent stromal cells to low oxygen increases their expression of CX3CR1 and CXCR4 and their engraftment in vivo . PLoS One. 2007; ; 2 : :e416.. 31.
de Wolf C, van de Bovenkamp M, Hoefnagel M. Regulatory perspective on in vitro potency assays for human mesenchymal stromal cells used in immunotherapy . Cytotherapy. 2017; ; 19 : :784.–797. 32.
Lee RH, Yu JM, Foskett AM, et al. TSG-6 as a biomarker to predict efficacy of human mesenchymal stem/progenitor cells (hMSCs) in modulating sterile inflammation in vivo . Proc Natl Acad Sci U S A. 2014; ; 111 : :16766.–16771. 33.
Thej C, Ramadasse B, Walvekar A, et al. Development of a surrogate potency assay to determine the angiogenic activity of Stempeucel(R), a pooled, ex-vivo expanded, allogeneic human bone marrow mesenchymal stromal cell product . Stem Cell Res Ther. 2017; ; 8 : :47.. 34.
Galipeau J, Krampera M, Barrett J, et al. International Society for Cellular Therapy perspective on immune functional assays for mesenchymal stromal cells as potency release criterion for advanced phase clinical trials . Cytotherapy. 2016; ; 18 : :151.–159. 35.
Tachikart Y, Malaise O, Constantinides M, et al. Cibler les cellules sénescentes : une révolution dans le traitement des pathologies ostéo-articulaires . Med Sci (Paris). 2018; ; 34 : :547.–553. 36.
Stik G, Laurence Petit L, Charbord P, et al. Vésicules extracellulaires stromales et régulation des cellules souches et progéniteurs hématopoïétiques . Med Sci (Paris). 2018; ; 34 : :114.–116. 37.
Le Lay S, Martinez MC, Andriantsitohaina R. Vésicules extracellulaires, biomarqueurs et bioeffecteurs du syndrome métabolique . Med Sci (Paris). 2018; ; 34 : :936.–943. |