La drépanocytose est une des maladies monogéniques les plus répandues dans le monde [1]. Chaque année, près de 300 000 enfants en sont atteints. Une mutation ponctuelle homogygote dans le codon 6 du gène de la b-globine entraîne la synthèse d’une protéine déficiente (βs) qui se polymérise à l’état désoxygéné et transforme les érythrocytes qui prennent une forme rigide de faucille. Outre l’hémolyse, l’essentiel de la pathologie est lié à une interaction complexe entre érythrocytes (et autres cellules hématopoïétiques), cellules endothéliales et facteurs plasmatiques qui aboutit à une vasculopathie s’exprimant à la fois sur le mode aigu vaso-occlusif, mais également chronique, altérant la fonction de différents organes. De considérables progrès thérapeutiques ont été réalisés ces 20-30 dernières années : qualité du support transfusionnel, chélation martiale1, sur-expression de l’hémoglobine fœtale par l’hydroxycarbamide (atténuant le phénomène de polymérisation de l’hémoglobine S), prévention anti-infectieuse [2]. La prise en charge précoce grâce au dépistage néonatal, l’établissement de circuits de soins, la formation des équipes médicales et l’éducation thérapeutique des patients ont également un rôle majeur dans l’amélioration globale de la santé des enfants et jeunes adultes atteints. Malgré ces progrès, une importante morbidité et mortalité persistent, et le devenir à l’âge adulte demeure incertain y compris dans le cadre d’un accès à des soins optimaux qui n’ont pas fait disparaître le besoin d’un traitement curateur [3].
à ce jour, seule l’allogreffe de cellules souches hématopoïétiques est capable de guérir la maladie après un conditionnement myélo-ablatif et immunosuppresseur [4]. Les résultats sont globalement remarquables au regard de l’évolution de la maladie, mais la procédure, conditionnée par la disponibilité d’un donneur HLA (human leucocyte antigen) géno-identique (greffe syngénique), reste grevée par le risque de morbidité propre à la greffe, parfois sévère. Des progrès substantiels sont apparus avec la possibilité de donneurs alternatifs (cellules de sang de cordon, donneur HLA phéno-identique, fichiers de donneurs intra-familiaux HLA haplo-identiques), mais le niveau de morbidité et de mortalité résiduelles de ce type de greffe apparaît encore trop élevé en comparaison du traitement conventionnel. Elles ne sont envisagées que dans des situations individuelles très spécifiques [5].
L’approche de thérapie génique développée par plusieurs équipes - d’abord chez l’animal puis récemment chez l’homme - apparaît donc aujourd’hui comme une alternative sérieuse pour les patients ne bénéficiant pas de donneur HLA géno-identique [6, 7] (→).
(→) Voir l’Éditorial de M. Cavazzana-Calvo et al., m/s n° 2, février 2010, page 115
Les résultats à moyen terme du premier patient traité viennent d’être publiés [8]. La stratégie retenue est celle d’un transfert de gène ex vivo dans les cellules souches hématopoïétiques. Le gène introduit est un variant du gène de l’hémoglobine A, modifié pour prévenir sa polymérisation (βA 87 Thr : Gln [βA-T87Q]) [9] (→). Cette modification empêche les contacts latéraux nécessaires à la polymérisation de l’hémoglobine S résiduelle [10].
(→) Voir la Brève de L. Coulombel, m/s n° 2, février 2002, page 156
Par opposition aux vecteurs β rétroviraux utilisés dans les premiers essais de thérapie génique ayant conduit à une mutagénèse d’insertion, le vecteur est, dans le cas présent, dérivé d’un lentivirus qui a la capacité de s’insérer au hasard dans les régions de transcription active plutôt qu’à proximité des promoteurs avec un biais en faveur des gènes « dangereux ». De plus, cette deuxième génération de vecteur est caractérisée par l’inactivation de la région amplificatrice du LTR (long terminal repeat) viral et est, par conséquent, inactive par elle-même, d’où son nom « self-inactive » [9, 11] (→). La collecte de cellules souches hématopoïétiques pour le transfert ex vivo est réalisée conventionnellement sous anesthésie générale et ponctions médullaires multiples au niveau des crêtes iliaques. La réinjection des cellules autologues modifiées est précédée d’une chimiothérapie myélo-ablative par busulfan qui induit une phase d’aplasie d’environ un mois. Contrairement à une allogreffe, le conditionnement est dépourvu, en pré et post-greffe, de tout immunosuppresseur puisqu’il n’y a, en situation autologue, ni risque de rejet, ni risque de réaction du greffon contre l’hôte (GvHD). Le transgène est détecté dès la sortie d’aplasie et reste stable dans la totalité des neutrophiles, avec un recul de 18 mois. La production de l’hémoglobine thérapeutique (identifiable par sa mutation anti-polymérisation) est détectée parallèlement (Figure 1) pour se stabiliser à environ 50 %, c’est à dire à égalité avec la production résiduelle d’hémoglobine S. Cliniquement, ce mélange d’hémoglobines (équivalent à celui d’une personne hétérozygote) permet la disparition de tous les symptômes cliniques et biologiques de la maladie : indépendance transfusionnelle, absence de symptôme de vasculopathie. Une série de marqueurs fonctionnels érythrocytaires confirme l’efficacité de l’hémoglobine thérapeutique : déformabilité, densité, profil des courbes de désoxygénation (Figure 2).
(→) Voir la Synthèse de A. Rossi et A. Salvetti, m/s n° 2 février 2016, page 167
| Figure 1.
Greffe avec des cellules modifiées et expression du gène thérapeutique chez le patient. A. Nombre de copies de vecteurs présentes dans les cellules nucléées du sang et les neutrophiles CD15+ à courte durée de vie pendant les 15 mois suivant la transduction des progéniteurs CD34+. Les valeurs initiales dans ces cellules, avant la perfusion, sont indiquées sur la partie gauche. B. Taux d’hémoglobines totaux et spécifiques de chaque fraction, calculés à partir des résultats d’une analyse HPLC (high-performance liquid chromatography). La contribution de chaque type d’hémoglobine au cours du 15e mois est également indiquée. Le niveau d’hémoglobine A (HbA) est la conséquence des perfusions de globules rouges reçues par le patient avant le traitement de thérapie génique et au début de celui-ci (jusqu’au jour 88). HbA2 est une hémoglobine adulte ne provenant pas des transfusions. HbF : hémoglobine fœtale ; HbS : hémoglobine falciforme (figure adaptée de [8]). |
| Figure 2.
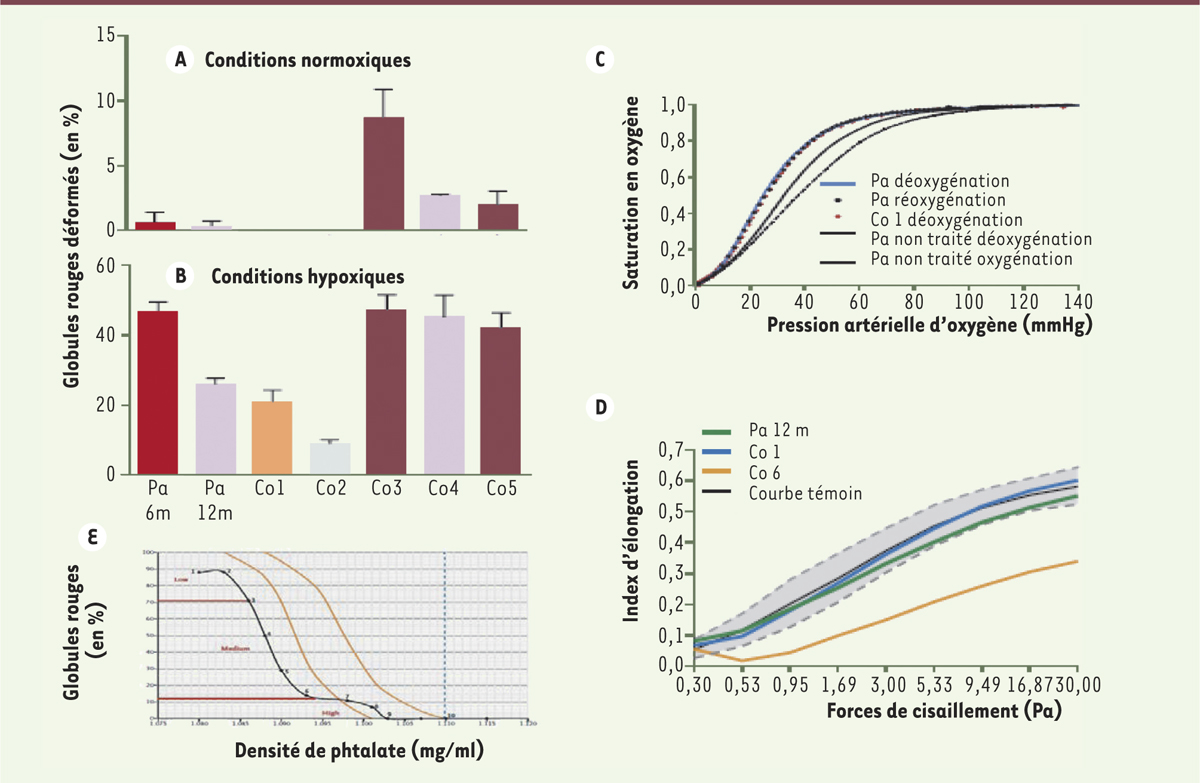
Résultats des tests de globules rouges spécifiques à une maladie falciforme. A. Taux de globules rouges déformés (en forme de faucille) en conditions normoxiques (20 % de saturation en oxygène). B. Taux de globules rouges déformés en conditions hypoxiques (10 % de saturation en oxygène) chez le patient, 6 (Pa 6m) et 12 mois (Pa 12m) après la thérapie génique. Comparaison avec des prélèvements témoins de patients soit hétérozygotes pour l’hémoglobine A/S (HbS ou hémoglobine faucille ; contrôles Co1 et Co2 ; le prélèvement 1 étant celui de la mère du patient), soit porteurs de la maladie (contrôles Co3 à Co5). Les barres représentent l’erreur standard. C. Courbe de dissociation de l’oxygène des globules rouges du patient, 12 mois après la thérapie génique à comparer à celle de sa mère (patient hétérozygote HbA/S, contrôle 1 [Co1]). Des courbes moyennes de déoxygénation des globules rouges (ligne continue) et de leur réoxygénation (ligne discontinue) sont obtenues en prélevant 15 patients porteurs de la maladie et n’ayant pas bénéficié du traitement. D. La capacité de déformation des globules rouges du patient, 12 mois après la thérapie, est comparée à celles des globules rouges de la mère (HbA/S) et d’un autre patient porteur de la maladie (contrôles Co1 et Co6, respectivement). 95 % des globules rouges de patients sains sont dans la zone grisée, la moyenne étant représentée par la courbe noire. L’index d’élongation est le rapport entre la longueur A et la largeur B de la cellule, calculé par la formule (A-B)/(A+B), sa valeur varie entre 0 et 1. E. Densité de globules rouges chez le patient, un an après la thérapie génique. Cette estimation est réalisée sur 10 prélèvements et en utilisant un gradient de phtalate. Les lignes oranges indiquent la limite d’un profil normal. Les valeurs mesurées pour le patient sont inférieures en raison de la suppression d’un seul gène d’α-globine (figure adaptée de [8]). |
Cette première observation apporte « la preuve de concept » que le transfert ex vivo du gène de l’hémoglobine A dans les cellules souches hématopoïétiques permet de corriger toutes les complications liées à la polymérisation de l’hémoglobine S et ses conséquences vasculaires. L’évaluation doit être poursuivie sur un plus grand nombre de patients et étudiée sur le long terme pour s’assurer de la stabilité de la production des cellules modifiées et, bien sûr, de l’absence d’effets adverses. Cette avancée thérapeutique ouvre ainsi des perspectives pour les patients ne bénéficiant pas d’un donneur HLA identique et, à terme, pour ceux résidant dans un pays dans lequel la réalisation d’une allogreffe de moelle osseuse n’est pas possible, ce processus étant éminemment plus complexe que celui d’une autogreffe. Des progrès substantiels sont attendus en ce qui concerne les modalités du conditionnement et du recueil de cellules souches, et sur l’automatisation du procédé afin de rendre plus aisée sa diffusion à tous les pays confrontés à cette maladie dévastatrice.