| |
| Med Sci (Paris). 2014 March; 30(3): 244–246. Published online 2014 March 31. doi: 10.1051/medsci/20143003008.Cholestérol, activité neuronale et maladie d’Alzheimer Nathalie Pierrot1 and Jean-Noël Octave1* 1Université catholique de Louvain, Institute of neuroscience, avenue Hippocrate 54, Bte 1.5410, B-1200Bruxelles, Belgique MeSH keywords: Maladie d'Alzheimer, étiologie, métabolisme, Précurseur de la protéine bêta-amyloïde, pharmacologie, Animaux, Cholestérol, physiologie, Humains, Inhibiteurs de l'hydroxyméthylglutaryl-CoA réductase, Neurones, Protéines de liaison à l'élément de régulation des stérols |
Récemment, Alzheimer’s disease international annonçait qu’en 2013, le nombre de personnes atteintes de démence dans le monde est estimé à 44 millions. Les chiffres atteindraient 76 millions en 2030 et 135 millions d’ici 2050 [
1]. La maladie d’Alzheimer (MA) est la principale cause de démence et se caractérise, d’un point de vue neuropathologique, par la coexistence dans le cerveau des plaques séniles et des dégénérescences neurofibrillaires. Les plaques séniles sont des lésions extracellulaires contenant un noyau de peptide amyloïde β (Aβ) provenant du clivage de son précurseur appelé amyloid precursor protein (ou APP). Bien que le métabolisme cellulaire permettant le clivage de l’APP en peptide Aβ ait été étudié en détail, la fonction de l’APP reste encore très mal connue. La méta-analyse de la séquence de dizaines de milliers d’échantillons d’ADN a permis récemment de confirmer et d’identifier de nouveaux facteurs de risques génétiques de développer la maladie d’Alzheimer [
2], parmi lesquels l’allèle ε4 du gène codant l’apolipoprotéine E [
11], principal transporteur du cholestérol dans le cerveau, ainsi que plusieurs nouveaux gènes codant des protéines jouant un rôle important dans le transport, l’approvisionnement, le stockage et l’hydroxylation du cholestérol. Ces données suggèrent clairement qu’une perturbation de l’homéostasie du cholestérol peut favoriser le développement de la maladie d’Alzheimer. La fonction de l’APP étant mal connue, cette protéine pourrait-elle contrôler l’homéostasie du cholestérol neuronal ? |
APP inhibe l’HMG-CoA réductase via une interaction avec SREBP Dans des neurones en culture, une légère expression d’APP diminue considérablement la biosynthèse du cholestérol [
3]. Le mévalonate, précurseur du cholestérol, est produit par réduction du 3-hydroxy-3-méthylglutarylcoenzyme A (HMG-CoA), réaction catalysée par l’HMG-CoA réductase (HMGCR). L’expression neuronale d’APP inhibe la transcription du gène codant l’HMGCR. À l’inverse, une diminution de l’expression d’APP endogène augmente la transcription du gène HMGCR, et par conséquent la synthèse neuronale de cholestérol. Les travaux de Brown et Goldstein ont démontré que l’homéostasie cellulaire du cholestérol est contrôlée par une famille de facteurs de transcription membranaires appelés collectivement sterol regulatory element binding protein (ou SREBP) [
4]. Les protéines SREBP sont localisées dans la membrane du réticulum endoplasmique (RE) et formées de deux domaines transmembranaires. En réponse à une diminution du cholestérol intracellulaire, SREBP est acheminée du RE vers l’appareil de Golgi pour être clivée séquentiellement par deux protéases, conduisant à la libération du domaine amino-terminal de SREBP dans le cytosol. Ce fragment mSREBP – qui appartient à la famille des facteurs de transcription de type hélice-boucle-hélice – migre vers le noyau pour activer la transcription de différents gènes cibles, dont le gène HMGCR. Dans les neurones, au niveau de l’appareil de Golgi, il y a interaction entre SREBP et APP. Si l’APP est en léger excès, SREBP n’est plus clivée en mSREBP, et la transcription du gène HMGCR et, par conséquent, la biosynthèse de cholestérol sont inhibées. À l’inverse, si l’APP est en défaut, le clivage de SREBP, la transcription du gène HMGCR et la biosynthèse de cholestérol sont augmentés [3]. Les astrocytes jouent un rôle majeur dans la production de cholestérol par le système nerveux central. Néanmoins, l’APP, beaucoup moins présent au niveau de l’appareil de Golgi des astrocytes, n’y interagit pas avec SREBP, ne modifie pas son clivage ni la transcription du gène HMGCR. L’APP régule donc la biosynthèse du cholestérol spécifiquement dans les neurones [3]. |
APP contrôle le renouvellement du cholestérol dans les neurones Bien qu’une inhibition spectaculaire de la biosynthèse de cholestérol soit observée dans des neurones exprimant l’APP, les taux de cholestérol membranaire restent inchangés [3]. Ces observations paradoxales, voire contradictoires, pourraient s’expliquer par une demi-vie très longue du cholestérol. Dans le cerveau, le cholestérol de la substance blanche est métaboliquement très stable avec une demi-vie de plusieurs mois [
5]. Néanmoins, les neurones sont les seules cellules qui synthétisent la 24-cholestérol hydroxylase, capable d’hydroxyler le cholestérol en 24S-hydroxycholestérol [
6]. Dès lors, l’équilibre entre biosynthèse et hydroxylation du cholestérol par les neurones est à l’origine d’un renouvellement du cholestérol neuronal particulièrement rapide et efficace. Dans les neurones, l’APP contrôle non seulement la transcription du gène HMGCR, mais également celle du gène CYP46A1 codant la 24-cholestérol hydroxylase. L’APP contrôle donc biosynthèse et hydroxylation du cholestérol, et par conséquent le turnover du cholestérol neuronal. |
Connexion entre la perte d’activité neuronale et l’inhibition du turnover du cholestérol dans les neurones de la maladie d’Alzheimer Après une période de différenciation, les neurones en culture forment des réseaux exprimant une activité neuronale caractérisée par des oscillations calciques spontanées et synchrones. Ces oscillations reflètent la dépolarisation périodique des neurones en réponse à l’influx de calcium extracellulaire résultant de l’activation des récepteurs 2-amino-3-(3-hydroxy-5-méthyl-isoxazol-4-yl) propionate (AMPA), N-méthyl-D-aspartate (NMDA), acide gamma-aminobutyrique (GABAa) et de l’activation concomitante des canaux calciques dépendants du voltage de type-L (CCDVL). In vivo, cette synchronisation joue un rôle crucial dans l’établissement, la coordination et le renforcement des connexions synaptiques au sein d’un réseau neuronal, contribuant à l’établissement des processus d’apprentissage et de mémorisation. L’expression d’APP dans environ 10 % des neurones d’un réseau provoque une entrée de calcium par les CCDVL dans ces neurones, ce qui active ensuite les canaux potassiques sensibles au calcium (canaux SK) [
7], provoquant une hyperpolarisation membranaire et la perte des oscillations calciques. Un léger excès d’APP dans les neurones induit donc à la fois la perte d’activité neuronale et l’inhibition du turnover du cholestérol (Figure 1). Ces deux effets de l’APP semblent être connectés. En effet, l’inhibition de l’activité HMGCR par la mévastatine provoque la perte des oscillations calciques [3]. L’activité neuronale inhibée par la mévastatine ou par l’APP est restaurée par le géranylgéraniol produit lors de la stimulation du turnover du cholestérol [3]. L’ensemble de ces résultats démontre donc que le turnover du cholestérol est nécessaire à l’activité neuronale.
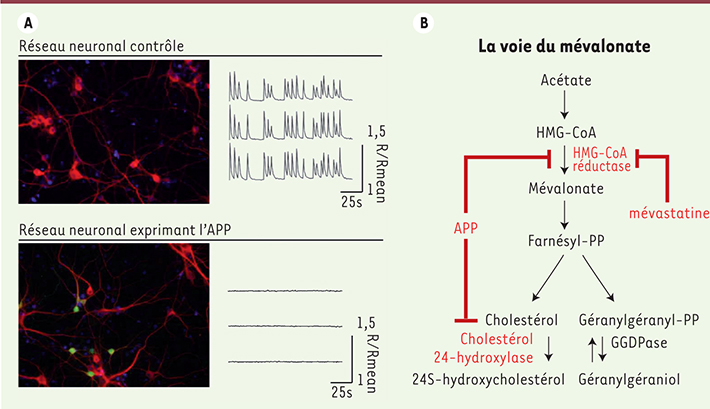
 | Figure 1.
L’expression d’APP dans les neurones conduit à la perte d’activité neuronale en inhibant le turnover du cholestérol. A. Inhibition de l’activité neuronale. Les neurones en culture forment un réseau (rouge) ayant une activité neuronale caractérisée par des oscillations calciques spontanées et synchrones. Cette activité est totalement inhibée suite à l’expression de l’APP (vert) dans les neurones. B. Cibles de l’APP sur la voie de biosynthèse du cholestérol. L’HMG-CoA réductase (3-hydroxy-3-méthylglutaryl-coenzyme A réductase), enzyme essentielle à la biosynthèse du cholestérol, et la 24 cholestérol hydroxylase, enzyme hydroxylant le cholestérol en 24S-hydroxycholestérol, assurent le turnover du cholestérol. L’HMG-CoA réductase est inhibée par les statines, dont la mévastatine, mais aussi après expression neuronale de l’APP. Le farnésyl disphosphate (farnésyl-PP), le géranylgéranyl disphosphate (géranylgéranyl-PP) et le géranylgéraniol sont produits lors de la stimulation du turnover du cholestérol. GGDPase : géranylgéranyl disphosphatase. |
Le cholestérol cérébral, qui représente 20 % du cholestérol corporel, est produit in situ étant donné l’imperméabilité de la barrière hémato-encéphalique [
8]. En cas d’excès, le cholestérol cérébral est hydroxylé en 24S-hydroxycholestérol, capable de traverser la barrière hémato-encéphalique pour être éliminé par le foie. Chez les patients atteints de la maladie d’Alzheimer, une surcharge en cholestérol cérébral [
9] et une diminution de la concentration en 24S-hydroxycholestérol plasmatique [
10] sont le reflet d’une inhibition du turnover du cholestérol cérébral qui semble être essentiel à l’activité neuronale. En résumé, l’APP contrôle le turnover du cholestérol nécessaire à l’activité neuronale. Cette fonction physiologique de l’APP pourrait être la cible de traitements pharmacologiques visant à stimuler le turnover du cholestérol cérébral et ainsi à restaurer les dysfonctionnements synaptiques observés dans la maladie d’Alzheimer. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
1.
Alzheimer’s Disease International . Policy brief for heads of government: the global impact of dementia 2013–2050 . London: : ADI, décembre;
2013. 2.
Lambert
JC
,
Ibrahim-Verbaas
CA
,
Harold
D
, et al.
Meta-analysis of 74, 046 individuals identifies 11 new susceptibility loci for Alzheimer’s disease . Nat Genet.
2013; ; 45 : :1452.–1458. 3.
Pierrot
N
,
Tyteca
D
,
D’Auria
L
, et al.
Amyloid precursor protein controls cholesterol turnover needed for neuronal activity . EMBO Mol Med.
2013; ; 5 : :608.–625. 4.
Brown
MS
,
Goldstein
JL
. A proteolytic pathway that controls the cholesterol content of membranes, cells, and blood . Proc Natl Acad Sci USA.
1999; ; 96 : :11041.–11048. 5.
Bjorkhem
I
,
Lutjohann
D
,
Diczfalusy
U
, et al.
Cholesterol homeostasis in human brain: turnover of 24S-hydroxycholesterol and evidence for a cerebral origin of most of this oxysterol in the circulation . J Lipid Res.
1998; ; 39 : :1594.–1600. 6.
Lund
EG
,
Guileyardo
JM
,
Russell
DW
. cDNA cloning of cholesterol 24-hydroxylase, a mediator of cholesterol homeostasis in the brain . Proc Natl Acad Sci USA.
1999; ; 96 : :7238.–7243. 7.
Santos
SF
,
Pierrot
N
,
Morel
N
, et al.
Expression of human amyloid precursor protein in rat cortical neurons inhibits calcium oscillations . J Neurosci.
2009; ; 29 : :4708.–4718. 8.
Turley
SD
,
Burns
DK
,
Rosenfeld
CR
,
Dietschy
JM
. Brain does not utilize low density lipoprotein-cholesterol during fetal and neonatal development in the sheep . J Lipid Res.
1996; ; 37 : :1953.–1961. 9.
Lazar
AN
,
Bich
C
,
Panchal
M
,
Desbenoit
N
, et al.
Time-of-flight secondary ion mass spectrometry (TOF-SIMS) imaging reveals cholesterol overload in the cerebral cortex of Alzheimer disease patients . Acta Neuropathol.
2013; ; 125 : :133.–144. 10.
Hughes
TM
,
Rosano
C
,
Evans
RW
,
Kuller
LH
. Brain cholesterol metabolism, oxysterols, and dementia . J Alzheimer Dis.
2013; ; 33 : :891.–911. 11.
Gosselet
F
. Apolipoprotéine E et intégrité de la barrière hémato-encéphalique . Med Sci (Paris).
2012; ; 28 : :920.–923. |