| |
| Med Sci (Paris). 2013 August; 29(8-9): 800–806. Published online 2013 September 5. doi: 10.1051/medsci/2013298021.Le microbiote intestinal à l’origine de nouvelles perspectives thérapeutiques pour les maladies métaboliques ? Rémy Burcelin,1,2* Chantal Chabo,1,2,3 Vincent Blasco-Baque,1,2 Matteo Sérino,1,2 and Jacques Amar1,2,4 1Inserm U1048, Institut des maladies métaboliques et cardiovasculaires (I2MC), hôpital Rangueil, BP 84225, 31432Toulouse Cedex, France 2Université de Toulouse Paul Sabatier, Institut de médecine moléculaire de Rangueil (I2MR), IFR31, 31432Toulouse Cedex 4, France 3Vaiomer SAS, Prologue Biotech, Labège Innopole, 31670Labège, France 4Département de thérapeutique, hôpital Rangueil, 31432Toulouse, France. |
De l’origine de la symbiose hôte microbiote aux maladies métaboliques
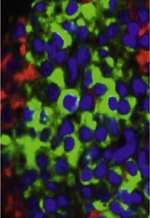
L’ensemble des cœlomates possèdent une cavité interne définissant le tractus digestif recouvert d’un épithélium qui abrite un symbionte appelé microbiote. Cependant, il n’en a pas été toujours ainsi. Les procaryotes, du grec signifiant « avant le noyau », ont été datés d’environ 3,5 milliards d’années [
1] (Figure 1). Ces bactéries primitives, qui font partie du domaine des Archaea, existaient donc bien avant le développement des espèces supérieures multi-organiques. Principalement anaérobies, les ancêtres des bactéries ont dû trouver un refuge lors de la production des premières molécules d’oxygène par les algues, puis les plantes [
2]. Elles ont alors vu, en l’apparition des premiers cœlomates, une opportunité unique d’être protégées contre l’oxydation mortelle de la nouvelle atmosphère. Cependant, c’est leur évolution en « bactéries vraies » possédant une paroi épaisse contenant du peptidoglycane qui leur a permis de parfaire leur équilibre symbiotique avec l’hôte, car résistant alors aux contraintes physicochimiques conférées par l’hôte [
3]. L’hôte a ainsi évolué afin d’établir une relation symbiotique avec les bactéries. Le microbiote constitué de plus de mille milliards de cellules vit en étroite collaboration fonctionnelle avec l’hôte. Il contribue à son développement biologique dès la naissance, le protège contre les pathogènes et l’informe des changements qualitatif et quantitatif de son alimentation [
4]. Certaines Archaea ont alors été endosymbiosées et ont abouti à la génération des mitochondries lorsque, il y a 1,5 à 2 milliards d’années, l’atmosphère primitive s’est enrichie en oxygène [
5,
6] (Figure 1). Ces mitochondries représentent la centrale énergétique de la cellule et assurent la biosynthèse de l’ATP. Ainsi, puisque le lien énergétique entre procaryotes et eucaryotes existe depuis plusieurs milliards d’années, il est intuitivement concevable que les bactéries soient, depuis tout temps, des régulateurs essentiels de notre métabolisme énergétique. Une perturbation dans l’écologie microbienne intestinale pourrait être à l’origine soit d’adaptations métaboliques bénéfiques, si ces changements sont coordonnés avec l’hôte, soit de perturbations de l’homéostasie énergétique, si la modification du microbiote n’est pas en harmonie avec le patrimoine génétique de l’hôte (Figure 1). Cette analyse suggère alors que l’identification des relations entre le microbiote et les maladies métaboliques puisse apporter des réponses moléculaires quant au développement pandémique des maladies métaboliques [
7].
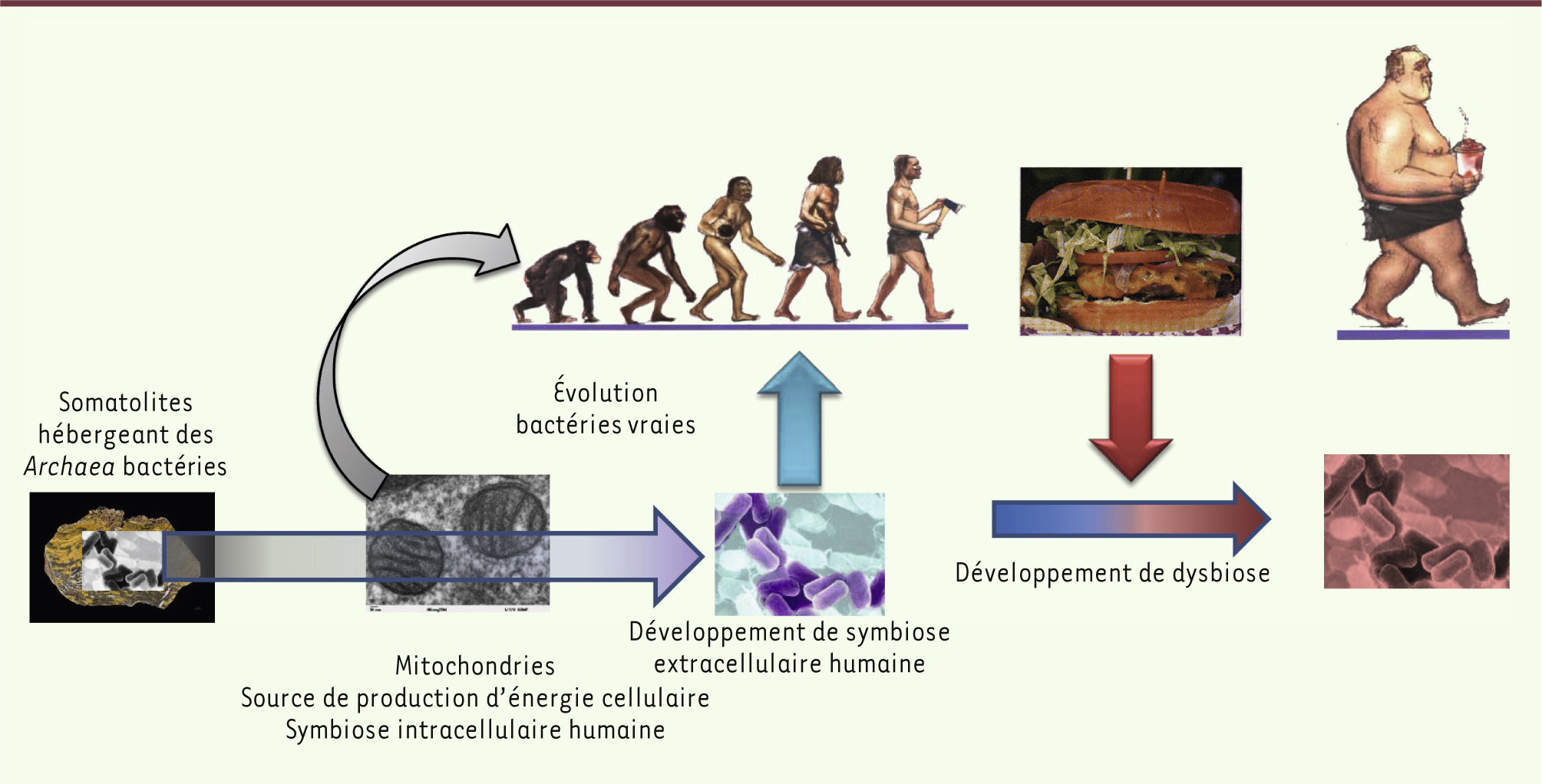
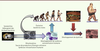 | Figure 1.
Évolution symbiotique des bactéries et de l’homme. Les très anciens stromatolithes abritaient des bactéries appelées Archea baccteria. Leur évolution endosymbiotique dans les cellules eucaryotes a permis la création de mitochondries, véritables centrales électriques pour les cellules et a ainsi favorisé le développement de l’homme. Une symbiose extracellulaire existe aujourd’hui avec l’ensemble des épithéliums qui, lors de stress nutritionnels, pourrait évoluer en dysbiose. |
|
Les maladies métaboliques et le microbiote : un état de fait et des hypothèses Cette pandémie, nourrie par les modifications des habitudes alimentaires, représente un défi pour le système de santé. En effet, elle a comme conséquence une augmentation des cas d’insuffisance rénale, d’infarctus du myocarde, d’insuffisance cardiaque et d’accidents vasculaires cérébraux [7]. La cause de cette incidence pourrait être l’inadaptation du génome humain aux conditions nutritionnelles, comportementales et sociétales actuelles. Le lien entre ces changements et le génome pourrait être le microbiote intestinal [
8]. La contribution du microbiote concernerait également l’athérosclérose [
9]. La particularité importante de ce microbiote est son caractère familial. Partiellement héréditaire, il pourrait expliquer la pandémie [
10,
11]. Chez l’animal, les premières démonstrations du rôle causal du microbiote intestinal sur le développement du diabète de type 2 et de l’obésité furent rapportées par Backhed en 2004 [
12]. Cet auteur montra que des souris totalement dépourvues de bactéries, appelées axéniques, ne prennent pas de poids en réponse à un régime obésogène et que le développement du tissu adipeux est extrêmement restreint. À l’inverse, la colonisation de ces mêmes souris par le microbiote issu d’une souris obèse induisait chez les premières un gain de poids important [
13]. Le mécanisme associé pourrait, en partie, être expliqué par une capacité accrue du microbiote des souris obèses à augmenter l’efficacité énergétique (Figure 2). Des bactéries caractéristiques de ce microbiote pourraient être responsables de la digestion de fibres indigestibles par l’hôte dont les résidus de digestion, tels que les acides gras à chaînes courtes et volatils, pourraient être alors assimilés par l’hôte. Les bactéries responsables ne sont pas connues, mais pourraient être en lien avec l’augmentation du phylum des Firmicutes par rapport à celui des Bacteroidetes. Ces deux phylums représentent 80-90 % de l’ensemble des espèces présentes dans l’intestin, et leur rôle est prépondérant. Le séquençage récent par des techniques assurant un très haut débit a permis au consortium européen MetaHIT (Metagenomics of the human intestinal tract) de réaliser le premier catalogue du génome bactérien intestinal [
14]. Une analyse précise montre que le microbiome est composé de plus de 4 millions de gènes différents composant plus de 1 500 espèces. Chaque individu ne possédant que 100-200 espèces différentes, il existe un microbiote consensuel entre tous les individus de la planète quel que soit leur genre, leur origine et leur pays, qui est formé d’une petite quinzaine d’espèces bactériennes. De manière importante, il est actuellement possible de classifier les individus en fonction de la prévalence de deux à trois groupes bactériens, parmi lesquels les Ruminococcus, les Prévotella, et les Bacteroidetes. Ainsi, chaque individu possède son propre microbiote qui s’est progressivement mis en place depuis la première colonisation maternelle à la naissance [10], puis a subi une série de variations, notamment au cours de la transition allaitement-sevrage, sous l’influence du régime alimentaire à l’âge adulte [
15], lors de la grossesse [
16], puis lors du vieillissement [
17]. À l’image de la transmission du phénotype métabolique de prise de poids observé lors de la colonisation de souris axéniques par le microbiote d’une souris obèse [13], il est ainsi envisageable que le développement futur des maladies métaboliques puisse avoir pour origine la mise en place d’un microbiote obésogène et diabétogène au cours des premières années de la vie. Cette programmation du métabolisme pourrait alors être contrôlée par la mise en place de stratégies nutritionnelles adaptées à base de pré- et probiotiques, notamment pour ce qui concerne les nouveau-nés prématurés ou nés par césarienne, dont le microbiote est caractérisé par une augmentation notamment des Firmicutes [
18,
19], considérés comme obésogènes [13,
20]. À l’âge adulte, la découverte de traits métagénétiques spécifiques des maladies métaboliques est une révolution conceptuelle importante [
21]. Des groupes de gènes bactériens seraient associés avec non seulement l’obésité, mais également le diabète de type 2. Il est ainsi possible de définir des biomarqueurs, capables de diagnostiquer mais également de prédire l’apparition des maladies métaboliques et l’altération des fonctions physiologiques, telles que la résistance à l’insuline [
22], par l’analyse du métagénome intestinal. Ces gènes bactériens caractéristiques définissent notamment des fonctions métaboliques de fermentation variées [21].
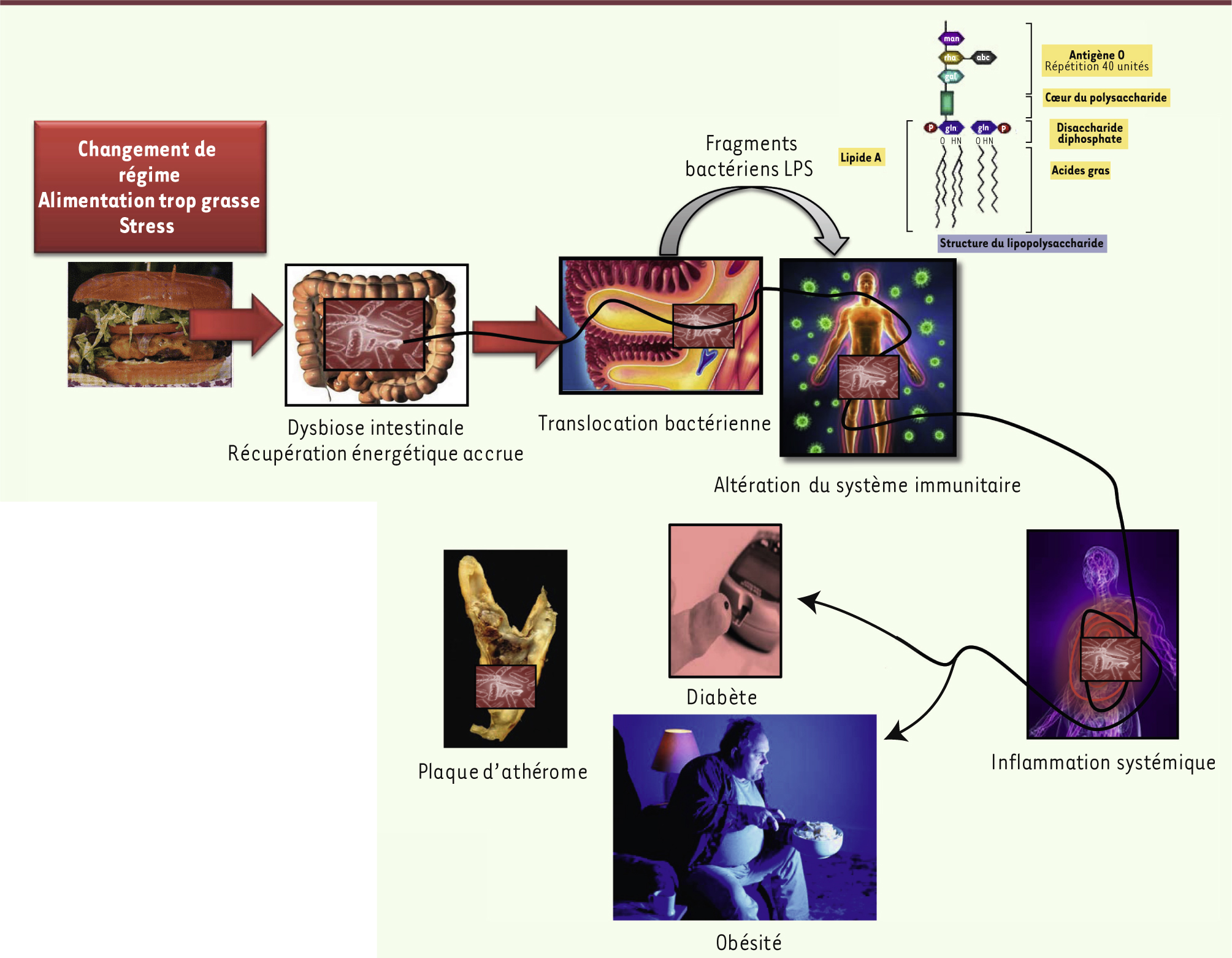
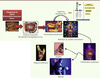 | Figure 2.
De la dysbiose intestinale aux maladies métaboliques. Un changement de régime, notamment riche en graisses, induit une dysbiose intestinale qui favorise la pullulation de bactéries capables d’augmenter la récupération énergétique et, ainsi, d’amener chez l’hôte un excès d’énergie. D’autre part, cette dysbiose se traduit par une augmentation de l’absorption de molécules bactériennes de type lipopolysaccharidiques (LPS) qui sont hautement inflammatoires pour l’organisme. Un nouveau mécanisme a été découvert qui montre qu’une partie du microbiote intestinal pourrait subir une translocation vers les tissus de l’organisme. Le système immunitaire est impliqué dans la reconnaissance de ces bactéries nouvellement présentes dans l’organisme, et dans l’initiation d’une réaction inflammatoire de type métabolique contribuant au développement du diabète de type 2 et de l’obésité, et à la production des plaques d’athérome. |
Une autre découverte plus récente concerne l’identification d’un métagénome présent dans les tissus de l’hôte [
23]. Il existe des fragments d’ADN bactériens circulant dans le sang chez l’homme. Ils sont issus principalement de Protéobactéries à 80-90 % et de Bacteroidetes à 10-20 % [
24]. Une augmentation de la concentration de l’ADN bactérien permet de prédire l’apparition d’un diabète de type 2 plus de six années avant le diagnostic de la maladie [24]. Cela suggère qu’une dysbiose tissulaire pourrait être un facteur contributif important du diabète de type 2 (Figure 2). Il en va de même en ce qui concerne la prédiction des événements cardiovasculaires par la quantification d’autres biomarqueurs d’origine bactérienne dans le sang [
25]. Ainsi, une relation de causalité est suspectée. Le microbiote tissulaire a également été caractérisé dans le tissu adipeux de souris [23] et pourrait contribuer à l’inflammation métabolique qui caractérise ce tissu, notamment par l’augmentation du nombre de macrophages et de cellules lymphocytaires [
26,
27,
48] (→).
(→) Voir l’article de A. Carrière et al., page 729 de ce numéro
Certaines de ces bactéries tissulaires sont vivantes et peuvent être cultivées [23]. Elles appartiennent également au phylum des Protéobactéries et sont particulièrement inflammatoires, car elles possèdent des antigènes de type lipopolysaccharidiques (LPS) capables de déclencher un choc septique et une vasodilatation importante. Une augmentation de ces composés inflammatoires a été rapportée dans le sang de sujets dont l’alimentation était particulièrement riche en lipides [8-
30] (Figure 3). Ces LPS ont été considérés comme responsables de l’initiation de l’inflammation métabolique, de la résistance à l’insuline, de l’infiltration des cellules immunitaires dans les tissus (Figure 4), ainsi que de la stéatose hépatique [
31-
33]. Leurs récepteurs, CD14 et TLR4 (Toll-4 receptor), sont alors considérés comme des cibles thérapeutiques potentielles. Des antagonistes pourraient réduire l’état inflammatoire associé aux maladies métaboliques. Une augmentation du rapport bactéries à Gram négatif/bactéries à Gram positif dans les selles a été rapportée chez des souris nourries d’un régime riche en graisse [
34] ; elle pourrait être associée à la translocation de ces bactéries inflammatoires vers les tissus de l’organisme en recrutant des cellules phagocytaires capables de transporter ces bactéries vivantes ou mortes vers le tissu adipeux et le foie notamment [23] (Figure 2).
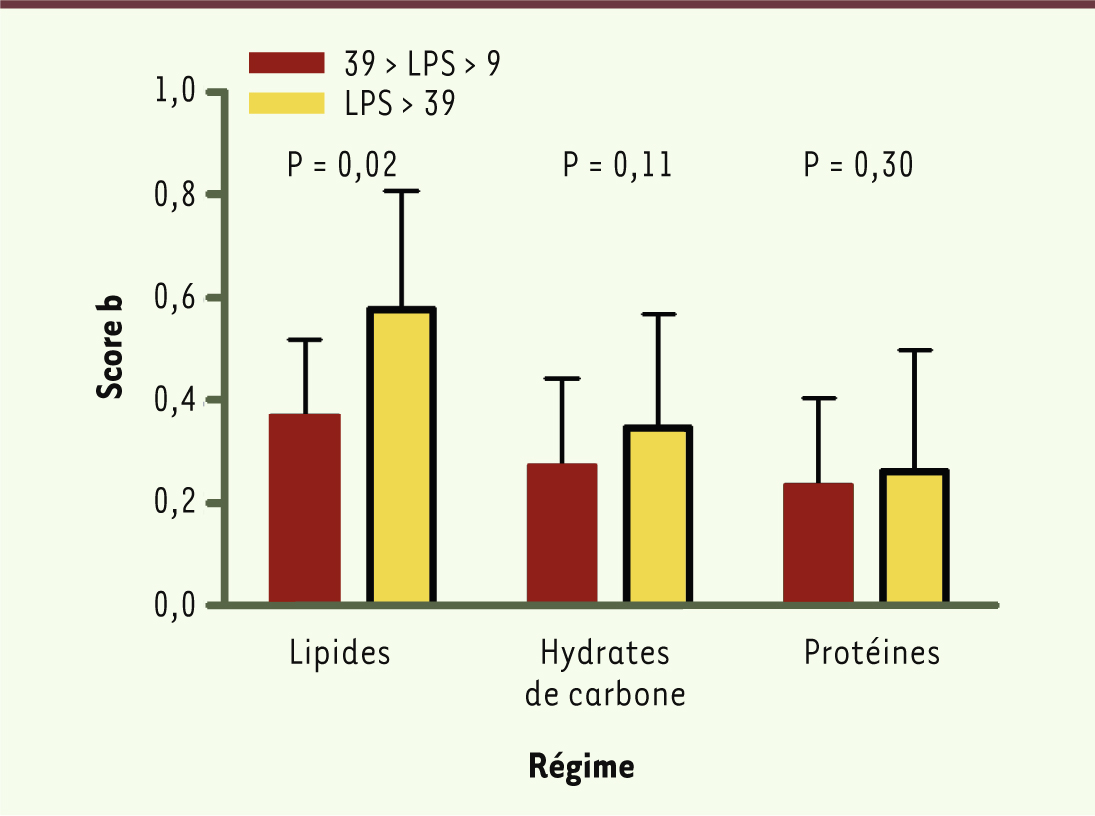
 | Figure 3.
Concentration plasmatique de LPS chez l’homme en fonction des habitudes alimentaires. La concentration plasmatique en LPS a été mesurée dans une cohorte humaine MONICA de population générale et selon le type de régime consommé durant les trois jours précédents le dosage. Les sujets ont été séparés selon qu’ils consommaient une alimentation riche en lipides, en hydrates de carbone, ou en protéines. Le score b a été calculé et est représenté. Les patients ont été séparés en deux groupes caractérisés par une concentration supérieure (colonnes jaunes) ou inférieure (colonne rouge) à 39 unités équivalents de LPS/ml (adapté de [
28]). |
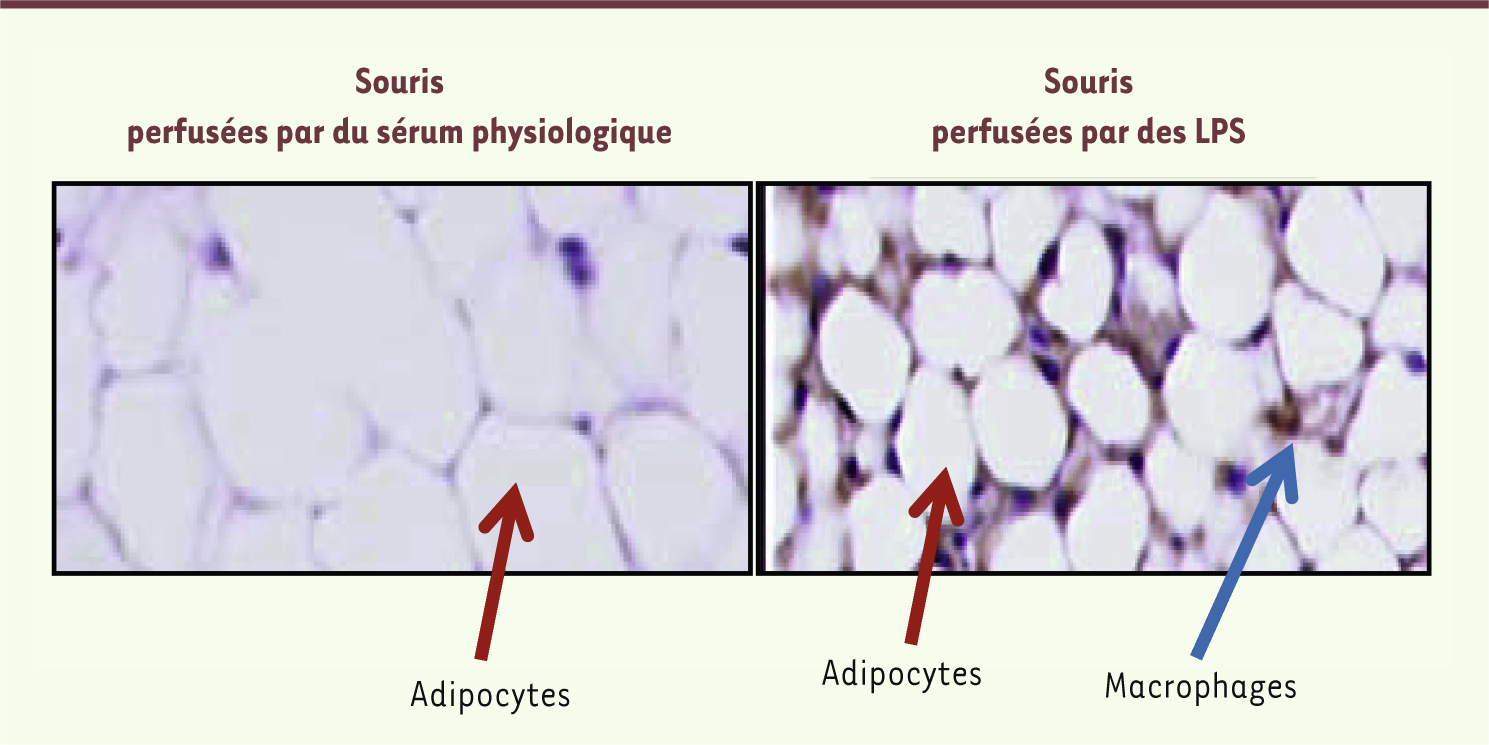
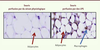 | Figure 4.
Infiltration du tissu adipeux par des cellules immunitaires du tissu adipeux de souris perfusées par des LPS. Coupes de tissus adipeux colorés par de l’hématoxiline et de l’éosine provenant de souris perfusées pendant un mois avec de faibles débits de LPS (droite) ou du sérum physiologique (gauche). Les adipocytes sont les cellules blanches. Un comarquage de cellules exprimant le marqueur de cellules immuno-inflammatoires de type macrophage (F4/80) a été réalisé et apparaît en brun. |
|
Perspectives thérapeutiques Le régime alimentaire est donc capable d’induire une dysbiose intestinale [15, 34] et tissulaire [23] pouvant contribuer au développement des maladies métaboliques [
35]. Cependant, en plus des maladies inflammatoires intestinales, d’autres maladies pourraient trouver leur origine dans le microbiote intestinal. En effet, de nombreux travaux suggèrent que l’étude de la relation hôte microbiote pourrait être à l’origine de nouvelles stratégies thérapeutiques efficaces en ciblant les origines des maladies plutôt que leurs conséquences. Des travaux récents démontrent le rôle des produits du métabolisme bactérien intestinal dans le contrôle de la pression artérielle par l’intermédiaire d’une détection quasi « olfactive » de produits bactériens d’acides gras à chaîne courte par le récepteur Olfr78 (olfactory receptor 78) des cellules spécialisées du rein [
36]. Leur rôle sur le développement de l’athérosclérose a été aussi montré, car des bactéries issues du parodonte sont retrouvées dans la plaque d’athérome [9,
37]. Ces bactéries sont particulièrement inflammatoires et semblent également interférer avec le métabolisme des lipides [37], notamment via les acides biliaires nécessaires à l’absorption des graisses [
38]. Le microbiote, dans sa fonction antigénique, contrôle également la maturation du système immunitaire et joue à ce titre un rôle important dans le diabète auto-immun de type 1 [
39] avec un effet régulateur des œstrogènes sur ces phénomènes [
40]. Les cellules immunitaires sont essentielles pour notre protection. Leur voisinage avec la plus importante source d’antigènes de l’organisme, que représente le microbiote intestinal, suggère que ces mécanismes de défense ont dû évoluer avec le microbiote [
41,
42]. Ainsi, un changement de microbiote trop rapide faisant suite à un stress nutritionnel pourrait conduire à diminuer l’efficacité des défenses intestinales [
43], favorisant la translocation d’antigènes bactériens et de bactéries entières vers les tissus de l’organisme [23]. Cette rupture d’équilibre conduirait alors à l’inflammation métabolique. En plus du système immunitaire, le microbiote contrôle l’attitude alimentaire, et l’anxiété [
44-
46]. Les informations nutritionnelles sont véhiculées également lors d’un repas par le nerf vague. Des travaux récent démontrent le rôle important du microbiote sur la transmission de ce signal jusqu’au cerveau. Enfin, le développement à la naissance du système intestinal vasculaire est aussi sous la dépendance du microbiote par un mécanisme impliquant le facteur tissulaire et le récepteur de protéase PAR1 [
47]. Le développement approprié du système vasculaire intestinal permettrait l’afflux de cellules immunitaires, mais également des nutriments et hormones, vers les tissus périphériques pour une meilleure prise en charge du métabolisme. |
Le microbiote dévoile peu à peu son rôle physiologique et son action sur des pathologies [48,
49], telles que le diabète de type 2, l’obésité, l’athérosclérose, l’auto-immunité, etc. Cependant, il reste à mettre en place des procédés permettant d’identifier les acteurs moléculaires et les « métafacteurs » du microbiote responsables du contrôle de ces fonctions physiologiques métaboliques. Il reste, d’autre part, à identifier les cibles eucaryotes de ces « métafacteurs » afin de développer des approches pharmacologiques thérapeutiques. D’un point de vue thérapeutique, cibler la relation hôte microbiote possède un avantage majeur : les cibles bactériennes représentent le milieu extérieur ! Ainsi, des fibres alimentaires prébiotiques ou des bactéries de type probiotique agissent directement sur le métagénome pour en modifier de façon bénéfique l’équilibre sans pénétrer dans l’organisme et avec, de fait, un risque plus faible de déclencher des effets indésirables. Cette approche n’est cependant pas à l’heure actuelle ciblée et spécifique. Elle ne peut aboutir à un traitement très précis. Cependant, l’analyse de nombreuses souches bactériennes permettant l’identification très précise de probiotique-prébiotique et de symbiotique pourrait conduire à établir des stratégies thérapeutiques précises selon les caractéristiques microbiotiques des patients. Il s’agirait alors de méthodes préventives, voire même thérapeutiques, ciblant une fonction donnée telle que l’inflammation métabolique. Par extension, les maladies inflammatoires buccales, telles que les parodontites, pourraient alors être traitées. Une approche pharmacologique sera envisageable dès lors que l’identification des acteurs moléculaires de l’hôte sera réalisée. La contribution jouée par le microbiote très en amont du développement des maladies métaboliques représente un atout conceptuel majeur, car les stratégies thérapeutiques basées sur sa régulation ne se limiteront non plus à traiter les conséquences de la maladie, mais pourront cibler son origine. De fait, nous sommes à l’aube d’une avancée majeure vers la médecine personnalisée. La diversité du microbiote intestinal et tissulaire devrait permettre l’identification de biomarqueurs prédictifs, stratifiant et classifiant de nombreuses pathologies susceptibles de mieux positionner les actifs thérapeutiques pour des sous-groupes de patients et ouvrir la voie à de nouvelles avenues thérapeutiques. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
1.
Knoll
AH
,
Barghoorn
ES
. Archean microfossils showing cell division from the swaziland system of South Africa . Science.
1977; ; 198 : :396.–398. 2.
Donoghue
PC
,
Antcliffe
JB
. Early life. Origins of multicellularity . Nature.
2010; ; 466 : :41.–42. 3.
Payne
JL
,
Boyer
AG
,
Brown
JH
, et al.
Two-phase increase in the maximum size of life over 3.5 billion years reflects biological innovation and environmental opportunity . Proc Natl Acad Sci USA.
2009; ; 106 : :24.–27. 4.
Nicholson
JK
,
Holmes
E
,
Kinross
J
, et al.
Host-gut microbiota metabolic interactions . Science.
2012; ; 336 : :1262.–1267. 5.
Sagan
L
. On the origin of mitosing cells . J Theor Biol.
1967; ; 14 : :255.–274. 6.
Gray
MW
,
Burger
G
,
Lang
BF.
, The origin early evolution of mitochondria . Genome Biol.
2001; ; 2 : :1018.. 7.
Shaw
JE
,
Sicree
RA
,
Zimmet
PZ
. Global estimates of the prevalence of diabetes for 2010 and 2030 . Diabetes Res Clin Pract.
2010; ; 87 : :4.–14. 8.
Holmes
E
,
Kinross
J
,
Gibson
GR
, et al.
Therapeutic modulation of microbiota-host metabolic interactions . Sci Transl Med.
2012; ; 4 : :137. rv 136. 9.
Caesar
R
,
Fak
F
,
Backhed
F
. Effects of gut microbiota on obesity and atherosclerosis via modulation of inflammation and lipid metabolism . J Intern Med.
2010; ; 268 : :320.–328. 10.
Dethlefsen
L
,
Eckburg
PB
,
Bik
EM
,
Relman
DA
. Assembly of the human intestinal microbiota . Trends Ecol Evol.
2006; ; 21 : :517.–523. 11.
Turnbaugh
PJ
,
Hamady
M
,
Yatsunenko
T
, et al.
A core gut microbiome in obese and lean twins . Nature.
2009; ; 457 : :480.–484. 12.
Backhed
F
,
Ding
H
,
Wang
T
, et al.
The gut microbiota as an environmental factor that regulates fat storage . Proc Natl Acad Sci USA.
2004; ; 101 : :15718.–15723. 13.
Turnbaugh
PJ
,
Ley
RE
,
Mahowald
MA
, et al.
An obesity-associated gut microbiome with increased capacity for energy harvest . Nature.
2006; ; 444 : :1027.–1031. 14.
Qin
J
,
Li
R
,
Raes
J
, et al.
A human gut microbial gene catalogue established by metagenomic sequencing . Nature.
2010; ; 464 : :59.–65. 15.
Turnbaugh
P
,
Ridaura
V
,
Faith
J
, et al.
The effect of diet on the human gut microbiome: A metagenomic analysis in humanized gnotobiotic mice . Sci Transl Med.
2009; ; 1 : :6.–14. 16.
Koren
O
,
Goodrich
JK
,
Cullender
TC
, et al.
Host remodeling of the gut microbiome and metabolic changes during pregnancy . Cell.
2012; ; 150 : :470.–480. 17.
Biagi
E
,
Candela
M
,
Fairweather-Tait
S
, et al.
Aging of the human metaorganism: the microbial counterpart . Age (Dordr).
2012; ; 34 : :247.–267. 18.
Barrett
E
,
Guinane
CM
,
Ryan
CA
, et al.
Microbiota diversity and stability of the preterm neonatal ileum and colon of two infants . Microbiology Open.
2013; ; 2 : :215.–225. 19.
Azad
MB
,
Konya
T
,
Maughan
H
, et al.
Gut microbiota of healthy Canadian infants: profiles by mode of delivery and infant diet at 4 months . CMAJ.
2013; ; 185 : :385.–394. 20.
Ley
RE
,
Backhed
F
,
Turnbaugh
P
, et al.
Obesity alters gut microbial ecology . Proc Natl Acad Sci USA.
2005; ; 102 : :11070.–11075. 21.
Qin
J
,
Li
Y
,
Cai
Z
, et al.
A metagenome-wide association study of gut microbiota in type 2 diabetes . Nature.
2012; ; 490 : :55.–60. 22.
Serino
M
,
Fernandez-Real
JM
,
Fuentes
EG
, et al.
The gut microbiota profile is associated with insulin action in humans . Acta Diabetol.
2012 ; DOI : 10.1007/s00592-012-0410-5
23.
Amar
J
,
Chabo
C
,
Waget
A
, et al.
Intestinal mucosal adherence and translocation of commensal bacteria at the early onset of type 2 diabetes: molecular mechanisms and probiotic treatment . EMBO Mol Med.
2011; ; 3 : :559.–572. 24.
Amar
J
,
Serino
M
,
Lange
C
, et al.
Involvement of tissue bacteria in the onset of diabetes in humans: evidence for a concept . Diabetologia.
2011; ; 54 : :3055.–3061. 25.
Amar
J
,
Lange
C
,
Payros
G
, et al.
Blood microbiota dysbiosis is associated with the onset of cardiovascular events in a large general population: the DESIR study group . PLoS One.
2013; ; 8 : :e54461.. 26.
Bouloumie
A
,
Casteilla
L
,
Lafontan
M
. Adipose tissue lymphocytes and macrophages in obesity and insulin resistance: makers or markers, and which comes first?
Arterioscler Thromb Vasc Biol.
2008; ; 28 : :1211.–1213. 27.
Bourlier
V
,
Bouloumie
A
. Role of macrophage tissue infiltration in obesity and insulin resistance . Diabetes Metab.
2009; ; 35 : :251.–260. 28.
Amar
J
,
Burcelin
R
,
Ruidavets
JB
, et al.
Energy intake is associated with endotoxemia in apparently healthy men . Am J Clin Nutr.
2008; ; 87 : :1219.–1223. 29.
Pendyala
S
,
Walker
J
,
Holt
PR
. A high-fat diet is associated with endotoxemia that originates from the gut . Gastroenterology.
2012; ; 142 : :1100.–1101. 30.
Moreira
AP
,
Texeira
TF
,
Ferreira
AB
, et al.
Influence of a high-fat diet on gut microbiota, intestinal permeability and metabolic endotoxaemia . Br J Nutr.
2012; ; 108 : :801.–809. 31.
Fiorini
RN
,
Shafizadeh
SF
,
Polito
C
, et al.
Anti-endotoxin monoclonal antibodies are protective against hepatic ischemia/reperfusion injury in steatotic mice . Am J Transplant.
2004; ; 4 : :1567.–1573. 32.
Pappo
I
,
Becovier
H
,
Berry
EM
,
Freund
HR
. Polymyxin B reduces cecal flora, TNF production and hepatic steatosis during total parenteral nutrition in the rat . J Surg Res.
1991; ; 51 : :106.–112. 33.
Chen
F
,
Liu
Y
,
Zhu
H
, et al.
Fish oil attenuates liver injury caused by LPS in weaned pigs associated with inhibition of TLR4 and nucleotide-binding oligomerization domain protein signaling pathways . Innate Immun.
2013 ; DOI : 10.1177/1753425912472003
34.
Cani
PD
,
Bibiloni
R
,
Knauf
C
, et al.
Changes in gut microbiota control metabolic endotoxemia-induced inflammation in high-fat diet-induced obesity and diabetes in mice . Diabetes.
2008; ; 57 : :1470.–1481. 35.
Burcelin
R
,
Luche
E
,
Serino
M
,
Amar
J
. The gut microbiota ecology: a new opportunity for the treatment of metabolic diseases?
Front Biosci.
2009; ; 14 : :5107.–5117. 36.
Pluznick
JL
,
Protzko
RJ
,
Gevorgyan
H
, et al.
Olfactory receptor responding to gut microbiota-derived signals plays a role in renin secretion and blood pressure regulation . Proc Natl Acad Sci USA.
2013; ; 110 : :4410.–4415. 37.
Koren
O
,
Spor
A
,
Felin
J
, et al.
Human oral, gut, and plaque microbiota in patients with atherosclerosis . Proc Natl Acad Sci USA.
2011; ; 108 : :4592.–4598. 38.
Sayin
SI
,
Wahlstrom
A
,
Felin
J
, et al.
Gut microbiota regulates bile acid metabolism by reducing the levels of Tauro-beta-muricholic acid, a naturally occurring FXR antagonist . Cell Metab.
2013; ; 17 : :225.–235. 39.
Wen
L
,
Ley
RE
,
Volchkov
PY
, et al.
Innate immunity and intestinal microbiota in the development of Type 1 diabetes . Nature.
2008; ; 455 : :1109.–1113. 40.
Markle
JG
,
Frank
DN
,
Mortin-Toth
S
, et al.
Sex differences in the gut microbiome drive hormone-dependent regulation of autoimmunity . Science.
2013; ; 339 : :1084.–1088. 41.
Hooper
LV
,
Littman
DR
,
Macpherson
AJ
. Interactions between the microbiota and the immune system . Science.
2012; ; 336 : :1268.–1273. 42.
Ivanov, II
,
Frutos Rde
L
,
Manel
N
, et al.
Specific microbiota direct the differentiation of IL-17-producing T-helper cells in the mucosa of the small intestine . Cell Host Microbe.
2008; ; 4 : :337.–349. 43.
Burcelin
R
,
Garidou
L
,
Pomie
C
. Immuno-microbiota cross and talk: The new paradigm of metabolic diseases . Semin Immunol.
2012; ; 24 : :67.–74. 44.
Bercik
P
,
Denou
E
,
Collins
J
, et al.
The intestinal microbiota affect central levels of brain-derived neurotropic factor and behavior in mice . Gastroenterology.
2011; ; 141 : :599.–609. 45.
Diaz Heijtz
R
,
Wang
S
,
Anuar
F
, et al.
Normal gut microbiota modulates brain development and behavior . Proc Natl Acad Sci USA.
2011; ; 108 : :3047.–3052. 46.
Neufeld
KA
,
Kang
N
,
Bienenstock
J
,
Foster
JA
. Effects of intestinal microbiota on anxiety-like behavior . Commun Integr Biol.
2011; ; 4 : :492.–494. 47.
Reinhardt
C
,
Bergentall
M
,
Greiner
TU
, et al.
Tissue factor and PAR1 promote microbiota-induced intestinal vascular remodelling . Nature.
2012; ; 483 : :627.–631. 48.
Carrière
A
,
Jeanson
Y
,
Cousin
B
, et al.
Le recrutement et l’activation d’adipocytes bruns et/ou BRITE : une perspective réelle pour le traitement des maladies métaboliques . Med Sci (Paris).
2013; ; 29 : :729.–735. 49.
Normand
S
,
Secher
T
,
Chamaillard
M
. La dysbiose, une nouvelle entité en médecine ?
Med Sci (Paris).
2013; ; 29 : :586.–589. |