| |
| Med Sci (Paris). 2013 August; 29(8-9): 785–790. Published online 2013 September 5. doi: 10.1051/medsci/2013298019.Petites structures - grands effets Charlotte Hinault,1,2,3 Olivier Dumortier,1,2 and Emmanuel Van Obberghen1,2,3* 1Institut de recherche sur le cancer et le vieillissement (IRCAN), CNRS UMR7284, Inserm U1081, équipe « vieillissement et diabète; », Faculté de médecine, 28, avenue de Valombrose, 06107Nice, France 2Université de Nice-Sophia Antipolis, France 3Laboratoire de biochimie, centre hospitalier universitaire, Nice, France |
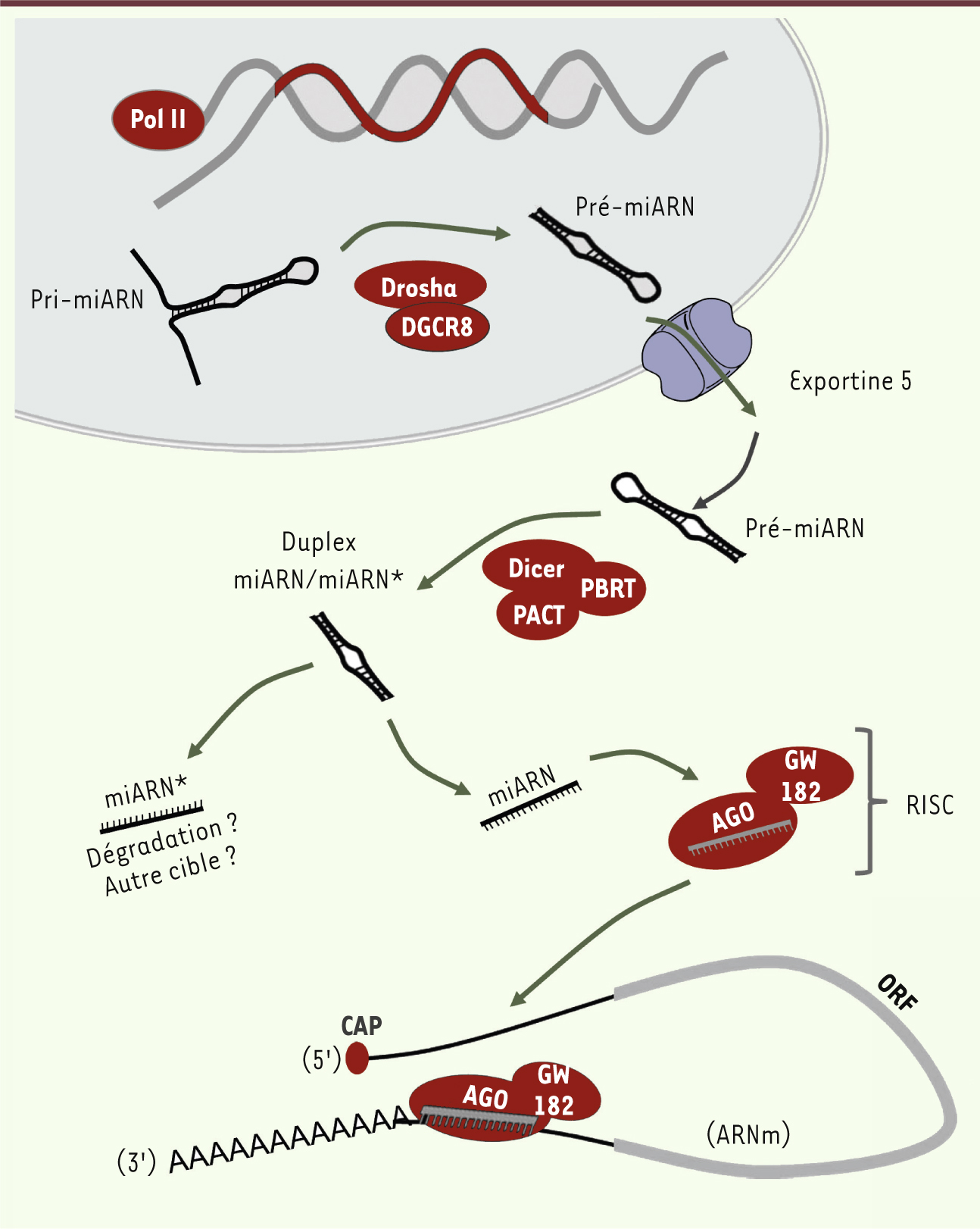
Le diabète est l’une des maladies chroniques les plus fréquentes et pose un défi majeur de santé publique. Il se caractérise par une hyperglycémie chronique due à une insuffisance pancréatique dans le cas du diabète de type 1 (DT1), et à la combinaison d’une résistance à l’insuline et d’une sécrétion insuffisante de l’hormone dans le cas du diabète de type 2 (DT2). L’étiologie du diabète comporte une composante génétique et une composante environnementale. Au cours des deux dernières décennies, une nouvelle classe d’ARN non codants, appelés microARN (miARN), s’est ajoutée aux mécanismes complexes de régulation de l’homéostasie glucidique. Les miARN forment une famille de produits géniques simple brin d’environ 20 à 22 nucléotides. Aujourd’hui, plus de mille miARN ont été identifiés chez l’homme. La plupart interagissent avec des séquences spécifiques au niveau de la partie 3’ non traduite de l’ARN (3’UTR) (Figure 1). L’appariement des miARN avec leurs ARNm cibles entraîne une répression de la traduction et/ou une dégradation de l’ARNm [
1]. Selon les prévisions bioinformatiques, environ 30 % des gènes humains pourrait être sous l’emprise des miARN. Les modifications de l’expression des miARN sont associées à de nombreuses situations pathologiques, telles que le cancer [
35], les maladies cardiovasculaires et le diabète.
 | Figure 1.
Biogenèse des miARN. Les miARN sont transcrits par l’ARN polymérase II (Pol II) sous forme d’un long transcrit primaire (pri-miARN). Ce pri-miARN est ensuite clivé par un complexe protéique, le microprocesseur, composé de l’enzyme Drosha et de son cofacteur DGCR8 (DiGeorge critical region 8). Ce clivage génère le pré-miARN, produit en épingle à cheveux d’environ 55 à 70 nucléotides. Par la suite, le pré-miARN est exporté vers le cytoplasme par le transporteur Exportine 5. Dans le cytoplasme, le précurseur est clivé par un complexe protéique composé de l’enzyme Dicer et de ses partenaires TRBP (TAR-RNA binding protein) et PACT (protein activator of PKR). Ce clivage aboutit à la formation d’un ARN double brin, d’environ 22 bases, constitué d’un miARN et d’un miARN*. En général, le miARN mature est défini comme le miARN biologiquement actif, tandis que son brin partenaire est considéré comme le brin porteur inactif, miARN* ou brin passager. Cependant, de récentes études suggèrent que miARN* pourrait avoir un impact biologique significatif et devrait donc être pris en compte lors de l’étude des miARN. Le miARN mature est ancré à une protéine Argonaute (AGO) formant le cæur du complexe multiprotéique RISC-miRNP (RNA-induced silencing complex-micro-ribonucleoprotein). Ce complexe guide ensuite le miARN vers la région 3’UTR de l’ARNm cible. L’hybridation du miARN à l’ARNm induit le blocage de la traduction et/ou la dégradation de l’ARNm. GW182 : glycine-tryptophan protein of 182 kDa ; CAP : coiffe ; ORF : open reading frame. |
Bien que la complexité des mécanismes d’action des miARN ne soit pas élucidée, des progrès importants ont été faits quant à l’identification du rôle précis de certains miARN dans des contextes biologiques définis. Nous résumerons dans cette synthèse les avancées récentes dans la compréhension du rôle des miARN dans le contrôle du métabolisme glucidique et l’apparition du diabète. |
Régulation de la sécrétion et de l’action de l’insuline par les miARN L’insuline est la seule hormone hypoglycémiante de l’organisme jouant un rôle majeur dans la régulation de l’homéostasie glucidique. La présence de l’hormone et la sensibilité des tissus cibles sont nécessaires pour générer le programme biologique approprié. Les miARN sont impliqués dans la régulation de l’expression de molécules clés régulant la sécrétion et l’action de l’insuline (Figure 2). Inversement, l’insuline module l’expression de certains miARN générant ainsi un lien fonctionnel bidirectionnel.
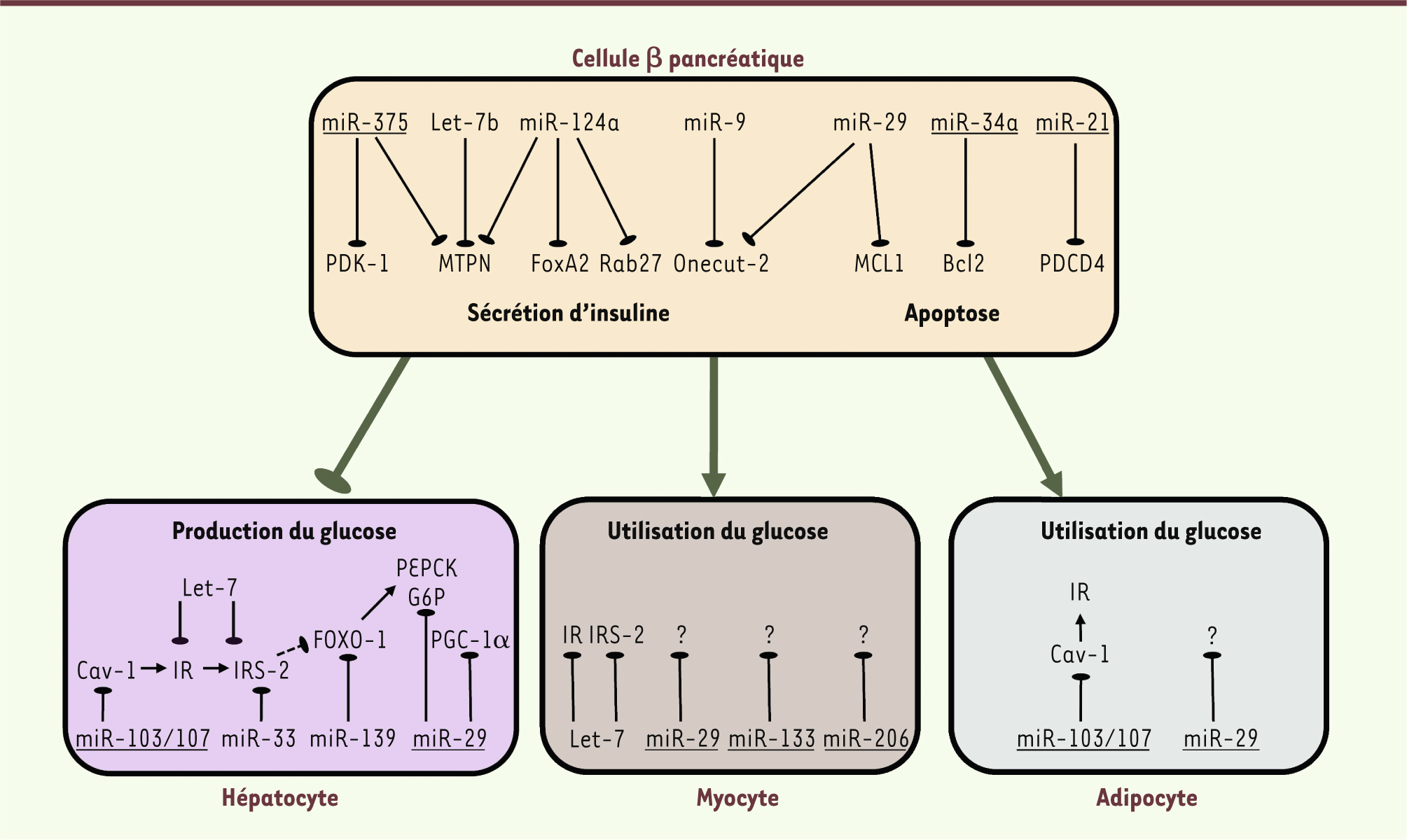
 | Figure 2.
miARN impliqués dans la sécrétion et l’action de l’insuline avec leurs cibles respectives dans les cellules sensibles à l’insuline. Les miARN impliqués dans le diabète sont soulignés. |
Le premier miARN impliqué dans la sécrétion de l’insuline est le miR-375 [
2]. En effet, l’expression forcée de ce miARN dans l’insulinome MIN6 réduit la sécrétion de l’insuline induite par le glucose en inhibant l’exocytose de l’hormone suite à son interaction avec l’ARNm de la myotrophine (MTPN)1. À l’inverse, lorsque le miR-375 est invalidé chez la souris, les cellules β sécrètent plus d’insuline en réponse au glucose [
3]. Par ailleurs, nous avons montré que le miR-375 diminue l’expression du gène de l’insuline dans l’insulinome INS-1E, et que son expression est inhibée par le glucose, faisant de miR-375 un élément régulateur important de la cellule β [
4]. miR-124a a également été décrit pour agir à différents niveaux du processus d’exocytose de l’insuline, notamment en ciblant directement MTPN [
5] et la GTPase Rab27 (member RAS oncogene family) [
6]. De plus nous avons révélé que miR-124a peut lier l’ARNm du facteur de transcription FoxA2 (forkhead box A2), un régulateur majeur du développement du pancréas, du métabolisme du glucose et de la sécrétion d’insuline [
7]. L’expression forcée de miR-124a dans la lignée MIN6 diminue la protéine FoxA2, réduisant ainsi l’expression de ses gènes cibles codant pour les protéines Kir6.2 et Sur-1 (ATP sensitive potassium channel subunit), impliquées dans la dépolarisation de la cellule β. D’autres miARN interviennent dans la régulation de la sécrétion d’insuline, comme Let-7b, ciblant également MTPN [5], et miR-96, régulant les niveaux d’ARNm et protéique de la synaptotagmin-like 4 (Sytl4), un inhibiteur de l’exocytose de l’insuline [6]. De plus, Sytl4 est régulée négativement par miR-9 via l’interaction de ce dernier avec l’ARNm du facteur de transcription Onecut-2 (one cut homeobox 2) [
8]. Enfin, les membres de la famille du miR-29 inhibent la sécrétion d’insuline en diminuant l’expression de la protéine Onecut-2 dans les cellules MIN6 et dans les cellules d’îlots dispersées [
9]. En plus d’un effet sur la sécrétion de l’insuline, les miARN régulent l’expression de nombreuses molécules capitales pour le réseau complexe de la signalisation de l’hormone. Selon une épure minimaliste, la plupart des actions métaboliques de l’insuline impliquent la PI3K (phosphatidylinositol-3 kinase) et la PKB (protein kinase B), alors que ses effets sur la différenciation et la croissance cellulaires passent par la voie MAPK (mitogen-activated protein kinase). Les miARN modulent l’expression des principaux composants des voies de signalisation de l’insuline en agissant à de multiples étapes. Par exemple, Let-7 inhibe la voie PI3K en interagissant avec les ARNm de l’IR (insulin receptor), de l’IGF1-R (insulin-like growth factor 1 receptor) et de l’IRS-2 (insulin receptor substrate-2) [
10]. Bien que les effets de Let-7 sur l’expression individuelle des gènes soient modestes, la modulation simultanée de plusieurs acteurs de la signalisation insulinique pourrait expliquer comment Let-7 régule, chez la souris et de manière coordonnée, la sensibilité à l’hormone et donc le métabolisme du glucose dans le muscle et le foie [10,
11]. Dans les adipocytes, l’inactivation de miR-103/107 augmente l’expression de la protéine cavéoline-1, qui stabilise l’IR au niveau des radeaux lipidiques, améliorant ainsi la signalisation insulinique [
12]. En effet, chez la souris, l’absence de miR-103/107 améliore la sensibilité à l’insuline et l’homéostasie glucidique, alors que sa surexpression augmente la néoglucogenèse [12]. Dans les hépatocytes, miR-126 cible IRS-1 [
13], alors que miR-33a/b interagissent avec IRS-2 [
14]. Concernant la PI3K, miR-29a réduit l’expression de la sous-unité régulatrice p85 en se liant à son ARNm. Ainsi, dans la lignée HepG2, l’expression forcée du miR-29a inhibe l’action de l’insuline sur l’expression du gène codant pour la PEPCK (phosphoenolpyruvate carboxykinase) [
15]. De plus, miR-29a/c ciblent l’ARNm du PGC-1α (peroxisome proliferative activated receptor gamma coactivator 1α) et de la G6P (glucose-6-phosphatase), réduisant ainsi la production de glucose par le foie [
16]. En aval de la PI3K, la PDK1 (phosphoinositide-dependent kinase-1) joue un rôle principal dans l’activation de la PKB. Nous avons montré dans les cellules INS-1E que miR-375 interagit directement avec l’ARNm de la PDK1 impliquée dans la régulation par le glucose de l’expression de l’insuline et de la croissance cellulaire [4]. En revanche, aucun miARN ne semble lier l’ARNm de PKB. Plus en aval, nos résultats montrent que miR-139 se fixe directement à l’ARNm de FOXO-1 (forkhead box O1) dans des cellules hépatiques [
17]. Ainsi, en régulant l’expression de molécules clés de la sécrétion et des voies de signalisation de l’insuline, les miARN gouvernent les principaux aspects de l’homéostasie glucidique. Inversement, l’insuline est capable de moduler l’expression de certains miARN créant de cette façon une régulation croisée. Par exemple, chez l’homme, l’insuline diminue l’expression de 39 miARN dans le muscle squelettique [
18]. |
Altération de l’expression des miARN au cours du diabète de type 1 et 2 Compte tenu de la forte influence des miARN sur la sécrétion et l’action de l’insuline, l’idée selon laquelle des modifications de leur expression pourraient être associées à la physiopathologie du diabète a émergé rapidement (Figure 2). Le DT1 est une maladie auto-immune, caractérisée par la destruction des cellules β. L’expression de différents miARN est modifiée dans les îlots pancréatiques de souris souffrant de DT1. Par exemple, miR-21, miR-29a/b/c et miR-34a sont augmentés dans les îlots de souris NOD (non-obese diabetic) [9,
19] ; ces miARN ciblent respectivement le suppresseur de tumeur PDCD4 (programmed cell death protein 4) [
20], les protéines anti-apoptotiques MCL1 (myeloid cell leukemia sequence 1) [9] et Bcl2 [
21] impliquées dans la mort des cellules β. Par ailleurs, l’expression du miR-34a est altérée dans le foie de souris traitées par la streptozotocine, autre modèle murin de DT1 [
22]. Le DT2 est une maladie multicausale et polygénique affectant de nombreux tissus. Les modèles animaux ont permis d’identifier une série de miARN dont l’expression est modifiée dans les tissus sensibles à l’insuline et les îlots pancréatiques de rongeurs atteints de DT2. Ainsi, l’expression du miR-34a et du miR-146 est augmentée dans les îlots de souris db/db (déficientes pour le récepteur de la leptine) [21]. Chez les rats GK (modèle polygénique Goto-Kakizaki de DT2), l’expression des membres de la famille miR-29a/b/c et miR-125a est accrue dans les tissus cibles de l’insuline [
23,
24]. Comme le DT2 est souvent associé à l’obésité, des études ont été réalisées chez la souris ob/ob (déficientes pour la leptine) ou dans des modèles d’obésité induite par l’alimentation (OIA). En effet, l’expression de miR-103/107 est modifiée dans le foie et le tissu adipeux des souris ob/ob et OIA [12]. Concernant les études chez l’homme, peu de rapports ont été publiés en raison des limitations inhérentes à l’accessibilité des tissus. Gallagher et al. [
25] ont effectué une analyse de l’ensemble du génome des ARNm et des miARN dans le muscle squelettique de patients diabétiques ou de sujets sains. Certains miARN différentiellement exprimés, dont miR-133 et miR-206, ont été identifiés, et plusieurs d’entre eux semblent cibler des molécules clés du métabolisme glucidique. En outre, Kloting et al. [
26] ont observé une corrélation entre l’expression de certains miARN, l’infiltration des macrophages au sein du tissu adipeux, l’augmentation de la taille des adipocytes et certains paramètres métaboliques clés, tels que la glycémie à jeun, ainsi que les taux circulants de leptine, d’adiponectine et d’IL-6 (interleukine 6). Plus récemment, l’analyse d’îlots humains a révélé que miR-21 et miR-375 sont significativement augmentés chez les sujets diabétiques comparés aux sujets sains [
27,
28]. Bien que des modulations de l’expression des miARN chez des sujets diabétiques semblent exister, les quelques données disponibles ne permettent pas, à ce jour, de dresser un tableau convaincant. Des limitations importantes existent en raison de la taille insuffisante des cohortes, du manque d’uniformisation des techniques de mesure des miARN, ou encore de l’existence de facteurs interférant comme les différences d’âge, l’indice de masse corporelle et le sexe [
29]. D’autre part, il faut souligner que l’altération de l’expression des miARN chez les patients diabétiques pourrait participer à la physiopathologie de la maladie ou simplement en être une conséquence [
30]. |
Bien que l’importance du rôle des miARN dans les cellules où ils sont produits soit incontestable, la découverte de miARN dans le sang suggère qu’ils pourraient jouer un rôle en dehors de la cellule qui les produit [
31]. La découverte de miARN pouvant agir à distance ouvre de nouvelles perspectives quant au rôle biologique de ces derniers. Les miARN circulants pourraient, soit être produits par des organes ou des tissus, soit être relargués par des cellules apoptotiques ou nécrotiques. Bien que le mécanisme de sécrétion des miARN reste obscur, différents scénarios ont été proposés pour leur transport. Selon un premier scénario, les miARN circulants seraient intégrés dans des microvésicules appelées exosomes ou liés aux HDL (high density lipoprotein). Un second scénario prétend que les miARN plasmatiques ne sont pas encapsulés, mais plutôt associés à des protéines liant l’ARNm, telles que l’Ago2 (Argonaute 2) ou la NPM1 (nucleophosmin 1). Une des retombées importantes liées à la découverte de miARN extracellulaires concerne leur utilisation éventuelle comme biomarqueurs d’un état pathologique. En effet, de nombreux travaux ont révélé un profil d’expression des miARN circulants modifié dans diverses maladies métaboliques dont le DT2. Par exemple, Zampetaki et al. [
32] ont identifié une signature particulière de miARN plasmatiques chez des diabétiques de type 2, dont 12 miARN sont significativement corrélés avec la maladie. Parmi eux, le niveau plasmatique de miR-126 diminue progressivement avec l’apparition de l’intolérance au glucose. miR-126 est normalement très abondant dans les cellules endothéliales où il joue un rôle prépondérant dans le maintien de l’intégrité vasculaire, la formation des vaisseaux ainsi que dans leur réparation. Le DT2 est un facteur de risque important des maladies cardiovasculaires et est associé à un dysfonctionnement endothélial et à de nombreuses complications micro- et macrovasculaires. La diminution de miR-126 dans le plasma des diabétiques pourrait refléter un dysfonctionnement endothélial et donc avoir une valeur pronostique pour le développement des atteintes vasculaires. Récemment, Kong et al. [
33] ont publié que sept miARN (miR-9, miR-29a, miR-30d, miR-34a, miR-124a, miR-146a et miR-375) impliqués dans la sécrétion et l’action de l’insuline sont significativement augmentés dans le sérum des patients atteints de diabète de type 2. Parmi ceux-ci, miR-375 est le miARN dont l’expression est la plus forte dans les îlots murins et humains. Ainsi, le niveau élevé du miR-375 dans le sang des diabétiques pourrait provenir de cellules β lésées. Par conséquent, la mesure du miR-375 sanguin pourrait être un moyen non invasif pour estimer la masse de cellules β chez les patients résistants à l’insuline et donc servir de marqueur prédictif de l’insuffisance pancréatique. En effet, selon Erener et al. [
34], une perte massive des cellules β est associée à une augmentation des taux circulants de miR-375 chez des souris NOD ou traitées par la streptozotocine. En résumé, la démonstration de miARN dans les fluides corporels, tels que le sang, ouvre une voie prometteuse pour la découverte de nouveaux biomarqueurs pour les maladies métaboliques et/ou leurs complications associées. Ce dernier aspect serait particulièrement utile dans le cas du diabète pour lequel aucun marqueur de complications, comme l’insuffisance pancréatique et les atteintes cardiovasculaires, n’a été identifié. L’utilisation des miARN circulants comme biomarqueurs liés aux maladies doit cependant tenir compte de plusieurs éléments. Sur le plan technique, le manque d’uniformisation des méthodes de dosage des miARN circulants est limitant pour la validation des profils obtenus par différents laboratoires. L’utilisation des miARN comme biomarqueurs nécessite également l’uniformisation de la préparation pré-analytique des échantillons, qui est trop souvent négligée. Enfin, il reste à déterminer si les miARN extracellulaires reflètent simplement l’état pathologique et/ou participent activement au développement de la maladie. |
Conclusions et perspectives Alors qu’un millier de miARN ont été identifiés chez la souris et l’homme, nous devinons à peine la partie émergée de l’iceberg concernant leurs fonctions précises. Cependant, l’implication fondamentale des miARN dans le maintien de l’homéostasie glucidique est maintenant clairement acquise. Dans ce contexte, les miARN et le métabolisme semblent tisser des liens intimes. En effet, en agissant sur la production et/ou la signalisation d’acteurs clés dans la régulation métabolique, les miARN exercent des fonctions de première importance. En même temps, l’expression et la production des miARN sont modulées par certaines molécules majeures pour l’homéostasie, telles que l’insuline et le glucose. Cette relation bidirectionnelle entre les miARN et le métabolisme est un rouage clé dans la machinerie complexe de la régulation du métabolisme. Tout dysfonctionnement de cette machinerie est susceptible de générer des situations pathologiques telles que le diabète. Alors que le lexique élémentaire du langage des miARN vient d’être établi, une série d’interrogations demeure. Un problème essentiel concerne la difficulté de mesurer l’activité des miARN et de leur fonction au sein de l’organisme. En effet, chaque miARN vise potentiellement une centaine de cibles dont certaines sont interdépendantes et, inversement, plusieurs miARN peuvent cibler un même ARNm. À l’évidence l’effet biologique final du miARN sera déterminé par la concentration de celui-ci, mais aussi par celle de ses multiples cibles. La réflexion sur le potentiel thérapeutique éventuel des miARN doit prendre en compte l’idée qu’en visant plusieurs cibles, les miARN pourraient avoir des effets divergents. Une deuxième question centrale a trait à l’observation que certains miARN matures sont capables d’intégrer le noyau où ils officient de façon non classique en régulant directement la biogenèse de miARN et la fonction de longs ARN non codants. Cet effet « nucléaire » des miARN doit être pris en compte lors de l’évaluation du répertoire biologique global d’un miARN en particulier. Un troisième point au cœur de l’actualité concerne l’impact des rythmes circadiens dans la relation miARN-diabète. Ceci est de première importance si on considère le fait que la prise alimentaire module l’horloge circadienne et que celle-ci régule le métabolisme, ainsi que la transcription de certains gènes, et donc potentiellement celle des miARN impliqués dans le métabolisme [
37] (→). Enfin, certaines questions concernant les miARN extracellulaires restent également en suspens. Alors que l’utilisation de miARN extracellulaires comme biomarqueurs de pathologies est envisagée, leur fonction biologique doit être élucidée. La démonstration que les miARN extracellulaires, et en particulier ceux qui circulent dans le sang, sont des acteurs dans la communication intercellulaire, représenterait une découverte notoire en biologie fondamentale, mais offrirait également de réelles promesses comme nouveaux outils thérapeutiques. Cependant, compte tenu des actions pléiotropes de la plupart des miARN, dont certaines pourraient être opposées, il reste à déterminer s’il faut utiliser comme biomarqueurs des miARN aléatoires dont l’expression est aberrante mais ne faisant pas partie d’une voie de signalisation particulière, ou plutôt des miARN dont l’expression anormale perturbe une voie de signalisation compatible avec la pathologie. Les recherches en cours détermineront l’utilité éventuelle des miARN dans le traitement de pathologies, soit comme outils thérapeutiques, soit comme cibles de traitements. Vu le grand potentiel de ces molécules, des efforts multidisciplinaires sont nécessaires pour établir leur juste place dans l’arsenal thérapeutique de pathologies humaines, dont le diabète. |
E. Van Obberghen déclare participer à des conférences/colloques pour les entreprises Servier et Lilly.
C. Hinault et O. Dumortier déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
Nos recherches sont soutenues par l’Inserm, l’université de Nice Sophia-Antipolis, le centre hospitalier universitaire de Nice, le Conseil régional PACA, le Conseil général des Alpes-Maritimes, l’Agence nationale pour la recherche (ANR blanc n°RPV12004AAA) et la Fondation européenne pour l’étude du diabète (EFSD/Lilly ; european diabetes research programme, 2011). Nous prions certains auteurs de bien vouloir nous excuser de ne pas avoir cité leurs travaux faute de place.
|
Footnotes |
1.
Bartel
DP
. MicroRNAs : genomics, biogenesis, mechanism, and function . Cell.
2004; ; 116 : :281.–297. 2.
Poy
MN
,
Eliasson
L
,
Krutzfeldt
J
, et al.
A pancreatic islet-specific microRNA regulates insulin secretion . Nature.
2004; ; 432 : :226.–230. 3.
Poy
MN
,
Hausser
J
,
Trajkovski
M
, et al.
miR-375 maintains normal pancreatic alpha- and beta-cell mass . Proc Natl Acad Sci USA.
2009; ; 106 : :5813.–5818. 4.
El Ouaamari
A
,
Baroukh
N
,
Martens
GA
, et al.
miR-375 targets 3’-phosphoinositide-dependent protein kinase-1 and regulates glucose-induced biological responses in pancreatic beta-cells . Diabetes.
2008; ; 57 : :2708.–2717. 5.
Krek
A
,
Grun
D
,
Poy
MN
, et al.
Combinatorial microRNA target predictions . Nat Genet.
2005; ; 37 : :495.–500. 6.
Lovis
P
,
Gattesco
S
,
Regazzi
R
. Regulation of the expression of components of the exocytotic machinery of insulin-secreting cells by microRNAs . Biol Chem.
2008; ; 389 : :305.–312. 7.
Baroukh
N
,
Ravier
MA
,
Loder
MK
, et al.
MicroRNA-124a regulates Foxa2 expression and intracellular signaling in pancreatic beta-cell lines . J Biol Chem.
2007; ; 282 : :19575.–19588. 8.
Plaisance
V
,
Abderrahmani
A
,
Perret-Menoud
V
, et al.
MicroRNA-9 controls the expression of Granuphilin/Slp4 and the secretory response of insulin-producing cells . J Biol Chem.
2006; ; 281 : :26932.–26942. 9.
Roggli
E
,
Gattesco
S
,
Caille
D
, et al.
Changes in microRNA expression contribute to pancreatic beta-cell dysfunction in prediabetic NOD mice . Diabetes.
2012; ; 61 : :1742.–1751. 10.
Zhu
H
,
Shyh-Chang
N
,
Segre
AV
, et al.
The Lin28/let-7 axis regulates glucose metabolism . Cell.
2011; ; 147 : :81.–94. 11.
Frost
RJ
,
Olson
EN
. Control of glucose homeostasis and insulin sensitivity by the Let-7 family of microRNAs . Proc Natl Acad Sci USA.
2011; ; 108 : :21075.–21080. 12.
Trajkovski
M
,
Hausser
J
,
Soutschek
J
, et al.
MicroRNAs 103 and 107 regulate insulin sensitivity . Nature.
2011; ; 474 : :649.–653. 13.
Ryu
HS
,
Park
SY
,
Ma
D
, et al.
The induction of microRNA targeting IRS-1 is involved in the development of insulin resistance under conditions of mitochondrial dysfunction in hepatocytes . PLoS One.
2011; ; 6 : :e17343.. 14.
Davalos
A
,
Goedeke
L
,
Smibert
P
, et al.
miR-33a/b contribute to the regulation of fatty acid metabolism and insulin signaling . Proc Natl Acad Sci USA.
2011; ; 108 : :9232.–9237. 15.
Pandey
AK
,
Verma
G
,
Vig
S
, et al.
miR-29a levels are elevated in the db/db mice liver and its overexpression leads to attenuation of insulin action on PEPCK gene expression in HepG2 cells . Mol Cell Endocrinol.
332 : :125.–133. 16.
Liang
J
,
Liu
C
,
Qiao
A
, et al.
MicroRNA-29a-c decrease fasting blood glucose levels by negatively regulating hepatic gluconeogenesis . J Hepatol.
2013; ; 58 : :535.–542. 17.
Hasseine
LK
,
Hinault
C
,
Lebrun
P
, et al.
miR-139 impacts FoxO1 action by decreasing FoxO1 protein in mouse hepatocytes . Biochem Biophys Res Commun.
2009; ; 390 : :1278.–1282. 18.
Granjon
A
,
Gustin
MP
,
Rieusset
J
, et al.
The microRNA signature in response to insulin reveals its implication in the transcriptional action of insulin in human skeletal muscle and the role of a sterol regulatory element-binding protein-1c/myocyte enhancer factor 2C pathway . Diabetes.
2009; ; 58 : :2555.–2564. 19.
Roggli
E
,
Britan
A
,
Gattesco
S
, et al.
Involvement of microRNAs in the cytotoxic effects exerted by proinflammatory cytokines on pancreatic beta-cells . Diabetes.
2010; ; 59 : :978.–986. 20.
Ruan
Q
,
Wang
T
,
Kameswaran
V
, et al.
The microRNA-21-PDCD4 axis prevents type 1 diabetes by blocking pancreatic beta cell death . Proc Natl Acad Sci USA.
2011; ; 108 : :12030.–12051. 21.
Lovis
P
,
Roggli
E
,
Laybutt
DR
, et al.
Alterations in microRNA expression contribute to fatty acid-induced pancreatic beta-cell dysfunction . Diabetes.
2008; ; 57 : :2728.–2736. 22.
Li
S
,
Chen
X
,
Zhang
H
, et al.
Differential expression of microRNAs in mouse liver under aberrant energy metabolic status . J Lipid Res.
2009; ; 50 : :1756.–1765. 23.
He
A
,
Zhu
L
,
Gupta
N
, et al.
Overexpression of micro ribonucleic acid 29, highly up-regulated in diabetic rats, leads to insulin resistance in 3T3-L1 adipocytes . Mol Endocrinol.
2007; ; 21 : :2785.–2794. 24.
Herrera
BM
,
Lockstone
HE
,
Taylor
JM
, et al.
MicroRNA-125a is over-expressed in insulin target tissues in a spontaneous rat model of type 2 diabetes . BMC Med Genomics.
2009; ; 2 : :54.. 25.
Gallagher
IJ
,
Scheele
C
,
Keller
P
, et al.
Integration of microRNA changes in vivo identifies novel molecular features of muscle insulin resistance in type 2 diabetes . Genome Med.
2010; ; 2 : :9.. 26.
Kloting
N
,
Berthold
S
,
Kovacs
P
, et al.
MicroRNA expression in human omental and subcutaneous adipose tissue . PLoS One.
2009; ; 3 : :e4699.. 27.
Bolmeson
C
,
Esguerra
JL
,
Salehi
A
, et al.
Differences in islet-enriched miRNAs in healthy and glucose intolerant human subjects . Biochem Biophys Res Commun.
2011; ; 404 : :16.–22. 28.
Zhao
H
,
Guan
J
,
Lee
HM
, et al.
Up-regulated pancreatic tissue microRNA-375 associates with human type 2 diabetes through beta-cell deficit and islet amyloid deposition . Pancreas.
2010; ; 39 : :843.–846. 29.
Becker
N
,
Lockwood
CM
. Pre-analytical variables in miRNA analysis . Clin Biochem.
2013 ; doi : 10.1016/j.clinbiochem.2013.02.015. 30.
Jacovetti
C
,
Abderrahmani
A
,
Parnaud
G
, et al.
MicroRNAs contribute to compensatory beta cell expansion during pregnancy and obesity . J Clin Invest.
2012; ; 122 : :3541.–3551. 31.
Zampetaki
A
,
Willeit
P
,
Drozdov
I
, et al.
Profiling of circulating microRNAs : from single biomarkers to re-wired networks . Cardiovasc Res.
2012; ; 93 : :555.–562. 32.
Zampetaki
A
,
Kiechl
S
,
Drozdov
I
, et al.
Plasma microRNA profiling reveals loss of endothelial miR-126 and other microRNAs in type 2 diabetes . Circ Res.
2010; ; 107 : :810.–817. 33.
Kong
L
,
Zhu
J
,
Han
W
, et al.
Significance of serum microRNAs in pre-diabetes and newly diagnosed type 2 diabetes : a clinical study . Acta Diabetol.
2011; ; 48 : :61.–69. 34.
Erener
S
,
Mojibian
M
,
Fox
JK
, et al.
Circulating miR-375 as a biomarker of beta-cell death and diabetes in mice . Endocrinology.
2013; ; 154 : :603.–608. 35.
Ladeiro
Y
,
Zucman-Rossi
J
. Micro-ARN (miARN) et cancer : le cas des tumeurs hépatocellulaires . Med Sci (Paris).
2009; ; 25 : :467.–472. 36.
Gauthier
BR
,
Wollheim
CB
. MicroARN : ribo-régulateurs de l’homéostasie du glucose . Med Sci (Paris).
2006; ; 22 : :463.–465. 37.
Duez
H
,
Sebti
Y
,
Staels
B
. Horloges circadiennes et métabolisme : intégration des signaux métaboliques et environnementaux . Med Sci (Paris).
2013; ; 29 : :772.–777. |