| |
| Med Sci (Paris). 2012 March; 28(3): 239–241. Published online 2012 April 6. doi: 10.1051/medsci/2012283004.HIP/PAP, un nouveau médicament contre les hépatites aiguës graves Nicolas Moniaux,1,2 Marion Darnaud,1,2 Alexandre Dos Santos,1,2 Laure Jamot,3 Didier Samuel,1,2 Paul Amouyal,3 Gilles Amouyal,3 Christian Bréchot,1,2 and Jamila Faivre1,2* 1Inserm, U785, centre hépatobiliaire, Villejuif, 94800, France 2Université Paris-Sud, faculté de médecine, Villejuif, 94800, France 3ALFACT Innovation, Paris, 75001, France MeSH keywords: Acétaminophène, toxicité, Maladie aigüe, Animaux, Antigènes CD95, agonistes, Antigènes néoplasiques, effets indésirables, physiologie, usage thérapeutique, Marqueurs biologiques tumoraux, Lésions hépatiques dues aux substances, traitement médicamenteux, étiologie, Essais cliniques de phase I comme sujet, Essais cliniques de phase II comme sujet, Modèles animaux de maladie humaine, Évaluation préclinique de médicament, Hépatite, Humains, Lectines de type C, Défaillance hépatique, Régénération hépatique, Souris, Souris de lignée C57BL, Souris transgéniques, Études multicentriques comme sujet, Espèces réactives de l'oxygène, métabolisme, Protéines recombinantes |
L’hépatite aiguë sévère et fulminante : gravissime et sans traitement spécifique L’hépatite aiguë sévère et fulminante est une nécrose massive et brutale du foie conduisant à une défaillance plus ou moins rapide des fonctions hépatiques. Elle se définit par des troubles majeurs de l’hémostase - le taux de prothrombine est inférieur à 50 % - associés ou non à des troubles neurologiques (encéphalopathie hépatique et coma). Les causes de cette affection sont multiples : virales, médicamenteuses, toxiques, auto-immunes. Elles doivent être activement recherchées afin d’instaurer les traitements spécifiques qui conviennent. Cette affection survient la plupart du temps sur un foie sain. Elle peut évoluer soit vers la guérison spontanée (avec ou sans phase d’aggravation), soit vers la mort du patient (en absence de transplantation hépatique réalisée en urgence). Sur le plan moléculaire, l’activation de nombreuses voies de signalisation entraînant la mort cellulaire par apoptose, nécrose et stress oxydatif est responsable des dommages massifs du foie et de l’inhibition de la prolifération cellulaire. Il n’existe pas de biomarqueur prédictif du devenir des patients (guérison, transplantation ou décès). L’évolution clinique imprévisible de ce syndrome en fait une véritable urgence médicochirurgicale nécessitant une hospitalisation en soins intensifs à proximité d’un centre spécialisé en transplantation hépatique [1, 2]. Le traitement médical est essentiellement symptomatique et peut inclure une assistance hépatique extracorporelle de détoxification sanguine. Aucun traitement pharmacologique visant à protéger le foie et stimuler sa régénération n’a jusqu’à présent montré son efficacité. La seule drogue disponible, dans le cas d’une intoxication au paracétamol, est la N-acétylcystéine (NAC) qui, si elle est administrée très précocement, corrige l’insuffisance hépatique. Véritable antidote du surdosage au paracétamol, NAC restaure les stocks de glutathion hépatique dont la consommation inactive les métabolites réactifs cytotoxiques et réduit les lésions oxydatives du foie. Plus récemment, l’administration de NAC dans les hépatites fulminantes qui ne sont pas liées au paracétamol a été proposée, et une amélioration de la survie sans transplantation a été observée dans certains sous-groupes de patients [3]. Ce résultat clinique, associé à une absence d’effet iatrogène de NAC, a conduit certains auteurs à prescrire systématiquement NAC dans toute hépatite aiguë sévère ou fulminante, et cela malgré l’absence de preuve formelle de son efficacité. On ne saurait alors trop souligner combien le besoin médical de nouvelles molécules ciblant les insuffisances hépatocellulaires aiguës et sévères est important. |
La protéine HIP/PAP : une molécule antioxydante efficace dans les hépatites fulminantes Parmi les candidats pharmacologiques actuellement à l’étude, la protéine HIP/PAP (hepatocarcinoma-intestine-pancreas/pancreatitis associated protein) ou Reg-3α (regenerating islet-derived protein 3α) exerce des effets biologiques démontrés en matière de réparation et de régénération tissulaires, ainsi qu’une protection vis-à-vis du stress et de la mort cellulaires. HIP/PAP est une lectine de type C (possédant un seul domaine de liaison aux hydrates de carbone) de 16 kDa, qui est sécrétée et qui exerce ses activités biologiques de façon autocrine et paracrine. HIP/PAP exerce une activité anti-inflammatoire dans le pancréas [4] et antibactérienne dans le tube digestif [5, 6]. Elle favorise la survie et la guidance axonale des motoneurones [7], la prolifération des cellules de Schwann et, enfin, la survie et la régénération des cellules hépatiques [8–10]. Les mécanismes moléculaires que met en jeu HIP/PAP dans la protection tissulaire sont largement méconnus. Des modèles de souris génétiquement modifiées ont permis de montrer que HIP/PAP stimule la régénération hépatique après hépatectomie majeure et protège les animaux transgéniques d’une hépatite mortelle induite par l’acétaminophène ou par l’anticorps agoniste du récepteur de mort Fas/CD95 (Fas) [9–11]. Dès lors, la question des capacités thérapeutiques d’une protéine-médicament dans l’hépatite aiguë sévère se posait. Nous avons donc produit une protéine recombinante humaine HIP/PAP (rcHIP/PAP) et entrepris d’évaluer son effet curatif vis-à-vis de l’insuffisance hépatocellulaire aiguë, et de caractériser son mode d’action. La protéine rcHIP/PAP a été produite dans un système bactérien Escherichia coli puis purifiée à plus de 99 % suivant les normes réglementaires en vigueur pour une utilisation clinique. Le mécanisme d’action de HIP/PAP, les résultats des études précliniques ainsi que les premières données cliniques ont été publiés dans la revue Hepatology [11]. Une première série d’expériences a conclu à l’efficacité thérapeutique de rcHIP/PAP dans un modèle murin d’hépatite sévère induite par un agoniste du récepteur de mort Fas. Des souris sauvages de fond génétique C57Bl/6J ont reçu tout d’abord une dose d’anti-Fas calibrée pour induire 60 % de mortalité à 24 h, puis, à différents temps après l’agoniste de Fas, une dose de rcHIP/PAP (0,05 à 2,5 mg/kg par voie intraveineuse). L’étude dose-réponse a montré qu’une dose unique de rcHIP/PAP améliorait significativement la survie à 24 et 48 h des souris sauvages traitées par l’anti-Fas, la dose optimale étant de 0,750 mg/kg. Cette survie était statistiquement meilleure dans les groupes ayant reçu la molécule à un stade tardif (6 h), voire très tardif (9 h et 11 h), de la maladie hépatique induite par l’anti-Fas que dans les groupes ayant reçu rcHIP/PAP à un stade précoce, moins sévère, de la maladie. Les niveaux d’expression et d’activation des facteurs impliqués dans les voies de l’apoptose, de la prolifération ou de la survie étaient similaires dans le foie de souris traitées par rcHIP/PAP ou par le tampon. En revanche, une nette diminution de la quantité des biomolécules oxydées a été observée, qu’elle soit identifiée par la mesure de la peroxydation lipidique ou celle de la carbonylation protéique, suggérant le rôle majeur de l’effet antioxydant hépatique de rcHIP/PAP dans la survie des souris. Cette inhibition du stress oxydatif hépatique par rcHIP/PAP était associée à une nette diminution des lésions nécrotiques et inflammatoires à l’examen histologique et à un meilleur index de prolifération hépatocytaire comparé aux foies contrôles. Les expériences réalisées in vitro sur des cultures primaires d’hépatocytes murins et humains ont montré que rcHIP/PAP améliorait très nettement la viabilité des cellules primaires agressées par différents effecteurs de mort comme le tumor necrosis factor α (TNFα)/actinomycine D, le transforming growth factor β (TGFβ) ou encore le peroxyde d’hydrogène, et ce de manière dose dépendante. Cette cytoprotection était associée, comme dans les expériences in vivo, à une diminution du stress oxydatif des biomolécules. Enfin, nous avons montré que le pouvoir antioxydant de rcHIP/PAP reposait sur sa capacité à piéger les radicaux libres de type superoxyde et hydroxyle. Cette capacité de rcHIP/PAP à éliminer le radical hydroxyle est particulièrement intéressante en raison du caractère toxique de l’hydroxyle et de l’incapacité des cellules à l’éliminer, à la différence du radical superoxyde qui est détoxifié par la superoxyde dismutase. Prise dans son ensemble, cette étude préclinique montre que la protéine rcHIP/PAP est un candidat médicament très prometteur dans le traitement de l’insuffisance hépatocellulaire aiguë et sévère. Nous avons montré que rcHIP/PAP, par son action antioxydante importante, protège les cellules hépatiques de la mort cellulaire induite par divers signaux de mort et améliore la survie dans un modèle expérimental reconnu d’hépatite aiguë et sévère (Figure 1).
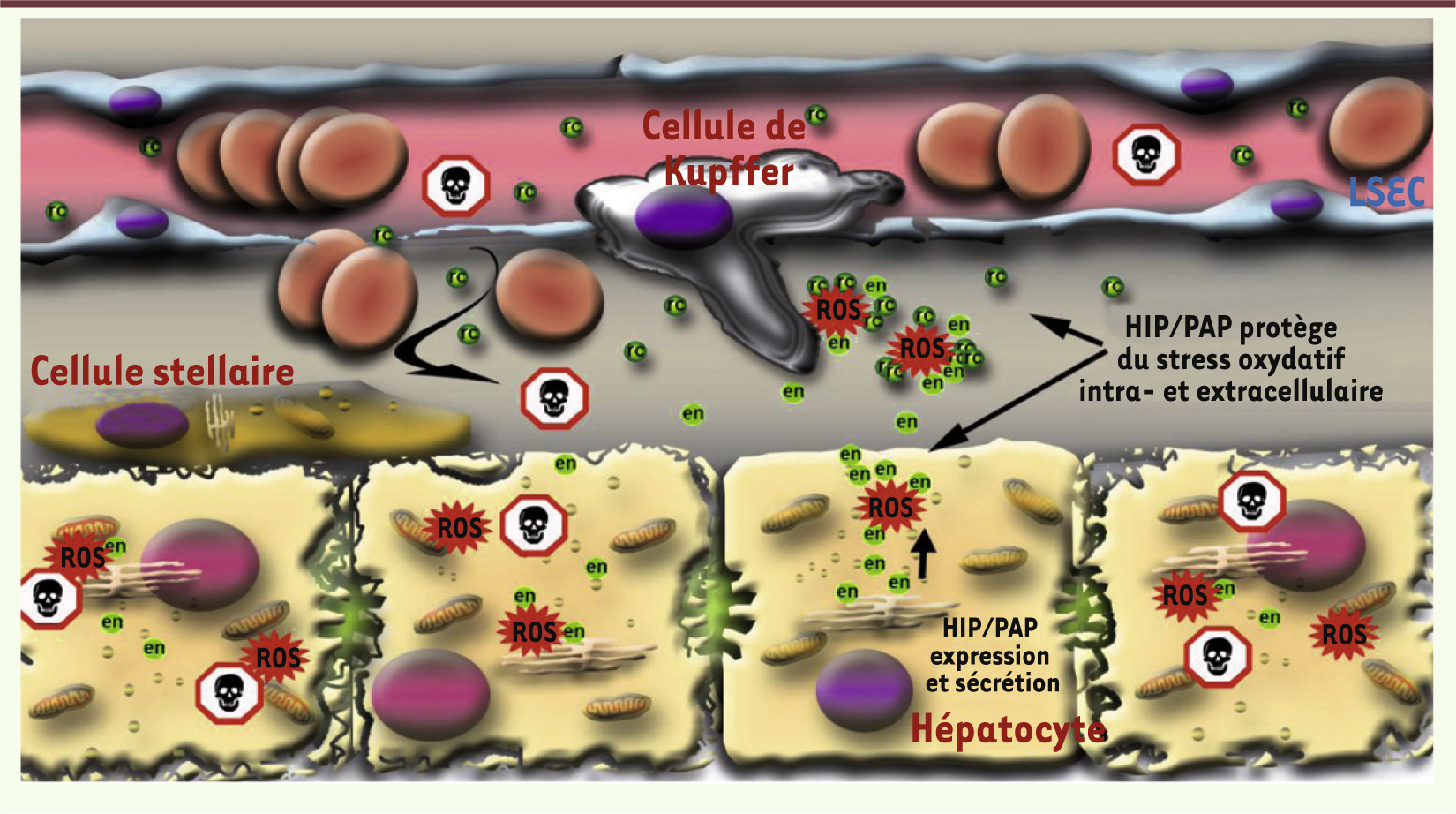
 | Figure 1.
Mode d’action de la protéine HIP/PAP dans le foie atteint d’hépatite aiguë sévère. L’agression du foie par un agent toxique (symbole avec une tête de mort) induit la production en excès d’espèces réactives de l’oxygène (ROS), aux niveaux intracellulaire (en réponse au stress du réticulum endoplasmique et de la mitochondrie) et extracellulaire (par les NADPH oxydases activées dans les macrophages). La protéine HIP/PAP, produite de façon endogène (symbole vert « en ») en réponse aux mécanismes d’inflammation et de stress oxydatif, ou administrée par voie intraveineuse sous sa forme recombinante (symbole vert « rc ») permet le piégeage des ROS (activité scavenger) (symbole rouge), et en particulier des radicaux hydroxyles très cytotoxiques. Cette action favorise la survie des différents types cellulaires du foie et, in fine, la régénération hépatique. LSEC : cellules endothéliales sinusoïdales ; cellule de Kuppfer : macrophages résidents ; cellule stellaire : péricytes spécialisés. |
|
De la découverte de la molécule à l’essai clinique Un essai clinique de phase 1 a été entrepris pour évaluer l’innocuité, la tolérance et les paramètres pharmacocinétiques de rcHIP/PAP chez le volontaire sain. Cette étude a conclu à une absence de toxicité de la protéine recombinante chez l’homme quelle que soit la dose testée. Fin 2010, un essai clinique de phase 2 multicentrique en double aveugle et contrôlé contre placebo a été débuté : il évalue l’innocuité et l’efficacité thérapeutique de rcHIP/PAP chez des patients atteints d’une hépatite aiguë sévère ou fulminante. Les premiers résultats sont attendus fin 2012. Il s’agit (à notre connaissance) de l’un des médicaments les plus prometteurs en phase de développement. Son développement thérapeutique permettra d’assurer la protection des cellules hépatiques contre une agression majeure, de stimuler la régénération et, peut-être ainsi, de limiter le besoin de recourir en urgence à la transplantation orthotopique. En conclusion, la protéine recombinante HIP/PAP est la seule lectine humaine possédant une activité antioxydante de piégeage des espèces oxygénées réactives. Cette propriété lui confère de réels atouts dans le traitement des hépatites aiguës sévères et fulminantes chez l’homme. Les perspectives d’avenir sont d’étendre les indications de la protéine recombinante HIP/PAP à d’autres pathologies sévères du foie, en particulier l’hépatite alcoolique aiguë et les poussées d’insuffisance hépatocellulaire aiguë sur foie cirrhotique, cause la plus fréquente de décompensation des cirrhoses. |
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
|
1. Stravitz RT, Kramer DJ. Management of acute liver failure . Nat Rev Gastroenterol Hepatol. 2009; ; 6 : :542.–553. 2. Ichai P, Samuel D. Epidemiology of liver failure . Clin Res Hepatol Gastroenterol. 2011; ; 35 : :610.–617. 3. Lee WM, Hynan LS, Rossaro L, et al. Intravenous N-acetylcysteine improves transplant-free survival in early stage non-acetaminophen acute liver failure . Gastroenterology. 2009; ; 137 : :856.–864. 4. Gironella M, Folch-Puy E, LeGoffic A, et al. Experimental acute pancreatitis in PAP/HIP knock-out mice . Gut. 2007; ; 56 : :1091.–1097. 5. Cash HL, Whitham CV, Behrendt CL, Hooper LV. Symbiotic bacteria direct expression of an intestinal bactericidal lectin . Science. 2006; ; 313 : :1126.–1130. 6. Vaishnava S, Yamamoto M, Severson KM, et al. The antibacterial lectin RegIIIgamma promotes the spatial segregation of microbiota and host in the intestine . Science. 2011; ; 334 : :255.–258. 7. Nishimune H, Vasseur S, Wiese S, et al. Reg-2 is a motoneuron neurotrophic factor and a signalling intermediate in the CNTF survival pathway . Nat Cell Biol. 2000; ; 2 : :906.–914. 8. Lieu HT, Batteux F, Simon MT, et al. HIP/PAP accelerates liver regeneration and protects against acetaminophen injury in mice . Hepatology. 2005; ; 42 : :618.–626. 9. Lieu HT, Simon MT, Nguyen-Khoa T, et al. Reg2 inactivation increases sensitivity to Fas hepatotoxicity and delays liver regeneration post-hepatectomy in mice . Hepatology. 2006; ; 44 : :1452.–1464. 10. Simon MT, Pauloin A, Normand G, et al. HIP/PAP stimulates liver regeneration after partial hepatectomy and combines mitogenic and anti-apoptotic functions through the PKA signaling pathway . FASEB J. 2003; ; 17 : :1441.–1450. 11. Moniaux N, Song H, Darnaud M, et al. Human hepatocarcinoma-intestine-pancreas/pancreatitis-associated protein cures fas-induced acute liver failure in mice by attenuating free-radical damage in injured livers . Hepatology. 2011; ; 53 : :618.–627. |