| |
| Med Sci (Paris). 2011 October; 27(10): 866–874. Published online 2011 October 21. doi: 10.1051/medsci/20112710015.Production in vitro de cellules germinales murines et humaines à partir de cellules souches pluripotentes Lucie Tosca,1,2* Anne-Marie Courtot,1 Annelise Bennaceur-Griscelli,1 and Gérard Tachdjian1,2 1Inserm U935, plate-forme des cellules souches pluripotentes ; Université Paris-Sud 11, hôpital Paul Brousse, 94800, Villejuif, France 2AP-HP, Service d’histologie, embryologie et cytogénétique, hôpital Antoine Béclère, Clamart, France |
De grandes avancées ont été réalisées dans le traitement des problèmes d’infertilité chez la femme et l’homme. Cependant, les techniques d’assistance médicale à la procréation (AMP) ne peuvent pas offrir une réponse à toutes les causes d’infertilité. Nos connaissances des stades précoces de la formation des gamètes sont réduites dans l’espèce humaine, ce qui explique le faible nombre, voire l’absence, de thérapeutiques, en particulier dans les anomalies de la genèse des gamètes. Un modèle de formation des gamètes humains in vitro à partir de cellules souches humaines aurait un impact considérable sur l’évolution des connaissances fondamentales et sur le développement de thérapeutiques adaptées. En effet, l’obtention in vitro de gamètes pourrait modifier les pratiques actuelles de l’AMP, car les laboratoires pourraient disposer d’une source abondante d’ovocytes ou de spermatozoïdes matures et fonctionnels [
1,
2]. Le terme de cellule souche humaine désigne les cellules souches embryonnaires (CSE), les cellules souches tissulaires fœtales et adultes. Jusqu’au stade de morula (jour 3 après la fécondation), les cellules embryonnaires sont totipotentes, c’est-à-dire que chacune est en théorie capable de générer un organisme entier. Au stade de blastocyste (jour 5), les cellules de la masse cellulaire interne (MCI) sont pluripotentes - du moins certaines d’entre elles - et peuvent se différencier en tous les types tissulaires à l’exception des annexes embryonnaires. Les lignées de CSE pluripotentes et douées d’autorenouvellement illimité sont dérivées des cellules de la MCI alors que les « cellules pluripotentes induites » (induced pluripotent stem cells ou iPS pour garder l’acronyme maintenant très célèbre) sont issues de la reprogrammation de cellules somatiques adultes ou fœtales différenciées et non pas de cellules embryonnaires. Les iPS ont été obtenues chez la souris (miPS) puis chez l’homme (hiPS) par l’expression forcée d’une combinaison de gènes définis tels que Oct3/4, Sox2, c-Myc et KLF4 impliqués dans la pluripotence et la prolifération cellulaire [
3,
4]. La formation des gamètes est un processus très complexe in vivo : elle comprend des étapes qui se succèdent dans le temps et dans l’espace. Les cellules de la MCI adoptent un destin de cellules germinales primordiales (CGP) pendant leur phase extra-embryonnaire ; les CGP migrent vers les crêtes génitales pour finalement devenir des gonocytes qui se transformeront en gamètes via des processus de méiose et de différenciation cellulaire. Les cellules, tout d’abord pluripotentes, évoluent au cours de leur trajet sous l’influence de signaux précis provenant des tissus avoisinants. Ainsi, à chaque étape, il existe des fenêtres de réceptivité qui se manifestent par l’existence d’inducteurs et l’apparition ou la disparition d’un ensemble de marqueurs spécifiques ou ubiquitaires dans un contexte de niches cellulaires
(Tableau I
,
Figure 1)
. De plus, ces cellules appartiennent à une lignée exceptionnelle dans l’organisme : elles deviennent haploïdes (via le processus de méiose [
31,
32]), se spécifient en gamètes mâles ou femelles et pérennisent l’espèce. L’ensemble de ces événements est sous la dépendance de facteurs génétiques (chromosomes sexuels X et Y) et épigénétiques (empreinte génomique parentale [
33]) qui se réactualisent à chaque génération.
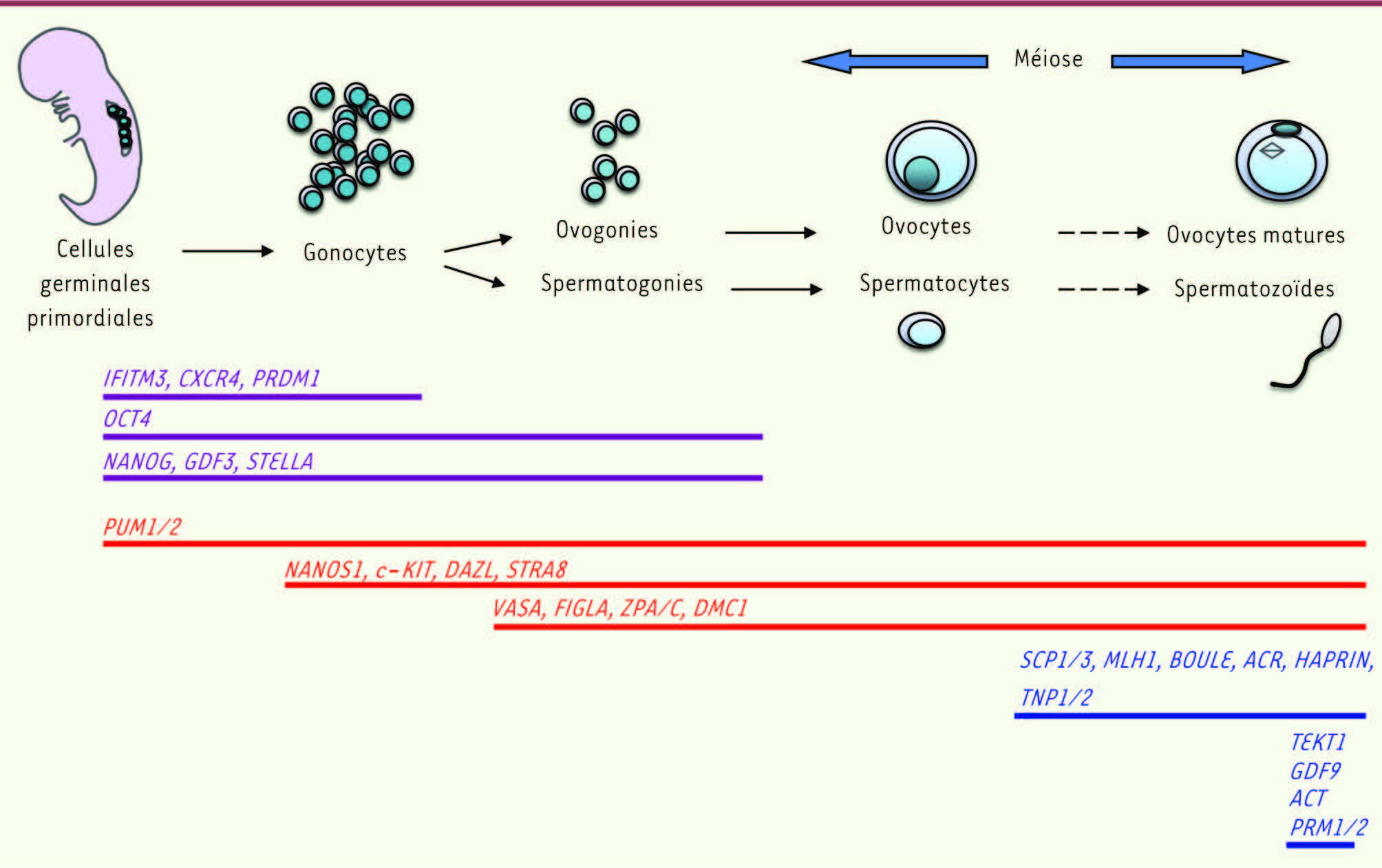
 | Figure 1.
Cascade d’induction lors de la différenciation germinale. Chronologie des événements de la différenciation germinale chez le mâle et la femelle. Profil d’expression des gènes de détermination germinale : préméiotique (violet), pré- et postméiotique (rouge) et exclusivement méiotique (bleu). |
Tableau I.
|
Stade d’expression |
Gène |
Signification des abréviations |
Références |
|
Marqueurs communs
|
Pluripotence |
SSEA1/3/4
|
Stage specific embryonic antigen 1/3
|
[
5,
7,
13,
16,
17,
22,
23] |
|
TRA-1-60
|
|
[7, 16, 22] |
|
TRA-1-81
|
|
[5, 22] |
| PGC migratoires |
CXCR4
|
Chemokine (C-X-C motif) receptor 4
|
[7] |
| Pluripotence, préméiotique |
POU5F1 (OCT3/4)
|
POU class 5 homeobox 1
|
[5,
8,
12,
15–17,
19,
20, 22–
25,
27,
28] |
|
Nanog
|
Nanog homeobox
|
[5, 7, 8, 15, 16, 22] |
| Préméiotique (cellules germinales prémigratoires) |
STELLA (DPPA3)
|
Developmental pluripotency associated 3
|
[5, 7, 8, 12, 15, 17–20, 22,
24, 25, 28] |
| Préméiotique |
GDF3
|
Growth differentiation factor 3
|
[5] |
| Préméiotique, testicule spécifique, ovaire fœtal |
STRA8
|
Stimulated by retinoic acid gene 8
|
[
18, 19, 24, 28] |
| Méiotique précoce |
SCP1/3 (SYCP1/3)
|
Synaptonemal complex protein 1/3
|
[5, 8, 15, 16, 18–20, 23, 25, 27, 28] |
|
DMC1
|
Meiosis-specific homologous recombination gene
|
[19, 27] |
| Pré et postméiotique |
NANOS1
|
Nanos homolog 1
|
[5, 15] |
|
VASA (DDX4, MVH)
|
DEAD (Asp-Glu-Ala-Asp) box polypeptide 4
|
[5, 7, 8, 13, 15, 16, 19, 20, 22, 24, 25, 27, 28] |
|
DAZL (DAZ, BOULE)
|
Deleted in azoospermia-like
|
[5, 7, 8, 15–19, 24, 28,] |
|
PUM1/2
|
Pumilio homolog 1
|
[5, 15] |
| Méiotique |
MLH1
|
MutL homolog 1, colon cancer, nonpolyposis type 2 |
[5, 15, 28] |
| Méiotique tardif |
TRIM36 (HAPRIN)
|
Tripartite motif-containing 36
|
[17] |
| Germinal précoce |
PRDM1 (BLIMP1)
|
PR domain containing 1, with ZNF domain
|
[7, 8, 12, 13, 28] |
| Germinal précoce et tardif |
KIT
|
V-kit Hardy-Zuckerman 4 feline sarcoma viral oncogene homolog
|
[5, 7, 13, 16, 19, 22, 24, 25, 27] |
| Cellules Sertoli, cellules Leydig, cellules de la granulosa, cellules de la thèque |
FSHR/LHR
|
Follicle stimulating hormone receptor/ luteinizing hormone receptor
|
[7, 8, 17] |
| Cellules Sertoli, cellules de la granulosa |
AMH (MIS)
|
Anti-Mullerian hormone
|
[7, 8, 13, 17] |
|
IFITM3 (FGLS)
|
Interferon induced transmembrane protein 3
|
[12, 15, 17, 19, 20, 25] |
|
|
Marqueurs mâles
|
Différenciation mâle |
SRY
|
Sex determining region Y
|
[13, 17, 20] |
| Spermatide |
TNP1/2
|
Transition nuclear protein 1/2
|
[16, 19] |
| Méiotique tardif, stade spermatocyte et spermatide ronde |
TEKT1
|
Tektin 1
|
[5] |
| Méiotique tardif, spermatozoïde mature |
ACR
|
Acrosin
|
[7, 8, 17, 19] |
| Postméiotique |
PRM1/2
|
Protamine 1/2
|
[16, 18, 19] |
| Spermiogenèse |
ACT
|
Activator of CREM in testis
|
[18] |
| Cellules Sertoli |
SOX9
|
SRY (sex determining region Y)-box 9
|
[7, 8] |
|
|
Marqueurs femelles
|
Ovocyte |
FIGLA (Figα)
|
Folliculogenesis specific basic helix-loop-helix
|
[19, 24, 25, 27] |
| Ovocyte |
GDF9
|
Growth differentiation factor 9
|
[5, 16, 22, 25, 27,
29] |
| Germinal tardif, ovocyte |
ZPA/C (ZAP1/3)
|
Zona pellucida glycoprotein (sperm receptor) A/C
|
[16, 24, 25, 27, 29] |
| Cellules folliculaires |
STAR
|
Steroidogenic acute regulatory protein
|
[27] |
| Cellules de la granulosa |
CYP19A1 (AROMATASE)
|
P450, family 19, subfamily A, polypeptide 1
|
[13, 27] |
| Cellules de la thèque |
Cyp17A1 (cytochrome P450)
|
P450, family 17, subfamily A, polypeptide 1
|
[27] |
Principaux marqueurs moléculaires de la différenciation germinale
|
Dans cette revue, nous décrivons les avancées scientifiques qui permettent d’obtenir, à partir des cellules souches pluripotentes humaines (CSE et iPS), des cellules germinales et leurs cellules nourricières associées, à la lumière des résultats obtenus chez la souris. |
Obtention de cellules germinales primordiales et de gonocytes humains in vitro: importance des déterminants moléculaires La formation des CGP est une étape-clé pour la réussite de leur différenciation ultérieure en gamètes. D’abord indiscernables des autres cellules embryonnaires voisines, elles acquièrent progressivement des déterminants germinaux (gènes s’exprimant à un stade précis du développement germinal) en activant un programme spécifique germinal et en inhibant un programme somatique. Cette double action s’accompagne d’une réactivation ou d’un maintien de la pluripotence. In vivo, c’est au moment où les cellules germinales atteignent les crêtes génitales qu’elles se transforment en gonocytes et se divisent activement. In vitro, il a été possible d’obtenir l’expression de marqueurs des stades CGP et gonocytes à partir principalement de lignées de CSE humaines (hCSE) et de souris (mCSE). Les transitions CSE-CGP et CGP-gonocytes ne sont pas nettes, car les marqueurs sont souvent communs aux deux stades. Nous décrivons les résultats obtenus en fonction des déterminants moléculaires les plus représentatifs de chaque stade. Clark et al. ont réalisé un travail pionnier en obtenant, à partir de hCSE, des cellules exprimant un gène spécifique de la lignée germinale, DAZL. Puis, lors de la différenciation des hCSE en corps embryoïdes, l’expression de VASA apparaît après 14 jours de culture, accompagnée d’autres marqueurs plus tardifs [5]. Depuis cette étude, les équipes ont cherché à obtenir in vitro une population enrichie en CGP. Chez la souris, l’expression de 500 gènes est régulée positivement et celle de 330 gènes négativement pendant cette période [
6]. De ce fait, la question de la pertinence des marqueurs spécifiques des CGP utilisés se pose de façon cruciale. Des gènes semblent plus significatifs que d’autres, car impliqués dans la pluripotence, l’orientation germinale ou la migration. Certains marqueurs commencent à être reconnus comme incontournables pour l’établissement du phénotype des CGP : ainsi PRDM1, sous le contrôle de la signalisation BMP/SMAD, est essentiel à l’orientation des cellules CSE vers une identité CGP chez la souris comme chez l’homme. Chez l’humain, deux équipes ont mis en évidence les transcrits PRDM1 dans des CGP obtenues à partir de hCSE par différents protocoles qui seront détaillés ci-après [7, 8]. La famille des gènes très conservés DAZL comporte en particulier les gènes DAZ (ou AZFc), DAZL et BOULE. Les souris knock-out pour Dazl sont stériles car dépourvues de cellules germinales [
9]. Par ailleurs, chez l’homme 15 % des patients azoospermes ou oligozoospermes sont porteurs d’une microdélétion des régions AZF. Kee et al. ont montré par des expériences de surexpression dans des hCSE que DAZL intervient dans la formation des CGP [8]. Régulé par DAZL, VASA reste le marqueur le plus robuste des CGP [8]. Une déficience du gène VASA altère la prolifération et la différenciation des cellules germinales mâles [
10], alors que sa surexpression dans des hCSE induit une différenciation en CGP [5, 8]. Le nombre de CGP augmente lorsque BOULE ou DAZ sont surexprimés [8]. Par ailleurs, plusieurs études ont montré que les CGP obtenues à partir de CSE expriment le gène STELLA [5, 8,
11]. Un autre marqueur pertinent est CXCR4 : l’interaction de CXCR4 avec son ligand SDF1/CXCL12 est nécessaire à la migration des CGP vers les gonades primitives. De plus, CXCR4 n’est pas exprimé par les CSE et c’est un des seuls marqueurs qui permet de distinguer CSE et CGP actuellement. Plusieurs stratégies sont utilisées pour enrichir les cultures en CGP, qui modulent l’environnement cellulaire ou le niveau d’expression des gènes (transfert de gènes). Bucay et al. ont utilisé des conditions de culture permettant l’obtention de petites colonies, et ont ainsi isolé une population contenant 20 à 30 % de cellules CXCR4+ à partir d’hCSE. Les cellules CXCR4+ se différencient plus efficacement en CGP que les cellules CXCR4- et expriment des marqueurs germinaux (KIT, DAZL, PRDM1, VASA) [7]. Une sous-population de CSE exprimant SSEA1 semble également enrichie en cellules capables de différenciation en CGP car elle exprime VASA, OCT4 et STELLA (phénotype des CGP) [11]. Enfin, l’importance de l’expression du gène STELLA dans le déterminisme germinal des mCSE a aussi été démontrée par la génération de souris transgéniques [12]. Park et al. améliorent le nombre de CGP obtenues à partir de CSE, mais également à partir de hIPS, en cocultivant ces cellules avec des cellules stromales gonadiques fœtales humaines. Dans ces conditions de culture, les auteurs sélectionnent à J7 une population SSEA1+KIT+VASA+ représentant 8 à 10 % des cellules et correspondant à des CGP qui expriment PRMD1, STELLA et DAZL. Des résultats identiques sont obtenus à partir de hCSE avec cette triple sélection [13]. Tous ces travaux concernent l’obtention de CGP à partir de cellules pluripotentes, CSE et iPS. Seuls, Clark et al. démontrent que des cellules de type gonocytes - donc à un stade en aval des CGP - peuvent être obtenues à partir de corps embryoïdes en culture. Cependant, ces cellules expriment des marqueurs germinaux spécifiques préméiotiques (OCT4, NANOG, STELLA, GDF3, PUM2, NANOS), postméiotiques (SCP1/3, MLH1, TEKT1, GDF9) ou les deux (DAZL, VASA) [5]. En conclusion, s’il a été possible d’isoler des populations enrichies en CGP, l’expression de marqueurs spécifiques des CGP est associée à celle de marqueurs plus tardifs soulignant l’absence de transition nette, in vitro, entre le stade CGP et les stades méiotiques ultérieurs. |
Différenciation germinale mâle à partir des CSE Dans le testicule, les gonocytes se divisent de façon importante et atteignent progressivement des points de transition critiques avant de s’engager dans les processus de méiose et de la différenciation mâle. Cette orientation dépend de facteurs locaux (BMP [bone morphogenic proteins], acide rétinoïque) et plus particulièrement de la niche cellulaire constituée par les cellules de Sertoli, de Leydig et les cellules myoïdes. À ces facteurs paracrines s’ajoutent à la puberté des facteurs hormonaux dépendants de l’axe hypothalamo-hypophysaire (LH [luteinizing hormone], FSH [follicle-stimulating hormone]) qui permettent une spermatogenèse complète [
14,
30]. Ces événements se succèdent selon une chronologie rigoureuse qu’il faut tenter de reproduire in vitro. Des études ont été réalisées à partir de CSE et ont permis d’obtenir in vitro des cellules germinales mâles à différents stades de la spermatogenèse (spermatogonies, spermatides, spermatozoïdes). La transition CGP ou gonocyte n’est pas caractérisée dans toutes les études. Clark et al. ont montré, en se basant sur la présence de marqueurs méiotiques (SCP1/3, MLH1, TEKT1), que les hCSE, une fois obtenu le stade gonocyte comme décrit ci-dessus, sont capables de différenciation spontanée en cellules germinales mâles. Cependant, aucun critère morphologique n’a été décrit [5]. D’autres auteurs ont induit la différenciation des hCSE en cellules germinales mâles par différents facteurs (acide rétinoïque, BMP, extraits testiculaires, laminine) ou par l’expression ciblée de gènes exprimés par les CGP
(Figure 2
,
Tableau II)
. Ainsi, Bucay et al. sélectionnent une population CGP CXCR4+ qu’ils cultivent en présence de laminine-1, et obtiennent des cellules qui expriment le récepteur de la FSH, l’AMH (antimullerian hormone) et le récepteur de la LH (exprimés en particulier par les cellules de Sertoli et de Leydig) et des marqueurs spécifiques de la différenciation mâle (SOX9, ACR) [7]. West et al., à partir d’une population OCT3+/VASA+ (stade CGP pré/postmigratoire) dont ils ont prolongé la différenciation, ont identifié l’expression de déterminants du stade spermatogonie (PUM2, DAZ1/4 et NANOS1) et des marqueurs méiotiques (SCP3 et MLH1) [15].
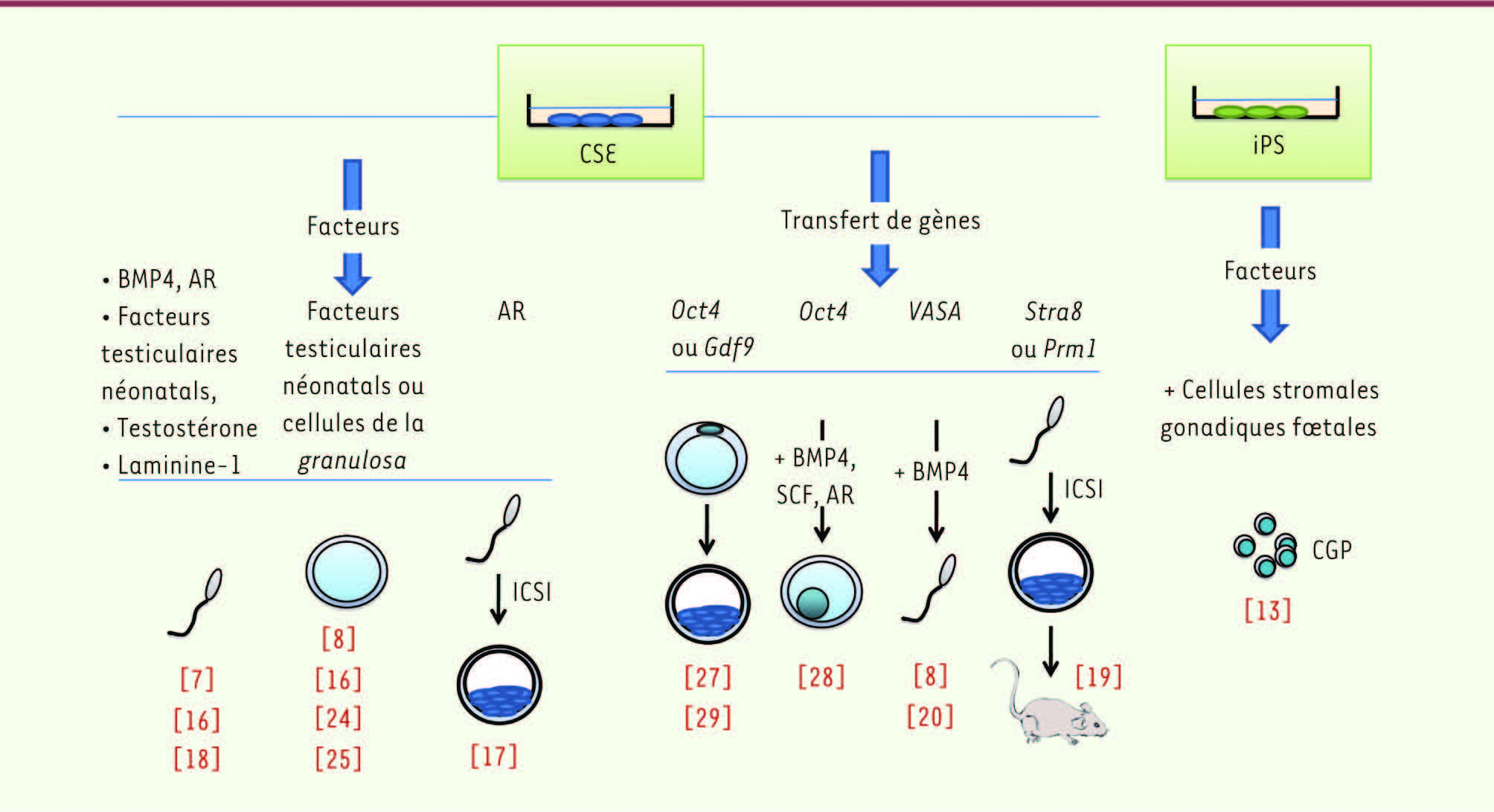
 | Figure 2.
Principaux protocoles de différenciation germinale in vitro à partir de CSE et d’iPS. La première stratégie utilise l’influence de microenvironnements cellulaires (facteurs/hormones solubles ajoutés dans le milieu de culture et/ou coculture cellulaire). La deuxième stratégie, uniquement testée sur les CSE, est basée sur un transfert de gènes associé ou non à l’ajout de facteurs/hormones dans le milieu de culture. AR : acide rétinoïque ; iPS : induced pluripotent stem cells ; CSE : cellules souches embryonnaires ; ICSI : intracytoplasmic sperm injection. |
Tableau II.
|
Phénotype |
Source |
Fonctionnalité
|
Techniques d’étude du phénotype
|
Références |
| Test |
Résultats |
Culture |
Ma |
Mo |
|
Précurseurs des cellules germinales
|
CGP |
hCSE,XX,XY |
- |
- |
CM |
+ |
- |
[13] |
| hiPS,XY |
- |
- |
CM |
+ |
- |
[13] |
| mCSE |
- |
- |
CE |
+ |
- |
[12] |
| hCSE,XX,XY |
- |
- |
CM |
+ |
+ |
[8] |
| CGP migrantes |
hCSE,XX |
- |
- |
CM |
+ |
+ |
[7] |
| CGP pré/postmigratoires |
hCSE,XY |
- |
- |
CM |
+ |
- |
[15] |
| CGP/gonocytes |
hCSE,XX,XY |
- |
- |
CE |
+ |
- |
[5] |
|
|
Différenciation mâle
|
Cellules germinales mâles |
hCSE,XX,XY |
- |
- |
CE |
+ |
- |
[5] |
| mCSE,XY |
ICSI, transplantation in vivo
|
Blastocystes |
CM |
+ |
+ |
[19] |
| mCSE,XY |
- |
- |
CE |
+ |
- |
[18] |
| hCSE,XX |
- |
- |
CM |
+ |
- |
[7] |
| Spermatogonies |
hCSE,XY |
- |
- |
CM |
+ |
- |
[15] |
| Spermatides rondes |
mCSE,XY |
ICSI |
Morulas, blastocystes |
CE |
+ |
+ |
[17] |
| hCSE,XX,XY |
- |
- |
CE |
+ |
+ |
[16] |
| hCSE,XX,XY |
- |
- |
CM |
+ |
+ |
[8] |
| Spermatozoïdes |
mCSE,XY |
- |
- |
CE |
+ |
+ |
[20] |
| Cellules somatiques |
hCSE,XX,XY |
Dosage |
Œstradiol, DHT |
CE |
- |
- |
[16] |
| Cellules de Sertoli |
hCSE,XX |
- |
- |
CM |
+ |
- |
[7] |
| Cellules de Leydig |
hCSE,XX |
- |
- |
CM |
+ |
+ |
[7] |
| Cellules de Sertoli/Leydig |
hCSE,XX,XY |
- |
- |
CM |
+ |
- |
[8] |
|
|
Différenciation femelle
|
Ovocytes |
mCSE,XY |
- |
- |
CE |
+ |
+ |
[25] |
| mCSE,XY |
- |
- |
CM/CE |
+ |
+ |
[23] |
| hCSE,XX |
- |
- |
CM/CE |
+ |
+ |
[22] |
| mCSE,XY |
- |
- |
CE |
+ |
+ |
[24] |
| hCSE |
- |
- |
CE |
+ |
+ |
[16] |
| Ovocytes (vésicule germinale) |
mCSE,XX,XY |
Transplantation in vivo
|
- |
CE |
+ |
+ |
[28] |
| Ovocytes, globules polaires |
mCSE,XX |
Culture |
Zygotes parthénogénétiques |
CE |
+ |
+ |
[29] |
| mCSE,XX,XY |
Culture |
Blastocystes parthénogénétiques |
CM |
+ |
+ |
[27] |
| Follicules |
mCSE,XY |
- |
- |
CE |
- |
+ |
[24] |
| hCSE,XX |
- |
- |
CM/CE |
- |
+ |
[22] |
| Follicules primordiaux |
hCSE |
Dosage |
Œstradiol, DHT |
CE |
+ |
+ |
[16] |
| Follicules primordiaux/primaires |
mCSE,XY |
Dosage |
Œstradiol |
CM/CE |
+ |
+ |
[23] |
| mCSE,XX,XY |
- |
- |
CE |
- |
+ |
[28] |
| Follicules primaires/secondaires |
mCSE,XX,XY |
Dosage |
Œstradiol |
CM |
+ |
+ |
[27] |
Principales études décrivant la différenciation in vitro de CGP et de cellules germinales à partir des CSE et iPS. CE : corps embryonnaires ; CGP : cellules germinales primordiales ; CM : culture en monocouche ; DHT : dihydrotestostérone ; hiPS : human induced pluripotent stem cells ; hCSE : cellules souches embryonnaires humaines ; ICSI : intracytoplasmic sperm injection ; mCSE : cellules souches embryonnaires murines ; Ma : marqueurs ; Mo : morphologie. |
Dans ces études, les cellules sélectionnées ont été cultivées avec différents facteurs (BMP4, acide rétinoïque ou une préparation de testicules néonataux) et l’acide rétinoïque semble être le plus efficace des inducteurs, chez l’homme comme chez la souris. Dans ces conditions (après sélection d’une population de CGP SSEA1+c-KIT+), Aflatoonian et al. ont obtenu des spermatides à partir de hCSE [16]. Les cellules humaines différenciées expriment progressivement des transcrits germinaux précoces (DAZL, VASA), méiotique (SCP3) et spermatiques (TNP1, PRM1/2). Dans cette étude, des spermatides rondes haploïdes avec un noyau compacté et l’émergence d’un flagelle ont été obtenues [16]. Parallèlement, les auteurs ont aussi observé une sécrétion de dihydrotestostérone et d’œstradiol dans le milieu de culture, deux hormones-clés de la spermatogenèse synthétisées par les cellules somatiques [16]. Chez la souris, Geijsen et al. ont également obtenu des cellules germinales mâles haploïdes par sélection d’une population de cellules SSEA1+Oct4+ sélectionnée à partir de corps embryoïdes dérivés de CSE. Cette différenciation se fait en présence d’acide rétinoïque [17]. L’effacement de l’empreinte génomique [
34] et l’expression des transcrits LHR, AMH et Sry et de ceux codant l’acrosine et l’haprine ont été mis en évidence. Des blastocystes, dont la diploïdie a été confirmée par hybridation in situ fluorescente, se sont développés après injection intracytoplasmique (ICSI, intracytoplasmic sperm injection) de ces spermatides rondes dans des ovocytes [17]. D’autres auteurs ont montré que l’acide rétinoïque, en association avec la testostérone, permet l’expression de gènes spécifiques de la lignée germinale mâle (Act et Prm1). Cependant, le phénotype morphologique des cellules obtenues n’a pas été décrit ni leur fonctionnalité testée [18]. Un certain nombre d’auteurs forcent l’expression de gènes spécifiques pour obtenir des cellules mâles différenciées. Ainsi, le transfert des gènes de fusion Stra8-EGFP (extended green fluorescent protein) ou Prm1-DsRed en présence d’acide rétinoïque a permis la formation de gamètes mâles haploïdes à partir de CSE de souris. Pour montrer que ces gamètes étaient fonctionnels après fécondation par ICSI, 65 embryons au stade 2 cellules ont été transférés dans les trompes de femelles pseudogestantes. Douze naissances ont été obtenues, mais tous les nouveau-nés sont décédés entre J5 et le 5e mois. L’hypothèse d’un défaut de l’empreinte génomique à l’origine de cette mortalité néonatale est la plus probable [19]. Chez l’humain, Kee et al. ont transfecté le gène rapporteur VASA-GFP dans des hCSE, puis, dans un second temps, ils ont surexprimé dans les cellules GFP+ sélectionnnées les gènes DAZ, DAZL et BOULE [8]. Des gamètes mâles de type spermatides rondes, haploïdes et exprimant des marqueurs méiotiques/germinaux (SCP3, ACR) ont été obtenus [8]. Chez la souris, Toyooka et al. ont cultivé des mCSE knock-in (vecteurs IRES-GFP et IRES-LacZ) pour le gène VASA [20]. Ces cellules VASA+ cocultivées avec des cellules produisant BMP4 se sont différenciées en CGP. La transplantation de ces CGP dans des testicules receveurs a induit la formation de spermatozoïdes matures, détectables dans la lumière des tubules séminifères. C’est la première démonstration de l’importance de la niche cellulaire pour le développement germinal [20]. Ainsi, les tentatives de différenciation de cellules souches pluripotentes en gamètes mâles font appel à une sélection de déterminants moléculaires précis. L’haploïdisation des cellules a été rapportée dans quatre études [8, 16, 17, 19] mais sur un nombre restreint de cellules. La différenciation mâle obtenue dans l’ensemble de ces études n’est pas totalement complète (morphologie peu décrite), et la fonctionnalité des cellules germinales obtenues n’a pas encore été testée chez l’humain. En revanche, chez la souris, les expériences d’ICSI se sont révélées encourageantes puisqu’elles aboutissent au développement d’embryons [17, 19]. |
Différenciation germinale femelle à partir des CSE L’ovogenèse est un processus discontinu au cours de la vie. La méiose débute pendant la vie fœtale, se bloque avant la naissance, reprend à la puberté, s’arrête à nouveau puis s’achève avec la fécondation. La formation des gamètes dans l’ovaire est un phénomène cyclique associé à une apoptose importante. La relation entre l’ovogenèse et la folliculogenèse souligne le lien étroit et essentiel qui existe entre les cellules somatiques et germinales dans l’ovaire. La folliculogenèse est d’abord sous la dépendance de facteurs locaux (système KIT/KIT ligand [ou stem cell factor], TGFβ, GDF9, AMH, androgènes) et devient ensuite sensible aux, puis dépendante des, gonadotrophines hypophysaires LH et FSH [
21]. Des structures de type follicule ovarien ont été obtenues à partir de hCSE en culture sans ajout d’inducteurs spécifiques [22]. Dans le cas de hCSE, ces structures, obtenues après 21 jours de culture, expriment les facteurs STELLA et GDF9 puis dégénèrent rapidement [22]. Celles qui sont obtenues à partir de mCSE sont de type follicules primordiaux et primaires mais n’ont pas une organisation chromosomique de type méiotique [23]. La protéine SCP3 - composant du complexe synaptonémal1 - est présente, mais sa localisation atypique et ses partenaires moléculaires n’ont pas été mis en évidence. La présence croissante d’œstradiol traduit la fonctionnalité des cellules de type somatique. Des facteurs testiculaires néonataux permettent la différenciation ovocytaire in vitro. En utilisant ce type de culture et en partant de hCSE SSEA1+, Aflatoonian et al. ont obtenu des cellules de type ovocyte ainsi que des structures de type follicule primordial [16]. L’expression de SCP3 et de GDF9 a été détectée mais aucune protéine constitutive de la zone pellucide n’a été mise en évidence [16]. Chez la souris, des ovocytes avec assises cellulaires de type folliculaires ont été obtenus à partir de CSE cultivées de la même façon. L’expression de Zp3 et de Figα a été détectée sans que la zone pellucide ne soit visible [24]. Qing et al., qui soulignent la nécessité de reproduire in vitro les interactions cellulaires entre cellules germinales et cellules somatiques, ont cocultivé des CGP dérivées de mCSE avec des cellules de la granulosa. Les ovocytes obtenus expriment les transcrits Gdf9, Zp1/3 et Scp3, ont une morphologie typique mais sans zone pellucide bien individualisable [25]. La différenciation ovocytaire la plus complète a été obtenue à partir de mCSE par expression forcée (transfert de gènes) des facteurs Oct4 ou Gdf9 chez la souris. Le facteur Oct4, exprimé dans les cellules pluripotentes, est réexprimé dans les ovocytes en croissance après leur arrêt en méiose I ; son expression reste faible au cours des derniers stades de la maturation ovocytaire [
26]. Dans des mCSE, Hubner et al. ont réalisé une expression ciblée d’Oct4 (gcOct4-GFP) puis, après sélection et culture d’une rare population coexprimant GFP et Kit, ont obtenu une population cellulaire exprimant des marqueurs spécifiques de la lignée germinale tels Gdf9 et Scp3 [27]. Les ovocytes obtenus sont entourés d’une zone pellucide et expriment les protéines membranaires Zp2 et Zp3. Les structures de type follicules ont une morphologie typique, une organisation tridimensionnelle, expriment des enzymes de la stéroïdogenèse et sécrètent de l’œstradiol. Leur stimulation par PMSG (pregnant mare serum gonadotropin) et hCG (human chorionic gonadotropin) induit l’expulsion des ovocytes et la formation d’une structure de type globule polaire suggérant l’achèvement de la première division méiotique. Des embryons parthénogénétiques ont été observés qui se développent jusqu’au stade blastocyste [27]. Toujours à partir de mCSE transgéniques surexprimant Oct4, Nicholas et al. ont obtenu des cellules ayant une structure de type ovocytaire en sélectionnant secondairement une population SSEA1- [28]. La culture est effectuée en présence de certains facteurs (BMP4, Kit-ligand/SCF et acide rétinoïque). Les auteurs montrent que ces cellules ont débuté leur méiose, mais la localisation chromosomique de SCP3 reste partielle. Ces cellules, greffées sous la capsule rénale de souris receveuses, sont capables de constituer des follicules primordiaux et primaires [28]. Enfin, la transfection du promoteur du gène Gdf9 dans des mCSE permet l’expression d’un phénotype ovocytaire (formation d’une zone pellucide avec expression de Zp3, fuseau métaphasique typique avec chromosomes condensés et globule polaire), puis l’obtention de zygotes parthénogénétiques aux stades 2 puis 4 cellules [29]. En conclusion, une ébauche de différenciation en gamètes femelles à partir de CSE est possible. Cependant, la fonctionnalité des ovocytes ainsi formés n’a pas été démontrée chez l’humain. Chez la souris, un développement parthénogénétique d’embryons a été décrit [27, 29]. |
Conclusions et perspectives La formation in vitro de gamètes à partir de cellules souches pluripotentes semble à bien des égards un parcours complexe et aucune équipe n’a obtenu, à ce jour, des gamètes humains totalement matures et fonctionnels. Cependant, les résultats dans l’espèce humaine évoluent de façon rapide et la naissance récente d’une portée chez la souris après fécondation d’ovocytes (ICSI) par des gamètes mâles provenant de cellules souches embryonnaires démontre la pertinence du modèle animal dans ce domaine. Néanmoins, d’autres modèles animaux dont la physiologie de la gamétogenèse est plus proche de celle de l’homme (porc, bovin) pourraient permettre des avancées plus rapides. L’ensemble des résultats montre qu’il est plus aisé d’obtenir des gamètes mâles avec une morphologie et des caractéristiques méiotiques typiques que des ovocytes matures. En effet, seule la fonctionnalité des spermatozoïdes murins a été testée par ICSI. Néanmoins, les souriceaux issus des expérimentations ont une durée de vie très limitée, pointant l’existence à ce jour de facteurs non maîtrisés pour une différenciation complète de la lignée mâle. Si le sexe chromosomique de la lignée de cellules souches de départ n’a pas d’influence sur l’orientation mâle ou femelle de la différenciation, des facteurs épigénétiques actuellement méconnus mais indispensables à l’établissement de l’empreinte ou à certains stades de la différenciation, peuvent être responsables de cette déficience. La réussite de la gamétogenèse est liée non seulement à des actions directes sur les cellules concernées, mais également à l’interaction des cellules germinales avec les cellules somatiques voisines. Les études actuelles ont été surtout centrées sur l’obtention d’un gamète mature. Les expérimentations ciblées sur les cellules somatiques associées aux gamètes et leurs facteurs régulateurs ont été très peu développées à ce jour. Or, la mise en place de l’axe gonadotrope et son impact sur les cellules somatiques, et indirectement sur le gamète, est une étape décisive pour l’accomplissement de la gamétogenèse. L’ensemble des données obtenues à ce jour participe à une meilleure compréhension des mécanismes impliqués dans la différenciation et le développement de la lignée germinale. Cependant, se posent de nouvelles questions dont la résolution est indispensable pour la réalisation d’une gamétogenèse fonctionnelle et par conséquent pour les perspectives thérapeutiques dans l’infertilité liée à des pathologies sévères de la gamétogenèse.
|
ACR
|
acrosomal
|
|
AMH
|
anti-mullerian hormone
|
|
AZF
|
azoospermia factor
|
|
BMP4
|
bone morphogenetic protein 4
|
|
c-MYC
|
c-myelocytomatosis oncogene
|
|
CGP
|
cellules germinales primordiales |
|
CSE
|
cellules souches embryonnaires |
|
CXCR4
|
récepteur de la chimiokine CXCL12 (ou SDF1) |
|
CYP26B1
|
cytochrome p450, family 26, subfamily B, polypeptide 1 |
|
DAZL
|
deleted in azoospermia
|
|
FIGα
|
factor in the germline alpha
|
|
GDF3, GDF9
|
growth differentiation factor-3 and -9
|
|
hCG
|
human chorionic gonadotropin
|
|
KLF4
|
kruppel-like factor 4
|
|
MLH1
|
MutL homolog 1
|
|
NANOS1
|
Nanos homolog 1 |
|
NANOG
|
Nanog homeobox
|
|
PMSG
|
pregnant mare’s serum gonadotropin
|
|
PRDM1 (ou Blimp1)
|
positive regulatory domain I
|
|
PRMT5
|
protein arginine methyltransferase 5
|
|
PUM2
|
pumilio homolog 2
|
|
SCF
|
stem cell factor (ligand de KIT)
|
|
SCP1/3
|
synaptonemal complex protein 1/3
|
|
SOX9
|
SRY (sex région de détermination de Y)-box 9
|
|
SSEA1
|
stage-specific embryonic antigen 1
|
|
TEKT1
|
tektin 1
|
|
TERT
|
telomerase reverse transcriptase
|
|
TGFβ
|
transforming growth factor beta
|
|
Zp2, Zp3
|
zone pellucide glycoprotéine 2/3 |
|
|
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
|
Footnotes |
-
Testart
J.
Des ovules en abondance ?
Med Sci (Paris).
2004; ; 20 : :1041.–1044.
-
Guenatri
M
,
Bourc’his
D.
Sperme express : est-il possible de produire des gamètes mâles in vitro en trois jours ?
Med Sci (Paris).
2007; ; 23 : :619.–625.
-
Takahashi
K
,
Yamanaka
S.
Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors . Cell.
2006; ; 126 : :663.–676.
-
Takahashi
K
,
Tanabe
K
,
Ohnuki
M
, et al.
Induction of pluripotent stem cells from adult human fibroblasts by defined factors . Cell.
2007; ; 131 : :861.–872.
-
Clark
AT
,
Bodnar
MS
,
Fox
M
, et al.
Spontaneous differentiation of germ cells from human embryonic stem cells in vitro . Hum Mol Genet.
2004; ; 13 : :727.–739.
-
Kurimoto
K
,
Yabuta
Y
,
Ohinata
Y
, et al.
Complex genome-wide transcription dynamics orchestrated by Blimp1 for the specification of the germ cell lineage in mice . Genes Dev.
2008; ; 22 : :1617.–1635.
-
Bucay
N
,
Yebra
M
,
Cirulli
V
, et al.
A novel approach for the derivation of putative primordial germ cells and sertoli cells from human embryonic stem cells . Stem Cells.
2008; ; 27 : :68.–77.
-
Kee
K
,
Angeles
VT
,
Flores
M
, et al.
Human DAZL, DAZ and BOULE genes modulate primordial germ-cell and haploid gamete formation . Nature.
2009; ; 462 : :222.–225.
-
Saunders
PT
,
Turner
JM
,
Ruggiu
M
, et al.
Absence of mDazl produces a final block on germ cell development at meiosis . Reproduction.
2003; ; 126 : :589.–597.
-
Tanaka
SS
,
Toyooka
Y
,
Akasu
R
, et al.
The mouse homolog of Drosophila Vasa is required for the development of male germ cells . Genes Dev.
2000; ; 14 : :841.–853.
-
Tilgner
K
,
Atkinson
SP
,
Golebiewska
A
, et al.
Isolation of primordial germ cells from differentiating human embryonic stem cells . Stem Cells.
2008; ; 26 : :3075.–3085.
-
Payer
B
,
Chuva de Sousa Lopes
SM
,
Barton
SC
, et al.
Generation of stella-GFP transgenic mice: a novel tool to study germ cell development . Genesis.
2006; ; 44 : :75.–83.
-
Park
TS
,
Galic
Z
,
Conway
AE
, et al.
Derivation of primordial germ cells from human embryonic and induced pluripotent stem cells is significantly improved by coculture with human fetal gonadal . Stem Cells.
2009; ; 27 : :783.–795.
-
Ruwanpura
SM
,
McLachlan
RI
,
Meachem
SJ.
Hormonal regulation of male germ cell development . J Endocrinol.
2010; ; 205 : :117.–131.
-
West
F
,
Machacek
D
,
Boyd
N
, et al.
Enrichment and differentiation of human germ-like cells mediated by feeder cells and basic fibroblast growth factor signaling . Stem Cells.
2008; ; 26 : :2768.–2776.
-
Aflatoonian
B
,
Ruban
L
,
Jones
M
, et al.
In vitro post-meiotic germ cell development from human embryonic stem cells . Hum Reprod.
2009; ; 24 : :3150.–3159.
-
Geijsen
N
,
Horoschak
M
,
Kim
K
, et al.
Derivation of embryonic germ cells and male gametes from embryonic stem cells . Nature.
2003; ; 427 : :148.–154.
-
Silva
C
,
Wood
JR
,
Salvador
L
, et al.
Expression profile of male germ cell-associated genes in mouse embryonic stem cell cultures treated with all-trans retinoic acid and testosterone . Mol Reprod Dev.
2009; ; 76 : :11.–21.
-
Nayernia
K
,
Nolte
J
,
Michelmann
HW
, et al.
In vitro-differentiated embryonic stem cells give rise to male gametes that can generate offspring mice . Dev Cell.
2006; ; 11 : :1125.–1132.
-
Toyooka
Y
,
Tsunekawa
N
,
Akasu
R
, et al.
Embryonic stem cells can form germ cells in vitro
. Proc Natl Acad Sci USA.
2003; ; 100 : :11457.–11462.
-
McGee
EA
,
Hsueh
AJ.
Initial and cyclic recruitment of ovarian follicles . Endocr Rev.
2000; ; 21 : :200.–214.
-
Chen
HF
,
Kuo
HC
,
Chien
CL
, et al.
Derivation, characterization and differentiation of human embryonic stem cells : comparing serum-containing versus serum-free media and evidence of germ cell differentiation . Hum Reprod.
2007; ; 22 : :567.–577.
-
Novak
I
,
Lightfoot
DA
,
Wang
H
, et al.
Mouse embryonic stem cells form follicle-like ovarian structures but do not progress through meiosis . Stem Cells.
2006; ; 24 : :1931.–1936.
-
Lacham-Kaplan
O
,
Chy
H
,
Trounson
A.
Testicular cell conditioned medium supports differentiation of embryonic stem cells into ovarian structures containing oocytes . Stem Cells.
2005; ; 24 : :266.–273.
-
Qing
T
,
Shi
Y
,
Qin
H
, et al.
Induction of oocyte-like cells from mouse embryonic stem cells by co-culture with ovarian granulosa cells . Differentiation.
2007; ; 75 : :902.–911.
-
Pesce
M
,
Wang
X
,
Wolgemuth
DJ
, et al.
Differential expression of the Oct-4 transcription factor during mouse germ cell differentiation . Mech Dev.
1998; ; 71 : :89.–98.
-
Hübner
K
,
Fuhrmann
G
,
Christenson
LK
, et al.
Derivation of oocytes from mouse embryonic stem cells . Science.
2003; ; 300 : :1251.–1256.
-
Nicholas
CR
,
Haston
KM
,
Grewall
AK
, et al.
Transplantation directs oocyte maturation from embryonic stem cells and provides a therapeutic strategy for female infertility . Hum Mol Genet.
2009; ; 18 : :4376.–4389.
-
Salvador
L
,
Silva
C
,
Kostetskii
I
, et al.
The promoter of the oocyte-specific gene, Gdf9, is active in population of cultured mouse embryonic with an oocyte-like phenotype methods . Stem Cells.
2008; ; 45 : :172.–181.
-
Méduri
G
,
Courtillot
C
,
Lahuna
O
, et al.
Spermatogenèse normale chez un homme avec défaut génétique de la LH . Med Sci (Paris).
2010; ; 26 : :690.–693.
-
Terret
ME
,
Wassmann
K.
Le point faible méiotique : la première division . Med Sci (Paris).
2008; ; 24 : :197.–203.
-
Grey
C
,
Sommermeyer
V
,
Borde
V
,
de Massy
B.
Déterminants de la carte génétique : le rôle-clé de la spécification des sites de recombinaison méiotique . Med Sci (Paris).
2011; ; 27 : :63.–69.
-
Gabory
A
,
Dandolo
L.
Épigénétique et développement : l’empreinte parentale . Med Sci (Paris).
2005; ; 21 : :390.–395.
-
Henckel
A
,
Feil
R.
Asymétrie des génomes parentaux : implications en pathologie . Med Sci (Paris).
2008; ; 24 : :747.–752.
|