| |
| Med Sci (Paris). 2007 October; 23(10): 800–803. Published online 2007 October 15. doi: 10.1051/medsci/20072310800.Association d’anticorps anti-EGFR et anti-HER2 Efficacité pré-clinique dans le traitement du cancer du pancreas Christel Larbouret, Bruno Robert, Isabelle Teulon, David Azria, and André Pèlegrin* Centre de Recherche en Cancérologie de Montpellier (CRCM) Inserm U860 Immunociblage et Radiobiologie en Oncologie Université Montpellier 1 CRLC Val d’Aurelle-Paul Lamarque, 34298 Montpellier, France MeSH keywords: Adénocarcinome, Animaux, Anticorps monoclonaux, Anticorps monoclonaux humanisés, Dimérisation, Humains, Immunothérapie, Souris, Protéines tumorales, Tumeurs du pancréas, Récepteur facteur croissance épidermique, Récepteur erbB-2, Tests d'activité antitumorale sur modèle de xénogreffe |
Les thérapies ciblées contre la famille des récepteurs de facteurs de croissance ont aujourd’hui une place incontournable dans l’arsenal thérapeutique en cancérologie, qu’il s’agisse d’inhibiteurs de tyrosine kinase (TKI) ou d’anticorps monoclonaux (AcM). Cela s’explique par le rôle crucial joué par ces récepteurs dans la prolifération cellulaire et l’accroissement de la masse tumorale. L’interaction entre le récepteur de l’EGF (EGFR, epidermal growth factor receptor ou HER1) et HER2 lorsqu’ils sont co-exprimés à la surface membranaire et leur coopérativité dans l’induction des signaux intracellulaires semblent être responsables d’une plus grande agressivité tumorale et font de ces deux récepteurs des cibles thérapeutiques. Depuis leur découverte, en 1978 pour l’EGFR, et en 1985 pour HER2, les nombreux travaux de recherche menés sur cette famille de récepteurs ont permis d’établir une passerelle entre la cible biologique impliquée dans la carcinogenèse et le développement de thérapies ciblées. |
La famille HER est composée de quatre récepteurs transmembranaires à activité tyrosine kinase dont l’EGFR et HER2 [
1]. Seul EGFR possède des ligands naturels qui peuvent participer à une boucle autocrine. La fixation d’un ligand tel que EGF sur la partie extracellulaire de son récepteur va induire un changement de conformation et une homodimérisation ou une hétérodimérisation avec un autre récepteur de la même famille (HER2, HER3, HER4). Les résidus tyrosines intracellulaires s’autophosphorylent et deviennent des points d’ancrage pour des complexes protéiques qui vont, à leur tour, activer de nombreuses cascades de signalisation, dont les voies MAPK ou AKT. Finalement, le complexe ligand/récepteur est internalisé et l’expression de gènes impliqués dans la croissance cellulaire, l’inhibition de l’apoptose, l’angiogenèse ou le processus métastatique est induite [
2]. Ces récepteurs ne sont donc actifs que sous forme de dimères dont la composition joue un rôle dans la diversification des signaux intracellulaires et dans le potentiel carcinogène [
3]. |
EGFR et HER2, cibles thérapeutiques EGFR et HER2 interviennent dans la carcinogenèse de différents cancers selon des modalités variées. Tout d’abord, des études immunohistochimiques ont montré leur forte expression au niveau membranaire dans différents cancers. Par exemple, le récepteur HER2 est exprimé dans 20 % à 30 % des cancers du sein mais également dans les cancers de l’ovaire, du côlon ou du pancréas. L’EGFR, lui, est fortement exprimé dans les cancers épidermoïdes de la tête et du cou, VADS (cancers des voies aérodigestives supérieures), cancers du côlon, du pancréas, de l’ovaire et de la vessie. Dans les cancers du sein, la surexpression de HER2 est associée à un mauvais pronostic et à une valeur prédictive de la réponse au trastuzumab (AcM dirigé contre HER2). En revanche, la corrélation entre la surexpression de EGFR et le pronostic tumoral ou la réponse thérapeutique à un agent anti-EGFR n’a pas été validée et reste controversée [
4]. La co-expression de ces deux récepteurs dans un même tissu est moins documentée mais semble associée à un plus mauvais pronostic dans les cancers du sein [
5] et du côlon [
6]. Par ailleurs, certaines conséquences de l’interaction d’EGFR avec HER2 telles que l’inhibition de l’endocytose de EGFR [
7], l’augmentation du recyclage de l’hétérodimère à la surface cellulaire [
8], ou la diminution de la dissociation du ligand EGF de son récepteur [
9], conduisent à prolonger l’activation et la signalisation de ces deux récepteurs. |
Ciblage de l’EGFR et HER2 en clinique Les deux stratégies actuellement validées en clinique sont les inhibiteurs de tyrosine kinase (TKI) qui agissent au niveau intracellulaire et les AcM dirigés contre le domaine extracellulaire de l’un ou l’autre de ces récepteurs [
10]. Plusieurs Ac dirigés contre l’EGFR ou HER2 ont été approuvés par la FDA et l’EMEA (European Agency for the Evaluation of Medicinal Products) et sont utilisés quotidiennement en clinique, comme le trastuzumab, dirigé contre HER2, pour le traitement du cancer du sein métastatique, ou le cetuximab, dirigé contre EGFR, utilisé en association avec une chimiothérapie dans le cancer du côlon. D’autres AcM sont en cours d’évaluation, comme le matuzumab et le panituzumab (anti-EGFR) ou le pertuzumab (anti-HER2). En oncologie, les associations thérapeutiques sont la règle car elles permettent d’optimiser les réponses thérapeutiques tout en permettant de traiter un plus grand nombre de patients. L’association de molécules ciblant différentes voies de signalisation peut être la clé d’une meilleure réponse thérapeutique [
11]. Concernant l’EGFR et HER2, certains auteurs ont associé des TKI à des AcM dirigés contre l’EGFR ou HER2 de manière à cibler les deux récepteurs à la fois [
12]. D’autres ont associé des AcM dirigés contre des épitopes différents d’une même cible comme la combinaison du trastuzumab et du pertuzumab [
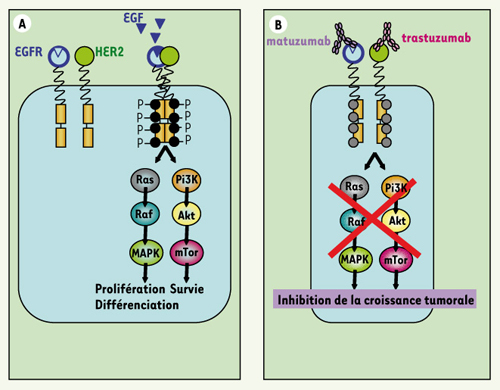
13]. Dans ce contexte d’association thérapeutique, la stratégie développée dans notre laboratoire est basée sur la biologie des récepteurs de la famille HER. L’EGFR et HER2 étant impliqués dans les cancers essentiellement sous forme d’hétérodimères EGFR-HER2, nous avons associé deux AcM humanisés, le matuzumab et le trastuzumab, respectivement dirigés contre l’EGFR et HER2 (Figure 1).  | Figure 1.
A.Représentation schématique de la signalisation des dimères EGFR/HER2.B. Stratégie utilisée pour bloquer l’activation des récepteurs EGFR et HER2.
|
|
Efficacité thérapeutique in vivo de l’association de deux anticorps monoclonaux dirigés contre l’EGFR et HER2 dans le traitement du cancer du pancréas L’association trastuzumab-matuzumab a été évaluée chez des souris immunodéficientes porteuses de carcinomes pancréatiques humains [
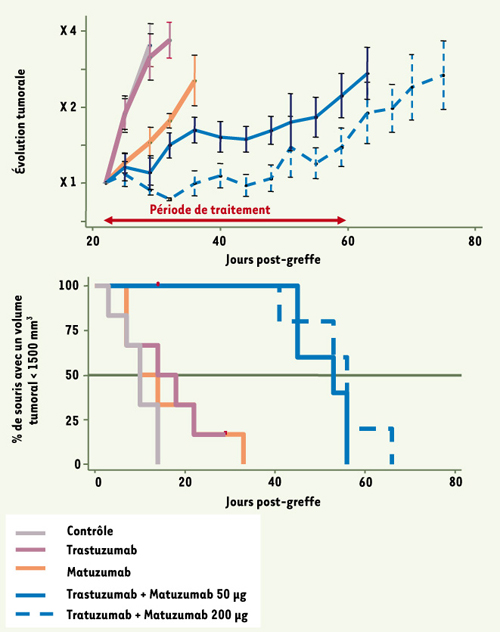
14]. Le traitement a consisté en l’injection par voie intrapéritonéale, deux fois par semaine pendant quatre semaines, des anticorps soit seuls, soit en association. L’étude a montré l’efficacité thérapeutique de l’association des deux AcM, incluant une inhibition significative de la croissance tumorale et la rémission complète de certaines tumeurs. Cet important ralentissement de la croissance tumorale a été observé lorsque le traitement a débuté avec des tumeurs de petits volumes mais également avec des tumeurs bien implantées, de gros volume. L’association d’anticorps a montré un effet anti-tumoral supérieur à celui obtenu avec des doses quatre fois plus importantes d’anticorps seuls, suggérant une synergie entre le matuzumab et le trastuzumab (Figure 2).  | Figure 2.
Effet in vivo du trastuzumab et du matuzumab, seuls ou en association, sur la croissance des tumeurs BxPC-3 d’un volume moyen de 500 mm3 au début du traitement. Les souris ont été traitées par voie intrapéritonéale deux fois par semaine pendant quatre semaines (200 mg d’anticorps pour les monothérapies, 50 ou 200 mg de chaque anticorps pour l’association). |
Les analyses in vitro suggèrent que cet effet thérapeutique passerait par une inhibition de l’activation des récepteurs EGFR et HER2 via leur phosphorylation ainsi qu’une inhibition des voies de signalisation intracellulaire contrôlant la survie et la différenciation, respectivement AKT et MAPK. L’efficacité thérapeutique de l’association des deux anticorps humanisés trastuzumab-matuzumab a été montrée dans deux modèles de carcinomes pancréatiques mais également dans un modèle de carcinome ovarien, permettant d’envisager le traitement d’autres cancers. Il est important de préciser que les deux carcinomes pancréatiques exprimant faiblement HER2 étaient a priori exclus des thérapies anti-HER2. En effet, le trastuzumab a une efficacité thérapeutique bien documentée dans le cancer du sein mais sa prescription est limitée et uniquement autorisée pour les tumeurs sur-exprimant le récepteur HER2. Actuellement, les patientes ayant des tumeurs exprimant faiblement le récepteur HER2 ne peuvent pas bénéficier de cette thérapie. |
Ces résultats précliniques obtenus in vivo lors de l’association du trastuzumab et du matuzumab dans le cancer du pancréas, la disponibilité de ces deux Ac humanisés et l’absence de thérapie efficace dans cette pathologie nous permettent d’envisager rapidement une étude clinique de phase II. |
1. Yarden Y, Ullrich A. Growth factor receptor tyrosine kinases. Annu Rev Biochem 1988; 57 : 443–78. 2. Hynes NE, Lane HA. ERBB receptors and cancer: the complexity of targeted inhibitors. Nat Rev Cancer 2005; 5 : 341–54. 3. Olayioye MA, Neve RM, Lane HA, et al. The ErbB signaling network: receptor heterodimerization in development and cancer. EMBO J 2000; 19 : 3159–67. 4. Chung KY, Shia J, Kemeny NE, et al. Cetuximab shows activity in colorectal cancer patients with tumors that do not express the epidermal growth factor receptor by immunohistochemistry. J Clin Oncol 2005; 23 : 1803–10. 5. DiGiovanna MP, Stern DF, Edgerton SM, et al. Relationship of epidermal growth factor receptor expression to ErbB-2 signaling activity and prognosis in breast cancer patients. J Clin Oncol 2005; 23 : 1152–60. 6. Porebska I, Harlozi´nska A, Bojarowski T. Expression of the tyrosine kinase activity growth factor receptors (EGFR, ERB B2, ERB B3) in colorectal adenocarcinomas and adenomas. Tumour Biol 2000; 21 : 105–15. 7. Wang Z, Zhang L, Yeung TK, et al. Endocytosis deficiency of epidermal growth factor (EGF) receptor-ErbB2 heterodimers in response to EGF stimulation. Mol Biol Cell 1999; 10 : 1621–36. 8. Baulida J, Kraus MH, Alimandi M, et al. All ErbB receptors other than the epidermal growth factor receptor are endocytosis impaired. J Biol Chem 1996; 271 : 5251–7. 9. Wilkinson JC, Staros JV. Effect of ErbB2 coexpression on the kinetic interactions of epidermal growth factor with its receptor in intact cells. Biochemistry 2002; 41 : 8–14. 10. Citri A, Yarden Y. EGF-ERBB signalling: towards the systems level. Nat Rev Mol Cell Biol 2006; 7 : 505–16. 11. Dancey JE, Chen HX. Strategies for optimizing combinations of molecularly targeted anticancer agents. Nat Rev Drug Discov 2006; 5 : 649–59. 12. Moulder SL, Yakes FM, Muthuswamy SK, et al. Epidermal growth factor receptor (HER1) tyrosine kinase inhibitor ZD1839 (Iressa) inhibits HER2/neu (erbB2)-overexpressing breast cancer cells in vitro and in vivo. Cancer Res 2001; 61 : 8887–95. 13. Walshe JM, Denduluri N, Berman AW, et al. A phase II trial with trastuzumab and pertuzumab in patients with HER2-overexpressed locally advanced and metastatic breast cancer. Clin Breast Cancer 2006; 6 : 535–9. 14. Larbouret C, Robert B, Teulon I, et al. In vivo therapeutic synergism of anti-EGFR and anti-HER2 monoclonal antibodies against pancreatic carcinomas. Clin Can Res 2007; 13 : 3356–62. |