| |
| Med Sci (Paris). 2005 June; 21(6-7): 663–668. Published online 2005 June 15. doi: 10.1051/medsci/2005216-7663.Collaboration entre recherche académique et industrie dans l’étude d’un nouveau médicament antiostéoporotique Romuald Mentaverri,1 Alice Wattel,1 Anne-Sophie Lemaire-Hurtel,1 Said Kamel,1 Alexia Blesius,2 and Michel Brazier1 1Unité de Recherche des mécanismes de la résorption osseuse, Faculté de Pharmacie, 1, rue des Louvels, 80037 Amiens, France 2Institut de Recherches Internationales Servier, Courbevoie, France |
L’ostéoporose est une ostéopathie fragilisante diffuse caractérisée par une masse osseuse basse et une détérioration de la micro-architecture du tissu osseux induisant une fragilité osseuse à l’origine d’un risque de fracture [
1]. En France, l’incidence annuelle des fractures ostéoporotiques est de 130 000, et on estime aujourd’hui qu’environ une femme sur deux sera concernée. Parmi ces fractures, on dénombre 50 000 fractures du col fémoral [
2], et on estime à 40 000 le nombre de fractures du poignet et à 40 000 le nombre de fractures asymptomatiques des vertèbres. De plus, malgré la difficulté d’évaluer le nombre de fractures vertébrales asymptomatiques, on estime qu’il est trois fois supérieur au nombre de fractures vertébrales symptomatiques. Actuellement dans le monde, 1 600 000 fractures de hanche par an ont des conséquences importantes sur la mortalité et la morbidité [2]. La fragilisation osseuse est liée à de multiple facteurs, principalement la masse osseuse, mais aussi la masse corporelle ainsi que des facteurs génétiques et environnementaux. Il a par exemple été décrit que 80 à 85 % de la densité minérale osseuse était déterminée par des facteurs génétiques [
3–
5], et on estime qu’en cas d’antécédent familial de fracture ostéoporotique chez un parent du premier degré, une femme a un risque doublé d’être victime à son tour d’ostéoporose [
6]. Par ailleurs, le vieillissement de la population, qui aura pour conséquence un doublement du nombre des personnes de plus de 65 ans, entraînera d’ici 2040 un doublement du nombre de fractures [
7]. Pour ces différentes raisons, il était important de proposer une prise en charge appropriée de l’ostéoporose, un dépistage élargi, un traitement par des médicaments freinant la perte osseuse et permettant aussi une stimulation de l’ostéogenèse. Les traitements disponibles actuellement sont surtout des médicaments antirésorptifs (bisphosphonates, traitement hormonal, modulateurs sélectifs des récepteurs des œstrogènes). Une nouvelle approche thérapeutique consiste à stimuler la formation osseuse, en particulier chez les sujets dont la perte de masse osseuse est importante (tériparatide). Une autre voie envisagée conjugue une action antirésorptive et une action ostéoformatrice. Servier a développé un médicament présentant cette double activité [
8–
11] et montrant un bénéfice significatif chez les patients traités : le ranélate de strontium formé de 2 atomes de strontium stable couplés à une molécule d’acide ranélique. Le ranélate de strontium permet de réduire significativement l’incidence des fractures vertébrales et de hanche [
12,
13]. Il est établi que le ranélate de strontium agit sur l’ostéoclaste, cellule en charge de la résorption osseuse, mais les mécanismes moléculaires à l’origine de ces effets restent encore mal connus. En raison de notre expertise dans ce domaine, en particulier des modèles cellulaires que nous avons développés, une collaboration scientifique avec Servier a pu être établie afin d’éclairer les mécanismes d’action du ranélate de strontium sur la résorption osseuse et les ostéoclastes. Ainsi, nous avons été amenés à élargir notre champ d’expertise et de nouvelles collaborations scientifiques se sont mises en place par l’intermédiaire de Servier. Cet article illustre la collaboration entre un laboratoire industriel et un laboratoire de recherche académique, décrit les moyens mis à disposition pour permettre une meilleure connaissance d’un produit et l’évolution de cette collaboration pour accéder à de nouveaux moyens d’investigation. |
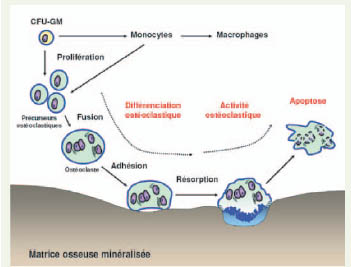
Les modèles cellulaires ostéoclastiques Physiologie de l’ostéoclaste Le processus de différenciation ostéoclastique permet d’obtenir à partir des précurseurs hématopoïétiques CFU-GM ( colony forming unit-granulocyte macrophage) des ostéoclastes matures (Figure 1). Ce processus est complexe et débute dans la moelle osseuse où se trouvent ces précurseurs [
14]. La différenciation des ostéoclastes nécessite une interaction étroite avec les cellules stromales exprimant à leur surface deux cytokines nécessaires à leur différenciation : le RANKL ( receptor activator of NFκB ligand) et le M-CSF ( macrophage-colony stimulating factor) [
15]. Ces cytokines déclenchent l’activation des voies de signalisation intracellulaire et permettent d’une part, l’expression de protéines spécifiques de l’ostéoclaste, telles que le récepteur de la calcitonine et la phosphatase résistante à l’acide tartrique (TRAP) et d’autre part, la fusion des précurseurs à l’origine de la formation de cellules multinucléées, incapables de se diviser. L’ostéoprotégérine, récepteur leurre du RANKL, également produit par les cellules stromales et les ostéoblastes, inhibe quant à elle la différenciation des ostéoclastes [
16]. Au cours de sa différenciation, l’ostéoclaste migre vers la surface osseuse destinée à être résorbée. L’étape d’adhésion qui en résulte, ainsi que la formation d’un compartiment sub-ostéoclastique, est très importante car nécessaire à l’activation des ostéoclastes. Elle se fait grâce à l’interaction étroite des intégrines exprimées à la surface des ostéoclastes, principalement αvβ3 [
17], avec certaines protéines de la matrice contenant la séquence RGD (Arg-Gly-Asp) telle que l’ostéopontine. Il semble que cette intégrine joue un rôle essentiel dans l’adhésion, la motilité et l’activation des ostéoclastes. Une fois attaché, l’ostéoclaste se polarise et une bordure en brosse, ou bordure plissée, se forme au niveau de la zone de contact entre ostéoclaste et matrice osseuse. L’ostéoclaste sécrète alors dans ce compartiment sub-ostéoclastique des protons induisant une déminéralisation de la matrice calcifiée et des enzymes protéolytiques (collagénases, métalloprotéases, cathepsine K) dégradant la partie organique de la matrice osseuse, composée à 90 % de collagène de type I. Au cours du phénomène de résorption, l’ostéoclaste se déplace à la surface de la matrice, créant ainsi une lacune de résorption et libérant des produits de dégradation issus de cette matrice. Après plusieurs cycles de résorption et de migration, l’ostéoclaste se détache de la matrice et entre en apoptose [
18]. Le déclenchement de l’apoptose n’est pas totalement élucidé, mais il semble que certains produits de dégradation de la matrice pourraient être en partie responsables de cette mort cellulaire programmée. Parmi eux, le calcium, principal constituant minéral de la matrice osseuse, présent en grande quantité dans le compartiment sub-ostéoclastique [
19], est capable d’induire in vitro l’apoptose des ostéoclastes [
20]. Cet effet sur l’apoptose pourrait être lié à la présence sur l’ostéoclaste d’un récepteur sensible au calcium couplé à une protéine G. L’apoptose des ostéoclastes est une étape clé dans le contrôle in vivo et in vitro de la résorption osseuse car elle détermine la durée pendant laquelle un ostéoclaste est capable de dégrader la matrice osseuse.  | Figure 1.
Différenciation et fonction des ostéoclastes.
|
Différentes périodes de la vie de l’ostéoclaste se trouvent donc être déterminantes dans la régulation de la résorption osseuse. Parmi elles, les phases de différenciation, de résorption osseuse et d’apoptose des ostéoclastes sont actuellement les trois cibles thérapeutiques majeures des médicaments anti-ostéoporotiques. Leur contrôle permet de réguler directement la résorption osseuse in vivo. Ainsi, il a été décrit que les bisphosphonates, famille majeure de substances anti-résorbantes, diminuaient la formation des ostéoclastes matures par une action anti-ostéoclastogénique et agissaient également sur les ostéoclastes matures en diminuant leur activité de résorption et leur durée de vie [
21]. D’autres voies de recherche sont actuellement en cours afin de développer de nouvelles thérapies anti-ostéoporotiques ayant des mécanismes d’action complètement innovants comme par exemple des antagonistes des récepteurs αvβ3, capables de réduire l’adhésion des ostéoclastes sur la matrice osseuse [
22]. Diversité des modèles ostéoclastiques Au sein du laboratoire, l’étude des mécanismes d’action cellulaires de substances potentiellement antirésorbantes et de leurs cibles a été rendue possible par le développement de plusieurs modèles cellulaires d’ostéoclastes. Certains de ces modèles proviennent de la dissection d’os longs d’animaux jeunes, principalement le rat, le poulet et le lapin. Les cellules ainsi obtenues constituent des cultures primaires d’ostéoclastes matures et fonctionnels. D’autres modèles sont obtenus par différenciation cellulaire de précurseurs hématopoïétiques retrouvés dans le foie, la rate, le sang et la moelle osseuse. La différenciation des précurseurs nécessite la présence de calcitriol et d’autres cellules, stromales ou ostéoblastiques, comme c’est le cas dans les cultures mixtes de calvariae et de moelle osseuse. Depuis l’enrichissement des connaissances sur la différenciation des ostéoclastes et particulièrement la découverte du rôle des facteurs RANKL et M-CSF dans ce processus, il est possible de s’affranchir des méthodes de co-cultures en utilisant les protéines recombinantes directement au contact des précurseurs ostéoclastiques. Dans le cadre des études sur le ranélate de strontium, nous avons utilisé des modèles cellulaires ostéoclastiques performants, à savoir des ostéoclastes matures de lapin et des cellules différenciées à partir de précurseurs hématopoïétiques. Évaluation de l’activité de résorption osseuse et de l’apoptose des ostéoclastes à l’aide d’un modèle d’ostéoclastes primaires matures Le modèle choisi pour cette étude est le modèle d’ostéoclastes matures isolés à partir d’os de lapin. Les cellules obtenues sont directement cultivées sur des lamelles osseuses préparées à partir d’os bovin ou d’ivoire (Figure 2A), ce qui permet de disposer d’un modèle parfaitement adapté à l’étude de substances actives sur la résorption osseuse [
23–
25]. Ce modèle a été validé avec des substances antirésorbantes connues, telles qu’un bisphosphonate (l’ibandronate) et l’œstradiol (Figure 3). L’évaluation de la résorption osseuse se fait de plusieurs manières : (1) avec un logiciel d’analyse d’images (CountScan ®, Biocom) mesurant la surface des lacunes de résorption présentes sur les lamelles osseuses (Figure 2B) ; (2) par différentes techniques de dosage des produits de dégradation de la matrice libérés dans les surnageants de culture au cours du processus de résorption. Le collagène osseux est constitué en majorité de collagène de type I et est stabilisé par des molécules de pontage qui sont libérées lors de la dégradation de l’os par les ostéoclastes. Pour mesurer ces produits de dégradation, nous avons utilisé une technique immunologique (kit Elisa, Nordic Bioscience Diagnostics A/S, Danemark) dosant spécifiquement les fragments C-télopeptidiques du collagène de type I, et développé une méthode utilisant la chromatographie liquide haute performance pour quantifier les molécules de pontage du collagène de type I (pyridinolines) [ 23]. Le modèle d’ostéoclastes matures de lapins offre également l’avantage de pouvoir obtenir, après traitement enzymatique, une population hautement purifiée d’ostéoclastes (99 %) (Figure 4), permettant notamment l’étude directe de l’activité pro-apoptotique de substances sur ces cellules. L’apoptose de l’ostéoclaste est un processus physiologique, résultant d’une cascade complexe d’événements intracellulaires. Elle se caractérise in vitro par une fragmentation de l’ADN mise en évidence par la révélation d’échelles d’ADN (migration de l’ADN sur un gel d’agarose); par ailleurs, la coloration Hœchst permet de distinguer les ostéoclastes apoptotiques des ostéoclastes non apoptotiques (Figure 5) [
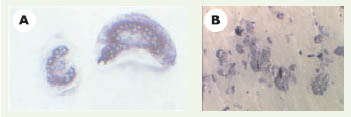
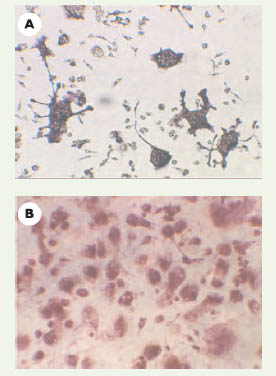
26]. En effet, l’ostéoclaste apoptotique se caractérise par une condensation et une hyperfluorescence de ses noyaux, ainsi que par la visualisation nette de leur fragmentation. L’évaluation du pourcentage d’apoptose se fait par comptage des ostéoclastes apoptotiques et non apoptotiques.  | Figure 2.
Caractérisation en microscopie optique des ostéoclastes de lapins. A. Photographie d’un ostéoclaste après coloration TRAP (Gx400). B. Photographie de lacunes de résorption sur lamelle osseuse après coloration au bleu de toluidine-1% borate (Gx100). |
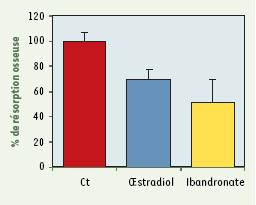
 | Figure 3.
Effets de l’œstradiol (10-8M) et de l’ibandronate (10−6M) sur la résorption osseuse ostéoclastique dans un modèle d’ostéoclastes matures de lapins après 48 heures de culture. La résorption osseuse a été évaluée par la mesure des surfaces de résorption à l’aide d’un logiciel d’analyse d’images (n = 5). *p < 0,05 et **p < 0,01. |
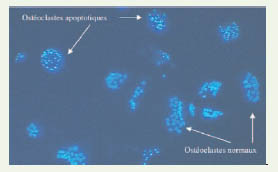
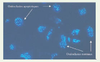 | Figure 4.
Photographie en microscopie optique (Gx400) d’une population purifiée d’ostéoclastes, apoptotiques et non apoptotiques, obtenue après culture sur plastique et coloration de Hœchst.
|
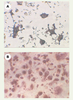 | Figure 5.
Photographies en microscopie optique d’ostéoclastes TRAP-positifs obtenus. A. À partir des cellules RAW 264.7 cultivées sur plastique pendant 5 jours en présence de RANKL (30 ng/ml). B. À partir de cellules PBMC (peripheral blood monocytic cell) cultivées pendant 14 jours sur lamelle osseuse en présence de RANKL (25 ng/ml) et M-CSF (30 ng/ml) |
Évaluation de la différenciation ostéoclastique Une des limites du modèle d’ostéoclastes matures réside dans le faible nombre d’ostéoclastes obtenus après le sacrifice d’un animal. De ce fait, afin d’accéder à des techniques de biologie moléculaire nécessitant de grandes quantités de cellules, nous avons utilisé dans nos études sur le ranélate de strontium deux modèles de différenciation permettant d’obtenir des populations cellulaires riches en ostéoclastes. Initialement, nous avons développé un modèle murin, à partir d’une lignée monocytaire-macrophagique RAW 264.7, puis un modèle humain, à partir d’une population cellulaire hétérogène de précurseurs monocytaires isolés du sang total de donneurs. Ces deux modèles conduisent à la formation de cellules multinucléées TRAP-positives capables de résorber [
27]. Les ostéoclastes- like (OCL) obtenus à partir de la lignée RAW 264.7, après seulement 5 jours de culture, en présence de RANKL seul, représentent une population cellulaire homogène et sont largement utilisés. Le modèle humain nécessite, quant à lui, la présence simultanée des cytokines RANKL et M-CSF pendant une durée moyenne de 14 jours et présente une variabilité inter-donneur non négligeable. Les OCL issus de ce modèle ont une capacité de résorption osseuse importante en comparaison des OCL obtenus à partir des cellules RAW 264.7. Dans les deux types de modèles de différenciation, l’évaluation du nombre d’ostéoclastes se fait classiquement après coloration par un comptage microscopique des cellules TRAP-positives multinucléées (> 3 noyaux). Ainsi, dans le cadre de la collaboration avec Servier, nous avons pu étudier le profil d’expression génique des OCL (RT-PCR, puces à ADN), l’activation des facteurs de transcription NFκB et AP-1 hautement impliqués dans la différenciation, l’activation et la survie des ostéoclastes [
28,
29] et l’activation des protéines MAPK telles que JNK, Erk et p38 ( Western blot). Toutes ces méthodes nous ont permis de mieux caractériser nos modèles d’étude. |
Le ranélate de strontium, modulateur de la signalisation intra-ostéoclastique ? Le tissu osseux constitue la principale réserve en calcium des organismes supérieurs. La mise à disposition du calcium, présent au niveau osseux sous la forme de cristaux d’hydroxyapatite, est un processus actif nécessitant la déminéralisation de la matrice, étape préliminaire indispensable à sa résorption. Les ostéoclastes sont alors confrontés à des concentrations très élevées de calcium ionisé [19]. Il est aujourd’hui établi que le calcium ainsi relargué participe au contrôle négatif du processus de résorption afin d’en limiter la durée et de réduire le volume osseux résorbé. Au cours des vingt dernières années, l’utilisation de modèles cellulaires tels que ceux précédemment décrits a permis de démontrer que l’exposition des ostéoclastes à de fortes concentrations en calcium : (1) induisait une augmentation rapide de la concentration en calcium intra-ostéoclastique [
30] ; (2) inhibait la sécrétion des protons et des enzymes protéolytiques impliqués dans la résorption osseuse [
31] ; et (3) stimulait l’apoptose des ostéoclastes matures [20]. Nos données suggèrent fortement que parmi les voies de signalisation calcique intra-ostéoclastiques (Figure 6), deux voies participent au contrôle de l’apoptose des ostéoclastes matures : l’une liée à l’entrée capacitive de calcium par le canal du récepteur du glutamate de type N-méthyl-D-aspartate, et une autre liée à l’activation de la voie de signalisation inositol-triphosphate (IP3)-dépendante [26,
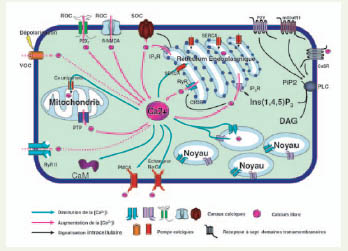
32]. Des concentrations élevées en calcium dans le proche environnement ostéoclastique agiraient quant à elles directement sur l’apoptose des ostéoclastes matures. Le calcium, messager primaire, se fixerait ainsi au niveau d’un récepteur couplé à une protéine G, le récepteur sensible au calcium (CaSR).  | Figure 6.
Voies impliquées dans la régulation de l’homéostasie calcique intra-ostéoclastique. L’homéostasie calcique intra-ostéoclastique est un processus complexe qui fait intervenir de nombreux acteurs. Ces acteurs sont capables, après stimulation, d’induire une réponse biologique calcium-dépendante et de permettre à la cellule de revenir à un état de repos présentant une concentration en calcium intra-ostéoclastique similaire à celle précédant la stimulation cellulaire. Deux familles de récepteurs sont capables d’induire de telles réponses au niveau ostéoclastique. Il s’agit de certains récepteurs de la famille des récepteurs couplés à une protéine G présentant sept domaines transmembranaires (récepteur sensible au calcium, récepteurs métabotropiques purinergiques et glutamatergiques) et de différents canaux calciques transmembranaires : canaux dont l’activité est stimulée par la vidange des réserves en calcium intracellulaire (SOC), par la fixation d’un ligand (ROC) ou par une dépolarisation membranaire (VOC). PLC : phospholipase C. PiP2 : phosphatidyl inositol 4,5-diphosphate. Ins(1,4,5)P3 : inositol 1,4,5-triphosphate. DAG : diacyl-glycérol. IP3R : récepteur de Ins(1,4,5)P3. RyR : récepteur de la ryanodine. CICR : vidange calcique induite par le calcium. CaM : calmoduline. PMCA : calcium-ATPase membranaire. SERCA : calcium-ATPase sarco-réticulo-endoplasmique. |
Le strontium présente un fort tropisme osseux ; ainsi, chez les patients traités par du ranélate de strontium, les ions strontium de la matrice osseuse libérés au cours de la résorption pourraient se concentrer dans l’environnement ostéoclastique et agir sur l’ostéoclaste. Nous avons confirmé in vitro, les effets inhibiteurs du ranélate de strontium sur la résorption osseuse, puis il nous a semblé judicieux d’évaluer ses effets sur l’apoptose des ostéoclastes. Nous avons montré pour la première fois que le ranélate de strontium stimulait, de façon dose-dépendante, l’apoptose des ostéoclastes matures. Parallèlement, grâce à l’utilisation conjointe de bloqueurs pharmacologiques tels que les inhibiteurs de la phospholipase C, de la voie de signalisation IP3-dépendante et de l’entrée capacitive de calcium (consécutive à la vidange des réserves intracellulaires de calcium), nous avons démontré l’importance de la voie de signalisation IP3-dépendante dans l’apoptose induite par le calcium. En effet, le calcium, en se liant au CaSR, stimule le clivage du phosphatidyl inositol diphosphate en IP3 et en diacyl-glycérol sous l’action de la phospholipase C (Figure 6). L’IP3 ainsi produit se lierait aux récepteurs de l’IP3 du réticulum endoplasmique et stimulerait la vidange des réserves calciques intracellulaires responsables des effets induits par le calcium. De façon similaire, l’apoptose induite par le ranélate de strontium serait associée à la stimulation d’un récepteur couplé à une protéine G et à l’activation d’une phospholipase C. Cependant, les effets de ces deux ions sur les ostéoclastes matures impliqueraient des voies de signalisation intracellulaire différentes et cumulatives [
33]. Simultanément, Servier travaillait avec l’équipe du Docteur Edward Meigs Brown (Harvard Medical School, Boston, États-Unis) sur le rôle du CaSR dans les effets induits par le ranélate de strontium. Ainsi, parallèlement à nos travaux, l’équipe du Dr Brown a démontré que le CaSR serait impliqué dans l’activité ostéo-formatrice observée in vitro sur des cultures d’ostéoblastes en présence de ranélate de strontium. Compte tenu de ces différents résultats et à l’initiative de Servier, nous avons poursuivi nos investigations sur les voies de signalisation intracellulaires impliquées dans les effets induits par le ranélate de strontium et le calcium sur les ostéoclastes en focalisant notre attention sur le CaSR. |
Implication du récepteur sensible au calcium dans les effets ostéoclastiques du ranélate de strontium L’expression du CaSR sur l’ostéoclaste est actuellement controversée. Cependant, la mise en commun des expertises respectives des différents laboratoires dans le cadre d’un travail post-doctoral a rapidement confirmé l’implication du CaSR dans les effets induits par le ranélate de strontium et le calcium sur l’ostéoclaste. En effet, simultanément à l’étude des voies de signalisation intracellulaires impliquées dans les effets induits par le ranélate de strontium, nous avons confirmé, avec deux méthodes d’immunohistochimie, que les ostéoclastes exprimaient de façon constitutive le CaSR. L’adaptation des méthodes de transfection cellulaire par voie rétrovirale et des méthodes d’immunohistochimie mises au point par l’équipe du Dr Brown à nos modèles d’ostéoclastes matures ou différenciés, a permis de mettre en évidence le rôle du CaSR dans les effets du ranélate de strontium sur l’ostéoclaste. En effet, l’action du ranélate de strontium sur les ostéoclastes est abolie lorsque le CaSR est inactivé après transfection des ostéoclastes par la forme dominant négatif du CaSR [
34]. Les données recueillies grâce à cette mise en commun de compétences scientifiques et techniques ouvrent aujourd’hui de nouvelles voies de recherche sur le contrôle des activités de l’ostéoclaste et de la résorption osseuse. |
Servier a rassemblé de nombreuses données cliniques et pharmacologiques apportant des preuves convaincantes sur les propriétés anti-ostéoporotiques du ranélate de strontium. À la différence d’autres composés pharmaceutiques anti-ostéoporotiques actuellement utilisés, le ranélate de strontium présente une activité originale : il stimule l’activité ostéo-formatrice des ostéoblastes et limite l’activité ostéo-destructrice des ostéoclastes. Cependant, les mécanismes responsables de ces effets au niveau cellulaire restaient mal connus. Les activités de recherche de notre groupe, axées sur l’étude du rôle des processus de contrôle de l’homéostasie calcique intra-ostéoclastique dans la régulation de la résorption osseuse et de l’apoptose des ostéoclastes, ont permis d’explorer les effets pharmacologiques du ranélate de strontium. Une collaboration s’est engagée avec Servier afin de définir les voies de signalisation impliquées dans les effets anti-ostéoclastiques du ranélate de strontium. Grâce à sa connaissance approfondie de la molécule, Servier à permis de donner un cadre structuré à ces travaux de recherche appliquée tout en permettant une démarche personnelle et fondamentale. Cette collaboration s’est montrée fructueuse car elle a permis d’y associer des étudiants en formation doctorale et, en outre, a fait l’objet d’une exploitation directe des résultats obtenus, notamment en terme de communication auprès des spécialistes. En conclusion, ce sont les capacités d’adaptation et de compréhension des objectifs réciproques des partenaires qui déterminent la réussite d’une telle collaboration. |
1. Organisation Mondiale de la Santé. Guidelines for preclinical evaluation and clinical trials in osteoporosis. Geneva : WHO, 1998. 2. Baudoin C, Fardellone P, Bean K, et al. Clinical outcomes and mortality after hip fracture : a 2-year follow-up study. Bone 1996; 18 (suppl 3) : S149–57. 3. McCreadie BR, Goldstein SA. Biomechanics of fracture : Is bone mineral density sufficient to assess risk ? J Bone Miner Res 2000; 15 : 2305–8. 4. Nguyen TV, Eisman JA. Genetics of fracture : challenges and opportunities. J Bone Miner Res 2000; 15 : 1253–6. 5. Ralston SH. The genetics of osteoporosis. Bone 1999; 25 : 85–6. 6. Harvey N, Cooper C. Determinants of fracture risk in osteoporosis. Curr Rheumatol Rep 2003; 5 : 75–81. 7. Jordan KM, Cooper C. Epidemiology of osteoporosis. Best Pract Res Clin Rheumatol 2002; 16 : 795–806. 8. Baron R, Tsouderos Y. In vitro effects of S12911-2 on osteoclast function and bone marrow macrophage differentiation. Eur J Pharmacol 2002; 450 : 11–7. 9. Takahashi N, Sasaki T, Tsouderos Y, Suda T. S12911-2 inhibits osteoclastic bone resorption in vitro. J Bone Miner Res 2003; 18 : 1082–7. 10. Canalis E, Hott M, Deloffre P, et al. The divalent strontium salt S12911 enhances bone cell replication and bone formation in vitro. Bone 1996; 18 : 517–23. 11. Chattopadhyay N, Yano S, Tfelt-Hansen J, et al. Strontium ranelate promotes chemotaxis, stimulates proliferation and induces genes involved in the differentiation of rat primary osteoblasts. Bone 2005; 36 : S400. 12. Meunier PJ, Roux C, Seeman E, et al. The effects of strontium ranelate on the risk of vertebral fracture in women with postmenopausal osteoporosis. N Engl J Med 2004; 350 : 459–68. 13. Reginster JY, Seeman E, De Vernejoul MC, et al. Strontium ranelate reduces the risk of nonvertebral fractures in postmenopausal women with osteoporosis : treatment of peripheral osteoporosis (TROPOS) study. J Clin Endocrinol Metab 2005; 90 : 2916–822. 14. Suda T, Takahashi N, Udagawa N, et al. Modulation of osteoclast differentiation and function by the new members of the tumor necrosis factor receptor and ligand families. Endocrinol Rev 1999; 20 : 345–57. 15. Teitelbaum SL. Bone resorption by osteoclasts. Science 2000; 289 : 1504–8. 16. Simonet WS, Lacey DL, Dunstan CR, et al. Osteoprotegerin : a novel secreted protein involved in the regulation of bone density. Cell 1997; 89 : 309–19. 17. Vaananen HK, Horton M. The osteoclast clear zone is a specialized cell-extracellular matrix adhesion structure. J Cell Sci 1995; 108 : 2729–32. 18. Manolagas SC. Birth and death of bone cells : basic regulatory mechanisms and implications for the pathogenesis and treatment of osteoporosis. Endocrinol Rev 2000; 21 : 115–37. 19. Silver IA, Murrills RJ, Etherington DJ. Microelectrode studies on the acid microenvironment beneath adherent macrophages and osteoclasts. Exp Cell Res 1988; 175 : 266–76. 20. Lorget F, Kamel S, Mentaverri R, et al. High extracellular calcium concentrations directly stimulate osteoclast apoptosis. Biochem Biophys Res Commun 2000; 268 : 899–903. 21. Zaïdi M, Blair HC, Moonga BS, et al. Osteoclastogenesis, bone resorption, and osteoclast-based therapeutics. J Bone Miner Res 2003; 18 :599–609. 22. Murphy MG, Cerchio K, Stoch SA, et al. Effect of L-000845704, an alphaVbeta3 integrin antagonist, on markers of bone turnover and bone mineral density in postmenopausal osteoporotic women. J Clin Endocrinol Metab 2005; 90 : 2022–8. 23. Lorget F, Mentaverri R, Meddah B, et al. Evaluation of in vitro bone resorption : high-performance liquid chromatography measurement of the pyridinolines released in osteoclast cultures. Anal Biochem 2000; 284 : 375–81. 24. Kameda T, Mano H, Yuasa T, et al. Estrogen inhibits bone resorption by directly inducing apoptosis of the bone-resorbing osteoclasts. J Exp Med 1997; 186 : 489–95. 25. Wattel A, Kamel S, Mentaverri R, et al. Potent inhibitory effect of naturally occurring flavonoids quercetin and kaempferol on in vitro osteoclastic bone resorption. Biochem Pharmacol 2003; 65 : 35–42. 26. Mentaverri R, Kamel S, Wattel A, et al. Regulation of bone resorption and osteoclast survival by nitric oxide : possible involvement of NMDA-receptor. J Cell Biochem 2003; 88 : 1145–56. 27. Wattel A, Kamel S, Prouillet C, et al. Flavonoid quercetin decreases osteoclastic differentiation induced by RANKL via a mechanism involving NFkappa B and AP-1. J Cell Biochem 2004; 92 : 285–95. 28. Iotsova V, Caamano J, Loy J, et al. Osteopetrosis in mice lacking NF-kappaB1 and NF-kappaB2. Nat Med 1997; 3 : 1285–9. 29. Grigoriadis AE, Wang ZQ, Cecchini MG, et al. c-Fos : a key regulator of osteoclast-macrophage lineage determination and bone remodeling. Science 1994; 266 : 443–8. 30. Malgaroli A, Meldolesi J, Zallone AZ, et al. Control of cytosolic free calcium in rat and chicken osteoclasts. The role of extracellular calcium and calcitonin. J Biol Chem 1989; 264 :14342–7. 31. Datta HK, MacIntyre I, Zaidi M. The effect of extracellular calcium elevation on morphology and function of isolated rat osteoclasts. Biosci Rep 1989; 9 : 747–51. 32. Mentaverri R, Kamel S, Brazier M. Involvement of capacitive calcium entry and calcium store refilling in osteoclastic survival and bone resorption process. Cell Calcium 2003; 34 : 169–75. 33. Mentaverri R, Hurtel AS, Kamel S, et al. Strontium ranelate directly stimulates osteoclast apoptosis. Osteoporos Int 2004; 15 (suppl 1) : P345MO. 34. Mentaverri R, Hurtel AS, Wattel A, et al. Calcium-sensing receptor mediates strontium ranelate-induced osteoclasts apoptosis. Bone 2005; 36 : S403. |