| |
| Med Sci (Paris). 2005 June; 21(6-7): 655–657. Published online 2005 June 15. doi: 10.1051/medsci/2005216-7655.Cellules sombres : l’histoire continue Gérard Friedlander* Rédacteur en chef, Faculté de Médecine Necker, 156, rue de Vaugirard, 75730 Paris Cedex 15, France MeSH keywords: Animaux, Communication cellulaire, Phénomènes physiologiques cellulaires, Cellules |
Trente-cinq ans après les observations fondatrices de Jacqueline Hagège et de Gabriel Richet, le feuilleton des cellules sombres rénales, ou cellules intercalaires, n’a pas trouvé son épilogue (→). Des données morphologiques et fonctionnelles nombreuses ont été fournies au dossier, des pistes susceptibles de donner la clé de l’apparition ou de la disparition de ces cellules et de leurs différents types ont été tracées. Ce sont ces éléments qui seront résumés ici. (→) m/s 2005, n° 6-7, p.652
|
Les différents types des cellules intercalaires C’est dans la partie terminale du tubule rénal, le canal collecteur, que les cellules intercalaires sont observées. Ces cellules représentent jusqu’à 30 % du nombre total de cellules épithéliales tubulaires. Deux types de cellules intercalaires ont été décrits à ce jour. Toutefois, des formes intermédiaires entre ces deux types peuvent être occasionnellement observées dans des situations métaboliques instables ou lors de changements rapides de l’équilibre acidobasique. Les cellules de type A (ou α) sont pourvues de structures tubulovésiculaires qui bombent dans la lumière tubulaire (Figure 1). Leur membrane apicale est différenciée en microvillosités ou en en microplicatures. Elles assurent une sécrétion de protons (ions H+) dans la lumière tubulaire et entraînent ainsi l’acidification de l’urine. Leur nombre et la surface de leur membrane apicale augmentent dans des situations d’acidose respiratoire ou métabolique. Les cellules de type B (ou β) apparaissent plus sombres en microscopie optique ou électronique en raison d’une plus grande densité en mitochondries (Figure 1). C’est leur nombre que J. Hagège et G. Richet a vu augmenter lors de l’alcalose métabolique. Elles assurent une sécrétion d’ions bicarbonates (HCO3
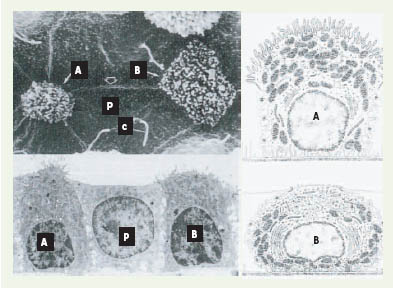
−) dans la lumière tubulaire et alcalinisent l’urine.  | Figure 1.
Aspect morphologique des cellules intercalaires. La partie gauche de la figure montre l’aspect, en microscopie électronique à balayage (en haut) et en transmission (en bas), des cellules intercalaires de type A et B, ainsi que des cellules principales (P). Ces dernières sont équipées d’un cil primaire apical (c). Sur la partie droite de la figure sont schématisées une cellule intercalaire de type A (en haut) et une cellule intercalaire de type B (en bas), montrant les différences majeures des domaines apicaux de la membrane plasmique. |
|
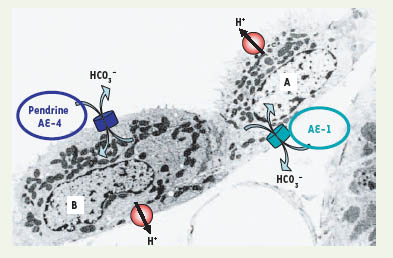
Les transporteurs dans les cellules intercalaires Ces différences de fonction sont sous-tendues par des équipements spécifiques en transporteurs membranaires (Figure 2). Les cellules de type A expriment dans leur membrane apicale une H+-ATPase de type vacuolaire, responsable de la sécrétion de protons, tandis qu’un échangeur chlore - bicarbonate du type de la bande 3 (AE-1) est inséré dans leur membrane basolatérale et assure la sortie de bicarbonate de la cellule. Dans la médullaire rénale, la sécrétion de protons fait également intervenir une H+,K+-ATPase qui échange un proton contre un ion potassium et dont la régulation pourrait être différente de celle de la H+-ATPase vacuolaire. La situation est (presque) symétrique en ce qui concerne l’organisation des transporteurs dans les cellules de type B : une H+-ATPase est insérée dans la membrane basolatérale et un transporteur de bicarbonate fonctionne dans la membrane apicale. Toutefois, ce dernier n’est pas apparenté à la bande 3 et pourrait correspondre à un nouvel échangeur d’anions, la pendrine, spécifiquement exprimé dans cette sous-population de cellules rénales.  | Figure 2.
Principaux transporteurs dans les cellules intercalaires. Les cellules intercalaires de type A et B (vues ici en microscopie électronique de transmission) sont équipées d’un système de transport de protons (H+-ATPase) situé au pôle apical dans les premières et au pôle basolatéral dans les secondes. Le système de transport de bicarbonate (échangeur anionique) est différent dans les deux types cellulaires : AE-1 basolatéral dans les cellules de type A ; pendrine et AE-4 apicaux dans les cellules de type B. La densité en mitochondries est supérieure dans les cellules de type B, qui apparaissent plus sombres pour cette raison. |
L’expression de la pendrine est augmentée au cours de l’alcalose métabolique et diminuée au cours de l’acidose métabolique. Des mutations de la pendrine sont responsables, chez l’homme, du syndrome de Pendred qui associe un goitre et une surdité (la pendrine est exprimée également par les cellules thyroïdiennes et celles de l’oreille interne) [
1–
3]. Les animaux dont la pendrine est invalidée par recombinaison homologue ont un défaut de sécrétion de bicarbonate dans l’urine en situation de charge alcaline [
4]. L’existence d’un autre échangeur d’anions, AE-4, dans les cellules intercalaires de type B de certaines espèces a été rapporté. |
Les cellules intercalaires et l’équilibre acide-base La question centrale, dont les conséquences en termes de plasticité cellulaire sont importantes, est de savoir si, en fonction des besoins de l’homéostasie acido-basique, une cellule de type A peut se transformer en une cellule de type B et réciproquement. Des arguments expérimentaux convaincants ont été apportés en faveur de cette hypothèse bien que le signal précis de cette transformation in vivo ne soit pas connu. Le groupe de Q. Al-Awqati a fourni une contribution majeure dans ce domaine [
5–
10] en étudiant une lignée immortalisée de cellules intercalaires de type B. Ensemencées de manière conventionnelle, non confluentes, ces cellules développent leur phénotype de type B caractérisé par la distribution des transporteurs membranaires décrite plus haut. En revanche, leur ensemencement à une forte densité modifie leur phénotype et les transforme en cellules de type A pourvues d’une H+-ATPase apicale et d’un échangeur anionique basolatéral. C’est dans la matrice extracellulaire qu’a été découverte la molécule impliquée dans la conversion de cellules B en cellules A. Il s’agit d’une protéine de 250 kDa qui a été baptisée hensine, dont le dépôt dans la matrice extracellulaire est stimulé par un milieu acide. Les propriétés de différenciation des cellules intercalaires par la hensine ne sont acquises qu’après une polymérisation de cette protéine, polymérisation qui requiert l’intervention d’autres partenaires, en particulier de la galectine-3, sécrétée par les cellules intercalaires de type A. Tout se passe donc comme si les cellules intercalaires de type A représentaient un stade ultime de différenciation alors que les cellules de type B seraient à un stade moins différencié. Tous les stades intermédiaires entre ces deux formes pourraient être observés lors d’un changement de l’environnement acido-basique. Un argument supplémentaire en faveur de cette différenciation aboutie représentée par les cellules intercalaires de type A provient des conséquences phénotypiques de l’invalidation d’un facteur de transcription de la famille Forkhead, Foxi1. Chez les animaux porteurs d’une mutation nulle de ce facteur, la partie distale du tubule rénale est dépourvue de cellules intercalaires et n’est constituée que d’un seul type cellulaire exprimant à la fois les transporteurs d’eau, de sel, de protons et d’anions. Ces animaux ont une acidose métabolique et sont incapables d’excréter normalement une charge acide. Parmi les gènes dont la transcription est contrôlée par Foxi1 figurent la pendrine et AE-1, ainsi qu’une sous-unité de la pompe à protons vacuolaire, toutes protéines caractéristiques des cellules intercalaires [
11,
12]. Quels sont les facteurs et les voies de transduction qui, sous l’effet de modifications de l’équilibre acide base, entraînent la différenciation terminale des cellules intercalaires ? Deux pistes au moins ont été tracées : l’une concerne l’activation de plusieurs tyrosine kinases (c-src, focal adhesion kinase FAK) qui jouent un rôle important dans l’adressage de protéines membranaires transporteuses de protons, l’autre met en jeu les récepteurs de l’endothéline, peptide dont la synthèse est stimulée par l’acidose. Reste à élucider la nature du détecteur, ce sensor capable de détecter des variations discrètes de pH. |
Les cellules intercalaires représentent donc un état abouti de la différenciation épithéliale et sont le siège d’une plasticité remarquable mise au service de l’homéostasie acidobasique. Les acteurs de cette différenciation sont multiples et certains, telle la hensine, pourraient jouer un rôle majeur dans la différenciation épithéliale dès les stades précoces de l’embryogenèse [
13]. L’avatar du début, loin d’être une mésaventure sans lendemain, est devenu au cours des ans une suite de découvertes qui, du néphron initial, concerne maintenant la différenciation épithéliale précoce dans ses aspects les plus fondamentaux. |
1. Everett LA, Glaser B, Beck JC, et al. Pendred syndrome is caused by mutations in a putative sulphate transporter gene (PDS). Nat Genet 1997; 17 : 411–22. 2. Scott DA, Wang R, Kreman TM, et al. The Pendred syndrome gene encodes a chloride-iodide transport protein. Nat Genet 1999; 21 : 440–3. 3. Royaux IE, Suzuki K, Mori A, et al. Pendrin, the protein encoded by the Pendred syndrome gene (PDS), is an apical porter of iodide in the thyroid and is regulated by thyroglobulin in FRTL-5 cells. Endocrinology 2000; 141 : 839–45. 4. Royaux IE, Wall SM, Karniski LP, et al. Pendrin, encoded by the Pendred syndrome gene, resides in the apical region of renal intercalated cells and mediates bicarbonate secretion. Proc Natl Acad Sci USA 2001; 98 : 4221–6. 5. Al-Awqati Q, Vijayakumar S, Takito J, et al. Terminal differentiation in epithelia : the Hensin pathway in intercalated cells. Semin Nephrol 1999; 19 : 415–20. 6. Al-Awqati Q, Vijayakumar S, Takito J, et al. Phenotypic plasticity and terminal differentiation of the intercalated cell : the hensin pathway. Exp Nephrol 2000; 8 : 66–71. 7. Al-Awqati Q, Vijayakumar S, Takito J. Terminal differentiation of epithelia. Biol Chem 2003; 384 : 1255–8. 8. Al-Awqati Q, Vijayakumar S, Takito J. Terminal differentiation of epithelia from trophectoderm to the intercalated cell : The role of hensin. J Am Soc Nephrol 2003; 14 (suppl 1) : S16–21. 9. Al-Awqati Q. Terminal differentiation of intercalated cells : The role of hensin. Annu Rev Physiol 2003; 65 : 567–83. 10. Schwartz GJ, Tsuruoka S, Vijayakumar S, et al. Acid incubation reverses the polarity of intercalated cell transporters, an effect mediated by hensin. J Clin Invest 2002; 109 : 89–99. 11. Al-Awqati Q, Schwartz GJ. A fork in the road of cell differentiation in the kidney tubule. J Clin Invest 2004; 113 : 1528–30. 12. Blomqvist SR, Vidarsson H, Fitzgerald S, et al. Distal renal tubular acidosis in mice that lack the forkhead transcription factor Foxi1. J Clin Invest 2004; 113 : 1560–70. 13. Takito J, Al-Awqati Q. Conversion of ES cells to columnar epithelia by hensin and to squamous epithelia by laminin. J Cell Biol 2004; 166 : 1093–102. |