Le rôle de la protéine Vif (viral infectivity factor) du VIH-1 est longtemps resté mystérieux. La récente identification de sa cible cellulaire, la protéine APOBEC3G, éclaire d’un jour nouveau les relations conflictuelles entre le virus et son hôte. APOBEC3G appartient à la famille des cytidine déaminases, enzymes connues jusqu’à présent par leur fonction dans « l’édition » de l’ARN et de l’ADN, et dans l’hypermutation des gènes d’immunoglobulines (→). L’enzyme APOBEC3G « attaque » le virus lors de l’étape de transcription inverse et provoque une hypermutation du matériel génétique viral. Vif neutralise cette ligne de défense antivirale en provoquant la dégradation d’APOBEC3G, permettant ainsi la propagation du virus.
(→) m/s 2000, n° 10, p. 1142 et 2002, n°2, p. 181
La protéine Vif est présente dans presque tous les lentivirus. Vif est indispensable à la multiplication virale in vivo chez l’hôte infecté. Le rôle de cette petite protéine (23 kDa pour le VIH) fortement basique, est longtemps resté mal compris. En culture cellulaire, on distingue deux types de cellules : les cellules dites restrictives (lymphocytes et macrophages primaires, par exemple) dans lesquelles le virus VIH dépourvu du gène vif (HIV∆vif) est incapable de se ré pliquer, et les cellules dites permissives (par exemple certaines lignées lymphocytaires tumorales) dans lesquelles le virus VIH³vif se réplique normalement. Les virions produits en l’absence de Vif dans une cellule restrictive semblent physiquement normaux, mais perdent leur pouvoir infectieux. Le défaut réplicatif est connu depuis longtemps. Il intervient à une étape précoce du cycle : l’efficacité de la transcription inverse est fortement diminuée. On savait aussi que le phénotype « restrictif » était dominant : les cellules restrictives expriment un facteur antiviral, qui est inhibé par Vif. Dans les cellules permissives, Vif n’est pas nécessaire, car le facteur antiviral est absent. Ce facteur cellulaire antiviral a été identifié en 2002 par l’équipe de Michael Malim, à Londres [ 1]. Il s’agit d’une protéine, d’abord appelée CEM15, puis APOBEC3G, car appartenant à la famille d’APOBEC1, une enzyme à activité cytidine désaminase, qui « édite » l’ARNm du gène de l’apolipoprotéine B. Les enzymes de cette famille possèdent la capacité de désaminer certains résidus cytidine (C) présents dans l’ARNm ou dans l’ADN, et de les transformer en uridine (U). Outre APOBEC1, la famille comprend la protéine AID (activation-induced cytidine deaminase), impliquée dans la production de la diversité des immunoglobulines (→).
(→) m/s 2000, n° 10, p. 1142
Après l’identification d’APOBEC3G, les recherches se sont accélérées, et l’effet antiviral de cette protéine a été caractérisé en quelques mois [ 2, 4– 6]. En l’absence de Vif, l’enzyme est incorporée dans les particules virales. Au cours de l’infection de nouvelles cellules, l’enzyme va éditer le matériel génétique viral. La désamination a lieu lors de la transcription inverse, et la cible de l’enzyme est le premier brin d’ADN (de polarité négative) synthétisé à partir de l’ARN viral. Lors de la copie du deuxième brin d’ADN, les mutations seront donc observées sous la forme complémentaire : guanidine (G) vers adénine (A). Les conséquences pour le virus sont drastiques : environ 1 à 2 % de tous les résidus G présents dans l’ADN viral sont transformés en A. Le matériel viral hypermuté subira ensuite deux destinées. Il sera reconnu par les enzymes cellulaires d’excision-réparation de l’ADN, et une partie sera clivée et dégradée, avant même l’intégration dans le génome de la cellule. Une partie des provirus échappe cependant à la dégradation, et, si la transcription inverse est complète, s’intègrera dans l’ADN cellulaire. Le taux très élevé de mutations empêchera alors la synthèse de protéines virales fonctionnelles, et le cycle viral sera arrêté. On peut noter que la présence de génomes hypermutés chez les patients infectés par le VIH était un phénomène connu [ 7]. On en comprend mieux maintenant l’origine.
Comment agit la protéine Vif pour neutraliser cette ligne de défense antirétrovirale ? Là aussi, le scénario a été très rapidement dévoilé. Vif empêche l’incorporation d’APOBEC3G dans les virions. En présence de Vif, les niveaux cellulaires d’APOBEC3G sont fortement réduits. Vif se fixe directement à APOBEC3G et entraîne sa dégradation [ 8, 9]. Les intermédiaires moléculaires ont même été identifiés : un complexe de type Skp1-cullin-F-box (SCF) se forme avec Vif [ 10], APOBEC3G sera alors rapidement ubiquitinylée et dégradée par le protéasome.
Les conséquences de cette découverte s’étendent bien au-delà du VIH. Les rétrovirus murins, par exemple, sont sensibles en culture cellulaire à l’effet d’APOBEC3G [ 3– 5]. Chez l’homme, des hypermutations G vers A ont été décrites chez quelques patients infectés par un autre rétrovirus, HTLV-I, ou par le virus de l’hépatite B [7]. APOBEC3G exerce donc certainement un rôle de défense cellulaire contre d’autres virus que le VIH.
APOBEC3G n’a pas encore livré tous ses mystères, et de nombreuses questions restent encore à résoudre. Y a-t-il une activation d’APOBEC3G lors de l’infection par le VIH ? Comment, en l’absence de Vif, cette protéine est-elle dirigée vers le virus en formation dans la cellule productrice et reconnaîtra ensuite l’ADN proviral après l’infection de nouvelles cellules ? Comment se débrouillent les virus ne possédant pas de protéine proche de Vif ? Ces passionnantes questions, et d’autres encore, nous permettront de mieux comprendre la batterie des défenses non immunitaires érigée par la cellule pour se protéger des agressions virales.
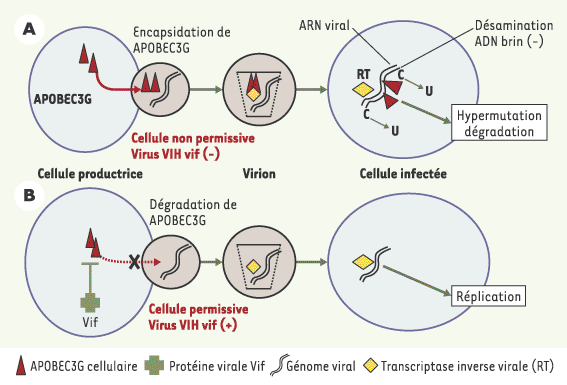
| Figure 1.
Interactions des protéines Vif et APOBEC3G. A. Dans une cellule infectée par un virus VIH dépourvu de la protéine Vif, les nouveaux virions produits encapsident l’enzyme APOBEC3G, ce qui entraîne l’hypermutation du brin d’ADN rétrotranscrit à partir de l’ARN viral lors de l’infection d’une cellule non permissive. B. Lorsque les virions contiennent la protéine Vif, APOBEC3G est exclue des nouveaux virions encapsidés, et le génome du virion est donc intact, ce qui conduit à une infection productive et à la réplication du virus dans les nouvelles cellules infectées. |