| |
| Med Sci (Paris). 2002 January; 18(1): 79–85. Published online 2002 January 15. doi: 10.1051/medsci/200218179.Hélicase RecQ, syndrome de Werner, et réparation de l’ADN par recombinaison homologue Yannick Saintigny and Raymond J. Monnat Jr Department of Pathology, University of Washington, Box 357705, 1959 N.E. Pacific St, Room K-065 HSB, Seattle, WA 98195-7705, États-Unis |
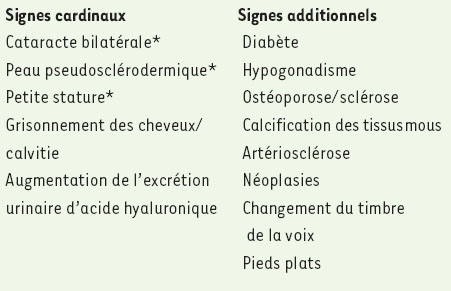
Le syndrome de Werner a été décrit pour la première fois par un médecin allemand au début du XXe siècle et apparaît dans toutes les régions du globe avec une fréquence de 1 à 2 cas pour 100 000 individus [1–3]. Le phénotype clinique majeur, évident et distinctif, est le développement rapide, à partir de la puberté, de signes et de symptômes qui caricaturent un vieillissement prématuré. Ce phénotype comprend un grisonnement prématuré des cheveux ou une calvitie précoce, une structure de la peau pseudo-sclérodermique avec des hyperkératoses aux points d’appui, une ostéoporose, une artériosclérose, la formation d’une cataracte bilatérale, un diabète non insulino-dépendant et un hypogonadisme (Tableau I). La plupart des patients décèdent vers l’âge de 47 ans de cancers ou de maladies cardiovasculaires. Le risque élevé de néoplasie chez ces patients est restreint aux ostéosarcomes, aux sarcomes des tissus mous, au mélanome acral lentigineux, aux carcinomes de la thyroïde et aux méningiomes [4, 5].  | Tableau 1. Phénotype clinique du syndrome de Werner. La première colonne (signes cardinaux) indique les signes constamment observés chez les patients. Les trois signes marqués par une astérisque (*) sont observés dans 90 à 100% des cas au moment du diagnostic. Outre ces signes cardinaux, les patients atteints du syndrome présentent généralement une consanguinité élevée. La seconde colonne (signes additionnels) indique les signes observés dans 10 % à 90 % des cas. Un diagnostic définitif du syndrome de Werner peut être donné lorsque les 6 signes cardinaux sont présents et un diagnostic probable est donné lorsqu’au moins 3 signes cardinaux sont présents et associés à deux signes additionnels chez des patients suivis depuis l’âge de 10 ans. Des informations complémentaires sont disponibles sur : http://www.pathology.washington.edu/wer-ner/registery/diagnostic.html |
Bien qu’incomplète, la ressemblance phénotypique entre le syndrome de Werner et le vieillissement humain normal est importante. Une meilleure compréhension des mécanismes partagés par le syndrome de Werner et le vieillissement normal pourrait permettre d’identifier des réseaux métaboliques communs qui influent sur le développement de pathologies associées à la vieillesse comme les maladies cardiovasculaires, le diabète et certains types de cancers. |
Le gène et la protéine responsables du syndrome Le gène dont le dysfonctionnement est responsable du syndrome de Werner est localisé sur le chromosome 8 [6]. Il code pour une protéine nucléaire, WRN, qui est composée de 1432 acides aminés et comprend deux domaines aux activités biochimiques distinctes. L’un est un domaine hélicase homologue à l’hélicase RecQ d’E. coli, et l’autre un domaine exonucléase 3’->5’. Le domaine hélicase RecQ est très conservé et ubiquitaire : au moins un membre de cette famille a été localisé dans le génome d’un grand nombre d’eucaryotes, de procaryotes et d’archéobactéries. Les eucaryotes multicellulaires comme C. elegans, D. melanogaster et l’homme possèdent, chacun, plusieurs protéines hélicases de la famille RecQ [7, 8]. Chez l’homme, cinq hélicases de type RecQ ont été identifiées (Figure 1), et cette famille pourrait contenir d’autres gènes ou protéines variantes produites par épissage alternatif (RecQ5 [8]). Le domaine exonucléase 3’->5’ présente une séquence consensus similaire au domaine de correction 3’->5’ de la polymérase I et de la RNase D d’E. coli [9]. Le domaine exonucléase est uniquement présent sur la protéine WRN et n’a pas été retrouvé dans d’autres protéines de type RecQ.  | Figure 1.La protéine WRN et les autres membres de la famille des hélicases RecQ. A. WRN est l’unique hélicase RecQ à posséder un domaine exonucléase 3’->5’ à l’extrémité amino-terminale (en rose sur la figure) outre le domaine conservé hélicase RecQ 3’->5’ (en vert sur la figure) [ 14]. Outre WRN (RECQL2), il existe 4 autres hélicases de cette famille chez l’homme, dont deux (BLM et RTS) sont associées à des pathologies humaines. Des membres de cette famille existent aussi chez E.coli (EcRecQ) et chez la levure (ScSgs1 et SpRqh1). B. Mutations de WRN chez les patients atteints du syndrome de Werner. Les mutations peuvent être des substitutions conduisant à la création d’un codon stop (TER), des insertions ou des délétions avec décalage du cadre de lecture et arrêt prématuré (FS/TER), ou des mutations d’épissage. Toutes conduisent à une protéine tronquée avec la perte du signal de localisation nucléaire situé à l’extrémité carboxy-terminale. Les cellules de ces patients expriment peu ou pas de protéine WRN [ 10– 12]. Les astérisques (*) représentent les points de polymorphismes. La base de donnée internationale HUGO rassemblant les mutations de WRN et les polymorphismes peut être consultée sur : http://www.pathology.washington.edu/werner/ws_wrn.html |
Les mutations à l’origine du syndrome de Werner conduisent toutes à une protéine WRN tronquée, avec la perte du signal de localisation nucléaire situé à l’extrémité carboxy-terminale. Ces mutations déstabilisent aussi bien l’ARNm que la protéine, et provoquent donc une perte des deux fonctions hélicase et exonucléase [10–12]. Deux autres maladies ont été identifiées comme la conséquence d’une perte de fonction d’une hélicase de la famille RecQ : le syndrome de Bloom (BLM) et le syndrome de Rothmund-Thomson (RecQ4). Leurs manifestations cliniques sont certes différentes de celles du syndrome de Werner, mais toutes deux sont aussi de transmission autosomique récessive et caractérisées par une instabilité génétique et un risque élevé de tumeurs malignes [8, 13]. |
Fonctions biochimiques connues de la protéine WRN La caractérisation in vitro des substrats des deux sites catalytiques de WRN a permis d’envisager un rôle clé de cette protéine dans la résolution de structures d’ADN aberrantes qui apparaissent lors de processus comme la réplication, la réparation et la recombinaison homologue. D’une façon générale, le rôle des hélicases est de rompre les liaisons hydrogène qui assurent la cohésion de la double hélice d’ADN. Les données obtenues avec les hélicases de la famille RecQ suggèrent que ces protéines jouent un rôle dans la recombinaison ou le maintien de la stabilité du génome dans de nombreux organismes, en catalysant la migration des intermédiaires de recombinaison in vitro [7, 8]. L’activité hélicase de la protéine WRN participe aussi in vitro à la résolution de structures d’ADN à 3 ou 4 branches dont les jonctions de Holliday. En outre, elle permet de résoudre les structures secondaires à quatre brins, appelées G4 ou G-quadruplex, et formées par des séquences riches en guanines stabilisées par des liaisons hydrogène guanine-guanine de type non Watson-Crick [9, 14]. L’activité exonucléase de WRN semble cohérente avec l’activité hélicase. En effet, la fonction exonucléase 3’- >5’ hydrolyse in vitro préférentiellement les structures d’ADN qui contiennent des boucles sur-enroulées, des mésappariements de leur extrémité 3’, des structures en bulles (mésappariement de plusieurs bases contiguës), des jonctions 3 ou 4 branches [14]. Enfin, les activités hélicase et exonucléase dépendent toutes deux de l’activité ATPase de la protéine WRN [14]. Ces données biochimiques, obtenues in vitro, sont des pistes possibles pour rechercher la fonction de la protéine WRN, bien qu’elles ne permettent pas d’affirmer que ces différentes structures d’ADN sont aussi résolues par la proteine WRN in vivo dans les cellules. |
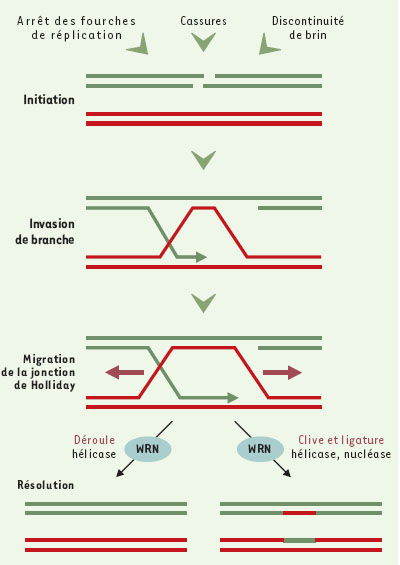
Une voie métabolique pour WRN : la recombinaison homologue Dans de précédents travaux, nous avions mis en évidence une augmentation de la fréquence ou du taux de mutations somatiques dans des cellules de patients atteints du syndrome ou dans des lignées dérivées de ces cellules. En particulier, les lignées de fibroblastes WRN ont un phénotype mutateur assez inhabituel, caractérisé par des délétions génomiques fréquentes et étendues [10, 15]. Comme les études biochimiques montraient que WRN et les autres hélicases de type RecQ sont capables de dérouler des structures d’ADN associées au processus de recombinaison de l’ADN, il paraissait logique d’envisager que WRN puisse jouer un rôle comparable dans les cellules humaines somatiques. Cette hypothèse a été explorée par la mesure des événements de recombinaison homologue grâce à l’intégration, dans le génome de cellules témoins et de cellules WRN, de deux allèles inactifs d’un gène rapporteur. L’activité de ce gène rapporteur ne sera détectable que dans les cellules ayant subi un événement de recombinaison génique entre ces deux allèles. Deux gènes rapporteurs codant l’un pour la ß-galactosidase, et l’autre pour la résistance à la néomycine ont été utilisés. Le premier permet de déterminer la fréquence de recombinaison par dénombrement direct des cellules recombinantes au sein de la population. Le second permet d’évaluer le nombre de colonies recombinantes, car seules les cellules recombinantes sont capables de se diviser et de constituer des colonies en présence de néomycine. L’analyse moléculaire de ce système rapporteur a montré une réduction de vingt fois du taux de production de recombi-nants WRN viables, notamment des événements de conversion génique (réparation fidèle de l’ADN avec conservation de la structure génomique) qui sont les produits principaux de recombinaison homologue dans les lignées cellulaires humaines normales. L’analyse des deux substrats utilisés, qui diffèrent par leur exigence de croissance cellulaire pour révéler les événements de recombinaison, nous a permis de préciser à quelle étape du processus de recombinaison homologue WRN intervient. Cette étape semble se situer à la fin du processus, lorsque les molécules filles recombinantes nouvellement produites sont résolues et ségrégées (Figure 2). La description récente de la sensibilité accrue des lignées Werner aux agents intercalant comme le cis-platine ou la mitomycine C est cohérente avec l’hypothèse d’un rôle de WRN dans le mécanisme de recombinaison. En effet, d’autres mutants de recombinaison ou de résolution chez les bactéries, levures ou mammifères sont sensibles à un spectre similaire d’agents [16, 17].  | Figure 2. Étapes mécanistiques de réparation par recombinaison homologue : un rôle pour WRN ? Un arrêt des fourches de réplication, l’interruption d’un brin ou des cassures double-brins de l’ADN peuvent déclencher une réparation par recombinaison homologue. La recombinaison conduit à la formation d’une structure à 3 ou 4 branches d’ADN ou jonction de Holliday. Cette jonction peut être résolue soit par une migration inverse des branches, soit par le clivage et et la ligation des produits de recombinaison. L’activité hélicase de WRN pourrait participer à la migration inverse des branches et résoudre les intermédiaires de recombinaison. La combinaison des activités hélicase et exonucléase avec d’autres protéines mpliquées dans la résolution pourrait cliver les jonctions de Holliday et permettre la ligation des produits de recombinaison. Une résolution correcte des produits de recombinaison, quels que soient les mécanismes utilisés est indispensable pour la production de cellules recombinantes viables. |
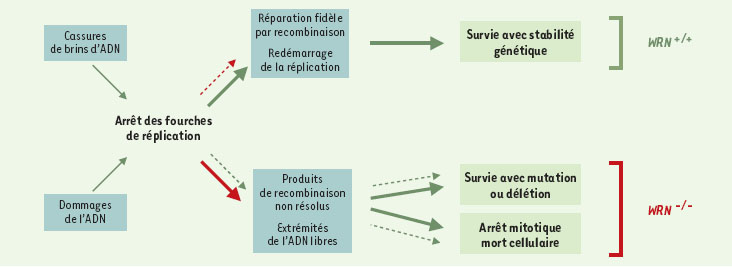
Un processus de recombinaison défectueux ou inefficace procure une explication plausible du phénotype cellulaire de Werner. Ce phénotype comprend une prolongation de la phase S du cycle cellulaire, une fraction élevée d’arrêts en phase S, une prolifération réduite, une sensibilité accrue aux agents provoquant des dommages de l’ADN (4NQO, camptothécine, cis-platine), des anomalies cytogénétiques et un phénotype mutateur par délétion [10]. À partir de l’ensemble de ces résultats, un modèle d’action de WRN peut être proposé (Figure 3). Des dommages de l’ADN, dus à des facteurs exogènes ou endogènes, peuvent conduire à un arrêt d’une fourche de réplication en cours de polymérisation. Un mécanisme de recombinaison homologue sera alors indispensable au traitement de la lésion et à la restauration d’une fourche opérationnelle. La protéine WRN interviendrait dans la ségrégation des molécules d’ADN après la restauration de la fourche de réplication. Elle pourrait en outre être impliquée dans la résolution des intermédiaires de recombinaison illégitime afin de prévenir les mutations ou les réarrangements géniques [14]. On peut souigner que le phénotype clinique de Werner est pratiquement inexistant dans les dix premières années de la vie, ce qui n’est pas le cas des autres pathologies associées à une instabilité génétique. Cela suggère l’existence d’une redondance partielle de la fonction de WRN, plusieurs activités pouvant résoudre alors les produits de recombinaison [17, 18].  | Figure 3. Modèle d’action de WRN et conséquences de la perte de fonction. L’échec ou l’inefficacité de la réparation par recombinaison homologue de l’ADN peut conduire à des cassures ou pertes de chromosomes, des réarrangements géniques, des mutations et à la mort cellulaire. La viabilité cellulaire en l’absence de WRN dépend du processus de réparation de cassures double brin par recombinaison non homologue ou non homologous end-joining (NHEJ) qui lui-même peut être mutagène pour la cellule ou provoquer des réarrangements géniques. |
|
Un rôle étendu de WRN dans les pathologies humaines ? WRN et les autres déficiences d’hélicases RecQ sont des pathologies fascinantes aussi bien pour le clinicien que pour le scientifique. Bien que le syndrome de Werner soit une maladie rare, il apparaît important de préciser la fonction de WRN dans la genèse de maladies humaines. Les patients atteints de ce syndrome ayant un risque important de développer des pathologies graves liées à l’age, comme les cancers, le diabète ou les maladies cardiovasculaires (artériosclérose) [2, 3], on peut envisager que des facteurs endogènes ou exogènes capables de moduler l’activité de WRN chez des individus sains puissent aussi augmenter le risque d’apparition de ces maladies. Nous ne connaissons pas encore de facteurs exogènes, environnementaux ou chimiques, qui modifient directement le réseau métabolique de protéines interagissant avec la proteine WRN. Cependant, nous savons qu’en l’absence de WRN, les cellules humaines sont plus sensibles aux agents endommageant l’ADN, qui induisent efficacement - ou requièrent - une réparation par recombinaison homologue. Des agents chimiques exogènes ou produits de façon endogène pourraient inhiber la fonction de WRN et permettre ainsi le maintien de dommages dans l’ADN. En compromettant l’action de WRN, ils imiteraient les effets d’une mutation inactivante. Enfin, trois types de fond génétique différents peuvent aussi révéler ou potentialiser les effets des agressions chimiques ou environnementales de l’ADN qui peuvent compromettre la fonction de WRN : polymorphisme du gène WRN ; hétérozygotie du locus WRN ; polymorphisme ou mutations d’autres gènes qui sont associés à WRN ou qui modulent son activité. Plusieurs polymorphismes ont été identifiés dans le gène WRN dont certains sont des substitutions d’acides aminés susceptibles de modifier la fonction de la protéine [19, 21]. En particulier, il a été montré que les individus porteurs d’un polymorphisme spécifique (WRN1347Arg->Cis) du locus WRN ont un risque plus élevé de développer une maladie cardiovasculaire. Bien que ce risque soit modéré, la population potentiellement affectée est très importante [19, 21]. L’étude des individus sains hétérozygotes dont un des allèles porte une mutation unique du gène WRN revêt une importance potentielle encore plus grande. En effet, nous avons récemment montré que ces porteurs sains hétérozygotes avaient in vivo une instabilité génétique intermédiaire entre les patients Werner et les individus témoins [22]. Cette étude a été réalisée par l’analyse de la fréquence de variant du marqueur glycophorine A (GPA) des globules rouges. Le test GPA mesure l’instabilité génétique in vivo en déterminant la fréquence de globules rouges variants pour l’expression de l’antigène de surface M/N impliqué dans le sérotypage des groupes sanguins. Cet antigène peut être altéré par mutation, délétion chromosomique ou extinction de gène pendant le développement des globules rouges [23]. La fréquence de globules rouges variants est plus importante chez les patients atteints de syndrome de Werner que chez les sujets hétérozygotes ; cependant, l’augmentation de cette fréquence avec l’âge n’est observée que chez les patients. Cette dernière observation est intrigante et semble indiquer un parallèle entre l’augmentation rapide de la fréquence des globules rouges variants et l’augmentation rapide des signes, des symptômes et des risques pathogènes chez les patients après la puberté. Ces résultats soutiennent l’hypothèse qu’une augmentation du taux de mutagenèse et/ou une accumulation des mutations peuvent être impliquées dans la pathogénie du syndrome de Werner. L’identification d’une instabilité génétique chez les hétérozygotes fut aussi surprenante qu’inattendue. Ces résultats sont, à notre connaissance, la première démonstration d’une instabilité génétique in vivo chez des sujets hétérozygotes pour des mutations responsables de syndromes autosomiques récessifs humains d’instabilité génétique (ataxie-télangiectasie, syndrome de Bloom, anémie de Fanconi). Une explication de ce phénotype pourrait résider dans un processus d’haploinsuffisance pour la fonction de cette protéine. En effet, les lignées cellulaires hétérozygotes ont une sensibilité aux agents provoquant des dommages de l’ADN qui est intermédiaire entre celle des lignées normales et des lignées homozygotes [24]. Cette haplo-insuffisance pour WRN pourrait être, de plus, potentialisée par les effets du fond génétique, de l’environnement ou de l’exposition à des agents thérapeutiques. Les hétérozygotes sont relativement fré-quents aux États-Unis, en Europe de l’ouest et au Japon avec une estimation de 2 à 5 cas pour 1 000 [2, 6, 25, 26], ce qui pourrait influencer le risque de pathologies de nombreux individus. On peut ainsi estimer le nombre de porteurs hétérozygotes à 65 000 au Canada, 120 000 en France et plus de 550 000 aux États-Unis. Une façon évidente d’examiner plus précisément le rôle de l’hétérozygotie WRN sur le risque pathogène serait d’analyser si un excès de mutations de WRN est décelable chez les patients atteints de néoplasies, en particulier des formes observées chez les patients Werner homozygotes. Une autre méthode consisterait à analyser les mutations WRN chez les patients qui présentent une toxicité plus élevée que la normale aux traitements par des drogues, comme le cis-platine ou la mitomycine C, qui détruisent sélectivement les cellules WRN [24, 27]. Le polymorphisme ou les mutations d’autres protéines impliquées dans le réseau fonctionnel de WRN pourrait aussi modifier la fonction de WRN elle-même. La protéine WRN interagit en effet avec plusieurs protéines comme la protéine de réplication A (RPA), l’ADN polymérase ∂, le PCNA (proliferating cell nuclear antigen), l’ADN topoisomérase I, la protéine p53 et les protéines de réparation de cassures double brin par recombinaison non homologue, Ku et ADN-PK (→) [13, 14]. Le polymorphisme des gènes codant pour ces protéines pourrait atténuer ou altérer la fonction de WRN. Ces gènes, grâce a un polymorphisme ne conservant pas d’interaction avec la protéine WRN, ou une perte de fonction par mutation pourraient être responsables des 10 % de cas de syndrome de Werner qui présentent tous les critères diagnostiques mais pas de mutation de WRN. Un exemple de ces patients est le cas d’une femme japonaise de 29 ans qui présente les phénotypes cliniques et cellulaires typiques du syndrome de Werner mais dont aucune mutation inactivant la protéine WRN n’a pu être mise en évidence [28, 29]. (→) m/s 2001, n°4, p. 480 |
Des progrès rapides ont été réalisés au cours des cinq dernières années pour déterminer et comprendre la pathogénie du syndrome de Werner et des autres déficiences humaines liées aux hélicases RecQ. De nombreuses questions restent toutefois encore en suspens. En particulier, nous n’avons pas encore de réponse satisfaisante sur la nécessité d’une perte conjointe des deux fonctions, hélicase et exonucléase, de WRN dans le syndrome de Werner, même si, à ce jour, toutes les mutations identifiées chez les patients éliminent ces deux fonctions dans la cellule. Quelles sont les autres fonctions in vivo de WRN dans le métabolisme des acides nucléiques ? Son rôle dans la réparation de l’ADN par recombinaison homologue permet certes d’expliquer clairement le phénotype observé, mais d’autres fonctions, notamment dans la réplication de l’ADN ou la transcription ont été aussi évoquées [30]. D’une façon plus générale, on ne connaît pas encore le rôle spécifique des différentes hélicases de la famille RecQ, ni comment leur activité est contrôlée. La compréhension approfondie de leur fonction normale et de leurs interconnexions devrait nous permettre de comprendre comment la perte d’un seul membre de cette famille conduit à un syndrome clinique et à un spectre tumoral distincts, et d’identifier de nouveaux outils ou de nouvelles cibles pour prévenir, diagnostiquer ou traiter les maladies qui accompagnent aussi bien la perte fonctionnelle des hélicases RecQ que le vieillissement normal d’un individu. |
1. Werner O. On cataract in conjunction with scleroderma (translated by H. Hoehn). In : Salk D, Fujiwara Y, Martin GM eds. Werner’s syndrome and human aging,1st ed New York : Plenum Press,1985 : 1–14 2. Epstein CJ, Martin GM, Schultz AL, Motulsky AG. Werner’s syndrome: A review of its symptomatology, natural his-tory, pathologic features, genetics and relationship to the natural aging process. Medicine 1966; 45 : 177–221. 3. Goto M. Werner’s syndrome: From clinics to genetics. Clin Exp Rheumatoi 2000; 18 : 760–6. 4. Goto M, Miller RW, Ishikawa Y, Sugano H. Excess of rare cancers in Werner syndrome (adult progeria). Cancer Epidemiol Biomarkers Prev 1996; 5 : 239–46. 5. Monnat RJ Jr. Cancer patho-genesis in the human RecQ helicase deficiency syndromes. In : Goto M., Miller RW eds. From premature gray hair to helicase: Werner syndrome implications for aging and cancer. Gann Monograph on Cancer Research 2001; 49:83–94. 6. Yu CE, Oshima J, Fu YH, et ai Positional cloning of the Werner’s syndrome gene. Science 1996; 272 : 258–62. 7. Chakraverty RK, Hickson ID. Defending genome integrity during DNA replication: a proposed role for RecQ family helicases. BioEssays 1999; 21 : 286–94. 8. van Brabant AJ, Stan R, Ellis NA. DNA helicases, genomic instability, and human gene-tic disease. Annu Rev Genêt 2000; 1 : 409–59. 9. Shen JC, Loeb LA. Unwinding the molecular basis of the Werner syndrome. Mech Ageing Dev 2001; 122 : 921–44. 10. Moser MJ, Oshima J, Monnat RJ Jr. WRN mutations in Werner syndrome. Hum Mutât 13: 271–9 11. Goto M, Yamabe Y, Shiratori M, et ai Immunological dia-gnosis of Werner syndrome by down-regulated and truncated gene products. Hum Genêt 1999; 105 : 301–7. 12. Moser MJ, Kamath-Loeb AS, Jacob JE, Bennett SE, Oshima J, Monnat RJ Jr. WRN helicase expression in Werner syndrome cell lines. Nucleic Acids Res 2000; 28 : 648–54. 13. Mohaghegh P, Hickson ID. DNA helicase deficiencies associated with cancer predisposition and premature ageing disorders. Hum Mol Genet 2001; 10: 741–6. 14. Shen JC, Loeb LA. The Werner syndrome gene: the molecular basis of RecQ helicasedeficiency diseases. Trends Genet 2000; 16 : 213–20. 15. Fukuchi K, Martin GM, Monnat RJ Jr. Mutator phenotype of Werner syndrome is characterized by extensive deletions. Proc Natl Acad Sci USA 1989; 86 : 5893–7. 16. Prince PR, Emond MJ, Monnat RJ Jr. Loss of Werner syndrome protein function promotes aberrant mitotic recombination. Genes Dev 2001;15 : 933–8. 17. Thompson LH, Schild D. Homologous recombinational repair of DNA ensures mammalian chromosome stability. Mutat Res 2001; 477 : 131–53. 18. Constantinou A, Davies AA, West SC. Branch migration and Holliday junction resolution catalyzed by activities from mammalian cells. Cell 2001; 104 : 259–68. 19. ye L, Miki T, Nakura J, et al. Association of a polymorphic variant of the Werner helicase gene with myocardial infarction in a Japanese population. Am J Hum Genet 1997; 68 : 494–8. 20. Castro E, Ogburn CE, Hunt KE, et al. Polymorphisms at the Werner locus: I. Newly identified polymorphisms, ethnic variability of 1367Cys/Arg, and its stability in a population of Finnish centenarians. Am J Med Genet 1999; 82 : 399–403. 21. Castro E, Edland SD, Lee L, et al. Polymorphisms at the Werner locus: II. 1074Leu/Phe, 1367Cys/Arg, longevity, and atherosclerosis. Am J Med Genet 2000; 95 : 374–80. 22. Moser MJ, Bigbee WL, Grant SG, et al. Genetic instability and hematologic disease risk in Werner syndrome patients and heterozygotes. Cancer Res 2000; 60 : 2492–6. 23. Jensen RH, Bigbee WL. Direct immunofluorescence labelling provides an improved method for the glycophorin A somatic mutation assay. Cytometry 1996; 23 : 337–43. 24. Poot M, Gollahon KA, Rabinovitch PS. Werner syndrome lymphoblastoid cells are sensitivie to camptothecin-induced apoptosis in S-phase. Hum Genet 1999; 104: 10–4. 25. Goto M, Tanimoto K, Horiuchi Y, Sasazuki T. Family analysis of Werner’s syndrome: a survey of 42 Japanese families with a review of the literature. Clin Genet 1981; 19 : 8–15. 26. Cerimele D, Cottoni F, Scappaticci SG, et al. 1982. High prevalence of Werner’s syndrome in Sardinia: description of six patients and estimate of the gene frequency. Hum Genet 1982; 62 : 25–30. 27. Poot M, Yom JS, Whang SH, Kato JT, Gollahon KA, Rabinovitch PS. Werner syndrome cells are sensitive to DNA cross-linking drugs. FASEB J 2001; 15 : 1224–6. 28. Matsumura T, Nagata M, Konishi R, Goto M. Studies of SV40-infected Werner syndrome fibroblasts. Adv Exp Med Biol 1985; 190 : 313–30. 29. Prince PR, Ogburn CE, Moser MJ, Emond MJ, Martin GM, Monnat RJ Jr. Cell fusion corrects the 4-nitroquinoline 1-oxide sensitivity of Werner syndrome fibroblast cell lines. Hum Genet 1999; 105 : 132–8. 30. Fry M, Loeb LA. The three faces of the WS helicase. Nat Genet 1998; 19 : 308–9. |