Consommations et mésusages : données épidémiologiques
2012
4-
Consommation et mésusages chez les sujets sous médicaments de substitution aux opiacés
Un traitement de substitution aux opiacés (TSO) repose sur la prescription de médicaments à base de dérivés morphiniques en vue de compenser les effets du manque à l’arrêt de la consommation d’opiacés illicites chez les sujets dépendants des opiacés.
Malgré une mise en place très polémique en France où le sevrage a longtemps été considéré comme la seule option thérapeutique, la substitution aux opiacés s’est rapidement développée au milieu des années 1990, en parallèle à la mise en œuvre d’une politique de réduction des risques, du fait de la nécessité de faire face à l’épidémie de contamination par voie injectable par le virus de l’immunodéficience humaine (VIH) chez les usagers de drogues. Le cadre de prescription s’est ainsi établi autour de deux médicaments de substitution aux opiacés (MSO) : la méthadone (MTD), mise sur le marché en 1995, et la buprénorphine haut dosage (BHD) rendue disponible l’année suivante et pour laquelle des formes génériques existent depuis 2006.
La méthadone, agoniste pur des récepteurs opiacés, appartient à la classe des stupéfiants
1
Du fait de son statut de stupéfiant, la prescription de MTD est limitée à 14 jours (versus 28 pour la BHD) et sa délivrance est fractionnée pour une durée de 7 jours, sauf en cas de mention « à délivrer en une fois » (idem pour ce point pour la BHD).
. Elle est disponible sous deux formes : sirop depuis sa mise sur le marché (flacons unidoses de 5, 10, 20, 40 et 60 mg) et gélule (1, 5, 10, 20 et 40 mg) depuis 2008. Cette molécule ne peut être utilisée que dans un cadre très strict puisque l’instauration du traitement n’est possible qu’en centre de soins spécialisés (Csapa : Centres de soins d’accompagnement et de prévention en addictologie) ou en établissement de santé où le cadre est en général plus contraignant qu’en médecine libérale (prescription et délivrance parfois quotidiennes en début de traitement dans certains centres et/ou contrôles urinaires
2
Les contrôles urinaires ont pour but de vérifier la prise de traitement et de s’assurer de l’absence de consommation récente d’opiacés.
) tout en offrant un éventuel soutien psychologique et social. Le relais en médecine de ville n’est possible qu’une fois le patient stabilisé, sous-entendant une posologie stable de méthadone, une gestion autonome du traitement voire des dosages urinaires négatifs aux opiacés. Le passage à la forme gélule n’intervient également que chez un patient cliniquement stabilisé. La dose d’entretien recommandée pour la méthadone est comprise entre 60 et 100 mg/jour, mais des posologies supérieures sont parfois nécessaires.
La buprénorphine est un agoniste partiel des récepteurs opiacés. Disponible en France depuis 1984 à faible dosage comme antalgique (Temgésic®, 0,2 mg), elle est depuis 1996 utilisée à haut dosage (BHD) (Subutex®) en tant que traitement de substitution qui se présente sous forme de comprimés sublinguaux dosés initialement à 0,4, 2 et 8 mg, et, depuis 2008, à 1, 4 et 6 mg. Elle peut être prescrite par tout médecin – ce qui explique sa plus grande disponibilité par rapport à la méthadone – et ne figure pas sur la liste des stupéfiants, même si elle en partage les règles de prescription et de délivrance. La posologie d’entretien recommandée est de 8 mg/jour avec une dose maximale fixée à 16 mg/jour.
La France a été le premier pays à introduire la BHD pour le traitement de la dépendance aux opiacés et par conséquence possède l’expérience la plus longue dans ce champ. Elle est l’un des rares pays en Europe (avec la République Tchèque et la Suède) à bénéficier d’une telle prédominance de prescription de cette molécule comparativement à la méthadone (80 % de l’ensemble des MSO délivrés en France) et d’une telle facilité d’accès par le biais de la médecine générale. En 1999, 85 % des prescriptions de BHD dans les Bouches du Rhône étaient ainsi effectuées par la médecine générale (Thirion et coll., 2002

).
Bien que ne disposant pas d’autorisation de mise sur le marché dans l’indication de traitement de substitution aux opiacés, les sulfates de morphine (Moscontin® et Skénan®), analgésiques majeurs utilisés pour les douleurs intenses ou rebelles, peuvent toutefois être prescrits à titre exceptionnel
3
En cas de nécessité thérapeutique (contre-indications, inadaptation des traitements à la méthadone et à la BHD aux besoins des patients) ou lorsque l’état du patient l’impose. Les ordonnances sécurisées s’y afférant doivent d’autre part porter systématiquement la mention « en concertation avec le médecin conseil ».
et seulement après avoir reçu l’accord du médecin conseil de la Caisse primaire d’Assurance maladie.
Impact de la diffusion des MSO depuis leur introductionen France
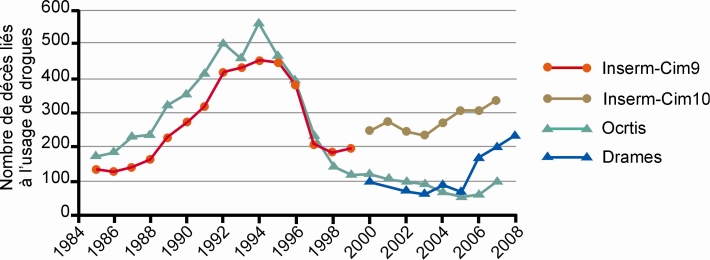
Au plan sanitaire, l’impact le plus marquant est lié à la diminution importante des décès par surdose durant la seconde moitié des années 1990 : ils ont été divisés par plus de cinq entre 1994 et 2002 d’après les décès enregistrés par l’Inserm (CepiDC) et les données de l’Ocrtis (Office central pour la répression du trafic illicite des stupéfiants). Néanmoins, une certaine reprise semble se dessiner à partir de 2003, en particulier à travers les données du CepiDC-Inserm et les données de l’enquête Drames (Décès en Relation avec Abus de Médicaments et de Substances) (Afssaps et CEIP, 2010a

) (figure 4.1

).
D’autres améliorations majeures sont à souligner en France, comme un meilleur accès aux soins, en particulier pour les traitements antiviraux, et une diminution des conduites à risques chez les usagers de drogues. Il a en effet été observé, au travers de différents travaux de suivi d’usagers traités, non seulement un moindre recours à l’injection (Fhima et coll., 2001

) et au partage des seringues et du petit matériel, mais aussi une plus faible consommation de substances illicites (Fhima et coll., 2001

; Costes et coll., 2004

). Selon l’étude Anisse
4
L’objectif de l’étude Anisse était de décrire les retombées économiques et sociales d’un traitement de substitution par buprénorphine haut dosage.
par exemple, l’injection au cours du mois écoulé, chez les usagers suivis, est passée de 65 % au moment de l’instauration du traitement à 34 % six mois plus tard (Batel et coll., 2001

). En parallèle, une baisse de la pratique du partage de seringues et de matériel a également été observée chez ces usagers, passant sur la même période respectivement de 15 % à 5,5 % et de 22 % à 8 % (Batel et coll., 2001

).
Sur le plan social, la mise en place de ces traitements a été associée à une amélioration des conditions de logement (Fhima et coll., 2001

; Bilal et coll., 2003

), de l’insertion professionnelle permanente (Batel et coll., 2001

) avec en parallèle une diminution de la délinquance (Sansfacon et coll., 2005

). Au niveau national, le nombre d’interpellations pour usage ou usage-revente d’héroïne a ainsi chuté de 76 % entre 1995 et 2002.
En outre, sur la base de plusieurs critères d’efficacité, la BHD et la méthadone apparaissent comparables en termes de bénéfices sanitaires et sociaux, exception faite d’un maintien en traitement plus long pour la méthadone, en particulier pour les patients présentant une dépendance plus sévère (Inserm, 2010

).
Niveaux d’usage de médicaments de substitutionaux opiacés
Diverses sources de données relatives à l’usage de MSO existent en France :
• les données de l’Assurance maladie qui permettent d’appréhender, à partir des remboursements de MSO prescrits en ville ou en structures de soins et délivrés en officine de ville, le niveau d’usage de ces molécules parmi les bénéficiaires affiliés au régime général de l’Assurance maladie ;
• les données recueillies dans le cadre d’enquêtes reproductibles menées auprès des populations usagères de drogues vues au travers de centres de soins (enquête Oppidum : Observation des produits psychotropes illicites ou détournés de leur utilisation médicamenteuse), en médecine de ville (enquête Opema : Observation des pharmacodépendances en médecine ambulatoire), ou au travers de structures dites de « bas seuil » (enquêtes ENa-Caarud et Prelud).
Ces différents types d’enquêtes ont pour point commun d’appréhender les niveaux d’usage de MSO ainsi que les modalités de traitement des populations concernées. Les niveaux d’utilisation des MSO sont le plus souvent appréhendés par le biais des doses quotidiennes moyennes
5
La dose quotidienne moyenne se calcule le plus souvent au travers des études en additionnant toutes les quantités prescrites par produit (BHD ou méthadone) de la première à l’avant dernière délivrance de l’année en les divisant par la durée de traitement (de la première à la dernière date de délivrance) (Canarelli et Coquelin, 2010

).
(DQM) reçues, alors que les types de traitement peuvent être approchés, suivant les cas, par la régularité des prescriptions ou par leur finalité (obtention dans le cadre d’un protocole thérapeutique de substitution ou non).
Approche du niveau d’usage chez les individus bénéficiant de remboursements de MSO
Les délivrances de psychotropes sont analysées à partir des bases de données de remboursement de l’Assurance maladie provenant de la transmission électronique des pharmacies, soit par interrogation directe des bases régionales du Système National d’Informations Inter-Régimes de l’Assurance Maladie (SNIIR-AM) pour le régime général de l’Assurance Maladie, soit lors de requêtes dans l’Échantillon Général des Bénéficiaires (EGB).
Les données de délivrance de MSO en ville obtenues à partir de l’étude des bases de remboursement de l’Assurance maladie sont analysées par l’OFDT et l’Assurance maladie (enquête Cnamts/OFDT) et permettent de faire un état des lieux régulier de l’usage mais aussi de certaines dimensions du mésusage de ces produits.
Ceux recevant un traitement en ville peuvent bénéficier d’une primo-prescription de BHD ou bien d’un relais de prescription de BHD ou de méthadone après prise en charge préalable en structure de soins et une fois stabilisés.
En 2007, l’Assurance maladie fait état d’environ 130 000 personnes ayant bénéficié d’au moins un remboursement en ville de MSO (BHD et/ou méthadone), avec, spécificité française, une nette prédominance pour la BHD, la méthadone n’étant prescrite qu’à un sujet sur cinq (Canarelli et Coquelin, 2009

). Cependant, la méthadone étant considérablement moins mésusée que la BHD (Canarelli et Coquelin, 2010

; Afssaps et CEIP, 2008

; Cadet-Taïrou et coll., 2010


), si l’on considère seulement les patients en traitement de substitution réellement encadrés médicalement et en processus de soins, la part des patients traités par méthadone est probablement plus haute que ne l’indiquent ces données de remboursement. Celles-ci n’incluent par ailleurs pas les patients non stabilisés sous méthadone qui reçoivent leur traitement directement en centre de soins.
L’analyse plus précise des données de remboursement pour l’année 2007 (Canarelli et Coquelin, 2010

) à partir d’un échantillon représentatif de près de 5 000 patients retrouve une DQM de 8,9 mg/jour pour la BHD (moyenne proche de la posologie d’entretien recommandée : 8 mg) (tableau 4.I

). L’analyse indique que 30 % des patients bénéficient de DQM de 4 mg ou moins et un patient sur dix bénéficie d’une DQM supérieure à 16 mg/jour (valeur de la dose maximale).
Concernant la méthadone, la dose quotidienne estimée (49,5 mg/jour) est inférieure au dosage minimal recommandé de 60 mg/jour. Un quart des sujets de cet échantillon bénéficie d’une DQM conforme aux préconisations (entre 60 et 100 mg/jour) et près des deux tiers ont un dosage compris entre 20 et 70 mg/jour. Le phénomène de DQM relativement basse pour la méthadone est sous-tendu par la diffusion progressive de la prescription de ce traitement – recommandation en particulier émise en 2004 lors de la Conférence de consensus sur les MSO (Fédération française d’addictologie et Anaes, 2004) – permettant d’atteindre des sujets plus jeunes et peut-être moins dépendants. Ceci pourrait expliquer la diminution de l’âge moyen des sujets recevant cette molécule et celle de leur dosage moyen prescrit (Canarelli et Coquelin, 2010

).
Quel que soit le MSO prescrit, les DQM sont légèrement plus élevées pour les patients bénéficiaires de la couverture maladie universelle (CMU), avec respectivement 11 et 53 mg/jour selon qu’ils reçoivent la BHD ou la méthadone. Ce phénomène avait déjà été observé dans diverses études et serait sous-tendu par une plus grande fragilité ou précarité de ces sujets, voire parfois aussi par des niveaux de dépendance supérieurs (Cadet-Taïrou et Cholley, 2004

; Plancke et coll., 2009

).
Il est d’autre part important de constater, dans cet échantillon représentatif, comme dans d’autres travaux (Cadet-Taïrou et Cholley, 2004

) que la majorité des patients bénéficiant de remboursements de MSO prescrits en médecine de ville (60,8 %) sont considérés comme étant en traitement régulier
6
La régularité d’un traitement repose non seulement sur la prise en compte de la durée de traitement sur l’année mais aussi du respect de l’intervalle entre deux délivrances de MSO. Un patient recevant sur l’année un traitement sur une durée courte (<300 jours) peut donc être considéré comme étant en traitement continu si les délais entre deux délivrances sont respectés.
correspondant à une prise en charge durable chez des patients ayant régulièrement consulté et présenté vraisemblablement l’ensemble des quantités de leur traitement au remboursement. Le tiers restant est donc en traitement « non régulier » défini comme un suivi intermittent associé à une plus grande précarité ou à des mésusages (acquisitions visant le marché noir ou un usage « toxicomaniaque
7
C’est-à-dire le même usage que n’importe quelle autre drogue.
»). Les patients bénéficiaires de BHD sont plus souvent en traitement régulier que ceux traités par méthadone (65 %
versus 43 %), ce qui pourrait être expliqué par une prise en charge plus entrecoupée chez ces derniers du fait d’une alternance ville/hôpital plus fréquente (Canarelli et Coquelin, 2010

).
Plusieurs CEIP ont de plus réalisé des travaux à partir cette fois des bases de données locales et régionales de l’Assurance maladie. Dans les Bouches-du-Rhône, de septembre à décembre 1999, 11 186 prescriptions de BHD concernant 2 078 patients ayant eu au moins une prescription avaient été collectées et analysées. La DQM avait été évaluée à 11,5 mg/jour pour un nombre moyen de 6,2 prescriptions par patient. Plus de 60 % des patients étaient suivis régulièrement alors que 18 % avaient un comportement irrégulier (DQM supérieure à 20 mg/jour ou plus de 2 prescripteurs) et plus de 20 % avaient moins d’une prescription par mois sur les 4 mois étudiés (Micallef et coll., 2004

).
Approche du niveau d’usage parmi les populations usagères de drogues
Les niveaux de consommation de BHD des patients vus dans des structures de soins de type Csapa (anciennement CSST) sont proches de ceux des patients suivis en médecine de ville.
Depuis 1995, l’enquête Oppidum (Observation des Produits Psychotropes Illicites ou Détournés de leur Utilisation Médicamenteuse), financée par l’Agence française de sécurité sanitaire des produits de santé (Afssaps), est une enquête pharmaco-épidémiologique nationale transversale menée annuellement pendant une période d’une semaine dans des structures (hospitalières ou ambulatoires) prenant en charge des patients présentant un abus, une pharmacodépendance de substances psychoactives ou encore recevant un MSO. Organisée par le réseau des 13 Centres d’évaluation et d’information sur la pharmacodépendance et d’addictovigilance (CEIP-A), ce programme inclut annuellement plus de 5 000 sujets présentant un abus ou une pharmacodépendance à une substance psychoactive (sauf tabac et alcool) et/ou consommant un médicament de substitution aux opiacés. Ces sujets sont recrutés par près de 150 centres de soins spécialisés dans la prise en charge des sujets pharmacodépendants (Csapa principalement, quelques Caarud et des services hospitaliers spécialisés en addictologie) dans plus de 51 départements.
Dans son édition de 2008 (Afssaps et CEIP, 2008

), l’enquête Oppidum observe que, dans les centres de soins, 40 % des personnes sous traitement de substitution reçoivent de la buprénorphine et 60 % de la méthadone. S’agissant de la BHD, elle fait état de doses quotidiennes moyennes de BHD différentes selon que les patients sont en protocole thérapeutique (92 % des cas) ou en dehors de tout protocole thérapeutique, ces derniers ayant des dosages moyens supérieurs (9,1 mg/jour
versus 8,2 mg/jour).
Depuis 2008, l’enquête Opema (Observation des Pharmacodépendances en Médecine Ambulatoire), est une enquête pharmaco-épidémiologique nationale transversale conduite annuellement auprès d’un réseau de médecins généralistes. Elle a pour objectif principal de recueillir des informations sur les caractéristiques sociodémographiques, les consommations de produits et l’état de santé des patients suivis en médecine de ville, qu’ils soient sous traitement de substitution de la dépendance aux opiacés ou usagers de substances actives illicites ou de médicaments détournés de leur usage thérapeutique. Parmi les patients sous traitement de substitution interrogés via l’enquête Opema en 2008, 68 % reçoivent de la BHD, 30 % de la méthadone et 2 % un autre traitement. Ces patients bénéficiant de BHD ont, pour l’année 2008 (Afssaps et CEIP, 2010b

) et pour la très grande majorité d’entre eux (97 %) des DQM de BHD nettement inférieures à la dose maximale fixée par l’AMM (16 mg/jour). Globalement mieux stabilisés que les patients vus en structures de soins, seuls 1 % sont considérés comme étant en dehors d’un protocole thérapeutique tel que défini dans l’enquête (tableau 4.I

).
Concernant la méthadone, les données obtenues au travers de l’enquête Oppidum font état pour 2008 de DQM plus élevées que celles des sujets vus en ville au travers de l’enquête Opema (62,5 mg/jour versus 54,7 mg/jour) ; ceci pourrait s’expliquer, là encore, par le fait que les patients vus en centres de soins ne sont pas forcément aussi bien stabilisés ou ont un niveau de dépendance plus élevé.
Tableau 4.I Indicateurs d’usage et de mésusage de MSO au travers diverses enquêtes
|
Population / Enquête
|
MSO
|
Indicateurs de niveau d’usage : DQM (mg/j)
|
Types de traitement
|
Indicateurs de mésusageet indicateurs comportementaux
|
Co-prescriptions
|
|
Enquête auprès des individus bénéficiant de remboursements de MSO
| | | | | |
|
Enquête Cnamts / OFDT (Données de remboursement en MSO d’un échantillon de plus de 4 500 patients en 2007 bénéficiaires du régime général de l’Assurance maladie)
|
BHD
|
8,9 mg/j
|
Régulier 66 %
Non régulier 34 %
|
DQM > 32 mg/j : 1,6 %
≥ 5 médecins : 9,3 %
≥ 5 pharmacies : 10,2 %
|
Benzodiazépines
|
|
MTD
|
49,5 mg/j
|
Régulier 43 %
Non régulier 57 %
| |
Benzodiazépines
|
|
Enquête en population usagère de drogues (structures de soins)
| | | | | |
|
Enquête Oppidum 2008
|
BHD
|
DQM (PT) : 8,2
DQM (PNT) : 9,1
|
PT : 92 %
PNT : 8 %
|
Voies (PT) :
orale : 94 % ; sniff : 8 % ; IV : 7 %
Voies (PNT) :
sniff : 58 % ; orale : 34 % ; IV : 18 %
Acquisition
PT : Illégale (9 %) ; PNT : Illégale (97 %)
|
Benzodiazépines
|
| |
MTD
|
DQM : 62,5 (sirop : 63,3 ; gélule : 53,4)
| | |
Benzodiazépines
|
|
Enquête en population usagère de drogues (médecine de ville)
| | | | | |
|
Enquête Opema 2008
|
BHD
|
97 % DQM <AMM
|
PT : 99 %
PNT : 1 %
|
Voies (PT) :
orale : 97 % ; sniff : 10 % ; IV : 9 % ;inhalation : 2 %
Acquisition :
prescription régulière : 94 % ; deal : 6 % ;prescription ponctuelle : 4 %
| |
| |
MTD
|
DQM : 54,7
|
Sirop : 79 %
Gélule : 21 %
PT : 98 % / PNT : 2 %
| | |
|
Enquêtes en population usagère de drogues (structures bas seuil)
| | | | | |
|
Enquête Prelud 2006
|
BHD
| | |
Type d’usage :
soins : 49 % ; défonce : 28 % ; les deux : 23 %
Voies :
IV : 58 % ; orale : 45 % ; sniff : 22 % ;inhalation : 3 %
Acquisition :
Prescription : 59 % ; mixte (prescription + marché parallèle) : 26 % ; marché parallèle seul : 15 %
| |
| |
MTD
| | |
PT : 71 % / PNT : 17 %
PT + PNT : 12 %
| |
|
Enquête ENa-Caarud 2008
|
BHD
| | |
Type d’usage :
- soins : 74 %
- consommé en dehors des soins (autre MSO ou pas de MSO) : 24 %
Voies :
IV : 56 % ; orale : 44 % ; sniff : 18 % ;inhalation : 4 %
|
Benzodiazépines
|
|
MTD
| | | | |
BHD : Buprénorphine haut dosage ; DQM : Dose quotidienne moyenne ; IV : Intraveineux ; MSO : Médicament de substitution aux opiacés ; MTD : Méthadone ; PT : Protocole thérapeutique ; PNT : En dehors d’un protocole thérapeutique.
Mésusages de MSO
Avec la généralisation des MSO ont émergé des pratiques de mésusage de ces produits. Le mésusage de la BHD, en particulier de sa forme princeps (Subutex®), est ainsi très vite apparu comme un des problèmes associés au traitement, au même titre que les surdoses pour la méthadone.
Mésusage et problématique de l’injection
Le mésusage de BHD peut revêtir différentes formes : un usage ne répondant pas aux recommandations du médecin prescripteur (injection, sniff, voire co-usage non préconisé d’autres substances psychoactives) ou une utilisation en dehors de toute prescription qui pourra se faire par voie sublinguale, injection ou sniff. Il peut également s’agir d’un détournement du produit en vue d’alimenter le marché noir dans le cadre d’un trafic.
Injection des MSO en France
L’injection de BHD a été, et reste la pratique la plus préoccupante (Costes, 2010

). Si, pour de nombreux individus, l’accès au MSO signifie l’arrêt de la pratique d’injection, pour d’autres la BHD remplace l’héroïne comme produit principalement injecté. Un pourcentage non négligeable de personnes substituées perçoit les MSO, et en particulier la BHD, comme plus problématiques que l’héroïne elle-même. Par exemple, 21,6 % des usagers des Caarud (2008) et 53,6 % des usagers de BHD citent ou considèrent la BHD comme le produit leur posant le plus de problèmes (Cadet-Taïrou et coll., 2008

). Dès 2001 ont été identifiés des cas de « primo-usagers de Subutex® »
8
Cette molécule est alors le premier opiacé consommé chez des individus ou le premier à être à l’origine d’une dépendance.
pour lesquels ce produit constitue la porte d’entrée dans l’usage d’opiacés (Escots et Fahet, 2004

; Modelon et coll., 2007

; Afssaps et CEIP, 2011

).
Il s’agit le plus souvent d’une population hétérogène plutôt jeune et aux conditions de vie précaires (« errants » ou « nomades ») et de personnes originaires d’Europe de l’Est et du Maghreb (Costes, 2010

). La BHD a acquis depuis près d’une dizaine d’années une réputation de « drogue de rue » qui a entraîné une mauvaise image auprès de la plupart des sujets qui en font un mésusage. Son injection a par ailleurs engendré de nouveaux problèmes de santé. Le dispositif Trend (Tendances récentes et nouvelles drogues)
9
Mis en œuvre à l’OFDT en 1999, à l’initiative du plan triennal de la Mission interministérielle de lutte contre la drogue et la toxicomanie (Mildt), le dispositif Trend est chargé de fournir aux pouvoirs publics des éléments de connaissance sur les profils, les conditions de vie et les pratiques des usagers de produits psychotropes essentiellement illicites et d’identifier d’éventuels phénomènes émergents. Il permet de recueillir directement ces informations qualitatives sur le terrain auprès d’usagers vus notamment dans les milieux urbain et festif.
a identifié très tôt au sein de la population utilisant la BHD par voie intraveineuse une augmentation du nombre de sujets présentant un gonflement des mains et des avants bras (« syndrome de Popeye »). Ces effets sont liés au blocage des petits réseaux veineux par certains excipients de la BHD (particulièrement pour la forme princeps, le Subutex®) entraînant une inflammation chronique des tissus et du réseau lymphatique. L’injection présente également des risques de complications locales (abcès cutanés, nécrose tissulaire), voire parfois générales (endocardite, embolie pulmonaire, septicémie) (Grau et coll., 2010

).
Le mésusage de BHD par injection (au cours du dernier mois) concernerait, selon certaines études, environ 15 % des patients en traitement (Fhima et coll., 2001

; Inserm, 2010

). Les différents travaux montrent qu’il s’agit en général d’une population ayant un niveau de dépendance plus sévère vis-à-vis des opiacés mais aussi de l’alcool, plus souvent polyconsommatrice et encline à des comorbidités psychiatriques. Ces sujets percevraient plus souvent leurs posologies journalières de BHD comme inadéquates (Vidal-Trecan et coll., 2003

; Inserm, 2010

).
Des études, même si certaines sont plus anciennes, ont parfois fait état de taux élevés (atteignant 28 à près de 60 %) de sujets bénéficiant de BHD et s’injectant ce produit (Obadia et coll., 2001

; Varescon et coll., 2002

; Guichard et coll., 2003

; Vidal-Trecan et coll., 2003

)
10
Des méthodologies différentes selon les études peuvent sous-tendre des niveaux de prévalence différents (populations en traitement ou non, vues en structures de soins ou au travers de structures de bas seuil...).
. C’est le cas de l’étude de Varescon et coll. (2002

) menée à la fin des années 1990 qui montrait, au sein d’une population d’usagers de drogues ayant bénéficié de BHD dans le cadre d’un protocole thérapeutique, un recours à l’injection pour la moitié d’entre eux (49,5 %). Le plus souvent le produit était injecté au cours du mois suivant sa découverte (2/3 des cas), en groupe (54 %) et après initiation par d’autres usagers (57 %). Les motivations à l’injection mises en avant dans ce travail et retrouvées dans de nombreuses autres études sont la curiosité, la recherche de sensation mais aussi l’importance donnée par certains usagers au rituel de l’injection. Certains auteurs évoquent un sous-dosage des sujets pouvant expliquer en partie ces pratiques (Varescon et coll., 2002

; Vidal-Trécan et coll., 2003

; Roux et coll., 2008

). Dans l’étude de Vidal-Trécan et coll. (2003

), sur 404 sujets recevant un traitement par BHD, la prise de BHD la semaine précédant la première injection était inférieure aux doses recommandées dans 64,6 % des cas.
Enfin, l’injection semble être le mode d’usage le plus répandu lorsque la BHD est détournée de son usage thérapeutique. Ainsi, en 2008, parmi les usagers des Caarud (dont beaucoup sont des usagers de drogues actifs et connaissent des niveaux de précarité importants), la part des consommateurs de BHD au cours du mois précédent l’ayant injectée (au moins une fois au cours du mois) s’élève à 56,4 % (Cadet-Taïrou et coll., 2010b

). L’injection parmi les patients qui déclarent prendre la BHD dans le cadre d’un traitement régulier atteint 58 % (Cadet-Taïrou et coll., 2010b

). Dans cette même population, l’enquête Prelud en 2006 montrait que la part des injecteurs de BHD variait avec l’intentionnalité de l’usage et apparaissait maximale pour les personnes mêlant intentionnalité de « défonce » et d’arrêt de l’héroïne (74 %) (Cadet-Taïrou et coll., 2006

).
Au total, interrogés sur l’image qu’ils ont de la BHD, les usagers vus au travers du dispositif Trend mettent en avant les risques liés à sa dépendance, perçue comme plus tenace que celle liée à l’héroïne, et à son injection. Pour nombre d’usagers de drogues, la BHD a donc perdu au fil du temps son statut de médicament et son image s’est dégradée. À l’inverse, la méthadone conserve toujours une image plutôt positive auprès des usagers en tant que MSO. Ils mettent en effet en avant son efficacité contre le manque psychique et physique et son mode de délivrance plus encadré, renforçant la perception de son statut de médicament. La rareté de la méthadone sur le marché parallèle,
a contrario de la BHD, en fait de plus aux yeux des usagers un produit dont l’image est associée à des usagers mieux insérés socialement. L’injection de méthadone n’est d’autre part pas une pratique observée en France, et les très rares tentatives rapportées avec le sirop ont été infructueuses (Cadet-Taïrou et coll., 2010b

).
Injection des MSO : données dans d’autres pays
D’autres pays rapportent également des problèmes liés à l’injection de BHD. En Europe, en dehors de la France, la Géorgie et la Finlande sont confrontées à des prévalences élevées d’injection de cette molécule. En Finlande en particulier, d’importantes consommations problématiques de BHD ont été observées puisque cette molécule serait rapportée comme « drogue principale » pour 90 % des usagers problématiques d’opiacés et 30 % des patients vus en centres de soins (EMCDDA, 2005

). En Géorgie, de la même manière qu’au travers d’autres études (Obadia et coll., 2001

; Moratti et coll., 2010

), les observations récentes d’injection de BHD se rencontrent plus fréquemment chez des sujets jeunes, vivant le plus souvent dans des conditions instables sur le plan du logement et du revenu, et souvent polyconsommateurs (Cadet-Taïrou et coll., 2010a

). Dans ce pays, une étude récente menée auprès des sujets injecteurs vus dans des structures d’échange de seringues ou dans des structures bas seuil (Otiashvili et coll., 2010

) montre que 27 % des plus jeunes citent la BHD comme la molécule les ayant rendus dépendants aux opiacés (
versus 9 % des injecteurs plus âgés (p=0,001)), signant l’apparition relativement récente sur le marché parallèle de cette molécule et son attractivité croissante. Si l’usage de ce produit par voie injectable s’explique pour près de la moitié des injecteurs par une recherche de plaisir et de « défonce » (48 %), 42 % disent y recourir à l’inverse pour une tentative de sevrage volontaire (pour « faire face »), ou, dans une moindre mesure, comme auto-substitution pour « arrêter les drogues » (6 %).
Il est à noter que les doses moyennes utilisées par injection sont plus basses en Géorgie qu’en France. En effet, 44,7 % de ces usagers disent injecter à chaque occasion une dose moyenne de 1 mg (soit 1/8 d’une tablette de 8 mg), 46 % 2 mg et seuls 9 % 4 mg, ceci pour des raisons économiques, une tablette entière étant utilisée dans la grande majorité des cas par un groupe de 4 à 8 usagers. Cet usage contraste avec celui des pays économiquement développés, comme la France, où peuvent être injectés par occasion entre 6 et 10 mg de BHD. Selon les auteurs, une autre raison pourrait expliquer cette faible dose injectée : la volonté pour la plupart des sujets de se sevrer des opiacés plutôt que de rechercher un effet euphorisant (Otiashvili et coll., 2010

).
Une étude réalisée en Australie (Winstock et Lea, 2010

) précise que le mésusage de la BHD ne se fait pas uniquement, ni même majoritairement, par voie injectable. En effet, les auteurs montrent que si 26 % des sujets suivis en centres de soins en 2005
11
Neuf centres de soins publics de la région de Nouvelle Galles du Sud.
disent s’être déjà injecté de la BHD, le mésusage, quand il existe, repose le plus souvent sur une utilisation orale
12
Seuls 6 % des patients de cette étude bénéficiant d’un traitement par BHD disent l’avoir injectée au cours de plus de 10 occasions – 23 % l’ayant déjà injecté une fois ou plus - la majorité préférant le mésuser « directement » (par voie sublinguale ou orale).
, le comprimé étant considéré comme facile d’emploi (du fait de sa petite taille et de sa dissolution rapide). Sont surtout rapportées dans ce pays des problématiques d’injection de méthadone : sur 350 patients bénéficiaires de méthadone vus dans ces mêmes centres de soins, les deux tiers (65,9 %) auraient rapporté s’être injecté au moins une fois le produit. Le risque de mésusage de ce traitement était 6 fois plus élevé si les sujets avaient consommé la méthadone avant leur mise sous traitement (primo-usage), ce qui était le cas pour la moitié d’entre eux. Il semble toutefois que ces patients n’aient pas une grande expérience de l’injection et que la régularité de ce mésusage ne concernait donc qu’une faible proportion d’entre eux.
Données sur les autres dimensions du mésusage des MSO en France
Le mésusage des MSO, et en particulier de la BHD, peut s’appréhender de plusieurs manières selon le type d’étude menée. Des indicateurs de mésusage relatifs aux doses quotidiennes moyennes reçues (DQM>32 mg/jour) ou au nombre de professionnels de santé sollicités au cours de l’année (nombre de médecins et/ou de pharmacies ≥ 5) sont fréquemment utilisés dans les analyses de données de remboursement de MSO (Cholley et coll., 2001

; Claroux-Bellocq et coll., 2003

; Cadet-Taïrou et Cholley, 2004

). Ainsi, un indicateur de polyprescription permettant de mesurer les quantités obtenues en excès par des usagers se faisant prescrire des médicaments par plusieurs prescripteurs en même temps (chevauchement d’ordonnances) a été défini (Thirion et coll., 2002

; Micallef et coll., 2004

; Pradel et coll., 2009

).
Les enquêtes menées auprès de populations usagères de drogues explorent quant à elles plus largement le mésusage en appréhendant les finalités d’usages (soins et/ou « défonce »), les voies d’administration (orale, intraveineuse, sniff, inhalation), les modes d’acquisition (prescription et/ou marché parallèle) ou parfois le devenir du traitement (usage substitutif et/ou revente).
Approche du niveau de mésusage chez les individus bénéficiant de remboursements de MSO
Au cours du deuxième semestre 2002, l’analyse de données de remboursement de MSO sur plusieurs sites français
13
Étude menée sur 13 sites régionaux en 2002.
faisait état d’une prévalence de 6 % de sujets bénéficiaires de BHD ayant reçu une DQM supérieure ou égale à 32 mg/jour, et d’une prévalence identique de prescriptions obtenues par au moins cinq médecins sur la même période. Les sujets concernés étaient essentiellement localisés sur les sites de Paris, sa banlieue nord et Marseille (Cadet-Taïrou et Cholley, 2004

). Les deux éditions suivantes
14
Études menées au niveau national, à partir de deux échantillons indépendants de patients ayant reçu en 2006 et en 2007 au moins un remboursement de BHD et/ou de méthadone sur chacune des deux années.
menées sur des échantillons nationaux représentatifs de patients au cours des années 2006 et 2007 (Canarelli et Coquelin, 2010

) ont fait apparaître une diminution importante de ces dosages supérieurs à 32 mg/jour qui ne concernaient plus que 2 % de l’ensemble des sujets en 2006 (n=84) puis 1,6 % l’année suivante (n=61). Il s’agit de sujets très majoritairement de sexe masculin (respectivement 84 et 88 %), plus âgés que la moyenne de l’échantillon (36 et 38,6 ans
versus 35 ans) et principalement repérés en Île-de-France, PACA et Alsace. Par ailleurs, le nomadisme médical diminue entre 2006 et 2007 puisque le taux de sujets s’adressant à 5 médecins ou plus passe de 10 % à 6 %. La diminution de ces indicateurs de mésusage au niveau national est une conséquence directe de la mise en place depuis 2004 d’un plan de contrôle de l’Assurance maladie auprès des assurés suspects de détournement voire de trafic de BHD, plan renforcé à partir de 2006 (Cnamts, 2004

).
Approche du niveau de mésusage en populations usagères de drogues
Les finalités de traitement ne sont pas les mêmes suivant les populations enquêtées puisque si la grande majorité des patients vus en ville (via leurs données de remboursement ou leur suivi en médecine générale à travers l’enquête Opema) sont en processus de soins, la plupart de ceux vus dans les structures de bas seuil ne le sont pas. L’enquête Prelud montrait ainsi en 2006 que, sur l’ensemble des sujets vus au travers de ces structures, la moitié recevait la BHD dans un but thérapeutique (49 %), un peu plus du quart l’utilisaient à des fins de « défonce » (28 %), et les autres (23 %) y recouraient avec ces deux objectifs (tableau 4.I

). Si la voie d’usage la plus utilisée dans cette population est l’injection (56 % des usagers de BHD dans l’enquête ENa-Caarud 2008), les usagers ont également recours à la voie orale (45 %) mais également à la voie sniffée (18 %) et inhalée (4 %). L’acquisition de la BHD se fait le plus souvent par prescription pour 60 % des sujets vus dans l’enquête Prelud, 15 % l’obtenant exclusivement à partir du marché parallèle et un quart des sujets par ces deux biais. Le mode d’acquisition de la BHD est différent dans une population plus insérée : l’enquête Oppidum retrouve que l’acquisition illégale ne concerne que 9 % des patients en protocole thérapeutique
versus 97 % des sujets en dehors de tout protocole. Le même constat est fait pour les patients interrogés en médecine de ville (enquête Opema), puisque la grande majorité bénéficie de BHD par le biais d’une prescription régulière (94 %) plutôt que par
deal (6 %) (tableau 4.I

).
Quelques données relatives au trafic de MSO en France
Le trafic de la BHD s’est progressivement développé sur le territoire français avec l’apparition, dans un premier temps, de petits trafiquants non usagers à Paris et Marseille puis, dans un second temps, de l’implantation de petites scènes ouvertes
15
Il s’agit de lieux de vente et de consommation de produits où habitants et citoyens non-consommateurs sont confrontés à l’usage et au petit trafic de produits illicites dans des espaces publics.
de BHD (Subutex®) où vendeurs et usagers peuvent se rencontrer directement sans avoir recours à des intermédiaires (Costes, 2010

). L’expansion de ce marché noir de BHD est sous-tendue par plusieurs phénomènes : la demande soutenue du produit par une population très marginalisée comme celle des migrants n’ayant pas ou ne souhaitant pas avoir accès au système de soins (ORS PACA, 2009

; Costes, 2010

) ; l’insatisfaction de certains concernant leurs dosages les conduisant à compléter leur traitement par un achat dans la rue où l’offre est abondante ; le trafic à destination de pays où la BHD est moins disponible. Ce trafic fonctionne à l’heure actuelle toujours selon deux modalités : une activité diffuse de « petite revente » par des patients traités s’assurant un petit revenu – ou l’achat d’autres substances par ce biais – et une autre activité de « recueil » et de revente par un nombre réduit de personnes non nécessairement traitées mais envoyées en tant que « mules »
16
Trafic professionnalisé visant le marché international essentiellement, de manière à ne pas être repérés par les caisses régionales de l’Assurance maladie.
. La facilité de prescription auprès de certains médecins, voire la délivrance d’ordonnances de « complaisance », permet également d’alimenter le trafic (ORS PACA, 2009

; Costes, 2010

). Le plan de contrôle de l’Assurance maladie, lancé dès l’année 2004, en menant diverses actions auprès des professionnels de santé et/ou des patients a toutefois permis – même s’il n’a pas été décliné de manière aussi homogène selon les départements – de diminuer fortement ce phénomène au regard des prévalences de détournement actuellement constatées. Les patients stabilisés et les moins précaires, notamment, ont ainsi rejoint le cadre thérapeutique. Cependant, on constate que la BHD est toujours considérée comme étant très disponible sur le marché noir (Cadet-Taïrou et coll., 2010a

), même si cette situation est probablement en partie due à une diminution conjoncturelle de la demande, elle-même liée à l’accroissement depuis 2006 environ de la disponibilité de l’héroïne en France.
Quant au trafic de méthadone, il est presque inexistant en France. Ceci s’explique notamment par le fait que cette molécule est associée à une utilisation par des usagers globalement plus insérés d’un point de vue social. La méthadone vendue sur le marché parallèle provient ainsi quasiment exclusivement de stocks et de surplus accumulés par des patients substitués, qui, pour diverses raisons
17
Du fait des règles de prescription strictes en termes de prescription et de délivrance, il arrive que des patients « économisent » leur traitement pour éviter d’éventuelles ruptures de traitement de quelques jours. Ceci explique qu’ils peuvent alors parfois « dépanner » d’autres patients, échanger leur méthadone contre d’autres produits ou en revendre un peu. Les logiques commerciales en lien avec ce produit restent toutefois marginales.
, ne consomment pas la totalité de ce qui leur a été prescrit et délivré. Elle y est d’ailleurs plus souvent échangée (« troquée ») que vendue (Cadet-Taïrou et coll., 2010a

). Des observations récentes font également état d’une tendance chez certains usagers de drogues à recourir à la méthadone en auto-substitution, en amont de toute prise en charge. L’auto-substitution peut être liée à la gestion de manque ponctuel d’héroïne pour certains usagers ou s’inscrire dans une démarche durable (chez des usagers refusant de s’intégrer dans un protocole de substitution qu’ils jugent long et fastidieux ou par choix, pour les plus insérés, de ne pas mettre leur image sociale en danger en fréquentant un centre spécialisé) (Cadet-Taïrou et coll., 2010


).
Une enquête menée à Paris en 2007 sur 659 sujets en garde à vue (Sec et coll., 2009

) avait montré que près de 10 % d’entre eux avaient déclaré obtenir des médicaments psychotropes via le marché noir. Si le clonazépam (Rivotril®) arrivait en tête des médicaments illégalement obtenus (pour 42,6 % des sujets), les MSO arrivaient en deuxième position : 30,6 % s’étaient procuré de la BHD (dose moyenne de 13,7 mg/jour) et 21 % de la méthadone (dose moyenne de 54,6 mg/jour). Un peu moins d’un sujet sur cinq (18 %) s’était procuré des sulfates de morphine.
Co-prescriptions ou co-usages de médicaments chez les patients bénéficiant de MSO
Certains patients bénéficiant de MSO peuvent recevoir également des co-prescriptions, notamment de médicaments psychotropes. Ces molécules, en particulier les benzodiazépines, sont le plus souvent utilisées à visée thérapeutique, une part importante des patients étant confrontés à des problèmes de morbidité psychiatrique associés (Afssaps et CEIP, 2011

; Laqueille et coll., 2009

). Dans différents pays, 50 à 90 % des patients bénéficiant de MSO et suivis en ambulatoire recevraient une prescription de médicaments psychotropes tout comme jusqu’à 50 % des patients pris en charge en structures de soins, même si les recommandations nationales, quand elles existent, tentent de décourager ces types d’associations du fait des risques de complications en termes de morbidité mais aussi de mortalité (Backmund et coll., 2005

; Fatséas et coll., 2009

). Tout usage associé de ces médicaments n’est pas synonyme de recherche de « défonce », même si certaines benzodiazépines sont connues pour être détournées et abusées, comme c’est le cas du flunitrazépam (Rohypnol®) , dont la prescription est pourtant encadrée depuis 2001 du fait des mésusages dont il a fait l’objet, mais qui est encore détourné chez des sujets socialement très marginalisés. Le clonazépam (Rivotril®) est également détourné, mais de manière plus limitée en raison d’un effet « défonce » moins marqué.
L’étude de Fatséas et coll. (2009

), menée en région Aquitaine, a tenté de mettre à jour les motivations de recours aux benzodiazépines chez des sujets traités, en ville ou en structure de soins, par BHD ou méthadone depuis au moins un mois. La majorité des sujets interrogés (53 %) a rapporté une consommation « mixte », à la fois à visée thérapeutique et à visée hédonique, voire de « défonce », un tiers des sujets utilisant ces molécules uniquement à visée thérapeutique, et 15 % dans une optique uniquement hédonique. Ceux ayant recours à ces molécules à des fins exclusivement thérapeutiques les obtenaient plus souvent par prescription médicale que ceux les utilisant à visée de défonce (p<10
-3). Le premier objectif était d’obtenir un effet anxiolytique (p<10
-2), tout en recourant plus fréquemment à la voie d’administration adaptée (voie orale, p<10
-4). Les molécules identifiées étaient principalement celles habituellement prescrites en population générale (bromazépam et oxazépam en particulier). À l’inverse, les sujets recourant aux médicaments à visée hédonique ou de « défonce » seule avaient davantage recours à la polyconsommation de produits, obtenaient les benzodiazépines, en particulier le flunitrazépam (Rohypnol®), sur le marché noir et utilisaient des voies d’administration non-conformes (intraveineuse ou nasale notamment).
En Allemagne, une étude de Backmund et coll. (2005

) s’est intéressée aux facteurs qui sous-tendraient une plus grande consommation de benzodiazépines chez les patients bénéficiant de MSO que chez les sujets consommateurs d’héroïne sans prise en charge thérapeutique. Sur 1 049 sujets interrogés et ayant pris de manière quotidienne soit de la méthadone, soit de la codéine ou encore de l’héroïne, un peu moins de la moitié de l’ensemble de ces sujets pris en charge (44 %) avaient ainsi consommé des benzodiazépines quotidiennement, et parmi eux, 20 % prenaient des doses élevées de benzodiazépines (60 mg/jour de Valium®, c’est-à-dire de diazépam, ou d’une molécule équivalente). De plus, au sein des 3 groupes, les prévalences de consommation de benzodiazépines les plus élevées se trouvaient chez les sujets bénéficiant d’un des deux traitements (méthadone ou codéine) plutôt que parmi ceux s’injectant de l’héroïne. Selon cette étude, le recours aux benzodiazépines serait d’autant plus fréquent que les sujets seraient de sexe masculin, plus dépendants aux opiacés et avec un parcours de consommation plus long, et qu’ils seraient davantage polyconsommateurs (alcool et barbituriques en particulier). Les auteurs suggèrent également que ce recours « complémentaire » aux benzodiazépines pourrait également s’expliquer en partie par la recherche d’un plaisir que ne procureraient pas les seuls traitements.
L’enquête Cnamts/OFDT a analysé les co-prescriptions éventuelles de benzodiazépines au cours de l’année 2007 chez les patients ayant bénéficié d’un MSO (Canarelli et Coquelin, 2010

) (tableau 4.II

). D’autres médicaments, qu’ils soient suspects de mésusage comme le trihexyphénidyle ou Artane® (antiparkinsonien de synthèse consommé pour ses effets psychotropes), marqueur indirect d’une injection potentielle comme l’acide flucidique ou Fucidine® (antibiotique local fréquemment utilisé en cas d’abcès cutanés et donc marqueur possible d’une utilisation intraveineuse) voire suspects de trafic plus organisé comme le Cytotec®
18
Antisécrétoire gastrique détourné et exporté comme produit abortif. Il existe en effet depuis quelques années un trafic à visée abortive de ce produit à destination de pays d’Afrique de l’Ouest (réseau prostitutionnel).
ont également été analysés dans ce travail. L’intérêt était également de comparer le recours à ces molécules en termes de prévalence au sein de différents groupes de patients (échantillon global, patients bénéficiaires de la CMU et, pour la BHD, patients bénéficiant d’une DQM>32 mg/jour). Même s’il n’est pas possible de déterminer dans ce travail si ces prescriptions ont été effectuées sur la même ordonnance que les MSO, l’étude de consommations associées est informative.
Trois types de consommation s’individualisent ainsi chez les bénéficiaires de la BHD selon qu’ils ont un profil « standard » (selon qu’ils sont issus de l’ensemble de l’échantillon), qu’ils sont bénéficiaires de la CMU (environ 1/5e de la population bénéficiant de BHD) ou qu’ils reçoivent des DQM>32 mg/jour (1,6 % de la population). Le profil « standard » fait ainsi état d’une consommation de benzodiazépines chez un peu moins de la moitié des sujets (40 %) avec des molécules habituellement prescrites en population générale (prédominance du bromazépam ou Lexomil® et d’hypnotiques) et un recours quasi nul aux produits suspects de mésusage (Artane® et Cytotec®) prouvant que, dans leur grande majorité, ces sujets ne se livrent probablement pas à un trafic. Les sujets bénéficiant de méthadone ont un profil de consommation très similaire. Les individus bénéficiant de la CMU (respectivement 21,4 % et 18,7 % de ceux recevant de la BHD et de la méthadone), ont des niveaux légèrement supérieurs de prescription en benzodiazépines (53 %) et une comorbidité psychiatrique plus élevée puisque 10 % des bénéficiaires de BHD reçoivent de la cyamémazine (Tercian®) versus 8 % de l’ensemble de l’échantillon. Ils sont par ailleurs plus nombreux à recourir à l’acide fucidique (Fucidine®), marqueur probable d’injection (13 % versus 8 %) mais ne sont pas dans une dynamique de trafic (seuls 0,7 % reçoivent du Cytotec®). Les sujets recevant la CMU, plus précarisés et fragilisés que les autres, ont donc des consommations plus problématiques (Canarelli et Coquelin, 2009) avec un probable recours plus fréquent à l’injection, mais ne sont pas concernés par le trafic. En revanche, les quelques sujets recevant plus de 32 mg/jour de BHD ont un profil très différent. Bénéficiant pour la grande majorité (85 %) de benzodiazépines, avec une prédominance de recours à des molécules davantage problématiques du fait de leur risque de détournement et de mésusage (clonazépam ou Rivotril® et flunitrazépam ou Rohypnol®), ces sujets ont également des niveaux importants de prescription de Cytotec® (15 %). Il doit en effet s’agir d’un groupe de patients tournés vers une activité de trafic, ou tout au moins suspects de mésusage, et de surcroît en grande difficulté (consommation, en plus des benzodiazépines, de cyamémazine ou Tercian® pour près de 20 % d’entre eux mais aussi de trihexyphénidyle ou Artane® pour 3 % et recours à l’injection pour certains puisque 15 % bénéficient de l’acide fucidique ou Fucidine®).
Environ 8 % des sujets bénéficiant de méthadone reçoivent également des prescriptions de Fucidine®, laissant supposer que la pratique d’injection n’est pas réservée aux sujets recevant de la BHD, et suggérant aussi que les injections concernent d’autres produits que la méthadone (Canarelli et Coquelin, 2009

).
D’autres travaux montrent également ces « choix » ou « préférences » de recours aux benzodiazépines selon le profil des patients bénéficiant de BHD. L’étude de Varescon et coll. (2002

) retrouvait, parmi les sujets injecteurs de BHD, une polyconsommation importante et une prescription préférentielle de flunitrazépam (Rohypnol®) (1/3 des sujets) suivi par le bromazépam (Lexomil®) (9 %) et le clorazépate (Tranxène®) (6 %). Une autre étude française menée entre 2001 et 2004 (Lavie et coll., 2009

) auprès de 170 patients recevant un traitement par BHD depuis au moins 3 mois et recrutés par leur médecin prescripteur, a montré que si les deux tiers des individus (67 %) rapportaient avoir consommé des benzodiazépines au cours de leur vie, 15 % en avaient fait un usage simple
19
L’usage simple est défini dans cette étude comme un usage de benzodiazépines au cours des 30 derniers jours sans critères d’abus ou de dépendance (à l’inverse de l’usage problématique sur la même période).
au cours des 30 derniers jours et 30,6 % un usage problématique sur la même période (dont 6,5 % de cas d’abus et 24,1 % de dépendance à ces molécules). Si l’usage simple de benzodiazépines était associé à un dosage faible de BHD (<4 mg/jour, p=0,01), l’usage problématique était associé avec différents facteurs de précarité (logement non stable et absence d’insertion professionnelle) et de comorbidité (symptômes anxieux et dépressifs). Étaient également observées plus fréquemment des co-consommations (alcool en particulier) et avec un dosage moyen de BHD plus élevé (>10 mg/jour).
Tableau 4.II Co-consommations de médicaments en particulier psychotropes au sein de différents groupes de patients bénéficiant de BHD ou de méthadone en 2007 (d’après Données CnamTS 2007, estimations OFDT)
|
MSO « groupe »
|
Médicaments co-consommés(%)
|
BHD « tous patients »
|
BHD « CMU+ »
|
BHD >32 mg/j
|
Méthadone « tous patients »
|
Méthadone « CMU+ »
|
|
EffectifPourcentageau sein de l’échantillon
| |
n=3 711
100 %
|
n=793
21,4 %
|
n=61
1,6 %
|
n=896
100 %
|
n=167
18,7 %
|
|
Médicaments psychotropes
|
|
Benzodiazépines :
Anxiolytiques
|
Tranxène® (%)
|
3,9
|
6,2
|
4,9
|
3,2
|
7,2
|
|
Lexomil® (%)
|
14,9
|
18,5
|
29,5
|
14,9
|
20,3
|
|
Valium 10 mg® (%)
|
6,3
|
10,6
|
21,3
|
8,5
|
12,6
|
|
Seresta® (%)
|
8,3
|
10,3
|
22,9
|
8,3
|
7,2
|
|
Rivotril® (%)
|
4,8
|
6,9
|
37,7
|
4,7
|
6,6
|
|
Rohypnol® (%)
|
3,7
|
6,3
|
49,2
|
3,0
|
4,2
|
|
Benzodiazépines :
Hypnotiques
|
Imovane® (%)
|
11,1
|
17,1
|
26,2
|
12,0
|
15,6
|
|
Stilnox® (%)
|
13,5
|
16,6
|
26,2
|
13,4
|
11,3
|
|
Prescription d’au moins une de ces benzodiazépines
|
(%)
|
40,0
|
53,0
|
85,0
|
44,0
|
54,0
|
|
Neuroleptique
|
Tercian® (%)
|
8,2
|
10,3
|
18,0
|
7,0
|
5,9
|
|
Médicaments suspects ouindicateurs de mésusage
|
|
Artane® (%)
|
0,3 (n=12)
|
0,5 (n=4)
|
3,3 (n=2)
|
0,2 (n=2)
|
0
|
|
Cytotec® (%)
|
0,4 (n=14)
|
0,7 (n=6)
|
14,8 (n=9)
|
0,3 (n=3)
|
0,6 (n=1)
|
|
Fucidine® (%)
|
8,0 (n=301)
|
13 (n=103)
|
14,8 (n=9)
|
7,8 (n=70)
|
12 (n=20)
|
En conclusion, le mésusage des MSO, en particulier de la BHD, a significativement diminué en France ces dernières années, les indicateurs ayant nettement décru entre 2002 et 2007, comme le montrent les études réalisées à partir des données de l’Assurance maladie. Le nombre de patients ayant bénéficié de DQM>32 mg/jour de BHD, indicateur clef de mésusage, est ainsi passé de 6 % à 1,6 % entre 2002 et 2007. Ce phénomène est une conséquence directe du plan de contrôle de l’Assurance maladie mené depuis 2004 auprès des assurés sociaux suspects de détournement voire de trafic de BHD, puis renforcé en 2006. Il est basé sur différents types d’actions selon les cas observés : établissement d’un protocole de soins, suspension de certaines prestations non médicalement justifiées voire poursuites pénales. Pour diminuer le mésusage et le détournement de certains médicaments, un arrêté en application de l’article L.162-4-2 du Code de la sécurité sociale a été adopté le 1er avril 2008. Il rend obligatoire pour la BHD (ainsi que pour la méthadone, le flunitrazépam et le méthylphénidate) l’inscription du nom du pharmacien désigné par le patient sur l’ordonnance et, en cas d’usage abusif ou de mésusage, l’établissement d’un protocole de soins entre médecin traitant, médecin conseil de la caisse d’assurance maladie et patient.
Bibliographie
[1]AFSSAPS, CEIP.OPPIDUM (Observation des produits psychotropes illicites ou détournés de leur utilisation médicamenteuse). Résultats de l’enquête 20, Octobre 2008. 2008.

[2]AFSSAPS, CEIP.DRAMES (Décès en relation avec l’abus de médicaments et de substances). Résultats de l’enquête 2008. 2010a.

[3]AFSSAPS, CEIP.OPEMA (Observation des pharmacodépendances en médecine ambulatoire). Résultats de l’enquête 1, Novembre 2008. 2010b.

[4]AFSSAPS, CEIP.OPEMA (Observation des pharmacodépendances en médecine ambulatoire). Résultats de l’enquête 2, Novembre 2009. 2011.

[5] BACKMUND M, MEYER K, HENKEL C, SOYKA M, REIMER J, et coll. Co-consumption of benzodiazepines in heroin users, methadone-substituted and codeine-substituted patients.
J Addict Dis. 2005;
24:17
-29

[6] BATEL P.Retombées économiques et sociales d’un traitement de substitution par Buprénorphine Haut Dosage. Résultats préliminaires après six mois de suivi. Étude ANISSE. 2001.

[7] BILAL S, MENARES J, DE LA SELLE P, TOUFIK A, PERDRIEUX Y. Effect of maintenance treatments on social life. A study with general practitioners.
Ann Med Interne (Paris). 2003;
154:S6
-S14

[8] CADET-TAÏROU A, CHOLLEY D.Approche régionale de la substitution aux opiacés 1999-2002 : pratiques et disparités à travers 13 sites français. OFDT, 2004.

[9] CADET-TAÏROU A, GANDILHON M, TOUFIK A, EVRARD I.Phénomènes émergents liés aux drogues en 2006. Huitième rapport national du dispositif Trend. OFDT, 2008.

[10] CADET-TAÏROU A, GANDILHON M, LAHAIE E, CHALUMEAU M, COQUELIN A, TOUFIK A.Drogues et usages de drogues en France. État des lieux et tendances récentes 2007-2009 en france. Neuvième édition du rapport national du dispositif trend. OFDT, 2010a.

[11] CADET-TAÏROU A, COQUELIN A, TOUFIK A. CAARUD . profils et pratiques des usagers en 2008.
Tendances. 2010b;
74:1
-4

[12] CANARELLI T, COQUELIN A.Données récentes relatives aux traitements de substitution aux opiacés. Premiers résultats d’une analyse de données de remboursement concernant plus de 4 500 patients en 2006 et 2007. OFDT, Tendances 2009, n° 65 : 6 p.

[13] CANARELLI T, COQUELIN A.Données récentes relatives aux traitements de substitution aux opiacés. Analyse de données de remboursement concernant un échantillon représentatif de patients en 2006 et en 2007. OFDT, Saint-Denis, 2010, 127 p.

[14] CHOLLEY D, GACHOT P, GAINET JM, OSTERMAN M, REMPP R, et coll. Traitement de substitution par buprénorphine haut dosage : quel rôle pour l’assurance maladie ?.
Revue médicale de l’Assurance Maladie. 2001;
32:295
-303

[15] CLAROUX-BELLOCQ D, DE BAILLIENCOURT S, SAINT-JEAN F, CHINAUD F, VALLIER N, et coll. Les traitements de substitution aux opiacés en France métropolitaine en 2000 : les données du régime général de l’assurance maladie.
Revue Médicale de l’Assurance Maladie. 2003;
34:93
-102

[16]CNAMTS.Prise en charge médicale des toxicomanes : un plan d’actions pour renforcer le suivi des patients qui bénéficient d’un traitement de substitution (Subutex, méthadone). Cnamts, 2004.

[17] COSTES JM.Les usages de drogues illicites en France depuis 1999 vus au travers du dispositif trend. OFDT, Saint-Denis, 2010, 192 p.

[18] COSTES JM, CADET-TAÏROU A, THIRION X, BELLO PY, PALLE C. Du point de vue de la santé publique, quels sont les résultats positifs que l’on peut attribuer aux traitements de substitution aux opiacés en termes de prise en charge médicale, psychologique et sociale des usagers et quels sont leurs effets défavorables ou non souhaités (mésusages...) ?.
Alcoologie et Addictologie. 2004;
26:38S
-54S

[19] ESCOTS S, FAHET G.Usages non substitutifs de la buprénorphine haut dosage : investigation menée en France en 2002-2003. OFDT, 2004.

[21] FATSEAS M, LAVIE E, DENIS C, AURIACOMBE M. Self-perceived motivation for benzodiazepine use and behavior related to benzodiazepine use among opiate-dependent patients.
J Subst Abuse Treat. 2009;
37:407
-411

[22]FÉDÉRATION FRANÇAISE D’ADDICTOLOGIE, ANAES.Conférence de consensus : Stratégies thérapeutiques pour les personnes dépendantes des opiacés : place des traitements de substitution. 23 et 24 juin 2004, Lyon.

[23] FHIMA A, HENRION R, LOWENSTEIN W, CHARPAK Y. Two-year follow-up of an opioid-user cohort treated with high-dose buprenorphine (Subutex).
Ann Med Interne (Paris). 2001;
152 (Suppl 3):IS26
-IS36

[24] GRAU D, VIDAL N, FAUCHERRE V, LEGLISE Y, PINZANI V, et coll. Complications infectieuses induites par le mésusage de la buprénorphine haut dosage (Subutex) : analyse rétrospective de 42 observations.
Rev Med Interne. 2010;
31:188
-193

[25] GUICHARD A, LERT F, CALDERON C, GAIGI H, MAGUET O, et coll. Illicit drug use and injection practices among drug users on methadone and buprenorphine maintenance treatment in France.
Addiction. 2003;
98:1585
-1597

[26]INSERM.Réduction des risques infectieux chez les usagers de drogues. Collection Expertise collective. Éditions Inserm;
Paris:2010;

[27] LAQUEILLE X, LAUNAY C, DERVAUX A, KANIT M. Abuse of alcohol and benzodiazepine during substitution therapy in heroin addicts: a review of the literature.
Encephale. 2009;
35:220225. Epub 2008 Oct 1.

[28] LAVIE E, FATSEAS M, DENIS C, AURIACOMBE M. Benzodiazepine use among opiate-dependent subjects in buprenorphine maintenance treatment: correlates of use, abuse and dependence.
Drug Alcohol Depend. 2009;
99:338
-344

[29] MICALLEF J, PRADEL V, THIRION X, JOLLIET P, LAPEYRE-MESTRE M. Use of the health insurance database by the centres for evaluation and information on pharmacodependance: examples, interests and future prospects.
Therapie. 2004;
59:581
-588

[30] MODELON H, FRAUGER E, LAURENCEAU D, THIRION X, MALLARET M, et coll. Psychotropic drug addiction: consumption study of specific population by the survey OPPIDUM 2004 from the CEIP network.
Therapie. 2007;
62:337346. Epub 2007 Nov 6.

[31] MORATTI E, KASHANPOUR H, LOMBARDELLI T, MAISTO M. Intravenous misuse of Buprenorphine. Characteristics and extent among patients undergoing drug maintenance therapy.
Clin Drug Investig. 2010;
30:3
-11

[32] OBADIA Y, PERRIN V, FERONI I, VLAHOV D, MOATTI JP. Injecting misuse of buprenorphine among french drug users.
Addiction. 2001;
96:267
-272

[33]ORS PACA. Pourquoi certains patients traités pour leur dépendance aux opiacés par la buprénorphine ne respectent-ils pas la prescription du médecin ?.
Regard Santé. 2009;
21: 4p.

[34] OTIASHVILI D, ZABRANSKY T, KIRTADZE I, PIRALISHVILI G, CHAVCHANIDZE M, MIOVSKY M. Why do the clients of georgian needle exchange programmes inject Buprenorphine?.
European Addiction Research. 2010;
16:1
-8

[35] PLANCKE L, AMARIEI A, DANEL T, BENOIT E, CHANTELOU ML, et coll.Influential factors in regular and intensive use of psychoactive drugs. Therapie. 2009;
64:371381

[36] PRADEL V, FRAUGER E, THIRION X, RONFLE E, LAPIERRE V, et coll. Impact of a prescription monitoring program on doctor-shopping for high dosage buprenorphine.
Pharmacoepidemiol Drug Saf. 2009;
18:36
-43

[37] ROUX P, VILLES V, BRY D, SPIRE B, FERONI I, et coll. Buprenorphine sniffing as a response to inadequate care in substituted patients: results from the Subazur survey in south-eastern France.
Addict Behav. 2008;
33:1625
-1629

[38] SANSFACON D, BARBECHAT O, LOPEZ D, VALADE C.Drogues et dommages sociaux. Revue de littérature internationale. OFDT, 2005.

[39] SEC I, QUESTEL F, REY C, POURRIAT JL. Misuse of psychotropic medications in a population of subjects held for custody in the city of Paris.
Therapie. 2009;
64:129
-134

[40] THIRION X, LAPIERRE V, MICALLEF J, RONFLE E, MASUT A, et coll. Buprenorphine prescription by general practitioners in a French region.
Drug Alcohol Depend. 2002;
65:197
-204

[41] VARESCON I, VIDAL-TRECAN G, NABET N, BOISSONNAS A. Buprenorphine abuse: high dose intravenous administration of buprenorphine.
Encephale. 2002;
28:397
-402

[42] VIDAL-TRECAN G, VARESCON I, NABET N, BOISSONNAS A. Intravenous use of prescribed sublingual buprenorphine tablets by drug users receiving maintenance therapy in France.
Drug Alcohol Depend. 2003;
69:175
-181

[43] WINSTOCK AR, LEA T.Diversion and injection of methadone and buprenorphine among clients in public opioid treatment clinics in New South Wales, Australia. Subst Use Misuse. 2010;
45:240252

→ Aller vers SYNTHESE
 ).
). ) (figure 4.1
) (figure 4.1 ).
).
 ) et au partage des seringues et du petit matériel, mais aussi une plus faible consommation de substances illicites (Fhima et coll., 2001
) et au partage des seringues et du petit matériel, mais aussi une plus faible consommation de substances illicites (Fhima et coll., 2001 ; Costes et coll., 2004
; Costes et coll., 2004 ). Selon l’étude Anisse4
par exemple, l’injection au cours du mois écoulé, chez les usagers suivis, est passée de 65 % au moment de l’instauration du traitement à 34 % six mois plus tard (Batel et coll., 2001
). Selon l’étude Anisse4
par exemple, l’injection au cours du mois écoulé, chez les usagers suivis, est passée de 65 % au moment de l’instauration du traitement à 34 % six mois plus tard (Batel et coll., 2001 ). En parallèle, une baisse de la pratique du partage de seringues et de matériel a également été observée chez ces usagers, passant sur la même période respectivement de 15 % à 5,5 % et de 22 % à 8 % (Batel et coll., 2001
). En parallèle, une baisse de la pratique du partage de seringues et de matériel a également été observée chez ces usagers, passant sur la même période respectivement de 15 % à 5,5 % et de 22 % à 8 % (Batel et coll., 2001 ).
). ; Bilal et coll., 2003
; Bilal et coll., 2003 ), de l’insertion professionnelle permanente (Batel et coll., 2001
), de l’insertion professionnelle permanente (Batel et coll., 2001 ) avec en parallèle une diminution de la délinquance (Sansfacon et coll., 2005
) avec en parallèle une diminution de la délinquance (Sansfacon et coll., 2005 ). Au niveau national, le nombre d’interpellations pour usage ou usage-revente d’héroïne a ainsi chuté de 76 % entre 1995 et 2002.
). Au niveau national, le nombre d’interpellations pour usage ou usage-revente d’héroïne a ainsi chuté de 76 % entre 1995 et 2002. ).
). ). Cependant, la méthadone étant considérablement moins mésusée que la BHD (Canarelli et Coquelin, 2010
). Cependant, la méthadone étant considérablement moins mésusée que la BHD (Canarelli et Coquelin, 2010 ; Afssaps et CEIP, 2008
; Afssaps et CEIP, 2008 ; Cadet-Taïrou et coll., 2010
; Cadet-Taïrou et coll., 2010
 ), si l’on considère seulement les patients en traitement de substitution réellement encadrés médicalement et en processus de soins, la part des patients traités par méthadone est probablement plus haute que ne l’indiquent ces données de remboursement. Celles-ci n’incluent par ailleurs pas les patients non stabilisés sous méthadone qui reçoivent leur traitement directement en centre de soins.
), si l’on considère seulement les patients en traitement de substitution réellement encadrés médicalement et en processus de soins, la part des patients traités par méthadone est probablement plus haute que ne l’indiquent ces données de remboursement. Celles-ci n’incluent par ailleurs pas les patients non stabilisés sous méthadone qui reçoivent leur traitement directement en centre de soins. ) à partir d’un échantillon représentatif de près de 5 000 patients retrouve une DQM de 8,9 mg/jour pour la BHD (moyenne proche de la posologie d’entretien recommandée : 8 mg) (tableau 4.I
) à partir d’un échantillon représentatif de près de 5 000 patients retrouve une DQM de 8,9 mg/jour pour la BHD (moyenne proche de la posologie d’entretien recommandée : 8 mg) (tableau 4.I ). L’analyse indique que 30 % des patients bénéficient de DQM de 4 mg ou moins et un patient sur dix bénéficie d’une DQM supérieure à 16 mg/jour (valeur de la dose maximale).
). L’analyse indique que 30 % des patients bénéficient de DQM de 4 mg ou moins et un patient sur dix bénéficie d’une DQM supérieure à 16 mg/jour (valeur de la dose maximale). ).
). ; Plancke et coll., 2009
; Plancke et coll., 2009 ).
). ) que la majorité des patients bénéficiant de remboursements de MSO prescrits en médecine de ville (60,8 %) sont considérés comme étant en traitement régulier6
correspondant à une prise en charge durable chez des patients ayant régulièrement consulté et présenté vraisemblablement l’ensemble des quantités de leur traitement au remboursement. Le tiers restant est donc en traitement « non régulier » défini comme un suivi intermittent associé à une plus grande précarité ou à des mésusages (acquisitions visant le marché noir ou un usage « toxicomaniaque7
»). Les patients bénéficiaires de BHD sont plus souvent en traitement régulier que ceux traités par méthadone (65 % versus 43 %), ce qui pourrait être expliqué par une prise en charge plus entrecoupée chez ces derniers du fait d’une alternance ville/hôpital plus fréquente (Canarelli et Coquelin, 2010
) que la majorité des patients bénéficiant de remboursements de MSO prescrits en médecine de ville (60,8 %) sont considérés comme étant en traitement régulier6
correspondant à une prise en charge durable chez des patients ayant régulièrement consulté et présenté vraisemblablement l’ensemble des quantités de leur traitement au remboursement. Le tiers restant est donc en traitement « non régulier » défini comme un suivi intermittent associé à une plus grande précarité ou à des mésusages (acquisitions visant le marché noir ou un usage « toxicomaniaque7
»). Les patients bénéficiaires de BHD sont plus souvent en traitement régulier que ceux traités par méthadone (65 % versus 43 %), ce qui pourrait être expliqué par une prise en charge plus entrecoupée chez ces derniers du fait d’une alternance ville/hôpital plus fréquente (Canarelli et Coquelin, 2010 ).
). ).
). ), l’enquête Oppidum observe que, dans les centres de soins, 40 % des personnes sous traitement de substitution reçoivent de la buprénorphine et 60 % de la méthadone. S’agissant de la BHD, elle fait état de doses quotidiennes moyennes de BHD différentes selon que les patients sont en protocole thérapeutique (92 % des cas) ou en dehors de tout protocole thérapeutique, ces derniers ayant des dosages moyens supérieurs (9,1 mg/jour versus 8,2 mg/jour).
), l’enquête Oppidum observe que, dans les centres de soins, 40 % des personnes sous traitement de substitution reçoivent de la buprénorphine et 60 % de la méthadone. S’agissant de la BHD, elle fait état de doses quotidiennes moyennes de BHD différentes selon que les patients sont en protocole thérapeutique (92 % des cas) ou en dehors de tout protocole thérapeutique, ces derniers ayant des dosages moyens supérieurs (9,1 mg/jour versus 8,2 mg/jour). ) et pour la très grande majorité d’entre eux (97 %) des DQM de BHD nettement inférieures à la dose maximale fixée par l’AMM (16 mg/jour). Globalement mieux stabilisés que les patients vus en structures de soins, seuls 1 % sont considérés comme étant en dehors d’un protocole thérapeutique tel que défini dans l’enquête (tableau 4.I
) et pour la très grande majorité d’entre eux (97 %) des DQM de BHD nettement inférieures à la dose maximale fixée par l’AMM (16 mg/jour). Globalement mieux stabilisés que les patients vus en structures de soins, seuls 1 % sont considérés comme étant en dehors d’un protocole thérapeutique tel que défini dans l’enquête (tableau 4.I ).
). ). Si, pour de nombreux individus, l’accès au MSO signifie l’arrêt de la pratique d’injection, pour d’autres la BHD remplace l’héroïne comme produit principalement injecté. Un pourcentage non négligeable de personnes substituées perçoit les MSO, et en particulier la BHD, comme plus problématiques que l’héroïne elle-même. Par exemple, 21,6 % des usagers des Caarud (2008) et 53,6 % des usagers de BHD citent ou considèrent la BHD comme le produit leur posant le plus de problèmes (Cadet-Taïrou et coll., 2008
). Si, pour de nombreux individus, l’accès au MSO signifie l’arrêt de la pratique d’injection, pour d’autres la BHD remplace l’héroïne comme produit principalement injecté. Un pourcentage non négligeable de personnes substituées perçoit les MSO, et en particulier la BHD, comme plus problématiques que l’héroïne elle-même. Par exemple, 21,6 % des usagers des Caarud (2008) et 53,6 % des usagers de BHD citent ou considèrent la BHD comme le produit leur posant le plus de problèmes (Cadet-Taïrou et coll., 2008 ). Dès 2001 ont été identifiés des cas de « primo-usagers de Subutex® »8
pour lesquels ce produit constitue la porte d’entrée dans l’usage d’opiacés (Escots et Fahet, 2004
). Dès 2001 ont été identifiés des cas de « primo-usagers de Subutex® »8
pour lesquels ce produit constitue la porte d’entrée dans l’usage d’opiacés (Escots et Fahet, 2004 ; Modelon et coll., 2007
; Modelon et coll., 2007 ; Afssaps et CEIP, 2011
; Afssaps et CEIP, 2011 ).
). ). La BHD a acquis depuis près d’une dizaine d’années une réputation de « drogue de rue » qui a entraîné une mauvaise image auprès de la plupart des sujets qui en font un mésusage. Son injection a par ailleurs engendré de nouveaux problèmes de santé. Le dispositif Trend (Tendances récentes et nouvelles drogues)9
a identifié très tôt au sein de la population utilisant la BHD par voie intraveineuse une augmentation du nombre de sujets présentant un gonflement des mains et des avants bras (« syndrome de Popeye »). Ces effets sont liés au blocage des petits réseaux veineux par certains excipients de la BHD (particulièrement pour la forme princeps, le Subutex®) entraînant une inflammation chronique des tissus et du réseau lymphatique. L’injection présente également des risques de complications locales (abcès cutanés, nécrose tissulaire), voire parfois générales (endocardite, embolie pulmonaire, septicémie) (Grau et coll., 2010
). La BHD a acquis depuis près d’une dizaine d’années une réputation de « drogue de rue » qui a entraîné une mauvaise image auprès de la plupart des sujets qui en font un mésusage. Son injection a par ailleurs engendré de nouveaux problèmes de santé. Le dispositif Trend (Tendances récentes et nouvelles drogues)9
a identifié très tôt au sein de la population utilisant la BHD par voie intraveineuse une augmentation du nombre de sujets présentant un gonflement des mains et des avants bras (« syndrome de Popeye »). Ces effets sont liés au blocage des petits réseaux veineux par certains excipients de la BHD (particulièrement pour la forme princeps, le Subutex®) entraînant une inflammation chronique des tissus et du réseau lymphatique. L’injection présente également des risques de complications locales (abcès cutanés, nécrose tissulaire), voire parfois générales (endocardite, embolie pulmonaire, septicémie) (Grau et coll., 2010 ).
). ; Inserm, 2010
; Inserm, 2010 ). Les différents travaux montrent qu’il s’agit en général d’une population ayant un niveau de dépendance plus sévère vis-à-vis des opiacés mais aussi de l’alcool, plus souvent polyconsommatrice et encline à des comorbidités psychiatriques. Ces sujets percevraient plus souvent leurs posologies journalières de BHD comme inadéquates (Vidal-Trecan et coll., 2003
). Les différents travaux montrent qu’il s’agit en général d’une population ayant un niveau de dépendance plus sévère vis-à-vis des opiacés mais aussi de l’alcool, plus souvent polyconsommatrice et encline à des comorbidités psychiatriques. Ces sujets percevraient plus souvent leurs posologies journalières de BHD comme inadéquates (Vidal-Trecan et coll., 2003 ; Inserm, 2010
; Inserm, 2010 ).
). ; Varescon et coll., 2002
; Varescon et coll., 2002 ; Guichard et coll., 2003
; Guichard et coll., 2003 ; Vidal-Trecan et coll., 2003
; Vidal-Trecan et coll., 2003 )10
. C’est le cas de l’étude de Varescon et coll. (2002
)10
. C’est le cas de l’étude de Varescon et coll. (2002 ) menée à la fin des années 1990 qui montrait, au sein d’une population d’usagers de drogues ayant bénéficié de BHD dans le cadre d’un protocole thérapeutique, un recours à l’injection pour la moitié d’entre eux (49,5 %). Le plus souvent le produit était injecté au cours du mois suivant sa découverte (2/3 des cas), en groupe (54 %) et après initiation par d’autres usagers (57 %). Les motivations à l’injection mises en avant dans ce travail et retrouvées dans de nombreuses autres études sont la curiosité, la recherche de sensation mais aussi l’importance donnée par certains usagers au rituel de l’injection. Certains auteurs évoquent un sous-dosage des sujets pouvant expliquer en partie ces pratiques (Varescon et coll., 2002
) menée à la fin des années 1990 qui montrait, au sein d’une population d’usagers de drogues ayant bénéficié de BHD dans le cadre d’un protocole thérapeutique, un recours à l’injection pour la moitié d’entre eux (49,5 %). Le plus souvent le produit était injecté au cours du mois suivant sa découverte (2/3 des cas), en groupe (54 %) et après initiation par d’autres usagers (57 %). Les motivations à l’injection mises en avant dans ce travail et retrouvées dans de nombreuses autres études sont la curiosité, la recherche de sensation mais aussi l’importance donnée par certains usagers au rituel de l’injection. Certains auteurs évoquent un sous-dosage des sujets pouvant expliquer en partie ces pratiques (Varescon et coll., 2002 ; Vidal-Trécan et coll., 2003
; Vidal-Trécan et coll., 2003 ; Roux et coll., 2008
; Roux et coll., 2008 ). Dans l’étude de Vidal-Trécan et coll. (2003
). Dans l’étude de Vidal-Trécan et coll. (2003 ), sur 404 sujets recevant un traitement par BHD, la prise de BHD la semaine précédant la première injection était inférieure aux doses recommandées dans 64,6 % des cas.
), sur 404 sujets recevant un traitement par BHD, la prise de BHD la semaine précédant la première injection était inférieure aux doses recommandées dans 64,6 % des cas. ). L’injection parmi les patients qui déclarent prendre la BHD dans le cadre d’un traitement régulier atteint 58 % (Cadet-Taïrou et coll., 2010b
). L’injection parmi les patients qui déclarent prendre la BHD dans le cadre d’un traitement régulier atteint 58 % (Cadet-Taïrou et coll., 2010b ). Dans cette même population, l’enquête Prelud en 2006 montrait que la part des injecteurs de BHD variait avec l’intentionnalité de l’usage et apparaissait maximale pour les personnes mêlant intentionnalité de « défonce » et d’arrêt de l’héroïne (74 %) (Cadet-Taïrou et coll., 2006
). Dans cette même population, l’enquête Prelud en 2006 montrait que la part des injecteurs de BHD variait avec l’intentionnalité de l’usage et apparaissait maximale pour les personnes mêlant intentionnalité de « défonce » et d’arrêt de l’héroïne (74 %) (Cadet-Taïrou et coll., 2006 ).
). ).
). ). En Géorgie, de la même manière qu’au travers d’autres études (Obadia et coll., 2001
). En Géorgie, de la même manière qu’au travers d’autres études (Obadia et coll., 2001 ; Moratti et coll., 2010
; Moratti et coll., 2010 ), les observations récentes d’injection de BHD se rencontrent plus fréquemment chez des sujets jeunes, vivant le plus souvent dans des conditions instables sur le plan du logement et du revenu, et souvent polyconsommateurs (Cadet-Taïrou et coll., 2010a
), les observations récentes d’injection de BHD se rencontrent plus fréquemment chez des sujets jeunes, vivant le plus souvent dans des conditions instables sur le plan du logement et du revenu, et souvent polyconsommateurs (Cadet-Taïrou et coll., 2010a ). Dans ce pays, une étude récente menée auprès des sujets injecteurs vus dans des structures d’échange de seringues ou dans des structures bas seuil (Otiashvili et coll., 2010
). Dans ce pays, une étude récente menée auprès des sujets injecteurs vus dans des structures d’échange de seringues ou dans des structures bas seuil (Otiashvili et coll., 2010 ) montre que 27 % des plus jeunes citent la BHD comme la molécule les ayant rendus dépendants aux opiacés (versus 9 % des injecteurs plus âgés (p=0,001)), signant l’apparition relativement récente sur le marché parallèle de cette molécule et son attractivité croissante. Si l’usage de ce produit par voie injectable s’explique pour près de la moitié des injecteurs par une recherche de plaisir et de « défonce » (48 %), 42 % disent y recourir à l’inverse pour une tentative de sevrage volontaire (pour « faire face »), ou, dans une moindre mesure, comme auto-substitution pour « arrêter les drogues » (6 %).
) montre que 27 % des plus jeunes citent la BHD comme la molécule les ayant rendus dépendants aux opiacés (versus 9 % des injecteurs plus âgés (p=0,001)), signant l’apparition relativement récente sur le marché parallèle de cette molécule et son attractivité croissante. Si l’usage de ce produit par voie injectable s’explique pour près de la moitié des injecteurs par une recherche de plaisir et de « défonce » (48 %), 42 % disent y recourir à l’inverse pour une tentative de sevrage volontaire (pour « faire face »), ou, dans une moindre mesure, comme auto-substitution pour « arrêter les drogues » (6 %). ).
). ) précise que le mésusage de la BHD ne se fait pas uniquement, ni même majoritairement, par voie injectable. En effet, les auteurs montrent que si 26 % des sujets suivis en centres de soins en 200511
disent s’être déjà injecté de la BHD, le mésusage, quand il existe, repose le plus souvent sur une utilisation orale12
, le comprimé étant considéré comme facile d’emploi (du fait de sa petite taille et de sa dissolution rapide). Sont surtout rapportées dans ce pays des problématiques d’injection de méthadone : sur 350 patients bénéficiaires de méthadone vus dans ces mêmes centres de soins, les deux tiers (65,9 %) auraient rapporté s’être injecté au moins une fois le produit. Le risque de mésusage de ce traitement était 6 fois plus élevé si les sujets avaient consommé la méthadone avant leur mise sous traitement (primo-usage), ce qui était le cas pour la moitié d’entre eux. Il semble toutefois que ces patients n’aient pas une grande expérience de l’injection et que la régularité de ce mésusage ne concernait donc qu’une faible proportion d’entre eux.
) précise que le mésusage de la BHD ne se fait pas uniquement, ni même majoritairement, par voie injectable. En effet, les auteurs montrent que si 26 % des sujets suivis en centres de soins en 200511
disent s’être déjà injecté de la BHD, le mésusage, quand il existe, repose le plus souvent sur une utilisation orale12
, le comprimé étant considéré comme facile d’emploi (du fait de sa petite taille et de sa dissolution rapide). Sont surtout rapportées dans ce pays des problématiques d’injection de méthadone : sur 350 patients bénéficiaires de méthadone vus dans ces mêmes centres de soins, les deux tiers (65,9 %) auraient rapporté s’être injecté au moins une fois le produit. Le risque de mésusage de ce traitement était 6 fois plus élevé si les sujets avaient consommé la méthadone avant leur mise sous traitement (primo-usage), ce qui était le cas pour la moitié d’entre eux. Il semble toutefois que ces patients n’aient pas une grande expérience de l’injection et que la régularité de ce mésusage ne concernait donc qu’une faible proportion d’entre eux. ; Claroux-Bellocq et coll., 2003
; Claroux-Bellocq et coll., 2003 ; Cadet-Taïrou et Cholley, 2004
; Cadet-Taïrou et Cholley, 2004 ). Ainsi, un indicateur de polyprescription permettant de mesurer les quantités obtenues en excès par des usagers se faisant prescrire des médicaments par plusieurs prescripteurs en même temps (chevauchement d’ordonnances) a été défini (Thirion et coll., 2002
). Ainsi, un indicateur de polyprescription permettant de mesurer les quantités obtenues en excès par des usagers se faisant prescrire des médicaments par plusieurs prescripteurs en même temps (chevauchement d’ordonnances) a été défini (Thirion et coll., 2002 ; Micallef et coll., 2004
; Micallef et coll., 2004 ; Pradel et coll., 2009
; Pradel et coll., 2009 ).
). ). Les deux éditions suivantes14
menées sur des échantillons nationaux représentatifs de patients au cours des années 2006 et 2007 (Canarelli et Coquelin, 2010
). Les deux éditions suivantes14
menées sur des échantillons nationaux représentatifs de patients au cours des années 2006 et 2007 (Canarelli et Coquelin, 2010 ) ont fait apparaître une diminution importante de ces dosages supérieurs à 32 mg/jour qui ne concernaient plus que 2 % de l’ensemble des sujets en 2006 (n=84) puis 1,6 % l’année suivante (n=61). Il s’agit de sujets très majoritairement de sexe masculin (respectivement 84 et 88 %), plus âgés que la moyenne de l’échantillon (36 et 38,6 ans versus 35 ans) et principalement repérés en Île-de-France, PACA et Alsace. Par ailleurs, le nomadisme médical diminue entre 2006 et 2007 puisque le taux de sujets s’adressant à 5 médecins ou plus passe de 10 % à 6 %. La diminution de ces indicateurs de mésusage au niveau national est une conséquence directe de la mise en place depuis 2004 d’un plan de contrôle de l’Assurance maladie auprès des assurés suspects de détournement voire de trafic de BHD, plan renforcé à partir de 2006 (Cnamts, 2004
) ont fait apparaître une diminution importante de ces dosages supérieurs à 32 mg/jour qui ne concernaient plus que 2 % de l’ensemble des sujets en 2006 (n=84) puis 1,6 % l’année suivante (n=61). Il s’agit de sujets très majoritairement de sexe masculin (respectivement 84 et 88 %), plus âgés que la moyenne de l’échantillon (36 et 38,6 ans versus 35 ans) et principalement repérés en Île-de-France, PACA et Alsace. Par ailleurs, le nomadisme médical diminue entre 2006 et 2007 puisque le taux de sujets s’adressant à 5 médecins ou plus passe de 10 % à 6 %. La diminution de ces indicateurs de mésusage au niveau national est une conséquence directe de la mise en place depuis 2004 d’un plan de contrôle de l’Assurance maladie auprès des assurés suspects de détournement voire de trafic de BHD, plan renforcé à partir de 2006 (Cnamts, 2004 ).
). ). Si la voie d’usage la plus utilisée dans cette population est l’injection (56 % des usagers de BHD dans l’enquête ENa-Caarud 2008), les usagers ont également recours à la voie orale (45 %) mais également à la voie sniffée (18 %) et inhalée (4 %). L’acquisition de la BHD se fait le plus souvent par prescription pour 60 % des sujets vus dans l’enquête Prelud, 15 % l’obtenant exclusivement à partir du marché parallèle et un quart des sujets par ces deux biais. Le mode d’acquisition de la BHD est différent dans une population plus insérée : l’enquête Oppidum retrouve que l’acquisition illégale ne concerne que 9 % des patients en protocole thérapeutique versus 97 % des sujets en dehors de tout protocole. Le même constat est fait pour les patients interrogés en médecine de ville (enquête Opema), puisque la grande majorité bénéficie de BHD par le biais d’une prescription régulière (94 %) plutôt que par deal (6 %) (tableau 4.I
). Si la voie d’usage la plus utilisée dans cette population est l’injection (56 % des usagers de BHD dans l’enquête ENa-Caarud 2008), les usagers ont également recours à la voie orale (45 %) mais également à la voie sniffée (18 %) et inhalée (4 %). L’acquisition de la BHD se fait le plus souvent par prescription pour 60 % des sujets vus dans l’enquête Prelud, 15 % l’obtenant exclusivement à partir du marché parallèle et un quart des sujets par ces deux biais. Le mode d’acquisition de la BHD est différent dans une population plus insérée : l’enquête Oppidum retrouve que l’acquisition illégale ne concerne que 9 % des patients en protocole thérapeutique versus 97 % des sujets en dehors de tout protocole. Le même constat est fait pour les patients interrogés en médecine de ville (enquête Opema), puisque la grande majorité bénéficie de BHD par le biais d’une prescription régulière (94 %) plutôt que par deal (6 %) (tableau 4.I ).
). ). L’expansion de ce marché noir de BHD est sous-tendue par plusieurs phénomènes : la demande soutenue du produit par une population très marginalisée comme celle des migrants n’ayant pas ou ne souhaitant pas avoir accès au système de soins (ORS PACA, 2009
). L’expansion de ce marché noir de BHD est sous-tendue par plusieurs phénomènes : la demande soutenue du produit par une population très marginalisée comme celle des migrants n’ayant pas ou ne souhaitant pas avoir accès au système de soins (ORS PACA, 2009 ; Costes, 2010
; Costes, 2010 ) ; l’insatisfaction de certains concernant leurs dosages les conduisant à compléter leur traitement par un achat dans la rue où l’offre est abondante ; le trafic à destination de pays où la BHD est moins disponible. Ce trafic fonctionne à l’heure actuelle toujours selon deux modalités : une activité diffuse de « petite revente » par des patients traités s’assurant un petit revenu – ou l’achat d’autres substances par ce biais – et une autre activité de « recueil » et de revente par un nombre réduit de personnes non nécessairement traitées mais envoyées en tant que « mules »16
. La facilité de prescription auprès de certains médecins, voire la délivrance d’ordonnances de « complaisance », permet également d’alimenter le trafic (ORS PACA, 2009
) ; l’insatisfaction de certains concernant leurs dosages les conduisant à compléter leur traitement par un achat dans la rue où l’offre est abondante ; le trafic à destination de pays où la BHD est moins disponible. Ce trafic fonctionne à l’heure actuelle toujours selon deux modalités : une activité diffuse de « petite revente » par des patients traités s’assurant un petit revenu – ou l’achat d’autres substances par ce biais – et une autre activité de « recueil » et de revente par un nombre réduit de personnes non nécessairement traitées mais envoyées en tant que « mules »16
. La facilité de prescription auprès de certains médecins, voire la délivrance d’ordonnances de « complaisance », permet également d’alimenter le trafic (ORS PACA, 2009 ; Costes, 2010
; Costes, 2010 ). Le plan de contrôle de l’Assurance maladie, lancé dès l’année 2004, en menant diverses actions auprès des professionnels de santé et/ou des patients a toutefois permis – même s’il n’a pas été décliné de manière aussi homogène selon les départements – de diminuer fortement ce phénomène au regard des prévalences de détournement actuellement constatées. Les patients stabilisés et les moins précaires, notamment, ont ainsi rejoint le cadre thérapeutique. Cependant, on constate que la BHD est toujours considérée comme étant très disponible sur le marché noir (Cadet-Taïrou et coll., 2010a
). Le plan de contrôle de l’Assurance maladie, lancé dès l’année 2004, en menant diverses actions auprès des professionnels de santé et/ou des patients a toutefois permis – même s’il n’a pas été décliné de manière aussi homogène selon les départements – de diminuer fortement ce phénomène au regard des prévalences de détournement actuellement constatées. Les patients stabilisés et les moins précaires, notamment, ont ainsi rejoint le cadre thérapeutique. Cependant, on constate que la BHD est toujours considérée comme étant très disponible sur le marché noir (Cadet-Taïrou et coll., 2010a ), même si cette situation est probablement en partie due à une diminution conjoncturelle de la demande, elle-même liée à l’accroissement depuis 2006 environ de la disponibilité de l’héroïne en France.
), même si cette situation est probablement en partie due à une diminution conjoncturelle de la demande, elle-même liée à l’accroissement depuis 2006 environ de la disponibilité de l’héroïne en France. ). Des observations récentes font également état d’une tendance chez certains usagers de drogues à recourir à la méthadone en auto-substitution, en amont de toute prise en charge. L’auto-substitution peut être liée à la gestion de manque ponctuel d’héroïne pour certains usagers ou s’inscrire dans une démarche durable (chez des usagers refusant de s’intégrer dans un protocole de substitution qu’ils jugent long et fastidieux ou par choix, pour les plus insérés, de ne pas mettre leur image sociale en danger en fréquentant un centre spécialisé) (Cadet-Taïrou et coll., 2010
). Des observations récentes font également état d’une tendance chez certains usagers de drogues à recourir à la méthadone en auto-substitution, en amont de toute prise en charge. L’auto-substitution peut être liée à la gestion de manque ponctuel d’héroïne pour certains usagers ou s’inscrire dans une démarche durable (chez des usagers refusant de s’intégrer dans un protocole de substitution qu’ils jugent long et fastidieux ou par choix, pour les plus insérés, de ne pas mettre leur image sociale en danger en fréquentant un centre spécialisé) (Cadet-Taïrou et coll., 2010
 ).
). ) avait montré que près de 10 % d’entre eux avaient déclaré obtenir des médicaments psychotropes via le marché noir. Si le clonazépam (Rivotril®) arrivait en tête des médicaments illégalement obtenus (pour 42,6 % des sujets), les MSO arrivaient en deuxième position : 30,6 % s’étaient procuré de la BHD (dose moyenne de 13,7 mg/jour) et 21 % de la méthadone (dose moyenne de 54,6 mg/jour). Un peu moins d’un sujet sur cinq (18 %) s’était procuré des sulfates de morphine.
) avait montré que près de 10 % d’entre eux avaient déclaré obtenir des médicaments psychotropes via le marché noir. Si le clonazépam (Rivotril®) arrivait en tête des médicaments illégalement obtenus (pour 42,6 % des sujets), les MSO arrivaient en deuxième position : 30,6 % s’étaient procuré de la BHD (dose moyenne de 13,7 mg/jour) et 21 % de la méthadone (dose moyenne de 54,6 mg/jour). Un peu moins d’un sujet sur cinq (18 %) s’était procuré des sulfates de morphine. ; Laqueille et coll., 2009
; Laqueille et coll., 2009 ). Dans différents pays, 50 à 90 % des patients bénéficiant de MSO et suivis en ambulatoire recevraient une prescription de médicaments psychotropes tout comme jusqu’à 50 % des patients pris en charge en structures de soins, même si les recommandations nationales, quand elles existent, tentent de décourager ces types d’associations du fait des risques de complications en termes de morbidité mais aussi de mortalité (Backmund et coll., 2005
). Dans différents pays, 50 à 90 % des patients bénéficiant de MSO et suivis en ambulatoire recevraient une prescription de médicaments psychotropes tout comme jusqu’à 50 % des patients pris en charge en structures de soins, même si les recommandations nationales, quand elles existent, tentent de décourager ces types d’associations du fait des risques de complications en termes de morbidité mais aussi de mortalité (Backmund et coll., 2005 ; Fatséas et coll., 2009
; Fatséas et coll., 2009 ). Tout usage associé de ces médicaments n’est pas synonyme de recherche de « défonce », même si certaines benzodiazépines sont connues pour être détournées et abusées, comme c’est le cas du flunitrazépam (Rohypnol®) , dont la prescription est pourtant encadrée depuis 2001 du fait des mésusages dont il a fait l’objet, mais qui est encore détourné chez des sujets socialement très marginalisés. Le clonazépam (Rivotril®) est également détourné, mais de manière plus limitée en raison d’un effet « défonce » moins marqué.
). Tout usage associé de ces médicaments n’est pas synonyme de recherche de « défonce », même si certaines benzodiazépines sont connues pour être détournées et abusées, comme c’est le cas du flunitrazépam (Rohypnol®) , dont la prescription est pourtant encadrée depuis 2001 du fait des mésusages dont il a fait l’objet, mais qui est encore détourné chez des sujets socialement très marginalisés. Le clonazépam (Rivotril®) est également détourné, mais de manière plus limitée en raison d’un effet « défonce » moins marqué. ), menée en région Aquitaine, a tenté de mettre à jour les motivations de recours aux benzodiazépines chez des sujets traités, en ville ou en structure de soins, par BHD ou méthadone depuis au moins un mois. La majorité des sujets interrogés (53 %) a rapporté une consommation « mixte », à la fois à visée thérapeutique et à visée hédonique, voire de « défonce », un tiers des sujets utilisant ces molécules uniquement à visée thérapeutique, et 15 % dans une optique uniquement hédonique. Ceux ayant recours à ces molécules à des fins exclusivement thérapeutiques les obtenaient plus souvent par prescription médicale que ceux les utilisant à visée de défonce (p<10-3). Le premier objectif était d’obtenir un effet anxiolytique (p<10-2), tout en recourant plus fréquemment à la voie d’administration adaptée (voie orale, p<10-4). Les molécules identifiées étaient principalement celles habituellement prescrites en population générale (bromazépam et oxazépam en particulier). À l’inverse, les sujets recourant aux médicaments à visée hédonique ou de « défonce » seule avaient davantage recours à la polyconsommation de produits, obtenaient les benzodiazépines, en particulier le flunitrazépam (Rohypnol®), sur le marché noir et utilisaient des voies d’administration non-conformes (intraveineuse ou nasale notamment).
), menée en région Aquitaine, a tenté de mettre à jour les motivations de recours aux benzodiazépines chez des sujets traités, en ville ou en structure de soins, par BHD ou méthadone depuis au moins un mois. La majorité des sujets interrogés (53 %) a rapporté une consommation « mixte », à la fois à visée thérapeutique et à visée hédonique, voire de « défonce », un tiers des sujets utilisant ces molécules uniquement à visée thérapeutique, et 15 % dans une optique uniquement hédonique. Ceux ayant recours à ces molécules à des fins exclusivement thérapeutiques les obtenaient plus souvent par prescription médicale que ceux les utilisant à visée de défonce (p<10-3). Le premier objectif était d’obtenir un effet anxiolytique (p<10-2), tout en recourant plus fréquemment à la voie d’administration adaptée (voie orale, p<10-4). Les molécules identifiées étaient principalement celles habituellement prescrites en population générale (bromazépam et oxazépam en particulier). À l’inverse, les sujets recourant aux médicaments à visée hédonique ou de « défonce » seule avaient davantage recours à la polyconsommation de produits, obtenaient les benzodiazépines, en particulier le flunitrazépam (Rohypnol®), sur le marché noir et utilisaient des voies d’administration non-conformes (intraveineuse ou nasale notamment). ) s’est intéressée aux facteurs qui sous-tendraient une plus grande consommation de benzodiazépines chez les patients bénéficiant de MSO que chez les sujets consommateurs d’héroïne sans prise en charge thérapeutique. Sur 1 049 sujets interrogés et ayant pris de manière quotidienne soit de la méthadone, soit de la codéine ou encore de l’héroïne, un peu moins de la moitié de l’ensemble de ces sujets pris en charge (44 %) avaient ainsi consommé des benzodiazépines quotidiennement, et parmi eux, 20 % prenaient des doses élevées de benzodiazépines (60 mg/jour de Valium®, c’est-à-dire de diazépam, ou d’une molécule équivalente). De plus, au sein des 3 groupes, les prévalences de consommation de benzodiazépines les plus élevées se trouvaient chez les sujets bénéficiant d’un des deux traitements (méthadone ou codéine) plutôt que parmi ceux s’injectant de l’héroïne. Selon cette étude, le recours aux benzodiazépines serait d’autant plus fréquent que les sujets seraient de sexe masculin, plus dépendants aux opiacés et avec un parcours de consommation plus long, et qu’ils seraient davantage polyconsommateurs (alcool et barbituriques en particulier). Les auteurs suggèrent également que ce recours « complémentaire » aux benzodiazépines pourrait également s’expliquer en partie par la recherche d’un plaisir que ne procureraient pas les seuls traitements.
) s’est intéressée aux facteurs qui sous-tendraient une plus grande consommation de benzodiazépines chez les patients bénéficiant de MSO que chez les sujets consommateurs d’héroïne sans prise en charge thérapeutique. Sur 1 049 sujets interrogés et ayant pris de manière quotidienne soit de la méthadone, soit de la codéine ou encore de l’héroïne, un peu moins de la moitié de l’ensemble de ces sujets pris en charge (44 %) avaient ainsi consommé des benzodiazépines quotidiennement, et parmi eux, 20 % prenaient des doses élevées de benzodiazépines (60 mg/jour de Valium®, c’est-à-dire de diazépam, ou d’une molécule équivalente). De plus, au sein des 3 groupes, les prévalences de consommation de benzodiazépines les plus élevées se trouvaient chez les sujets bénéficiant d’un des deux traitements (méthadone ou codéine) plutôt que parmi ceux s’injectant de l’héroïne. Selon cette étude, le recours aux benzodiazépines serait d’autant plus fréquent que les sujets seraient de sexe masculin, plus dépendants aux opiacés et avec un parcours de consommation plus long, et qu’ils seraient davantage polyconsommateurs (alcool et barbituriques en particulier). Les auteurs suggèrent également que ce recours « complémentaire » aux benzodiazépines pourrait également s’expliquer en partie par la recherche d’un plaisir que ne procureraient pas les seuls traitements. ) (tableau 4.II
) (tableau 4.II ). D’autres médicaments, qu’ils soient suspects de mésusage comme le trihexyphénidyle ou Artane® (antiparkinsonien de synthèse consommé pour ses effets psychotropes), marqueur indirect d’une injection potentielle comme l’acide flucidique ou Fucidine® (antibiotique local fréquemment utilisé en cas d’abcès cutanés et donc marqueur possible d’une utilisation intraveineuse) voire suspects de trafic plus organisé comme le Cytotec®18
ont également été analysés dans ce travail. L’intérêt était également de comparer le recours à ces molécules en termes de prévalence au sein de différents groupes de patients (échantillon global, patients bénéficiaires de la CMU et, pour la BHD, patients bénéficiant d’une DQM>32 mg/jour). Même s’il n’est pas possible de déterminer dans ce travail si ces prescriptions ont été effectuées sur la même ordonnance que les MSO, l’étude de consommations associées est informative.
). D’autres médicaments, qu’ils soient suspects de mésusage comme le trihexyphénidyle ou Artane® (antiparkinsonien de synthèse consommé pour ses effets psychotropes), marqueur indirect d’une injection potentielle comme l’acide flucidique ou Fucidine® (antibiotique local fréquemment utilisé en cas d’abcès cutanés et donc marqueur possible d’une utilisation intraveineuse) voire suspects de trafic plus organisé comme le Cytotec®18
ont également été analysés dans ce travail. L’intérêt était également de comparer le recours à ces molécules en termes de prévalence au sein de différents groupes de patients (échantillon global, patients bénéficiaires de la CMU et, pour la BHD, patients bénéficiant d’une DQM>32 mg/jour). Même s’il n’est pas possible de déterminer dans ce travail si ces prescriptions ont été effectuées sur la même ordonnance que les MSO, l’étude de consommations associées est informative. ).
). ) retrouvait, parmi les sujets injecteurs de BHD, une polyconsommation importante et une prescription préférentielle de flunitrazépam (Rohypnol®) (1/3 des sujets) suivi par le bromazépam (Lexomil®) (9 %) et le clorazépate (Tranxène®) (6 %). Une autre étude française menée entre 2001 et 2004 (Lavie et coll., 2009
) retrouvait, parmi les sujets injecteurs de BHD, une polyconsommation importante et une prescription préférentielle de flunitrazépam (Rohypnol®) (1/3 des sujets) suivi par le bromazépam (Lexomil®) (9 %) et le clorazépate (Tranxène®) (6 %). Une autre étude française menée entre 2001 et 2004 (Lavie et coll., 2009 ) auprès de 170 patients recevant un traitement par BHD depuis au moins 3 mois et recrutés par leur médecin prescripteur, a montré que si les deux tiers des individus (67 %) rapportaient avoir consommé des benzodiazépines au cours de leur vie, 15 % en avaient fait un usage simple19
au cours des 30 derniers jours et 30,6 % un usage problématique sur la même période (dont 6,5 % de cas d’abus et 24,1 % de dépendance à ces molécules). Si l’usage simple de benzodiazépines était associé à un dosage faible de BHD (<4 mg/jour, p=0,01), l’usage problématique était associé avec différents facteurs de précarité (logement non stable et absence d’insertion professionnelle) et de comorbidité (symptômes anxieux et dépressifs). Étaient également observées plus fréquemment des co-consommations (alcool en particulier) et avec un dosage moyen de BHD plus élevé (>10 mg/jour).
) auprès de 170 patients recevant un traitement par BHD depuis au moins 3 mois et recrutés par leur médecin prescripteur, a montré que si les deux tiers des individus (67 %) rapportaient avoir consommé des benzodiazépines au cours de leur vie, 15 % en avaient fait un usage simple19
au cours des 30 derniers jours et 30,6 % un usage problématique sur la même période (dont 6,5 % de cas d’abus et 24,1 % de dépendance à ces molécules). Si l’usage simple de benzodiazépines était associé à un dosage faible de BHD (<4 mg/jour, p=0,01), l’usage problématique était associé avec différents facteurs de précarité (logement non stable et absence d’insertion professionnelle) et de comorbidité (symptômes anxieux et dépressifs). Étaient également observées plus fréquemment des co-consommations (alcool en particulier) et avec un dosage moyen de BHD plus élevé (>10 mg/jour).