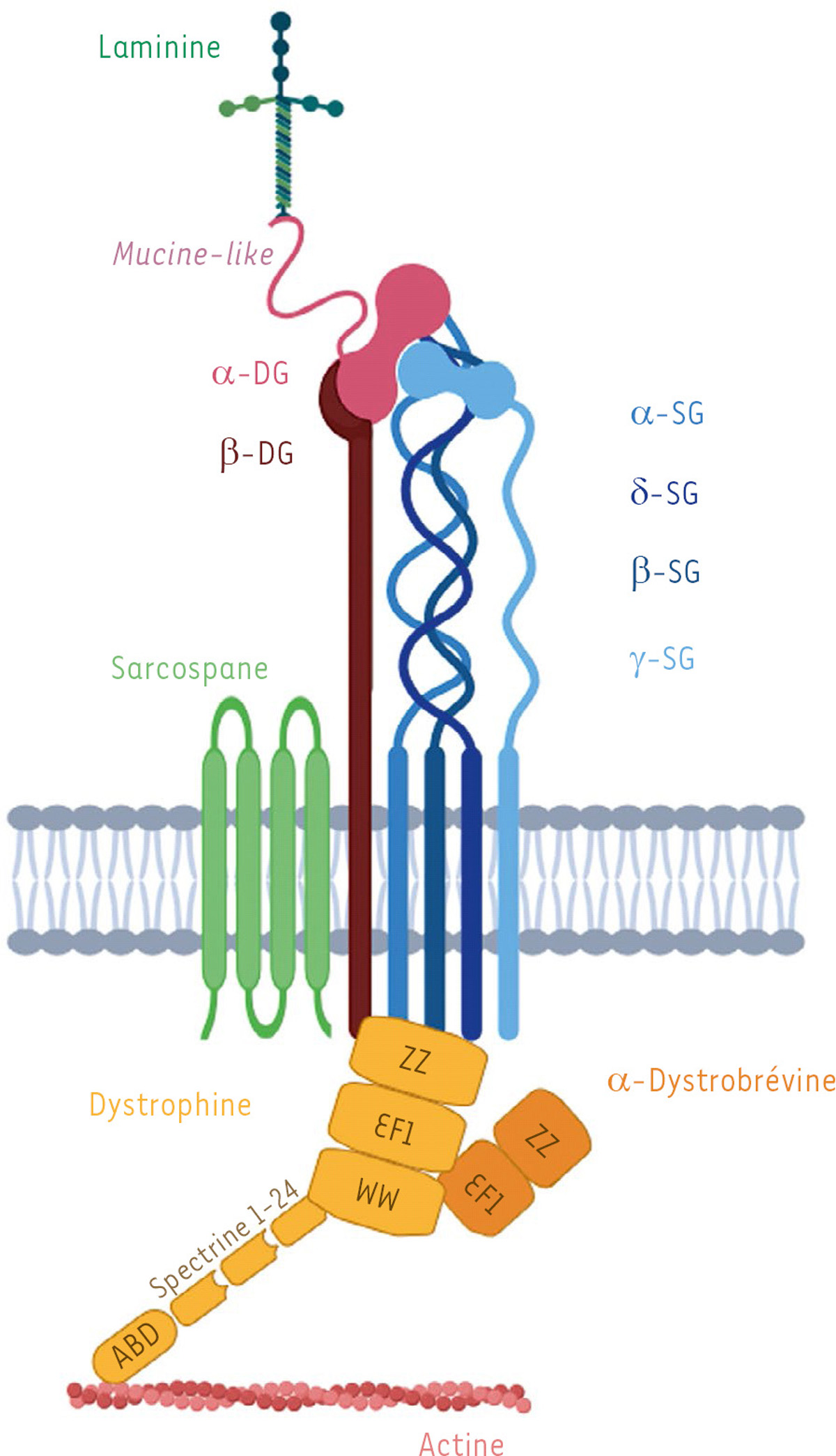
Le DGC comprend 10 protéines localisées au sarcolemme : la dystrophine, deux dystroglycanes (α-DG et β-DG), quatre sarcoglycanes (α-SG, β-SG, γ-SG et δ-SG), le sarcospane, l’α-dystrobrévine et les syntrophines. Il est organisé autour du sarcolemme dans trois régions : la région extracellulaire (α-DG), la région transmembranaire (β-DG, SGs, sarcospane) et la région intracellulaire ou cytoplasmique (dystrophine, α-dystrobrévine, syntrophines).
Dans la région extracellulaire, l’α-DG peut lier les éléments de la matrice extracellulaire par une région flexible, ses domaines mucine-like, dont l’importante glycosylation permet la liaison à la laminine 211. L’α-DG est fortement liée à la β-DG qui est une protéine transmembranaire et qui lie la dystrophine du côté intracellulaire.
Au niveau transmembranaire, outre la β-DG, les quatre SG qui ont de longs prolongements extracellulaires et un domaine transmembranaire, sont étroitement associés entre eux. Le sarcospane, avec quatre domaines transmembranaires, est également associé avec les SG dans la membrane.
Dans le cytoplasme, la dystrophine maintient sa localisation sous-sarcolemmale par sa liaison à la β-DG. De l’autre côté, au niveau N terminal, la dystrophine lie l’actine filamentaire. Ainsi, le DGC permet la connexion entre matrice extracellulaire et réseau de filaments d’actine. Enfin, l’α-dystrobrévine interagit avec la dystrophine sous le sarcolemme, et les syntrophines servent d’adaptateurs pour l’association entre la dystrophine et des protéines de signalisation comme la
nitric oxide synthase
neuronale (nNOS) ou la cavéoline-3.
Au niveau pathologique, l’importance du DGC est connue au travers des mutations de ses composants qui ont été identifiées comme causes primaires de plusieurs types de dystrophies musculaires. Dans la région extracellulaire, des anomalies de l’α-DG perturbent ses interactions avec la matrice extracellulaire, conduisant à certaines formes de dystrophies musculaires des ceintures (LGMD pour
limb-girdle muscular dystrophy
) et de dystrophies musculaires congénitales. Les mutations affectant le β-DG entraînent des dystroglycanopathies, caractérisées par une dégénérescence musculaire et des anomalies morphologiques du cerveau et des yeux. Au niveau transmembranaire, les mutations dans les SG γ, α, β et δ conduisent aux LGMD de types R5, R3, R4, R6 (respectivement ex LGMD 2C, 2D, 2E et 2F). Les mutations affectant le sarcospane ont montré chez la souris un phénotype musculaire moins sévère, mais qui s’accroit avec l’âge. Dans la région cytoplasmique, toujours chez la souris, le déficit en α-dystrobrévine induit des myopathies squelettiques et cardiaques, des anomalies des jonctions neuromusculaires et myotendineuses, bien que le reste du DGC apparaît intact. Enfin, les mutations du gène de la dystrophine entraînent des dystrophinopathies, la dystrophie musculaire de Duchenne (DMD) et la dystrophie musculaire de Becker (BMD pour
Becker muscular dystrophy
).