| |
| Med Sci (Paris). 41(8-9): 693–700. doi: 10.1051/medsci/2025109.Nouvelles pistes thérapeutiques pour le traitement de la cholangite biliaire primitive Corentin Brice1* and Alexandre Louvet1** 1Service des maladies de l’appareil digestif. Centre de compétence Maladies rares « Maladies inflammatoires des voies biliaires et hépatites autoimmunes », Hôpital Huriez
,
Lille
,
France |
Vignette (© Inserm).
La cholangite biliaire primitive (CBP) est une maladie cholestatique
1
auto-immune qui se caractérise par la destruction des canaux biliaires de petite taille liée à l’infiltration lymphocytaire. La physiopathologie de cette maladie auto-immune fait intervenir des facteurs génétiques et environnementaux (tabac, microbiote intestinal) [
1
,
2
] (
Figure 1
).
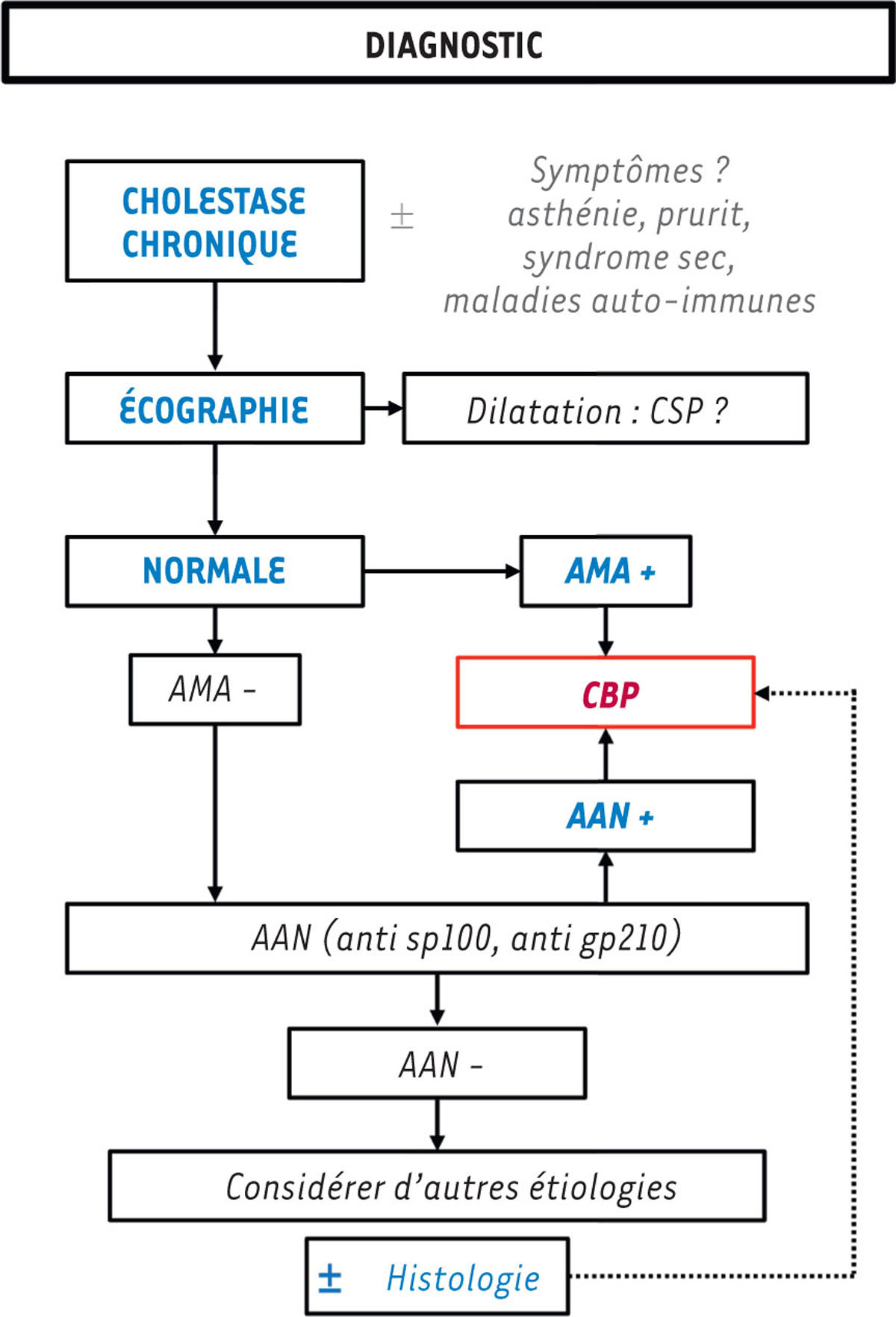
 | Figure 1.
Diagnostic de la cholangite biliaire primitive
.
AAN : anticorps antinucléaires ; AMA : anticorps anti-mitochondries ; CSP : cholangite sclérosante primitive.
|
|
Les études les plus anciennes faisaient état d’un sex-ratio de 9 femmes pour 1 homme et d’un âge médian de 55 ans au moment du diagnostic, la prévalence de la CBP chez la femme de plus de 40 ans s’établissant à 1/1 000 [
3
]. Nous n’avons pour l’heure pas d’explication claire à cette surreprésentation féminine bien que l’impact des œstrogènes, l’utilisation de cosmétiques ou le rôle d’un facteur de transcription codé par le chromosome X soient suspectés. Des études plus récentes retrouvent cependant un sex-ratio moins important, de 4 femmes pour 1 homme, et révèlent le facteur pronostique péjoratif que constitue le sexe masculin [
4
]. Il n’existe pas de forme pédiatrique, en dehors de rares cas rapportés de CBP dès l’âge de 15 ans [
5
].
|
Présentation clinico-biologique
La présentation clinico-biologique au diagnostic est variable. La CBP doit donc être suspectée devant l’association inconstante (50 % au diagnostic) de symptômes tels que le prurit et l’asthénie à une cholestase chronique évoluant depuis plus de 6 mois, plus ou moins associée à une ascension de la bilirubine ou à une cytolyse modérée [
1
]. Le bilan biologique peut également montrer une élévation des IgM et un déficit en vitamines liposolubles (notamment la vitamine D) ainsi qu’une hypercholestérolémie. La CBP peut être découverte chez des patients asymptomatiques ou au stade de cirrhose compensée ou décompensée.
Il faut enfin rechercher l’association à d’autres maladies auto-immunes (syndrome de Gougerot-Sjögren, dysthyroï die auto-immune, sclé rodermie, polyarthrite rhumatoï de, lupus et maladie cœliaque). Parmi ces dernières, les pathologies thyroïdiennes sont les plus fréquentes (en particulier l’hypothyroïdie). |
Le diagnostic de CBP est désormais défini par l’association d’une cholestase chronique avec une positivité des anticorps spécifiques sans nécessité d’une preuve histologique [
1
] (
Figure 2
).
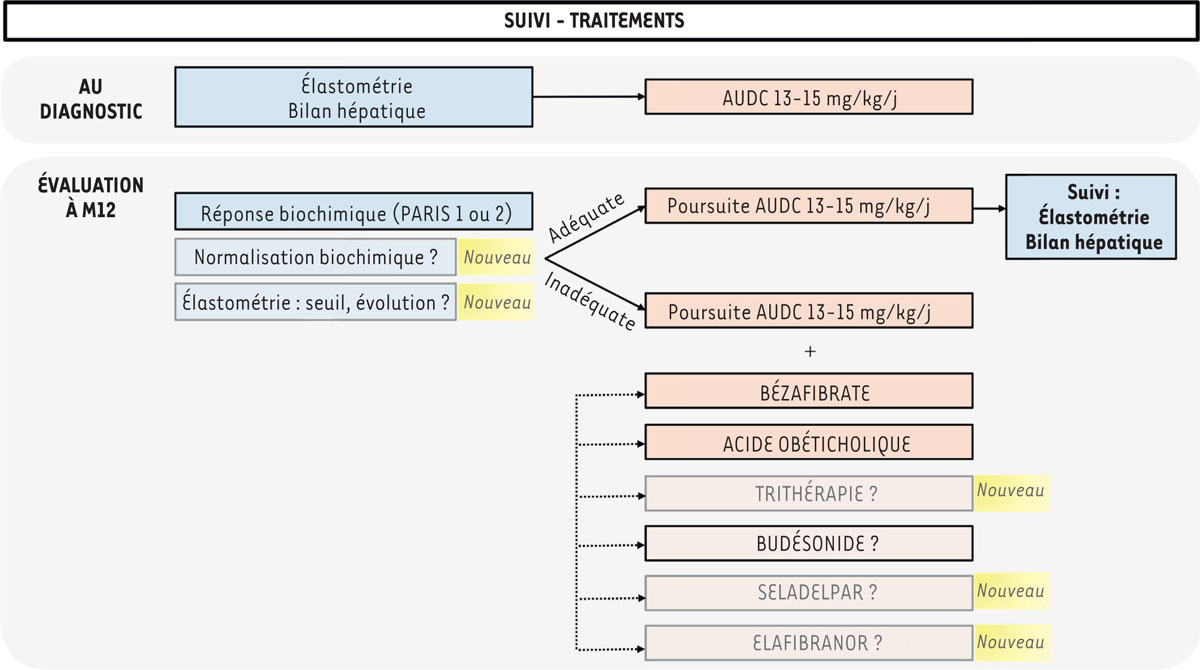
 | Figure 2.
Nouveautés thérapeutiques dans la cholangite biliaire primitive
.
AUDC : acide ursodésoxycholique.
|
On recherchera donc en première intention une positivité (titre minimal de 1/40) des anticorps anti-mitochondries de spécificité M2 qui reste l’examen clef avec une sensibilité de 90 % et une spécificité de 97 % bien qu’il faille rester prudent en cas d’insuffisance hépatique aiguë où la spécificité est alors plus faible [
1
,
6
]. En cas de négativité des anticorps anti-mitochondries, on complète le diagnostic par le dosage des anticorps antinucléaires, anti-gp210 et anti-Sp100, qui ont une spécificité > 95 % pour la CBP.
L’histologie n’est donc pas indispensable au diagnostic et sera proposée dans les rares cas de CBP séronégatives (10 %) et en cas de suspicion de syndrome de chevauchement, c’est-à-dire l’association à une hépatopathie auto-immune qui sera évoquée lorsqu’à la cholestase biologique est associée une cytolyse importante (transaminases supérieures à 5 fois la normale supérieure), ou une augmentation des immunoglobulines G (IgG).
Dans la situation de positivité isolée des anticorps anti-mitochondries sans cholestase, il est recommandé de réaliser un simple bilan hépatique annuel car seulement 1 patient sur 6 développera une CBP après 5 ans [
1
,
7
].
Bilan au diagnostic
Il est nécessaire de réaliser une échographie abdominale afin de rechercher une cause intra ou extra-hépatique à la cholestase. Une élastométrie (par exemple par Fibroscan®), qui mesure l’élasticité du foie en kilopascals (kPa) afin d’évaluer le degré de fibrose du foie, doit être réalisée chez tout patient et permettra de différencier une CBP débutante d’une CBP avec fibrose avancée. Une étude française publiée en 2022 identifie des patients à risque faible, modéré ou élevé en utilisant les seuils de 8 et 15 kPa qui correspondent à une fibrose significative et à une cirrhose, respectivement. Les patients à risque modéré (8 à 15 kPa) et élevé (> 15 kPa), représentant 40 % de la cohorte, présentent respectivement 4 fois et 16 fois plus d’évènements cliniques que le groupe à risque faible (< 8 kPa). Les évènements cliniques sont définis par le décès, la transplantation hépatique ou l’inscription sur liste d’attente de transplantation et les complications de cirrhose (rupture de varice, ascite, encéphalopathie hépatique, carcinome hépatocellulaire) [
8
].
Le suivi de la CBP devra comporter des mesures d’élastométrie de contrôle. En effet, l’évolution de l’élasticité hépatique est un marqueur pronostique utilisable dans la CBP comme démontré dans une étude multicentrique rétrospective menée chez 3 078 patients traités par de l’acide ursodésoxycholique (AUDC), suivis par élastométrie entre 2003 et 2022 et publiée en décembre 2024. Après ajustement (notamment sur l’élastométrie à l’inclusion), toute variation relative de l’élastométrie est associée à la survenue d’évènements cliniques graves (complications de cirrhose, transplantation hépatique ou décès). À titre d’exemple, une variation annuelle de 20 % de l’élastométrie est associée à un HR
2
de 2,13 (1,89-2,45) en cas d’augmentation, et à un HR de 0,40 (0,33-0,46) en cas de diminution [
9
].
|
De nombreux facteurs de mauvais pronostic ont été identifiés. Les deux plus importants sont l’âge jeune au diagnostic (< 45 ans) et la présence d’une CBP avancée au diagnostic [
10
]. On peut également citer le sexe masculin, les marqueurs biologiques de CBP avancés (hyperbilirubinémie, hypoalbuminémie), la positivité des anticorps antinucléaires spécifiques ou la présence d’une fibrose ou d’une ductopénie (raréfaction des canaux biliaires) en histologie [
10
–
14
].
Des scores pronostiques existent, principalement utiles pour stratifier le pronostic des patients dans les études à large échelle, mais restent peu utilisés en pratique clinique quotidienne. Les plus utilisés sont le score GLOBE, constitué à partir d’une cohorte internationale de près de 4 000 patients et le score UK-PBC constitué à partir d’une cohorte britannique de plus de 7 000 patients, tous traités par AUDC, qui prennent notamment en compte le sexe, l’âge, le taux d’anticorps anti-mitochondries et l’évolution du bilan biochimique.
Enfin, dans la CBP, le pronostic de la maladie repose avant tout sur la réponse au traitement médical. En effet, en l’absence de traitement, la survie sans transplantation à 10 ans est de 60 % contre 80 % chez les patients qui reçoivent un traitement médical [
15
,
16
]. La réponse au traitement est donc l’objectif à atteindre dans le suivi des patients atteints de CBP. Celle-ci est principalement évaluée par la réponse biologique. Il en existe de nombreuses définitions qualitatives ou quantitatives [
1
,
11
,
17
]. Les définitions les plus utilisées en France sont celles de Paris-1 et 2 évaluant la réponse biologique à 1 an de traitement et déterminant des seuils définissant l’échec thérapeutique
3
. Ainsi, en accord avec ces définitions, les traitements de seconde de ligne ne sont couramment proposés que pour des taux de PAL > 1,5 LSN après 12 mois de traitement par AUDC.
Cependant, plusieurs études ont récemment remis en question ce seuil avec l’évaluation d’objectifs plus ambitieux tels que la normalisation des taux de bilirubine ou de phosphatases alcalines sanguines. Ainsi, une étude rétrospective publiée en 2024 menée sur plus de 1 000 patients, a montré qu’obtenir la normalisation des phosphatases alcalines sanguines est associée à un gain de survie sans complication à 10 ans. Cela se vérifie d’autant plus dans le sous-groupe de patients ayant une élastométrie supérieure ou égale à 10 kPa et/ou un âge inférieur ou égal à 62 ans, avec un gain de survie sans complication à 10 ans de 52,8 mois [
18
,
19
]. La mise à disposition des nouveaux traitements (cf.
infra
) va permettre de tendre plus souvent et plus facilement vers ces objectifs de normalisation complète du bilan biologique hépatique.
|
L’acide ursodésoxycholique
L’acide ursodéxoxycholique (AUDC) est un acide biliaire naturel dont le mode d’action repose sur divers mécanismes. Il rend la bile plus hydrophile, augmente le flux biliaire notamment
via
l’activation de l’expression du transporteur des phospholipides vers la bile ABCB4
(ATP-binding cassette subfamily B member 4
)
4
, a un effet anti-apoptotique et entre en compétition avec la réabsorption iléale des acides biliaires endogènes [
20
]. L’AUDC permet une amélioration histologique et un gain de survie sans transplantation [
21
–
24
] et doit être introduit dès le diagnostic quel que soit le degré de fibrose. La tolérance du traitement est bonne, le principal effet indésirable étant la diarrhée. Cependant, d’après le score GLOBE, 40 % des patients sous AUDC ont une survie sans transplantation plus courte que des individus sains et comparables [
25
].
En cas d’absence de réponse à l’AUDC, il faut en premier lieu rechercher un défaut d’observance, une association à une hépatite auto-immune ou à d’autres maladies auto-immunes pouvant être à l’origine de perturbation des tests hépatiques (maladie cœliaque, hyperthyroïdie, hypothyroïdie). Ensuite, l’absence de réponse, au vu du pronostic défavorable qui y est associé doit faire proposer l’incrémentation des thérapeutiques. L’acide obéticholique
L’acide obéticholique est un acide biliaire qui agit comme agoniste du récepteur FXR
5
(
farnesoid-X receptor)
avec des propriétés anti-cholestatiques et anti-fibrosantes. Son efficacité sur les paramètres biologiques est bien établie depuis l’étude contrôlée randomisée en double aveugle POISE qui compare après stratification, selon la poursuite d’un traitement par AUDC et selon les critères de Paris-1, l’efficacité d’un traitement par acide obéticholique à un placebo, chez des patients avec intolérance ou inefficacité de l’AUDC. Le taux d’efficacité biochimique évalué à 12 mois est significativement différent chez les patients traités par acide obéticholique [
26
,
27
] (
Tableau I
).
Tableau I.
| Traitement |
Étude |
Objectif principal |
Groupes |
Résultats |
|
Acide obéticholique
|
POISE |
PAL < 1,67 LSN associées à une réduction de 15 % par rapport à la valeur initiale et à une bilirubine ≤ LSN Évaluation à 12 mois |
Placebo (n = 73)
Acide obéticholique 5 mg majoré à 10 mg à 6 mois selon tolérance (n = 71)
Acide obéticholique 10 mg (n = 73)
|
10 % 46 % 47 %
(p
<
0,001 pour les groupes OCA VS placebo)
|
|
|
Bézafibrate
|
BEZURSO |
Normalisation des paramètres biochimiques (PAL, ASAT, ALAT, bilirubine, albumine, TP) Évaluation à 24 mois |
Placebo (n = 50) Bézafibrate 400 mg/j (n = 50) |
0 % 31 %
Différence
31 % (IC 95 %, 10 à 50 ;
P
<0,001)
|
|
|
Elafibranor
|
ELATIVE |
PAL < 1,67 LSN associées à une réduction de 15 % par rapport à la valeur initiale et à une bilirubine ≤ LSN Évaluation à 52 semaines |
Placebo (n = 53) Elafibranor 80 mg (n = 108) |
4 % 51 %
Différence
47 % (
IC
95 %, 32 à 57 ;
P
<0,001)
|
|
|
Séladelpar
|
RESPONSE |
Identique à l’étude ELAFIBRANOR |
Placebo (n = 65) Seladelpar 10 mg (n = 128) |
20 % 61,7 %
Différence
41,7 % (
IC
95 %, 27,7 à 53,4;
P
<0,001)
|
Les nouveaux traitements dans la cholangite biliaire primitive
.
|
Une amélioration de la survie sans transplantation des patients de l’étude POISE comparée à des patients contrôles des registres GLOBAL-PBC et UK-PBC a par la suite été démontrée [
28
].
Le principal effet indésirable du traitement est la majoration du prurit pouvant conduire à l’arrêt du traitement dans 10 à 25 % des cas [
26
,
27
].
Malgré ces premiers résultats encourageants, l’étude multicentrique randomisée contrôlée COBALT n’a pas permis de confirmer le bénéfice clinique du traitement faute d’avoir pu être menée à son terme ; d’autres études ont démontré un risque accru de décompensation de maladie hépatique sous traitement chez les patients présentant une cirrhose avancée (score de Child-Pugh B) [
29
]. Actuellement, ce médicament dispose toujours d’une autorisation de mise sur le marché dans cette indication mais la molécule reste peu utilisée en raison de discussions en cours sur son remboursement (actuellement seulement disponible dans le cadre d’une demande d’accès compassionnel).
Les fibrates
Les fibrates, utilisés comme hypolipémiants depuis les années 1960, sont des agonistes des récepteurs nucléaires PPAR (
peroxisome proliferator-activated receptors
). Les PPAR sont des facteurs de transcription dont on connaît 3 isoformes : α, γ et δ. Tous les fibrates sont des agonistes majoritaires de PPAR-α, et agissent donc sur le catabolisme des acides gras et la synthèse des acides biliaires. Le bézafibrate possède également une affinité pour les isoformes γ et δ avec pour conséquence un effet anti-inflammatoire.
L’efficacité biologique du bézafibrate a été démontrée par l’essai BEZURSO. Cet essai contrôlé randomisé sur 100 patients poursuivant un traitement par AUDC avec absence de réponse biochimique selon les critères de Paris-2 auquel est adjoint un placebo ou du bézafibrate à la posologie de 400 mg/j (à libération prolongée), a démontré une normalisation des paramètres biochimiques chez 31 % des patients du groupe bézafibrate contre aucun patient du groupe placebo. Bien que le critère de jugement principal soit atteint (normalisation biologique complète deux ans après le début du traitement), le relatif manque de puissance de cette étude n’a pas permis de démontrer l’efficacité du traitement sur la réduction des événements hépatiques cliniques [
30
,
31
] (
Tableau I
).
Avant l’essai BEZURSO, les fibrates (principalement bézafibrate et fénofibrate) avaient été utilisés de longue date par les investigateurs japonais. À titre d’exemple, une étude rétrospective japonaise a démontré une diminution de la mortalité toute cause, ou besoin de transplantation hépatique, avec un HR de 0,325 (intervalle de confiance (IC) de 95 % : 0,197-0,547 ; p < 0,0001), et une diminution de la mortalité de cause hépatique ou de transplantation hépatique avec un HR de 0,27 (95 % IC : 0,137-0,565 ; p < 0,0001), lors de l’adjonction du bézafibrate à l’AUDC [
32
].
Les principaux effets indésirables sont des myalgies et élévation de créatinine avec une tolérance restant satisfaisante. En effet, dans l’étude BEZURSO des myalgies sont décrites pour 20 % des patients traités par fibrates contre 10 % des patients traités par placebo, et il est observé une élévation de créatinine avec aggravation du stade de maladie rénale chronique pour un seul patient sur les 50 traités par bézafibrate. À la différence de l’acide obéticholique, on observe une amélioration du prurit lors d’une amélioration des paramètres biologiques.
Enfin, les recommandations de l’association européenne du foie (EASL), en 2017, soulignent la nécessité d’une attention particulière quant à l’importance de ne pas prescrire d’anti-inflammatoires non stéroïdiens chez les patients sous fortes doses de fibrates. En effet, les fibrates inhibent le cytochrome P450 2C9 (CYP2C9), une enzyme impliquée dans la pharmacocinétique de ces molécules [
1
]. Malgré l’importance du niveau de preuve de son efficacité, l’utilisation du bézafibrate pour le traitement de la CBP reste hors de l’autorisation de mise sur le marché (AMM) en France.
Pour l’instant, la stratégie thérapeutique du traitement de la CBP repose sur une monothérapie AUDC ou une bithérapie AUDC + bézafibrate, ou AUDC + acide obéticholique. En l’absence de réponse thérapeutique suffisante sous bithérapie, des études rétrospectives non contrôlées en ouvert, évaluant la réponse à une trithérapie AUDC + fibrate + acide obéticholique, ont fourni des résultats prometteurs qui nécessiteront d’être évalués dans des études de phases 2 et 3 [
33
,
34
].
Agonistes de PPAR non fibrates Deux essais récents de phase 3 ont testé l’adjonction d’un agoniste de PPAR à l’AUDC chez les patients non répondeurs à l’AUDC seul. Ces deux agonistes (élafibranor et séladelpar) ont comme mécanisme d’action complémentaire par rapport aux fibrates de cibler davantage PPAR delta. L’activation pharmacologique de PPAR-δ améliore la cholestase à la fois dans les hépatocytes et les cholangiocytes par répression de l’activité du cytochrome CYP7A1 (ou cholestérol 7-α hydroxylase), première enzyme de la synthèse des acides biliaires. L’action combinée des agonistes PPAR-δ sur les hépatocytes et les cholangiocytes représente un avantage par rapport aux agonistes PPAR-α qui ont une action très majoritairement hépatocytaire. Les agonistes de PPAR-δ ont également des propriétés anti-inflammatoires et anti-fibrosantes en agissant sur les cellules étoilées et les cellules de Küpffer. L’élafibranor
L’élafibranor est un agoniste des récepteurs PPAR-α et -δ. Les résultats de l’étude randomisée contrôlée en double aveugle multicentrique de phase 3, ELATIVE, publiés en 2024, font de cette molécule un traitement prometteur (
Tableau I
).
Cette étude évalue la réponse biochimique après 52 semaines de traitement élafibranor ou par placébo chez des patients poursuivant le traitement par AUDC. On observe 51 % de réponse sur le critère principal pour le groupe élafibranor contre 4 % pour le groupe placebo (différence significative). Il n’est pas démontré d’efficacité sur le prurit. La tolérance du traitement est bonne avec un taux d’évènements indésirables similaire dans les deux groupes. Les événements indésirables, observés de façon plus fréquente dans le groupe élafibranor, sont digestifs (douleurs abdominales, diarrhée, nausées, vomissements).
Des études sont en cours afin d’évaluer l’impact du traitement sur les événements cliniques [
35
].
Le séladelpar
Le séladelpar, un agoniste du récepteur PPAR delta, a également démontré son efficacité dans l’essai RESPONSE, essai de phase 3 mené en double aveugle, randomisé chez 193 patients recevant du séladelpar ou un placebo (
Tableau I
). Tout comme pour l’étude ELATIVE, les patients inclus n’ont pas répondu de manière satisfaisante à l’AUDC ou ont présenté des effets indésirables inacceptables à l’AUDC. Le critère de jugement principal est le même que pour l’étude ELATIVE. Ce critère est observé de façon plus importante et de façon significativement différente chez 61,7 % des patients traités contre 20 % des patients du groupe placebo. De plus, 25 % des patients du groupe séladelpar contre 0 % du groupe placebo atteignent un objectif de normalisation des PAL. On observe également une efficacité du séladelpar sur l’amélioration du prurit, contrairement à l’essai ELATIVE. Enfin, la tolérance du traitement est également bonne avec un taux d’effet indésirable similaire entre les deux groupes [
36
].
Une méta-analyse en réseau, publiée récemment, comparant élafibranor, séladelpar et acide obéticholique démontre une légère supériorité d’efficacité biochimique de l’élafibranor sur le séladelpar tandis que ce dernier est le seul médicament permettant une amélioration du prurit. L’acide obéticholique, bien que d’efficacité similaire, est associé à une augmentation du prurit [
37
].
Enfin, de nouvelles études évaluant d’autres agonistes de PPAR (pémafibrate et saroglitazar) sont encore en cours. Le budésonide
Le budésonide est un corticoïde à fort premier passage hépatique ayant moins d’effets indésirables que les corticoïdes systémiques classiques. Dans la CBP, il existe parfois des arguments histologiques (hépatite d’interface) ou biochimiques (élévation des transaminases) pour une part d’hépatite auto-immune concomitante. Plusieurs études ont suggéré une efficacité de l’adjonction du budésonide à l’AUDC sur les paramètres biochimiques et histologiques chez des patients ayant une CBP avec lésions histologiques d’hépatite d’interface. Le bénéfice est moins important et les effets indésirables plus fréquents chez les patients ayant une maladie plus avancée, raison pour laquelle le budésonide ne doit pas être utilisé chez les patients cirrhotiques. L’efficacité de la corticothérapie dans la CBP est sous-tendue par son action sur la part d’hépatite associée à la cholangite mais également par l’effet synergique prouvé
in vitro
du budésonide et de l’AUDC sur l’augmentation de l’expression au niveau biliaire de l’échangeur anion 2 chlore/bicarbonate.
L’étude BUC publiée en 2021 a comparé budésonide contre placebo chez des patients ayant une CBP avec inflammation histologique confirmée et réponse inadéquate après 6 mois de traitement par AUDC (définie comme des phosphatases alcalines sanguines > 1,5 fois la limite supérieure de la normale). Le taux d’amélioration histologique (objectif principal) et la réponse biochimique (objectif secondaire) sont évalués en comparant un traitement par budésonide 9 mg/j + AUDC 12-16 mg/kg (n = 40) à un placebo + AUDC 12-16 mg/kg (n = 22). L’efficacité sur l’amélioration histologique n’a pas été démontrée dans cette étude. Cependant, seuls 12 des 40 patients du groupe budésonide et 8 des 22 patients du groupe placebo sont analysés en per protocole
6
. Le schéma de l’étude (et notamment la nécessité de deux biopsies) à l’origine d’un défaut de puissance et la faible proportion de patients ayant suivi le protocole de façon adéquate, expliquent probablement ce résultat négatif sur le critère de jugement principal. Enfin, on observe une différence significative sur les critères de réponses biochimiques en faveur du groupe budésonide [
38
].
La transplantation hépatique
Bien que les progrès des traitements médicaux aient permis un moindre recours à la transplantation hépatique dans la CBP, le nombre absolu de transplantations hépatiques pour CBP reste approximativement de 200 chaque année en Europe. Cela représentait 4 % des transplantations hépatiques en Europe en 2015 [
39
].
L’EASL recommande d’évaluer pour la transplantation hépatique les patients présentant une CBP compliquée de prurit réfractaire au traitement médical, de cirrhose décompensée (MELD > 15), d’ictère avec bilirubinémie supérieure à 50 μmol/L [
1
]. La survie à 5 ans de la transplantation hépatique pour CBP est de 80 % [
40
].
La CBP est une maladie auto-immune qui peut récidiver sur le greffon dans 30 à 50 % des cas, 10 ans post transplantation. Les facteurs de risque de récidive de la maladie sont un âge jeune à la transplantation, l’utilisation d’une immunosuppression par tacrolimus, la présence d’une cholestase post-transplantation. Plusieurs études ont prouvé l’efficacité d’un traitement par AUDC comme traitement préventif de la CBP récidivante, à poursuivre donc au long cours chez le patient transplanté dans cette indication, mais également comme traitement de la CBP récidivante sur le greffon [
16
,
41
–
43
].
Traitements symptomatiques L’altération de la qualité de vie des patients suivis pour CBP est principalement liée aux symptômes qui doivent faire l’objet d’un traitement adapté. Afin de lutter contre le prurit, on peut proposer l’utilisation d’émollients ou d’eau froide. La cholestyramine peut être utilisée en prenant en compte son interférence avec l’absorption des médicaments, nécessitant d’attendre 2 à 4 heures de délai pour la prise des traitements.
Les autres traitements classiquement utilisés dans le prurit sont la rifampicine, la naltrexone, et la sertraline [
1
].
Une étude publiée dans le Lancet en 2017 a montré une diminution du prurit chez les patients traités par le linerixibat, un agoniste du transporteur de sels biliaires IBAT (
ileal sodium-dependent bile acid transporter
ou ASBT
apical sodium-dependent bile acid transporter
) responsable de la réabsorption iléale des acides biliaires. Cette nouvelle molécule pourrait être prometteuse dans cette indication et des études de phase 3 sont en cours afin de confirmer son efficacité [
44
]. D’autres inhibiteurs du transport iléal des acides biliaires sont disponibles ou en cours d’évaluation pour traiter les cholestases génétiques, comme le syndrome d’Alagille ou les cholestases familiales progressives (maralixibat, odevixibat).
Enfin, il est recommandé de rechercher et de traiter une anémie ou une hypothyroïdie afin d’améliorer l’asthénie. L’association de la maladie ou de ses traitements à l’ostéoporose invite à la supplémentation en vitamine D et en calcium. |
Ainsi, dans l’optique d’améliorer le pronostic des patients, les objectifs thérapeutiques dans la cholangite biliaire primitive deviennent plus ambitieux : seuils biochimiques plus stricts avec normalisation du bilan hépatique, amélioration de l’élastométrie. Pour y parvenir, de nouveaux traitements agissant par des mécanismes différents et complémentaires ont été développés. Les progrès dans ce domaine ne devraient cependant pas s’arrêter et nous devrions disposer d’un arsenal thérapeutique renforcé dans les années à venir. |
Footnotes |
Corentin Brice déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Alexandre Louvet déclare des liens d’intérêt avec Ipsen, Glaxo-Smith-Kline et Advanz en lien avec les données publiées dans cet article.
|
1.
Hirschfield
GM
,
Beuers
U
,
Corpechot
C
,
et al.
.
EASL Clinical Practice Guidelines: The diagnosis and management of patients with primary biliary cholangitis.
.
J Hepatol
.
2017;
;
67
:
:145.
–
72
.
2.
Corpechot
C
,
Gaouar
F
,
Chrétien
Y
,
et al.
.
Smoking as an independent risk factor of liver fibrosis in primary biliary cirrhosis.
.
J Hepatol
.
2012;
;
56
:
:218.
–
24
.
3.
Boonstra
K
,
Kunst
AE
,
Stadhouders
PH
,
et al.
.
Rising incidence and prevalence of primary biliary cirrhosis: a large population-based study.
.
Liver Int Off J Int Assoc Study Liver
.
2014;
;
34
:
:e31.
–
8
.
4.
Lleo
A
,
Jepsen
P
,
Morenghi
E
,
et al.
.
Evolving trends in female to male incidence and male mortality of primary biliary cholangitis.
.
Sci Rep
.
2016;
;
6
:
:25906.
.
5.
Dahlan
Y
,
Smith
L
,
Simmonds
D
,
et al.
.
Pediatric-onset primary biliary cirrhosis.
.
Gastroenterology
.
2003;
;
125
:
:1476.
–
9
.
6.
Leung
PSC
,
Rossaro
L
,
Davis
PA
,
et al.
.
Antimitochondrial antibodies in acute liver failure: Implications for primary biliary cirrhosis.
.
Hepatology
.
2007;
;
46
:
:1436.
.
7.
Dahlqvist
G
,
Gaouar
F
,
Carrat
F
,
et al.
.
Large-scale characterization study of patients with antimitochondrial antibodies but nonestablished primary biliary cholangitis.
.
Hepatol Baltim Md
.
2017;
;
65
:
:152.
–
63
.
8.
Corpechot
C
,
Carrat
F
,
Gaouar
F
,
et al.
.
Liver stiffness measurement by vibration-controlled transient elastography improves outcome prediction in primary biliary cholangitis.
.
J Hepatol
.
2022;
;
77
:
:1545.
–
53
.
9.
Lam
L
,
Soret
P-A
,
Lemoinne
S
,
et al.
.
Dynamics of liver stiffness measurement and clinical course of primary biliary cholangitis.
.
clin gastroenterol hepatol
.
2024;
;
22
:
:2432.
–
2441.e2
.
10.
Carbone
M
,
Mells
GF
,
Pells
G
,
et al.
.
Sex and age are determinants of the clinical phenotype of primary biliary cirrhosis and response to ursodeoxycholic acid.
.
Gastroenterology
.
2013;
;
144
:
:560.
–
69.e7
.
11.
Trivedi
PJ
,
Corpechot
C
,
Pares
A
,
et al.
.
Risk stratification in autoimmune cholestatic liver diseases: Opportunities for clinicians and trialists.
.
Hepatology
.
2016;
;
63
:
:644.
.
12.
Vleggaar
F
,
Buuren
HR
van
,
Zondervan P
,
et al.
.
Jaundice in non-cirrhotic primary biliary cirrhosis: the premature ductopenic variant.
.
Gut
.
2001;
;
49
:
:276.
–
81
.
13.
Gatselis
NK
,
Goet
JC
,
Zachou
K
,
et al.
.
Factors associated with progression and outcomes of early stage primary biliary cholangitis.
.
Clin Gastroenterol Hepatol
.
2020;
;
18
:
:684.
–
692.e6
.
14.
Björnsson
E
,
Boberg
KM
,
Cullen
S
,
et al.
.
Patients with small duct primary sclerosing cholangitis have a favourable long term prognosis.
.
Gut
.
2002;
;
51
:
:731.
–
5
.
15.
Prince
M
,
Chetwynd
A
,
Newman
W
,
et al.
.
Survival and symptom progression in a geographically based cohort of patients with primary biliary cirrhosis: Follow-up for up to 28 years.
.
Gastroenterology
.
2002;
;
123
:
:1044.
–
51
.
16.
Harms
MH
,
Buuren
HR
van
,
Corpechot C
,
et al.
.
Ursodeoxycholic acid therapy and liver transplant-free survival in patients with primary biliary cholangitis.
.
J Hepatol
.
2019;
;
71
:
:357.
–
65
.
17.
Corpechot
C
,
Chazouillères
O
,
Poupon
R.
Early primary biliary cirrhosis: Biochemical response to treatment and prediction of long-term outcome.
.
J Hepatol
.
2011;
;
55
:
:1361.
–
7
.
18.
Murillo Perez
CF
,
Harms
MH
,
Lindor
KD
,
et al.
.
Goals of treatment for improved survival in primary biliary cholangitis: treatment target should be bilirubin within the normal range and normalization of alkaline phosphatase.
.
Am J Gastroenterol
.
2020;
;
115
:
:1066.
–
74
.
19.
Corpechot
C
,
Lemoinne
S
,
Soret
P-A
,
et al.
.
Adequate versus deep response to ursodeoxycholic acid in primary biliary cholangitis: To what extent and under what conditions is normal alkaline phosphatase level associated with complication-free survival gain?
Hepatology
.
2024;
;
79
:
:39.
.
20.
Dilger
K
,
Hohenester
S
,
Winkler-Budenhofer
U
,
et al.
.
Corrigendum to: “Effect of ursodeoxycholic acid on bile acid profiles and intestinal detoxification machinery in primary biliary cirrhosis and health” [J Hepatol 2012;57:133-140].
.
J Hepatol
.
2014;
;
60
:
:684.
.
21.
Parés
A
,
Caballería
L
,
Rodés
J.
Excellent long-term survival in patients with primary biliary cirrhosis and biochemical response to ursodeoxycholic acid.
.
Gastroenterology
.
2006;
;
130
:
:715.
–
20
.
22.
Corpechot
C
,
Carrat
F
,
Bahr
A
,
et al.
.
The effect of ursodeoxycholic acid therapy on the natural course of primary biliary cirrhosis.
.
Gastroenterology
.
2005;
;
128
:
:297.
–
03
.
23.
Corpechot
C
,
Abenavoli
L
,
Rabahi
N
,
et al.
.
Biochemical response to ursodeoxycholic acid and long-term prognosis in primary biliary cirrhosis.
.
Hepatology
.
2008;
;
48
:
:871.
.
24.
Poupon
RE
,
Poupon
R
,
Balkau
B
,
et al.
.
Ursodiol for the long-term treatment of primary biliary cirrhosis.
.
N Engl J Med
.
1994;
;
330
:
:1342.
–
7
.
25.
Lammers
WJ
,
Hirschfield
GM
,
Corpechot
C
,
et al.
.
Development and validation of a scoring system to predict outcomes of patients with primary biliary cirrhosis receiving ursodeoxycholic acid therapy.
.
Gastroenterology
.
2015;
;
149
:
:1804.
–
12.e4
.
26.
Nevens
F
,
Andreone
P
,
Mazzella
G
,
et al.
.
A Placebo-controlled trial of obeticholic acid in primary biliary cholangitis.
.
N Engl J Med
.
2016;
;
375
:
:631.
–
43
.
27.
Hirschfield
GM
,
Mason
A
,
Luketic
V
,
et al.
.
Efficacy of obeticholic acid in patients with primary biliary cirrhosis and inadequate response to ursodeoxycholic acid.
.
Gastroenterology
.
2015;
;
148
:
:751.
–
61.e8
.
28.
Murillo Perez
CF
,
Fisher
H
,
Hiu
S
,
et al.
.
Greater transplant-free survival in patients receiving obeticholic acid for primary biliary cholangitis in a clinical trial setting compared to real-world external controls.
.
Gastroenterology
.
2022;
;
163
:
:1630.
–
42.e3
.
29.
Kowdley
KV
,
Hirschfield
GM
,
Coombs
C
,
et al.
.
COBALT: A Confirmatory Trial of obeticholic acid in primary biliary cholangitis with placebo and external controls.
.
Am J Gastroenterol
.
2025;
;
120
:
:390.
–
400
.
30.
Corpechot
C
,
Chazouillères
O
,
Rousseau
A
,
et al.
.
A Placebo-controlled trial of bezafibrate in primary biliary cholangitis.
.
N Engl J Med
.
2018;
;
378
:
:2171.
–
81
.
31.
Lens
S
,
Leoz
M
,
Nazal
L
,
et al.
.
Bezafibrate normalizes alkaline phosphatase in primary biliary cirrhosis patients with incomplete response to ursodeoxycholic acid.
.
Liver Int
.
2014;
;
34
:
:197.
–
203
.
32.
Tanaka
A
,
Hirohara
J
,
Nakano
T
,
et al.
.
Association of bezafibrate with transplant-free survival in patients with primary biliary cholangitis.
.
J Hepatol
.
2021;
;
75
:
:565.
–
71
.
33.
Smets
L
,
Verbeek
J
,
Korf
H
,
et al.
.
Improved markers of cholestatic liver injury in patients with primary biliary cholangitis treated with obeticholic acid and bezafibrate.
.
Hepatol Baltim Md
.
2021;
;
73
:
:2598.
–
600
.
34.
Soret
P-A
,
Lam
L
,
Carrat
F
,
et al.
.
Combination of fibrates with obeticholic acid is able to normalise biochemical liver tests in patients with difficult-to-treat primary biliary cholangitis.
.
Aliment Pharmacol Ther
.
2021;
;
53
:
:1138.
–
46
.
35.
Kowdley
KV
,
Bowlus
CL
,
Levy
C
,
et al.
.
Efficacy and safety of elafibranor in primary biliary cholangitis.
.
N Engl J Med
.
2024;
;
390
:
:795.
–
805
.
36.
Hirschfield
GM
,
Bowlus
CL
,
Mayo
MJ
,
et al.
.
A phase 3 trial of seladelpar in primary biliary cholangitis.
.
N Engl J Med
.
2024;
;
390
:
:783.
–
94
.
37.
Giannini
EG
,
Pasta
A
,
Calabrese
F
,
et al.
.
Second-line treatment for patients with primary biliary cholangitis: a systematic review with network meta-analysis.
.
Liver Int Off J Int Assoc Study Liver
.
2025;
;
45
:
:e16222.
.
38.
Hirschfield
GM
,
Beuers
U
,
Kupcinskas
L
,
et al.
.
A placebo-controlled randomised trial of budesonide for PBC following an insufficient response to UDCA.
.
J Hepatol
.
2021;
;
74
:
:321.
–
9
.
39.
Harms
MH
,
Janssen
QP
,
Adam
R
,
et al.
.
Trends in liver transplantation for primary biliary cholangitis in Europe over the past three decades.
.
Aliment Pharmacol Ther
.
2019;
;
49
:
:285.
–
95
.
40.
Liermann Garcia
RF
,
Garcia
CE
,
McMaster
P
,
et al.
.
Transplantation for primary biliary cirrhosis: retrospective analysis of 400 patients in a single center.
.
Hepatology
.
2001;
;
33
:
:22.
.
41.
Montano-Loza
AJ
,
Hansen
BE
,
Corpechot
C
,
et al.
.
Factors associated with recurrence of primary biliary cholangitis after liver transplantation and effects on graft and patient survival.
.
Gastroenterology
.
2019;
;
156
:
:96.
–
107.e1
.
42.
Montano-Loza
AJ
,
Lytvyak
E
,
Hirschfield
G
,
et al.
.
Prognostic scores for ursodeoxycholic acid-treated patients predict graft loss and mortality in recurrent primary biliary cholangitis after liver transplantation.
.
J Hepatol
.
2024;
;
81
:
:679.
–
89
.
43.
Corpechot
C
,
Chazouillères
O
,
Belnou
P
,
et al.
.
Long-term impact of preventive UDCA therapy after transplantation for primary biliary cholangitis.
.
J Hepatol
.
2020;
;
73
:
:559.
–
65
.
44.
Hegade
VS
,
Kendrick
SFW
,
Dobbins
RL
,
et al.
.
Effect of ileal bile acid transporter inhibitor GSK2330672 on pruritus in primary biliary cholangitis: a double-blind, randomised, placebo-controlled, crossover, phase 2a study.
.
Lancet
.
2017;
;
389
:
:1114.
–
23
.
|