| |
| Med Sci (Paris). 41(8-9): 666–675. doi: 10.1051/medsci/2025106.De l’émergence du mpox en République démocratique du Congo aux urgences sanitaires globales Eddy Kinganda-Lusamaki,1,2,3* Ahidjo Ayouba,2 Placide Mbala-Kingebeni,1,3 Steve Ahuka-Mundeke,1,3 Jean-Jacques Muyembe-Tamfum,1,3 Eric Delaporte,2 and Martine Peeters2 1INRB, Kinshasa, République Démocratique du Congo 2UMI233 TransVIHMI (Recherches translationnelles sur le VIH et les maladies infectieuses), Université de Montpellier, IRD, INSERM Unité 1175
,
Montpellier
,
France 3Service de microbiologie, département de biologie médicale, cliniques universitaires de Kinshasa, Université de Kinshasa, Kinshasa, République démocratique du Congo |
Vignette (© Creative commons).
Le monde fait actuellement face à plusieurs épidém ies de mpox et l’Organisation mondiale de la santé (OMS) a déclaré deux urgences de santé publique de portée internationale (USPPI), en seulement deux ans. L’infection par mpox est une zoonose éruptive pouvant entraîner le décès de la personne infectée. Du 1
er
janvier 2022 au 31 décembre 2024, plus de 124 700 cas confirmés, dont 272 mortels, ont été rapportés par l’OMS dans 128 pays. Dans la majorité des pays, le mpox est perçu comme une nouvelle maladie.
Le virus mpox (MPXV) a été découvert en 1958 à Copenhague chez des sin ges importés d’Asie. À cette époque, on a pensé que la maladie était une variante de la variole chez les primates non humains, d’où les noms de «
monkeypox
», «
orthopoxvirose simienne
», «
variole du singe
», ou «
variole simienne
» qui lui ont été attribués. Cependant, l’agent viral isolé à partir des lésions pustuleuses après mise en culture était distinct, quoique sérologiquement apparenté au virus de la vaccine (VACV) et doté d’un aspect en forme de brique typique du virus de la variole (VARV) [
1
].
La présente revue a pour objectif de parcourir les connaissances cumulées à ce jour sur les aspects virologiques et l’évolution du virus, et de décrire l’historique, l’épidémiologie, le diagnostic clinique et biologique, ainsi que les avancées dans la prise en charge de la maladie. |
Taxonomie
Le virus MPXV appartient à la famille des
Poxviridae
, sous-famille des
Chordopoxvirinae
. D’après la dernière mise à jour du comité international de la taxonomie des virus, le virus a été assigné à l’espèce
Orthopoxvirus monkeypox
[
2
]. Le nom d’espèce des orthopoxvirus (OPV) ne reflète pas toujours son réservoir naturel, c’est le cas du virus MPXV dont le singe n’est qu’un hôte accidentel. Parmi les OPV, 13 espèces ont été identifiées à ce jour, dont le virus Abatino macacapox (AMPV), le virus Akhmeta (AKMV), le virus camelpox (CMLV), le virus ectromelia (ECTV), le virus Taterapox (TATV), le virus de la variole (VARV), le virus de la vaccine (VACV), le virus de la variole bovine (CPXV), l’Alaskapox (AKPV), le virus raccoonpox (RCNV), le virus skunkpox (SKPV), le virus volepox (VPXV) et le virus de mpox (MPXV)
Morphologie, structure génomique et réplication
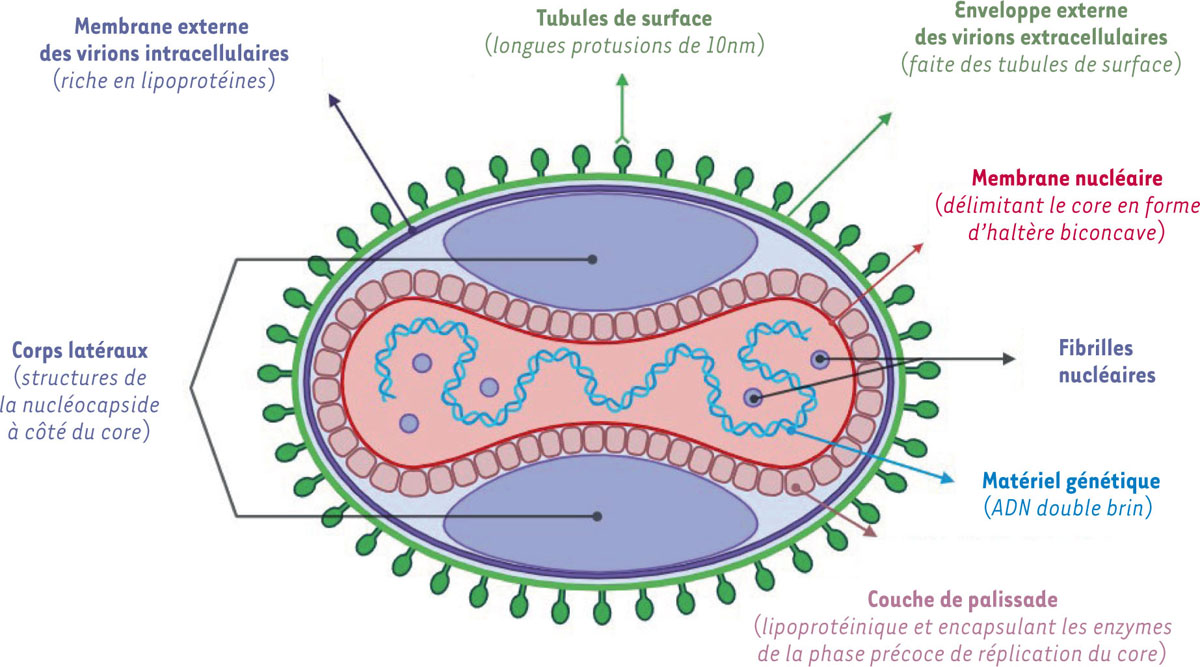
Le virus MPXV est un grand virus pléomorphe enveloppé doté d’une morphologie complexe avec une ultrastructure permettant de distinguer un core en forme bicon cave surplombé de deux corps latéraux et d’une enveloppe (
Figure 1
). Il mesure 140 à 260 nm de diamètre et 220 à 450 nm de longueur [
2
,
3
].
 | Figure 1.
Représentation schématique d’une particule de MPXV
.
La capside (ou core), en forme d’haltère biconcave, contient le matériel génétique (ADN double brin) ainsi que les fibrilles nucléaires ; le core est entouré d’une membrane ainsi que d’une couche pallisadique riche en lipoprotéines, et est adjacent à 2 corps latéraux au niveau des zones concaves. Le tout est enveloppé par une membrane et une enveloppe extérieure (propre aux virions enveloppés) qui porte des protusions qui sont les tubules de surface (figure réalisée avec BioRender).
|
Les génomes des poxvirus codent plus d’une centaine de protéines, ce qui pose des défis pour l’étude de l’histoire naturelle de l’infection, de la transmission et de la p athogénicité du virus [
4
]. La souche virale MPXV-ZAI de l’épidémie de 1996 au Sankuru en République démocratique du Congo (RDC), est le premier génome complet du virus MPXV décrit et rendu public en 2001
1
. Le génome du MPX est constitué d’environ 196 kilopaires de bases (kpb), avec environ 190 cadres de lecture ouverts (
open reading frames
, ORFs), un chiffre semblable à celui observé dans d’autres virus apparentés [
5
].
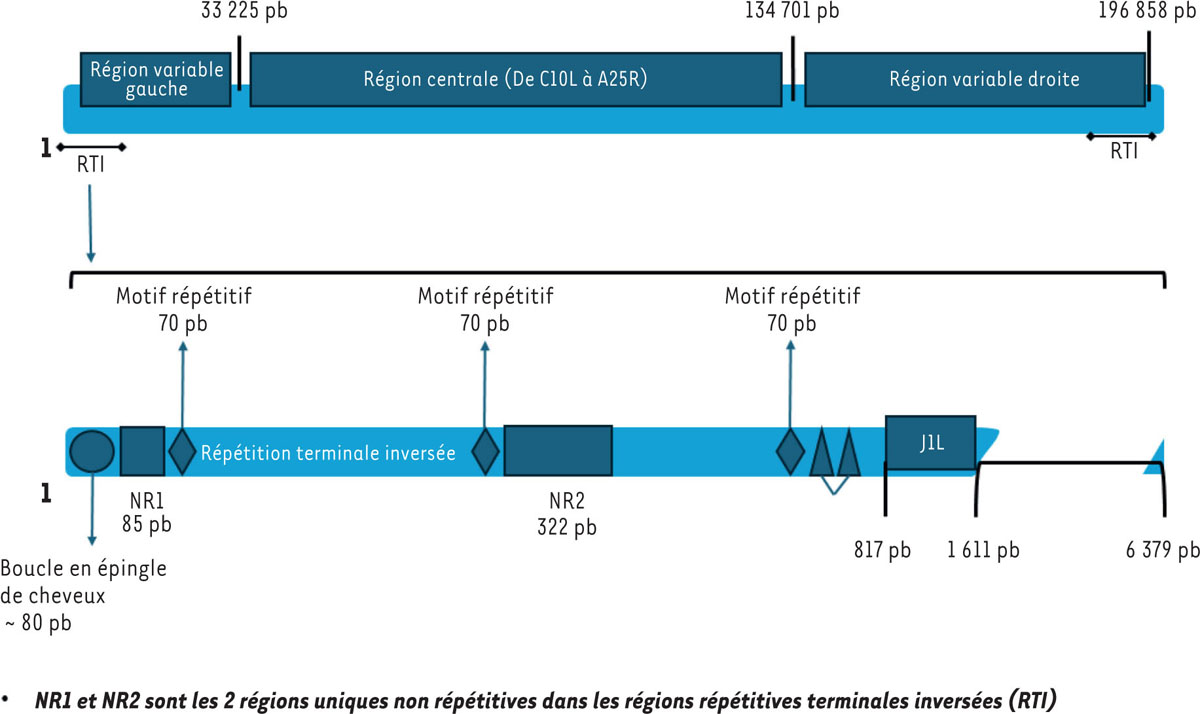
La région conservée centrale du génome code des protéines impliquées dans la réplication, la morphogenèse et la dissémination du virus. Cette région va de C10L à A25R, et est entourée par des extrémités variables d’environ 6 379 pb contenant les répétitions terminales inversées, avec un ensemble de courtes répétitions en tandem et des boucles terminales en épingle à cheveux, avec deux régions uniques non-répétitives de 85 pb et 322 pb (
Figure 2
) [
2
,
5
,
6
]. Ces régions aux extrémités codent des protéines différentes selon les espèces d’orthopoxvirus, et sont impliquées dans le contrôle de la réponse immunitaire de l’hôte [
2
,
5
]. La teneur en guanine et en cytosine (GC) de l’ADN du virus MPXV est faible (environ 33,1 %) [
5
,
6
].
 | Figure 2.
Représentation schématique de la souche Zaire-96-I-16
(MPXV-ZAI) NC_003310 (clade I). Souche isolée durant l’épidémie de 1996 au Sankuru en RDC. Pb : paires de bases. Figure adaptée de [
8
] et obtenue par courtoisie de Lebeni Liège.
|
Initialement, les gènes des orthopoxvirus avaient été nommés d’après les connaissances sur le virus de la vaccine (souche Copenhagen), identifiés d’après le profil de digestion de l’ADN viral obtenu à l’aide de l’enzyme de restriction HindIII. Les fragments de digestion ont été nommés selon l’ordre décroissant de taille de A à P, les gènes numérotés à l’intérieur de chaque fragment, et désignés selon leur sens de transcription, droite (R) ou gauche (L). Par exemple, J1R correspond au l
er
gène de la portion J (10
e
fragment en longueur) et se lit dans le sens (de 5’ à 3’, sur le brin supérieur), alors que A3L correspond au 3
e
gène du fragment A (le plus grand) et se lit en antisens (de 5’ à 3’ sur le brin inférieur). À partir de 2021, une nomenclature unifiée des orthopoxvirus a été établie avec des gènes désignés par le sigle OPG (pour
orthopoxvirus gene
) suivi d’un numéro [
7
]. Ainsi, les gènes J1R et A3L se nomment maintenant OPG100 et OPG126.
La réplication du virus MPXV est similaire à celle des autres orthopoxvirus. La transcription en ARNm se fait directement à partir de l’ADN viral en trois phases : précoce, intermédiaire et tardive [
8
]. Par ailleurs, il existe deux formes infectieuses différentes : les virions matures qui sont libérés suite à la lyse de la cellule, et les virions enveloppés, moins fréquents, qui proviennent d’un phénomène d’exocytose. Comme les autres grands virus à ADN dotés de leur propre A DN polymérase, le virus MPXV présente un faible taux de mutation. Cependant, sa transmission interhumaine soutenue est associée à des mutations attribuées à l’activité des cytosines désaminases cellulaires telles que l’enzyme APOBEC3 (enzyme éditrice de l’ARNm de l’apolipoprotéine B, polypeptide catalytique 3) [
9
]. Ces enzymes, qui font partie de l’arsenal de la réponse immunitaire innée cellulaire, désaminent les résidus de cytosine dans les génomes viraux, provoquant ainsi des mutations C → T ou G → A sur le brin complémentaire. Sur les génomes viraux, la modification dinucléotidique de TC → TT ou de son complément inverse GA → AA signe ce type de mutation [
9
].
Classification en clades du virus MPXV
Deux clades principaux du virus MPXV ont été décrits : les clades I et II endémiques respectivement en Afrique centrale et de l’Ouest. Avant 2024, le Cameroun était le seul pays où les clades I et II co-circulaient, tout en étant respectivement localisés dans les régions est et ouest du pays. Le clade II est subdivisé en sous-clade IIa, qui inclut les virus circulant à l’ouest du sillon dahoméen
2,
en Afrique de l’Ouest, et en sous-clade IIb, qui regroupe toutes les séquences de l’épidémie mondiale de mpox de 2022 ainsi que des séquences issues du Nigeria, à l’est du couloir dahoméen. Dans le sous-clade IIb, plusieurs variants
3
, annotés A à F ont ensuite été identifiés au cours de l’épidémie. Deux sous-clades a et b ont aussi été identifiés au sein du clade I, avec l’émergence de l’épidémie de mpox en 2023, dans l’est de la RDC [
10
,
11
]. Au sein du sousclade Ia, cinq groupes principaux (nommés de I à V) ont été décrits antérieurement [
12
]. Cette démarcation géographique entre les clades I et II est associée à une différence de pathogénicité et de mortalité, le clade I étant le plus sévère.
|
Hôtes naturels, potentiels réservoirs et transmission du virus MPXV
Malgré les avancées réalisées sur la connaissance des hôtes naturels et des réservoirs des orthopoxvirus, dont le virus MPXV, plusieurs zones d’ombre persistent. Des enquêtes de séroprévalence dans la faune sauvage ont montré qu’un grand nombre d’animaux pouvaient être infectés naturellement par le virus MPXV, y compris les primates non humains et les rongeurs (écureuils et rats). Bien que ces derniers soient fortement suspectés d’être les réservoirs naturels, le doute demeure encore sur les espèces impliquées comme réservoirs ou hôtes accidentels. Par ailleurs, les primates non humains ont été incriminés à tort, comme réservoir ou hôtes principaux du virus MPXV à la suite des épizooties observées [
13
,
14
]. Des études sérologiques, menées dans les forêts tropicales d’Afrique centrale et occidentale, ont montré que les rongeurs arboricoles, les singes et les chauves-souris présentaient des anticorps contre les orthopoxvirus, avec une forte prévalence chez les écureuils des genres
Funisciuris
et
Heliosciuris
en RDC, dans quatre régions très éloignées les unes des autres [
15
,
16
].
À l’issue de l’épidémie de Katako-Kombe au Sankuru en RDC en 1996, des anticorps ont été détectés chez différentes espèces d’écureuils (
Funisciurus anerythrus, F. congicus
et
Heliosciurus rufobrachium
), et chez d’autres mammifères forestiers, dont le sanglier (
Sus scrofa
), le rat de Gambie (
Cricetomys emini
) et le rat à trompe tétradactyle (
Petrodromus tetradactylus
) [
17
].
En 2003, l’épidémie humaine de virus MPXV aux États-Unis a été causée par la manipulation de chiens de prairie (
Cynomys sp
.), une espèce d’écureuils du continent Nord-Américain, qui avaient été exposés à des rats, des loirs et des écureuils africains infectés par le virus MPXV (clade IIa) dans une cargaison en provenance du Ghana [
18
]. Les rats géants de Gambie (
Cricetomys spp
) étaient cités parmi les animaux qui seraient à la base de cette épidémie aux États-Unis [
19
]. Par la suite, ces résultats ont été étayés par les enquêtes sérologiques chez de nombreux rongeurs au Ghana, notamment chez plusieurs espèces (
Cricetomys spp
,
Graphiurus spp
,
Funisciurus anerythrus
et
Heliosciurus rubobrachium
), malgré l’absence de cas humains à l’époque [
18
]. Une étude récente basée sur les comparaisons de niches écologiques suggère que les écureuils arboricoles en particulier
F. anerythrus
, pourraient être le réservoir primaire du virus MPXV, tandis que les primates non humains et autres animaux joueraient le rôle d’amplificateurs. Ils peuvent cependant tous être à l’origine de contaminations humaines directes. L’ADN du virus MPXV a été aussi retrouvé par analyse PCR (
polymerase chain reaction
) dans 9 % des peaux d’écureuils à corde provenant de musées d’Afrique centrale, la plus ancienne datant de 1899 [
20
].
De ce qui précède, deux types de mécanismes de transmission se distinguent : la transmission inter-espèces et la transmission intra-espèce. Peu de cas de transmission ont été décrits avec confirmation virologique. En Afrique, le virus a été retrouvé essentiellement dans la faune sauvage tandis qu’un cas de transmission de l’homme à un chien domestique a été décrit en France en juin 2022, suggérant la possibilité de propagation du mpox par les animaux de compagnie [
21
].
En Afrique, les cas de contamination humaine primaires ont eu lieu par contact direct avec du sang, des liquides organiques, des éruptions cutanées ou les morsures d’animaux infectés [
4
,
16
,
17
]. Les facteurs de risque pouvant conduire à l’infection mpox et à des épidémies sont multiples : les activités de chasse, la dissection ou le transport des proies infectées pendant la préparation pour la consommation de l’animal ou leur commercialisation, la manipulation par les enfants des carcasses d’animaux contaminés ou blessés, la morsure par un animal ou encore les jeux avec ces animaux sauvages [
16
,
22
].
Avant l’émergence du sous-clade IIb dans le monde, la transmission zoonotique était prépondérante, suivie de courtes chaînes de transmission interhumaine secondaires [
5
,
12
,
23
–
25
]. Cette transmission interhumaine est verticale par voie placentaire (mpox congénital) ou horizontale par contact direct, voire sexuel, avec une personne infectée, ou indirect à partir des objets contaminés (vêtements, draps de lit, etc.) [
26
–
28
]. La transmission du virus MPXV au sein des ménages se produit essentiellement par contact avec l’exsudat des lésions, et plusieurs études ont montré jusqu’à 6-7 événements de transmission intrafamiliale [
25
,
26
,
29
,
30
]. Par ailleurs, des études de modèles animaux ont suggéré une transmission par voie respiratoire et des études environnementales ont permis de détecter le virus dans l’air ; cependant, les données issues des épidémies et les descriptions de cas suggèrent que la probabilité de transmission respiratoire, mode principal observé dans la variole, reste très faible pour le virus MPXV [
31
].
Actuellement, les multiples introductions du virus dans la population humaine dont le flux de déplacement a augmenté significativement, induisent un changement évident du mode de transmission du virus MPXV avec des chaînes de transmission de plus en plus longues, signant une adaptation du virus MPXV à l’homme, avec accumulation de mutations APOBEC3 [
10
].
La première alerte enregistrée dans l’histoire de la maladie fut la grande flambée épidémique de Katako-Kombe (Province du Sankuru en RDC) en 1996, caractérisée par une transmission interhumaine très élevée, soit de 78 % [
17
,
32
]. Cependant, l’émergence de la maladie en zones rurales ou semi-urbaines, difficiles d’accès ou enclavées, a permis de contenir le virus MPXV dans ses niches écologiques naturelles. L’épidémie de 2017 au Nigéria a marqué un tournant considérable avec l’introduction de la maladie dans les grandes agglomérations urbaines qui ont ouvert les portes vers le monde, et entraîné l’épidémie globale de 2022 marquée par une transmission interhumaine soutenue [
9
,
33
].
|
Épidémiologie globale et risque pandémique L’épidémiologie du mpox peut se résumer en 4 grandes phases :
-
De 1958 à 1970 : premières évidences de l’émergence
. Depuis la découverte du virus MPXV en 1958 à Copenhague, plusieurs épizooties ont été observées parmi les primates non humains d’Afrique ou d’Asie, et dans les laboratoires de recherche en Europe et en Amérique, entre 1959 et 1968 [
13
]. Aucun cas n’a été signalé parmi les personnes en contact avec les animaux malades. Le mpox était donc considéré comme une maladie affectant les primates non humains jusqu’à la première description chez un enfant de 9 mois, dans le village de Bokenda, dans la province de l’Équateur en RDC en août 1970. La découverte quasi fortuite est survenue dans le cadre du programme national de surveillance et d’éradication de la variole [
3
]. Par la suite, six cas supplémentaires ont été identifiés chez l’être humain dans les pays d’Afrique de l’Ouest entre septembre 1970 et mars 1971, principalement chez des jeunes enfants, non vaccinés contre la variole, alors en phase d’éradication [
3
]. En plus des évidences sérologiques, diverses analyses ont permis la comparaison de leurs structures génomiques qui étaient très différentes dans les parties distales du génome viral, ce qui exclut l’idée d’une mutation du virus de la variole en virus MPVX et oriente plutôt vers des trajectoires évolutionnelles indépendantes de ces deux virus [
1
,
6
].
-
De 1971 à 2000 : de l’émergence à la négligence
. Malgré la certification de l’éradication de la variole en mai 1980, l’émergence du virus MPXV constituait un sujet d’inquiétude en raison du risque de transmission interhumaine. En conséquence, la commission mondiale pour la certification de l’éradication de la variole a désigné le virus MPXV comme l’infection à orthopoxvirus la plus importante chez l’homme dans l’ère post-éradication de la variole (à partir de 1980). Dans son rapport final de 1980, elle a recommandé la poursuite d’un programme de surveillance du virus MPXV, de son épidémiologie et de son écologie qui a été effectué entre 1981 et 1986, et à l’issue duquel, il a été conclu que la propagation interhumaine était limitée en l’absence de contaminations animales répétées [
26
]. Cette conclusion a relégué le mpox au statut de maladie négligée. Il s’en suivit une baisse de la surveillance durant les dix années suivantes, aggravée par le contexte d’insécurité et d’instabilité politique en RDC. De 1986 (fin de ce programme intensif de surveillance de l’OMS) à 1992, seuls 13 cas de mpox ont été rapportés au Gabon, au Cameroun et en RDC. Le contexte tumultueux en RDC, marqué par des conflits, a aggravé cette négligence faisant passer inaperçues de grandes alertes telle que l’épidémie survenue dans la province du Sankuru en 1996.
-
De 2001 à 2009 : de la négligence à la réémergence
. À partir du 3
e
millénaire, commence l’ère de la détection et de l’exportation du mpox humain en dehors des zones forestières du bassin du Congo et de la forêt de Guinée. De mai à juin 2003, les premiers cas humains ont été rapportés dans l’Etat de Wisconsin (USA). Aucune transmission interhumaine n’a été signalée, ni de décès enregistré [
19
,
34
]. Durant la même période, deux pays frontaliers de la RDC ont signalé des épidémies à mpox : la République du Congo (RC) (à Impfondo, en avril 2003) [
29
] et le Sud-Soudan (Soudan à l’époque) [
35
].
En 2005, la RDC, a initié un vaste programme de surveillance active du virus MPXV dans la province du Sankuru pendant deux ans, qui a permis de noter que l’incidence annuelle moyenne avait été multipliée par 20 dans la ville de Kole (de 0,7 à 14,4 pour 10 000 hab) et par 23 dans toutes les zones sous surveillance active (de 0,5 à 11,3 pour 10 000 hab), comparée aux années 1980 [
24
]. En plus de ce constat alarmant, dans un contexte d’arrêt de vaccination antivariolique, ces résultats étaient probablement sous-estimés en raison des ressources relativement limitées face au défi logistique immense. Durant cette décennie, la République du Congo a notifié 73 cas, alors que la RDC a notifié près de 10 027 cas suspects [
34
].
-
De 2010 à 2021 : de la réémergence à l’urgence
. La décennie 2010-2020 a enregistré des cas sporadiques de mpox d’exportation en dehors de l’Afrique [
34
,
36
]. En Afrique Centrale, la RDC a franchi le cap de 2 000 notifications par an. En effet, de nouvelles aires géographiques en RDC ont noté des cas de mpox, à l’instar des provinces du Nord-Kivu et du Sud-Kivu dans un contexte conflictuel [
23
,
34
]. D’autres pays frontaliers tels que, la République Centrafricaine et la République du Congo ont aussi rapporté une hausse des cas [
37
,
38
]. En Afrique de l’Ouest, des émergences ont été enregistrées en Sierra-Leone et au Nigeria. L’épidémie de mpox au Nigéria a eu la particularité de s’étendre en milieu urbain donnant lieu à des chaines de transmission interhumaines plus longues et des centaines de cas entre 2017 et 2019 [
33
,
34
]. Le virus MPXV est détecté en Israël, au Royaume-Uni, à Singapour et aux USA entre 2018 et 2021 chez des voyageurs en provenance du Nigéria [
36
].
|
Première déclaration d’urgence de santé publique de portée internationale en 2022
À partir de mai 2022, l’épidémiologie a brusquement changé avec une série de cas signalés simultanément dans plusieurs pays en Europe (initialement en Angleterre, au Portugal, et en Italie), quasi exclusivement chez les hommes ayant des relations sexuelles avec les hommes. L’OMS a déclaré le 23 juillet 2022 la première urgence de santé publique de portée internationale (USPPI). Le séquençage a permis la caractérisation de la souche qui se distinguait du clade II circulant traditionnellement (sous-clade IIa) par un taux élevé de mutations dues aux APOBEC3. Ce nouveau variant a été renommé sous-clade IIb
4,
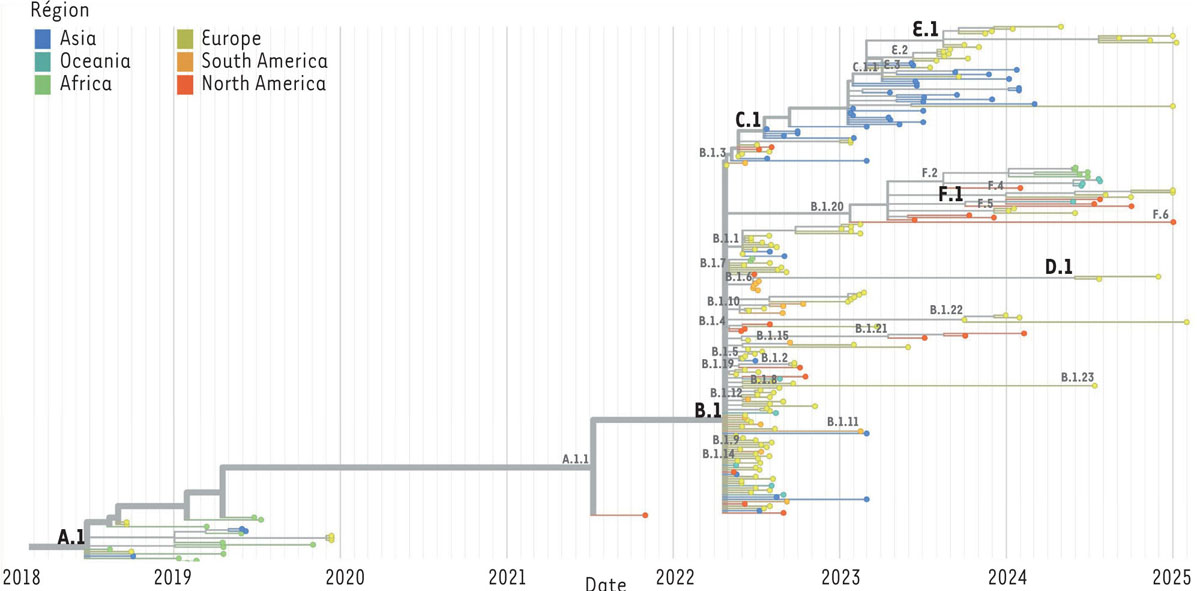
, et l’épidémie du Nigéria regroupait la lignée A (lineage A) de laquelle descend la lignée B, responsable de l’épidémie mondiale dans les autres pays non endémiques (
Figure 3
) [
9
].
 | Figure 3.
Reconstruction phylogénétique du sous-clade IIb
pendant la pandémie avec nextstrain/mpox, montrant 235 génomes échantillonnés entre août 2018 et janvier 2025. Données mises à jour le 15/02/2025 (
https://nextstrain.org/mpox/clade-IIb?p=full
).
|
Le pic de l’épidémie a été atteint en août 2022 (lignée B). Le facteur de risque le plus souvent identifié était le contact sexuel avec un sujet infecté. La flambée mondiale s’est propagée par l’intermédiaire de réseaux sexuels et a touché principalement (mais pas uniquement) les hommes ayant des relations sexuelles avec les hommes et les personnes ayant des comportements à risque tels que la multiplicité des partenaires. Au début de l’année 2023, la situation épidémiologique dans le monde faisait état d’environ 86 000 cas recensés dans 110 pays, dont les plus concernés, en nombre de cas, étaient les États-Unis, le Brésil, l’Espagne et la France. Les régions d’Asie ont également annoncé des cas avec un pic à partir du printemps 2023 (lignée C descendante de la lignée B.1). À ce jour, la reconstruction phylogénétique permet d’identifier six lignées d’épidémies de sous-clade IIb notées de A à F. L’épidémiologie du sous-clade IIb aura permis d’intégrer dans le paradigme de transmission, les contacts sexuels qui sont l’un des canaux prépondérants. Documentation de la diversité génomique du clade I
L’un des acquis de la première déclaration d’USPPI, aura été l’augmentation de l’intérêt et des connaissances sur le virus MPXV. En l’occurrence, avant 2022, seules 260 séquences (dont 100 couvertes à plus de 70 %, dont 50 de clade I et 50 de clade II) étaient rendues publiques, alors que 6 713 séquences ont été ajoutées entre 2022 et 2023 (dont 6 574 couvertes à plus de 70 %, parmi lesquelles seules 4 étaient du clade I). De toute évidence, plus d’attention était portée vers le clade IIb circulant dans les pays développés en Europe et en Amérique et responsable de l’épidémie multi-pays ; alors que le clade I continuait de circuler. Depuis 2020, on a observé une recrudescence des cas de mpox et des décès en RDC avec de nouvelles aires géographiques affectées. En 2023, le pays a notifié 14 659 cas suspects. L’un des faits marquants en 2023 a été la détection au mois d’août des premiers cas à Kinshasa, la capitale et la plus grande agglomération urbaine de la RDC avec plus de 15 millions d’habitants. Ces premières introductions étaient des cas importés consécutifs à des flambées dans les provinces de l’Equateur et du Mai-Ndombe [
10
].
Alors, que la transmission zoonotique avec un faible taux d’attaque secondaire restait la règle dans l’ensemble du pays, des clusters de transmission (homo/ hétéro) sexuelle ont été documentés pour la première fois dans la province de Kwango [
39
], dans un contexte de surveillance d’éventuelles introductions du clade IIb en RDC. Ce changement prendra plus d’ampleur en octobre 2023, lorsqu’une épidémie de mpox a été signalée dans la cité minière de Kamituga (Sud-Kivu), avec des clusters incluant des professionnels du sexe. Il s’en suivra la description d’un nouveau sous-clade (clade Ib), se transmettant essentiellement par contact sexuel et une transmission interhumaine soutenue, avec un taux élevé de mutations dues à APOBEC3 indiquant une adaptation à l’être humain [
10
,
11
]. Ce nouveau variant a une délétion de 1 114 pb dans le gène OPG032, posant des difficultés pour le diagnostic par PCR [
40
]. Par ailleurs, une étude récente sur la diversité moléculaire des souches de virus MPXV circulant en RDC (603 échantillons prélevés dans 14 des 26 provinces de 2018 à 2024), a permis de générer 429 génomes, tous du clade I, couverts à plus de 70 % [
10
] et a révélé que le sous-clade Ia restait majoritaire dans l’ensemble du pays, sur un fond d’introductions d’origine zoonotique continues (
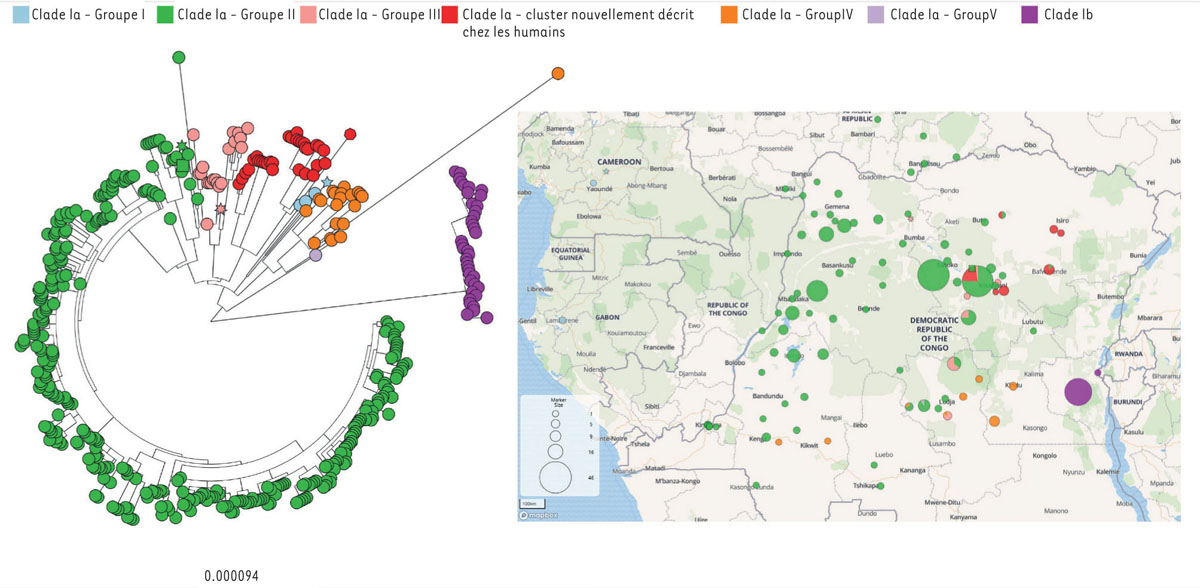
Figure 4
), contrairement au sous-clade Ib prévalent à l’Est jusqu’à mi-2024.
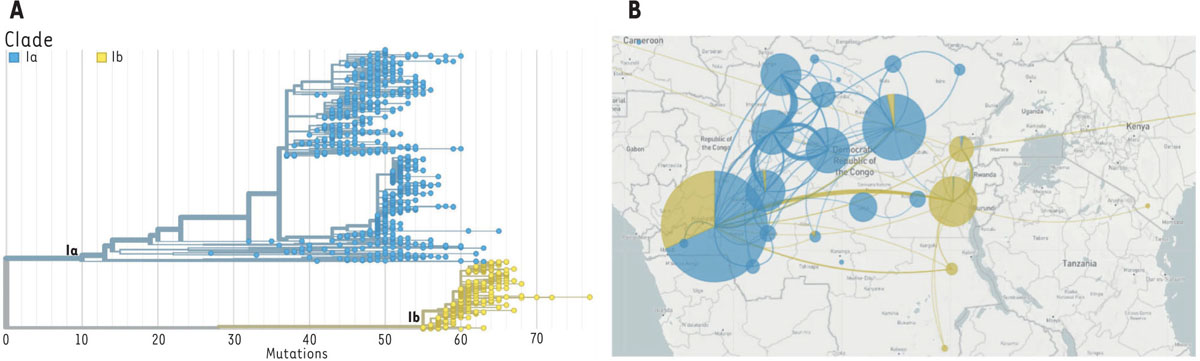
 | Figure 4.
Analyse phylogénétique des souches de virus MPXV
prélevées entre 2018 et 2024 et les aires de provenance des prélèvements.
|
Deuxième déclaration d’urgence de santé publique de portée internationale en 2024 Le sous-clade Ib s’est rapidement propagé du Sud-Kivu aux pays frontaliers, dont le Burundi, le Rwanda et l’Ouganda. La ville de Goma, au Nord-Kivu, a confirmé en juin 2024 ses premiers cas, dont certains n’avaient pas de lien épidémiologique direct avec la province du Sud -Kivu, notamment dans des camps de populations déplacées. Inéluctablement, s’en sont suivies des exportations du virus à Kinshasa (juillet 2024), dans les pays de l’Afrique de l’Est, et hors d’Afrique (Thaïlande et Suède).
Le fort potentiel d’expansion du sous-clade Ib, couplé à la hausse des cas de mpox de façon globale, a contribué aux déclarations d’urgence de santé publique de sécurité continentale le 13 août et d’USPPI le 14 août 2024. En effet, la région africaine avait enregistré une augmentation de 79 % du nombre de cas en 2023 par rapport à 2022. Une augmentation de, respectivement 160 % et 19 % du nombre de cas et de décès, a aussi été observée en 2024 par rapport à la même période [
41
].
Au moment de ces déclarations, 17 541 cas et 517 décès avaient été signalés dans 13 pays d’Afrique. En 2024, la RDC notifiait 64 173 cas suspects. En outre, la flambée des cas de sous-clade Ia dans la capitale Kinshasa à partir de juillet 2024 ainsi que l’apparition de foyers de co-circulation des sous-clades Ia et Ib soulèvent des inquiétudes avec l’émergence d’un variant associé à de longues chaînes de transmission interhumaine, et dont les génomes présentent des taux élevés de mutations dues à APOBEC3 [
42
]. Ce nouveau variant Ia s’est répandu vers d’autres provinces et a été détecté hors d’Afrique (Irlande, Chine). Enfin, aujourd’hui, plusieurs provinces sont sujettes à la co-circulation des sous-clades Ia/ Ib (
Figure 5
).
 | Figure 5.
Analyse phylogéographique du clade I focalisée sur la RDC
,
incluant 1 804 génomes de clades I de 1970 à 2025, et montrant la répartition des sous-clades Ia (en bleu) et Ib (en jaune) par provinces, avec les liens probables.
|
|
Diagnostic clinique et confirmation biologique Bien qu’une confirmation biologique soit indispensable pour établir l’infection, le diagnostic clinique est souvent utilisé dans les milieux reculés et ayant un accès limité aux ressources.
Après une incubation variant de 3 à 17 jours, l’évolution clinique du mpox est généralement divisée en une période prodromique de 1 à 3 jours (fièvre, céphalées, dorsalgies, myalgies, asthénie et lymphadénopathies) et une période d’état [
26
–
28
]. Celle-ci est déterminée par la présentation de six formes cliniques décrites dans le
Tableau I
[
27
,
43
].
Tableau I.
| Forme clinique |
Caractéristique de la phase d’état |
Autres remarques |
| Formes sans éruption |
La fièvre est le principal symptôme |
Essentiellement chez les sujets immunologiquement non naïfs |
|
| Formes atténuées ou paucisymptomatiques |
L’évolution est accélérée et les pustules sont petites ; |
Les lésions sont souvent localisées aux points d’entrée du virus |
|
| Formes plates |
Les pustules restent plates et ont habituellement une distribution confluente ou semi-confluente ; |
|
|
| Formes hémorragiques |
Pétéchies, saignements aux sites de ponction veineuse, saignements oraux, gingivaux, rectaux, nasaux, vaginaux et conjonctivaux. |
Autrefois observées dans la variole, elles ont aussi été décrites pour le mpox en particulier chez les femmes enceintes pour le clade la |
|
| Formes classiques |
Elles se caractérisent par des lésions cutanées progressant de macules aux papules entre 2 à 5 mm, aux vésicules, aux pustules et enfin aux croûtes. |
Distribution centrifuge et périphérique des lésions très sensibles, pouvant atteindre les muqueuses. Lésions durant 14 à 21 jours. |
|
| Formes atypiques |
Présentation clinique faite de lésions très variables |
Des complications telles les atteintes oculaires, adénites, peuvent constituer des signes d’appel |
Formes cliniques du mpox
(adapté de [
27
,
43
]).
|
Plusieurs organes peuvent être atteints entraînant des complications, dont des surinfections bactériennes secondaires (courantes), le choc septique, les abcès cutanés ou sous-cutanés, les dermatites, des infections broncho-pulmonaires, une déshydratation sévère due aux vomissements et diarrhées, des ulcérations cornéennes pouvant entraîner une cécité, des encéphalites, et une malnutrition aiguë avec un taux de létalité pouvant aller de 10 % à 15 % pour le clade I [
3
].
Plusieurs autres fièvres éruptives, à savoir la varicelle, la dermatite allergique, l’eczéma herpétique, les dermatites herpétiformes, le tanapox, les dermatites varioliques causées par les Rickettsies, et le
Molluscum contagiosum
peuvent être confondues avec le mpox. Cependant, le plus souvent, le mpox est confondu avec la forme sévère et atypique de la varicelle, particulièrement dans les lieux où cette maladie n’a pas été mise en évidence pendant plusieurs années [
8
]. Les prélèvements utilisés pour confirmer le diagnostic comprennent les croûtes, les écouvillons des vésicules ou des sécrétions des lésions cutanées, les biopsies, les écouvillons oropharyngés et le sang [
28
]. Pour le virus MPXV, les tests de diagnostic moléculaire basés sur la PCR quantitative (qPCR) pour identifier les orthopoxvirus en général sont les plus souvent utilisés. La PCR en temps réel est préférée à la PCR classique, en raison du temps réduit d’analyse et de détection, ainsi que pour sa sensibilité et sa spécificité plus élevée. La valeur de quantification du cycle (Cq) ou le cycle seuil (Ct pour
cycle threshold
) confirme la présence du virus MPXV et permet d’estimer la charge virale [
44
]. Récemment, des tests génériques de PCR en temps réel pour le virus MPXV ont été mis au point pour le distinguer d’autres orthopoxvirus [
45
]. Des stratégies innovantes sont de plus en plus développées afin de permettre de réduire le temps d’analyse, de manipulation et le risque de contamination croisée, tout en misant sur les performances, l’accessibilité et la possibilité de déploiement dans des zones à ressources et énergie limitées. Le séquençage du virus MPXV a joué un rôle crucial dans la caractérisation des épidémies et reste en plein essor.
|
Vaccination et traitements Vaccination
La similarité génétique et antigénique entre orthopoxvirus, suggère qu’une protection croisée est possible. Ainsi, il a été rapporté que la vaccination antivariolique conférait près de 85 % de protection croisée contre le virus MPXV [
46
]. La majorité de la population mondiale actuelle n’est plus vaccinée contre la variole, du fait de l’arrêt de la vaccination suite à l’éradication du virus. Par conséquent, la susceptibilité aux orthopoxvirus n’a fait que croître avec le temps.
Trois vaccins ont été homologués contre le mpox : le vaccin modifié Ankara-BN (par ex, MVA-BN ou JYNNEOS, Imvamune ou Imvanex) à 2 doses, hautement atténué et non-réplicatif ; le LC16-KMB (homologué au Japon), et le OrthopoxVac (homologué dans la Fédération de Russie) [
47
]. Les deux premiers ont démontré une certaine efficacité. Un autre vaccin de deuxième génération, l’ACAM2000, confèrerait également une immunité croisée contre la variole et le mpox [
48
]. Actuellement, l’OMS ne recommande pas la vaccination de masse contre le mpox, les stocks étant limités. Celle-ci est proposée aux groupes les plus touchés et à haut risque [
28
].
Thérapies disponibles
En général, le traitement est symptomatique (antipyrétiques
5
, analgésiques et antiseptiques cutanés) et tient compte de la sévérité de la maladie. L’administration d’antalgiques adaptés au degré de la douleur est préférée aux anti-inflammatoires, qui sont proscrits ; le nettoyage et la désinfection des plaies et des muqueuses doivent être systématiques pour prévenir les complications liées aux surinfections bactériennes. Le maintien d’une hydratation et d’une nutrition optimales garantit un bon pronostic.
Les traitements antiviraux sont recommandés en cas de formes sévères et des études sont en cours afin de définir la meilleure stratégie. Les molécules approuvées sont le técovirimat, le cidofovir et le brincidofovir. L’immunoglobuline anti-vaccine a été approuvée pour les complications de la vaccination [
48
]. Les cibles thérapeutiques virales potentielles sont la thymidylate kinase, l’ADN ligase, le complexe trimère protéique (D13L ou OPG125), la protéine majeure de l’enveloppe (F13L ou OPG057, cible du técovirimat) et la cystéine protéinase (I7L) [
49
].
Le tecovirimat (TPOXX, ST-246
®
), utilisable par voie orale ou intraveineuse, n’a pas été concluant dans plusieurs essais cliniques comme l’essai PALM007 en RDC et STOMP dans plusieurs pays où circule le sousclade IIb. Les résultats de l’essai PALM007 montrent que le tecovirimat ne réduisait pas la durée des lésions du mpox chez les enfants et les adultes atteints de mpox comparé aux soins standards [
50
].
|
En conclusion, les déclarations d’urgence constituent un appel impérieux à plus de surveillance. De nombreuses inconnues subsistent concernant la maladie. Les mesures mises en place pour répondre à l’épidémie devraient prioritairement viser le contrôle de la transmission du virus. Par ailleurs, plus d’études sur le réservoir animal devraient être réalisées pour mieux comprendre la dynamique de transmission zoonotique du virus MPXV. Après le clade II, le clade I a été identifié en dehors de l’Afrique. Dans un contexte de transmissions zoonotiques continues, l’épidémie multi-pays de 2022 (sous-clade IIb), l’épidémie du sous-clade Ib, ainsi que l’émergence récente d’un variant du sous-clade Ia à Kinshasa en 2024, doivent faire craindre d’autres émergences présentant un risque épidémique. L’ère posturgence sera certainement impactée par les diverses interventions thérapeutiques et les contre-mesures, ce qui impose de maintenir la vigilance et de rendre le diagnostic plus accessible dans les zones endémiques. La surveillance doit être renforcée, tant dans la caractérisation moléculaire que dans les investigations sur les lieux d’émergence, car les ressources y sont souvent limitées et l’accès aux soins et au diagnostic reste difficile, malgré le nombre élevé de patients ayant besoin d’assistance. |
Footnotes |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
1.
Magnus
PV
,
Andersen
EK
,
Petersen
KB
,
et al.
.
A pox-like disease in cynomolgus monkeys.
.
Acta Pathol Microbiol Scand
.
1959;
;
46
:
:156.
–
76
.
2.
McInnes
CJ
,
Damon
IK
,
Smith
GL
,
et al.
.
ICTV Virus taxonomy profile: poxviridae 2023: This article is part of the ICTV Virus Taxonomy Profiles collection.
.
J Gen Virol
.
2023
;
:104.
.
3.
Gessain
A
,
Nakoune
E
,
Yazdanpanah
Y.
Monkeypox.
.
N Engl J Med
.
2022;
;
387
:
:1783.
–
93
.
4.
Yang
C-H
,
Song
A-L
,
Qiu
Y
,
et al.
.
Cross-species transmission and host range genes in poxviruses.
.
Virol Sin
.
2024;
;
39
:
:177.
–
93
.
5.
Kugelman
JR
,
Johnston
SC
,
Mulembakani
PM
,
et al.
.
Genomic variability of monkeypox virus among humans, Democratic Republic of the Congo.
.
Emerg Infect Dis
.
2014
;
:20.
.
6.
Shchelkunov
S
,
Totmenin
A
,
Babkin
I
,
et al.
.
Human monkeypox and smallpox viruses: Genomic comparison.
.
FEBS Lett
.
2001;
;
509
:
:66.
–
70
.
7.
Senkevich
TG
,
Yutin
N
,
Wolf
YI
,
et al.
.
Ancient gene capture and recent gene loss shape the evolution of orthopoxvirus-host interaction genes.
.
mBio
.
2021
;
:12.
:
10.1128/mbio.01495-21
.
8.
Sklenovská
N.
Monkeypox Virus.
. In :
Malik
YS
,
Singh
RK
,
Dhama
K
, editors.
Animal-origin viral zoonoses. Livestock diseases and management
.
.
Singapore:
:
Springer Singapore;
,
2020
:
:39.
–
68
.
9.
O’Toole
Á
,
Neher
RA
,
Ndodo
N
,
et al.
.
APOBEC3 deaminase editing in mpox virus as evidence for sustained human transmission since at least 2016.
.
Science
.
2023;
;
382
:
:595.
–
600
.
10.
Kinganda Lusamaki
E
,
Amuri Aziza
A
,
Fernandez Nunez
N
,
et al.
.
Clade I monkeypox virus genomic diversity in the Democratic Republic of the Congo, 2018-2024: Predominance of zoonotic transmission.
.
Cell
.
2024;
;
188
:
:4.
–
14
.
11.
Vakaniaki
EH
,
Kacita
C
,
Kinganda-Lusamaki
E
,
et al.
.
Sustained human outbreak of a new MPXV clade I lineage in eastern Democratic Republic of the Congo.
.
Nat Med
.
2024;
;
30
:
:2791.
–
5
.
12.
Nakazawa
Y
,
Mauldin
M
,
Emerson
G
,
et al.
.
A phylogeographic investigation of African monkeypox.
.
Viruses
.
2015;
;
7
:
:2168.
–
84
.
13.
Arita
I
,
Henderson
DA.
Smallpox and monkeypox in non-human primates.
.
Bull World Health Organ
.
1968;
;
39
:
:277.
–
83
.
14.
Patrono
LV
,
Pléh
K
,
Samuni
L
,
et al.
.
Monkeypox virus emergence in wild chimpanzees reveals distinct clinical outcomes and viral diversity.
.
Nat Microbiol
.
2020;
;
5
:
:955.
–
65
.
15.
Doty
J
,
Malekani
J
,
Kalemba
L
,
et al.
.
Assessing monkeypox virus prevalence in small mammals at the human–animal interface in the Democratic Republic of the Congo.
.
Viruses
.
2017;
;
9
:
:283.
.
16.
Jezek
Z
,
Fenner
F.
Human monkeypox.
. In:
Melnick
JL
ed.
Monographs in virology
.
.
Basel:
:
Karger publisher;
,
1988
:
:6.
–
32
.
17.
Hutin
YJF
,
Williams
RJ
,
Malfait
P
,
et al.
.
Outbreak of human monkeypox, Democratic Republic of Congo, 1996 to 1997.
.
Emerg Infect Dis
.
2001;
;
7
:
:434.
–
8
.
18.
Reynolds
MG
,
Carroll
DS
,
Olson
VA
,
et al.
.
A silent enzootic of an orthopoxvirus in Ghana, West Africa: evidence for multi-species involvement in the absence of widespread human disease.
.
Am Soc Trop Med Hyg
.
2010;
;
82
:
:746.
–
54
.
19.
Reed
KD
,
Melski
JW
,
Graham
MB
,
et al.
.
The detection of monkeypox in Humans in the western hemisphere.
.
N Engl J Med
.
2004;
;
350
:
:342.
–
50
.
20.
Moss
B.
Understanding the biology of monkeypox virus to prevent future outbreaks.
.
Nat Microbiol
.
2024;
;
9
:
:1408.
–
16
.
21.
Seang
S
,
Burrel
S
,
Todesco
E
,
et al.
.
Evidence of human-to-dog transmission of monkeypox virus.
.
Lancet
.
2022;
;
400
:
:658.
–
9
.
22.
Jones
KE
,
Patel
NG
,
Levy
MA
,
et al.
.
Global trends in emerging infectious diseases.
.
Nature
.
2008;
;
451
:
:990.
–
993
.
23.
McCollum
AM
,
Nakazawa
Y
,
Ndongala
GM
,
et al.
.
Human monkeypox in the Kivus, a conflict region of the Democratic Republic of the Congo.
.
Am Soc Trop Med Hyg
.
2015;
;
93
:
:718.
–
21
.
24.
Rimoin
AW
,
Mulembakani
PM
,
Johnston
SC
,
et al.
.
Major increase in human monkeypox incidence 30 years after smallpox vaccination campaigns cease in the Democratic Republic of Congo.
.
Proc Natl Acad Sci USA
.
2010;
;
107
:
:16262.
–
7
.
25.
Tamfum
J-JM
,
Kabamba
J
,
Likofata
J
,
et al.
.
Introduction of monkeypox into a community and household: risk factors and zoonotic reservoirs in the Democratic Republic of the Congo.
.
Am J Trop Med Hyg
.
2015;
;
93
:
:410.
–
5
.
26.
Jezek
Z
,
Grab
B
,
Szczeniowski
MV
,
et al.
.
Human monkeypox: secondary attack rates.
.
Bull World Health Organ
.
1988;
;
66
:
:465.
–
70
.
27.
Pittman
PR
,
Martin
JW
,
Kingebeni
PM
,
et al.
.
Clinical characterization and placental pathology of mpox infection in hospitalized patients in the Democratic Republic of the Congo.
.
PLoS Negl Trop Dis
.
2023;
;
17
:
:e0010384.
.
28.
Cabanillas
B
,
Murdaca
G
,
Guemari
A
,
et al.
.
A compilation answering 50 questions on monkeypox virus and the current Monkeypox outbreak.
.
Allergy
.
2023
; all.15633.
29.
Learned
LA
,
Reynolds
MG
,
Wassa
DW
,
et al.
.
Extended interhuman transmission of monkeypox in a hospital community in the republic of the congo, 2003.
.
Am J Trop Med Hyg
.
2005;
;
73
:
:428.
–
34
.
30.
Nolen
LD
,
Osadebe
L
,
Katomba
J
,
et al.
.
Extended human-to-human transmission during a monkeypox outbreak in the Democratic Republic ofthe Congo.
.
Emerg Infect Dis
.
2016;
;
22
:
:1014.
–
21
.
31.
Hutson
CL
,
Carroll
DS
,
Gallardo-Romero
N
,
et al.
.
Monkeypox disease transmission in an experimental setting: prairie dog animal model.
.
PLoS ONE
.
2011;
;
6
:
:e28295.
.
32.
Chastel
C.
Le monkeypox humain.
.
Pathol Biol
.
2009;
;
57
:
:175.
–
83
.
33.
Alakunle
E
,
Moens
U
,
Nchinda
G
,
et al.
.
Monkeypox virus in Nigeria: infection biology, epidemiology, and evolution.
.
Viruses
.
2020;
;
12
:
:1257.
.
34.
Bunge
EM
,
Hoet
B
,
Chen
L
,
et al.
.
The changing epidemiology of human monkeypox-a potential threat? A systematic review.
.
PLoS Negl Trop Dis
.
2022;
;
16
:
:e0010141.
.
35.
Formenty
P
,
Muntasir
MO
,
Damon
I
,
et al.
.
Human monkeypox outbreak caused by novel virus belonging to Congo Basin Clade, Sudan, 2005.
.
Emerg Infect Dis
.
2010;
;
16
:
:1539.
–
45
.
36.
Mauldin
MR
,
McCollum
AM
,
Nakazawa
YJ
,
et al.
.
Exportation of monkeypox virus from the African continent.
.
J Infect Dis
.
2022;
;
225
:
:1367.
–
76
.
37.
Berthet
N
,
Descorps-Declère
S
,
Besombes
C
,
et al.
.
Genomic history of human monkey pox infections in the Central African Republic between 2001 and 2018.
.
Sci Rep
.
2021;
;
11
:
:13085.
.
38.
Sklenovská
N
,
Van Ranst
M.
Emergence of monkeypox as the most important orthopoxvirus infection in humans.
.
Front Public Health
.
2018;
;
6
:
:241.
.
39.
Kibungu
E
,
Vakaniaki
E
,
Kinganda-Lusamaki
E
,
et al.
.
Clade I-associated mpox cases associated with sexual contact, the Democratic republic of the Congo.
.
Emerg Infect Dis J
.
2024
;
:30.
.
40.
Masirika
LM
,
Udahemuka
JC
,
Schuele
L
,
et al.
.
Ongoing mpox outbreak in Kamituga, South Kivu province, associated with monkeypox virus of a novel Clade I sub-lineage, Democratic Republic of the Congo, 2024.
.
Eurosurveillance
.
2024
;
:29.
.
41.
Foláyan
MO.
Mpox, stigma and the public health emergency of continental security declaration: addressing public health challenges in Africa.
.
J Public Health Afr
.
2024
;
:15.
.
42.
Wawina-Bokalanga
T
,
Merritt
S
,
Kinganda-Lusamaki
E
,
et al.
.
Epidemiology and phylogenomic characterization of distinct 2023 and 2024 mpox outbreaks in Kinshasa, Democratic Republic of the Congo-Evidence for increasingly sustained human-to-human transmission of subclade Ia.
.
medRxiv
.
2024
;
2024.11.15.24317404
.
43.
Georges
A-J
,
Matton
T
,
Courbot-Georges
M-C.
Le monkey-pox, un paradigme de maladie émergente puis réémergente.
.
Med Mal Infect
.
2004;
;
34
:
:12.
–
9
.
44.
Li
Y
,
Zhao
H
,
Wilkins
K
,
et al.
.
Real-time PCR assays for the specific detection of monkeypox virus West African and Congo Basin strain DNA.
.
J Virol Methods
.
2010;
;
169
:
:223.
–
7
.
45.
Shchelkunov
SN
,
Shcherbakov
DN
,
Maksyutov
RA
,
et al.
.
Species-specific identification of variola, monkeypox, cowpox, and vaccinia viruses by multiplex real-time PCR assay.
.
J Virol Methods
.
2011;
;
175
:
:163.
–
169
.
46.
Li
H
,
Huang
Q-Z
,
Zhang
H
,
et al.
.
The land-scape of immune response to monkeypox virus.
.
eBioMedicine
.
2023;
;
87
:
:104424.
.
47.
Pischel
L
,
Martini
BA
,
Yu
N
,
et al.
.
Vaccine effectiveness of 3
rd
generation mpox vaccines against mpox and disease severity: A systematic review and meta-analysis
.
.
Vaccine
.
2024;
;
42
:
:126053.
.
48.
Duarte
PM
,
Adesola
RO
,
Priyadarsini
S
,
et al.
.
Unveiling the global surge of mpox (monkeypox): A comprehensive review of current evidence.
.
Microbe
.
2024;
;
4
:
:100141.
.
49.
Patel
M
,
Adnan
M
,
Aldarhami
A
,
et al.
.
Current Insights into diagnosis, prevention strategies, treatment, therapeutic targets, and challenges of monkeypox (mpox) infections in human populations.
.
Life
.
2023;
;
13
:
:249.
.
50.
The PALM007 Writing Group.
.
Tecovirimat for clade I MPXV infection in the Democratic Republic of Congo.
.
N Engl J Med
.
2025;
;
392
:
:1484.
–
96
.
|