Modèles de maladies oculaires inflammatoires Le glaucome
Le glaucome est une maladie neurodégénérative progressive et multifactorielle qui constitue l’une des causes les plus fréquentes de cécité irréversible. Il a été estimé que le nombre de patients atteints de glaucome dans le monde passera de 76,5 millions en 2020 à 111,8 millions en 2040, principalement à cause du vieillissement de la population [
4
]. Dans 60 % à 70 % des cas, le glaucome se caractérise par la dégénérescence continue des cellules ganglionnaires de la rétine et par des lésions axonales causées par une augm entation de la pression intraoculaire, qui induisent des dommages au nerf optique (
Figure 1
) [
5
].
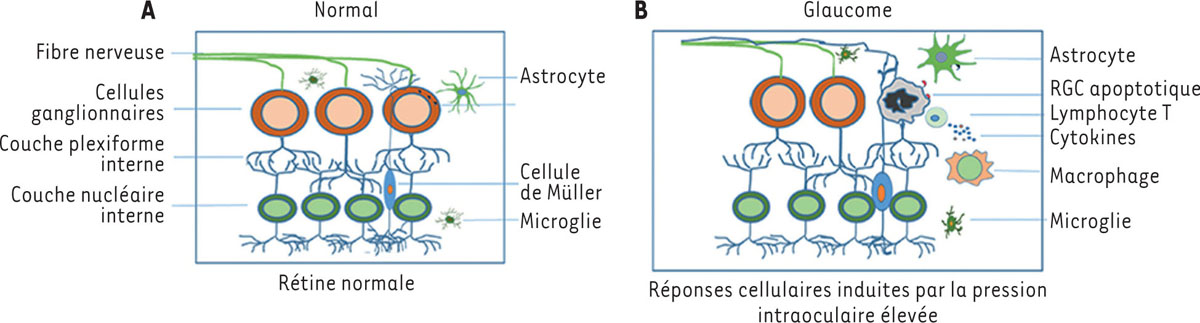
 | Figure 1.
Illustration schématique des réponses cellulaires induites par la pression intraoculaire élevée dans la rétine. A
.
Les cellules gliales résidentielles maintiennent l’homéostasie dans la rétine normale.
B
.
Dans la rétine glaucomateuse, une pression intraoculaire élevée régule à la hausse l’expression des protéines de choc thermique et déclenche les réponses immunitaires innées et adaptatives qui incluent l’activation microgliale et l’infiltration des lymphocytes T. Des réponses immunitaires soutenues et excessives conduisent à l’apoptose des cellules ganglionnaires rétiniennes (GC) et à une perte de vision [
53
] (figure originale sous licence CC BY 4.0.).
|
Dans des conditions physiologiques, des mécanismes vasculaires compensatoires, tels que l’autorégulation vasculaire (permettant aux vaisseaux rétiniens et choroïdiens d’ajuster leur c alibre en fonction de la pression de perfusion locale) et la régulation endothéliale (où l’endothélium vasculaire libère du monoxyde d’azote qui induit une vasodilatation locale ainsi que des prostaglandines et l’endothéline-1 qui participent à l’équilibre entre vasodilatation et vasoconstriction) peuvent contrebalancer les élévations de la pression intraoculaire. Chez les patients atteints de glaucome, ces mécanismes sont compromis et peuvent alors mener à des lésions d’ischémie reperfusion
3
et à de l’inflammation [
6
]. L’activité dérégulée des neurotransmetteurs dans la rétine conduit également à de l’excitotoxicité
4
avec, comme conséquence, la dysfonction des cellules ganglionnaires de la rétine. Le glaucome peut être classé comme un glaucome à angle ouvert ou un glaucome aigu par fermeture de l’angle, où l’angle irido-cornéen se ferme et empêche l’évacuation de l’humeur aqueuse qui est constamment produite, menant à une augmentation rapide de la pression intraoculaire [
7
]. Dans la forme ouverte, l’augmentation de la pression intraoculaire survient lorsque l’équilibre est rompu entre la sécrétion de l’humeur aqueuse de la chambre antérieure et son drainage, principalement réalisé par le trabéculum
5
. La dégénérescence du trabéculum, situé dans l’angle irido-cornéen, entraîne une accumulation de l’humeur aqueuse et une augmentation de la pression intraoculaire. Les mécanismes pathogéniques du processus dégénératif induit par le stress mécanique et vasculaire incluent l’ischémie reperfusion, la dysfonction mitochondriale, le stress oxydant chronique, l’excitotoxicité, le stress métabolique, la diminution des niveaux de nicotinamide, la déprivation en neurotrophines et la neuroinflammation [
8
]. Le stress oxydant, le dysfonctionnement mitochondrial et la sénescence cellulaire augmentent lorsque la rétine est vieillissante et sont les principaux facteurs de risque du glaucome [
9
]. Dans une rétine vieillissante, le stress oxydant et la peroxydation lipidique sont considérés comme la cause principale du stress tissulaire menant à l’activation d’une inflammation localisée d’intensité variable [
10
]. Les formes de glaucome à angle fermé, plus rares, sont causées par des défauts structurels du globe oculaire qui entraînent un blocage ultérieur de l’humeur aqueuse vers la chambre antérieure [
7
].
Afin de recréer
in vitro
les conséquences d’une pression intraoculaire élevée pendant une période limitée, plusieurs travaux rapportent l’utilisation de chambres pressurisées en thermoplastique avec un flux d’air/CO
2
connecté à un contrôleur de pression. Plusieurs types cellulaires ont été employés pour des expériences sous pression hydrostatique élevée : cellules neuronales B35
6,
, PC12
7,
, cellules gliales de Müller
8
, cellules microgliales et astrocytes de nerfs optiques humains [
11
,
12
]. Plusieurs études en chambres pressurisées ont démontré des dommages aux cellules neuronales B35 et PC12 menant à l’apoptose [
13
]. Il est également possible d’induire une pression hydrostatique élevée par l’immersion de cellules dans des colonnes remplies de milieu de culture et fabriquées sur mesure. Les cellules contrôles sont mises en culture dans le même volume de milieu mais dans des colonnes placées de façon horizontale. Dans ces conditions, il a été possible d’exposer des astrocytes à des pressions élevées sur une période allant jusqu’à 5 jours et de simuler la prolifération et la migration cellulaires en combinaison avec la production de fibres d’élastine solubles déjà observées dans le remodelage tissulaire causé par le glaucome [
14
]. Une version tridimensionnelle du trabéculum a été reconstruite par génie tissulaire et a été utilisée dans des conditions prolongées de stress oxydant afin d’étudier les changements moléculaires induits par une exposition quotidienne au peroxyde d’hydrogène. Dans ces conditions, il a été possible d’étudier l’activité métabolique des cellules, la variation d’expression et d’organisation de l’actine, l’expression de gènes pro-inflammatoires, l’expression de protéines pro- et anti-apoptotiques, la scission de PARP-1, et l’activation de la voie NF-κB [
15
].
Dégénérescence maculaire liée à l’âge
La dégénérescence maculaire liée à l’âge (DMLA) est une maladie multifactorielle, avec des facteurs de risque liés à l’âge, à l’environnement, au mode de vie et à la génétique. Elle est la première cause de cécité chez les personnes âgées de plus de 60 ans [
16
]. Avec le vieillissement, les cellules de l’épithélium pigmentaire rétinien (EPR) voient leur capacité à métaboliser les photorécepteurs diminuer, ce qui provoque un stress oxydatif local délétère pour la rétine. Le vieillissement de l’épithélium pigmentaire rétinien favorise également l’accumulation des drusen
9,
entre l’épithélium pigmentaire rétinien et la membrane de Bruch
10
. La formation de ces druses résulte d’un mélange de débris non digérés par l’épithélium pigmentaire rétinien et d’une inflammation chronique de faible intensité, impliquant le système du complément, des cellules immunitaires et des médiateurs inflammatoires [
17
]
(→)
.
(→) Voir
m/s
n° 12, 2023, page 958
Dans les stades précoces et intermédiaires de la maladie, des débris lipoprotéiques d’une taille croissante, en fonction du stade de la maladie (précoce et intermédiaire), sont retrouvés sous ou au-dessus de l’épithélium pigmentaire rétinien. En fonction de leur position, en dessous ou au-dessus de l’épithélium pigmentaire rétinien, ces drusen sont qualifiés de mous ou réticulés, respectivement. Dans les stades avancés, la DMLA se manifeste par une zone d’atrophie comprenant la mort de photorécepteurs et l’épithélium pigmentaire rétinien, appelée atrophie géographique, ou par la croissance de vaisseaux sanguins dans la macula, appelée DMLA néovasculaire. Lorsque ces nouveaux vaisseaux fuient, il est alors question de DMLA néovasculaire exsudative [
18
] (
Figure 2
).
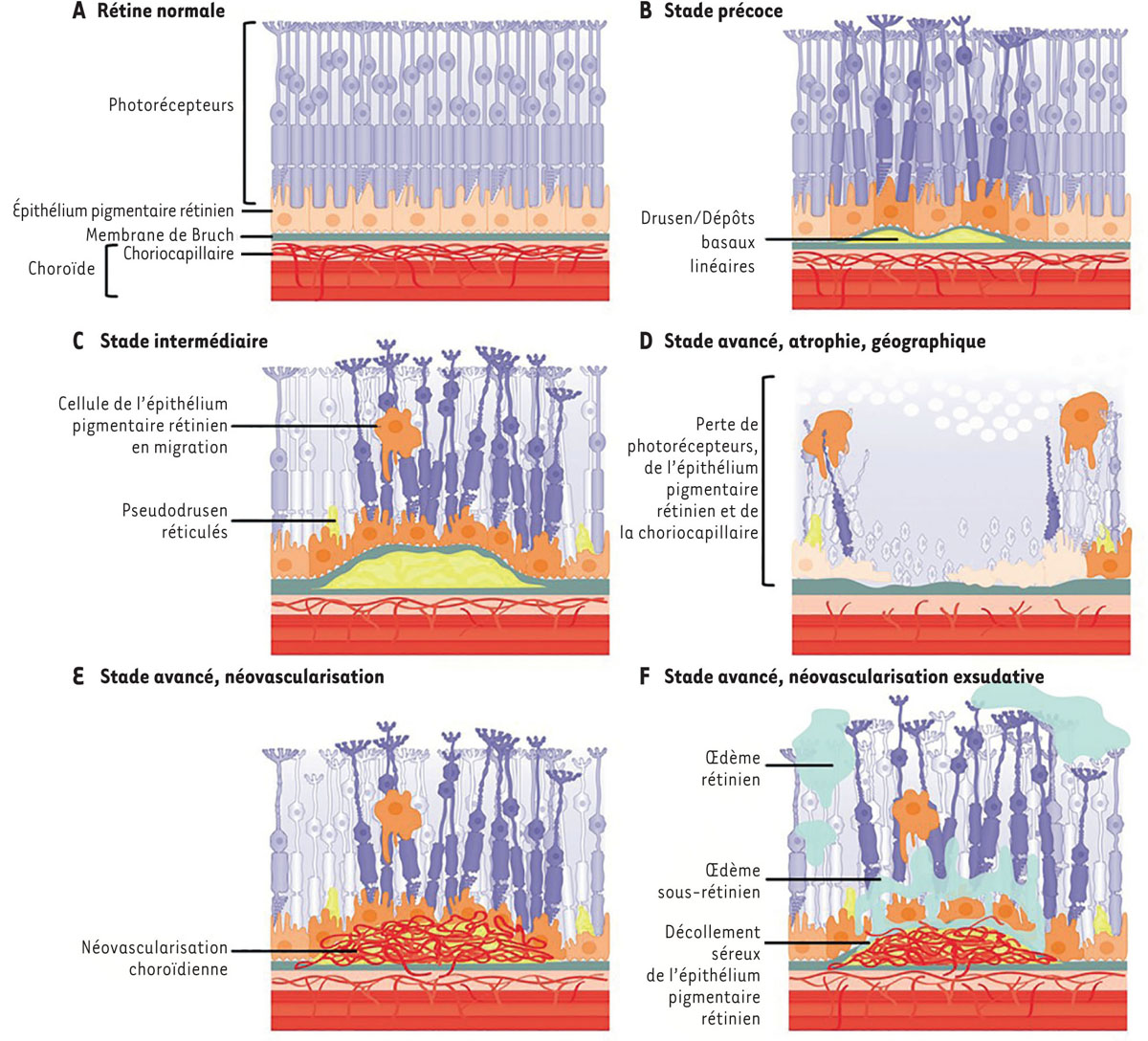
 | Figure 2.
Manifestions évolutives de la DMLA. A
.
Schéma d’une rétine saine comprenant la membrane de Bruch et la choroïde.
B
et
C
.
Stades précoce et intermédiaire de la DMLA, où des drusens ou des dépôts basaux linéaires et des pseudo-drusen réticulés sont observés. Des changements pathologiques de l’épithélium pigmentaire rétiniens surviennent, comprenant la migration de cellules de l’épithélium pigmentaire rétinien vers la rétine.
D
.
Stade avancé de la DMLA, atrophie géographique caractérisée par la perte de photorécepteurs, de cellules de l’épithélium pigmentaire rétinien et de la couche choriocapillaire.
E
.
Stade avancé de la DMLA, de néovascularisation, caractérisé par l’invasion de nouveaux vaisseaux sanguins provenant de la choroïde vers la paroi externe de la membrane de Bruch.
F
.
Stade avancé de la DMLA, de néovascularisation exsudative, qui survient lorsque les nouveaux vaisseaux sanguins exsudent ou saignent, causant des œdèmes et/ou des hémorragies (figure [
54
] traduite de l’anglais avec la permission de Springer Nature).
|
Anciennement, on distinguait deux types de DMLA : la forme sèche, caractérisée par une perte progressive des photorécepteurs et de l’épithélium pigmentaire rétinien, et la forme humide, reconnaissable par la naissance de nouveaux vaisseaux sanguins anormaux sous ou dans la rétine [
19
]
(→)
.
(→) Voir
m/s
n° 2, 2007, page 127
Les traitements à base d’anti-VEGF pour la DMLA néovasculaire exsudative ont mis en lumière différents stades évolutifs de la maladie [
20
]
(→)
.
(→) Voir
m/s
n° 12, 2009, page 1 105
De ce fait, des distinctions ne sont faites que dans les stades avancés de DMLA.
Parmi les multiples facteurs impliqués dans la DMLA, cette synthèse se concentre sur la dimension inflammatoire de cette maladie. Plusieurs médiateurs pro-inflammatoires, comme l’IL-1β, l’IL-6 (interleukine-6), le TNF-α (t
umor necrosis factor
) et la CCL2 (
chemokine ligand 2
), et plusieurs facteurs génétiques, comme un variant du gène codant le facteur H du complément, qui inhibe la voie principale de résolution de l’inflammation, sont impliqués dans la dégénérescence maculaire [
21
]
(→)
.
(→) Voir
m/s
n° 10, 2020, page 886
Des cellules rétiniennes, primaires ou immortalisées, soumises à des modulateurs chimiques de l’inflammation et du stress oxydant sont employées pour mimer,
in vitro
, la DMLA [
22
]. En effet, des cellules primaires de l’épithélium pigmentaire rétinien peuvent être isolées de fœtus décédés entre 18 et 20 semaines de gestation. Ce modèle cellulaire a été utilisé afin d’investiguer les effets protecteurs d’un inhibiteur d’histone désacétylases, la trichostatine A (TSA), contre le stress oxydant induit par le peroxyde d’hydrogène. De faibles concentrations de TSA ont permis de réduire le niveau des protéines HIF-1α (
hypoxia inducible factor-1α
) et VEGF (
vascular endothelial growth factor
), impliquées dans la signalisation de l’inflammation et de l’angiogenèse, respectivement [
22
].
D’autres molécules actives avec des propriétés anti-inflammatoires et anti-angiogéniques, comme le resvératrol et ses dérivés, sont aussi testées,
in vitro
, sur des cellules de l’épithélium pigmentaire rétinien immortalisées ARPE-19. Cette famille de molécules protège les cellules ARPE-19 contre les dommages oxydants induits par le peroxyde d’hydrogène et l’inflammation stimulée par les lipopolysaccharides (LPS) via la réduction des cytokines pro-inflammatoires IL-6 et IL-8 [
23
]. Le potentiel anti-angiogénique de ces molécules a été mesuré par l’inhibition de la sécrétion de VEGF-α. La lignée cellulaire ARPE-19, des lignées cellulaires murines, des cellules humaines de l’épithélium pigmentaire rétinien, des cellules microvasculaires endothéliales et des macrophages, modèles dans lesquels l’inflammation a été stimulée par l’ajout de TNF-α, ont été mises en culture séparément pour valider les effets anti-inflammatoires de l’astaxanthine
11
sur les différents types cellulaires. L’astaxanthine a conduit à une suppression significative de la néovascularisation choroïdienne. Les mécanismes cellulaires et moléculaires impliqués dans les effets de l’astaxanthine incluent une inhibition de l’infiltration des macrophages lors de la néovascularisation choroïdienne, et une réduction de l’inflammation dans l’épithélium pigmentaire rétinien-choroïde. Le traitement a aussi mené à l’inhibition de l’activation de la voie de signalisation NF-κB. En l’absence d’inhibition, la voie NF-κB active la transcription de gènes
ICAM-1
(
intercellular adhesion molecule
),
MCP-1
(monocyte chemoattractant protein-1) et
IL-6
. L’inhibition de la voie NF-κB avec un inhibiteur de la translocation nucléaire de la protéine p65 (un composant de NF-κB) a mené à la suppression de la néovascularisation expérimentale. L’un des rôles des macrophages dans la néovascularisation consiste à sécréter du VEGF au niveau du site lésé, où l’épithélium pigmentaire rétinien et les cellules endothéliales produisent MCP-1, qui permet de recruter les macrophages. Le traitement par l’inhibiteur de NF-kB a réduit de façon significative la sécrétion d’IL-6 et de VEGFR-1, conduisant à une réduction de la néovascularisation. Dans les cellules humaines ARPE-19, la sécrétion de MCP-1 a été réduite, alors que dans les cellules murines, ce sont les niveaux protéiques de MCP-1, d’ICAM-1 et de VEGFR-2 qui ont diminué [
24
].
La lignée cellulaire RF/6A, composée des cellule de l’endothélium choroïdien dérivées de singes rhésus (
Macaca mulatta
), est aussi employée dans des études,
in vitro
, pour étudier les effets de plusieurs facteurs de croissance liés à la DMLA (thrombine, facteur de croissance dérivé des plaquettes [PDGF], facteur de croissance analogue à l’insuline [ILGF] et VEGF) sur la synthèse des protéoglycanes [
25
]. Les protéoglycanes peuvent promouvoir l’accumulation de druses et ainsi induire l’inflammation. Les facteurs de croissance précédemment nommés, à l’exception du VEGF, induisent la synthèse du protéoglycanes [
25
]. Cette même lignée cellulaire a été traitée avec du chlorure de cobalt pour créer des conditions hypoxiques qui miment les conditions inflammatoires de la DMLA [
26
]. L’expression de la protéine d’échafaudage RACK1, le récepteur de la kinase C-1 activée, qui déclenche l’angiogenèse a été examinée [
26
]. Une augmentation simultanée de l’expression des gènes
RACK1
,
HIF-1α
, et
VEGF
a été observée. Ces modèles
in vitro
peuvent facilement être modulés et manipulés, offrant ainsi un moyen efficace pour tester des gammes complètes de paramètres expérimentaux, notamment les réponses aux différentes molécules actives, et le comportement cellulaire en conditions de stress.
Des cellules de l’épithélium pigmentaire rétinien de porcs d’abattoir ont été aussi prélevées et mises en culture. Dans ces cultures, du
N
-rétinylidène-
N
-rétinyléthanolamine (A2E) a été ajouté afin d’induire de l’inflammation et de l’angiogenèse, via la transactivation des gènes cellulaires par le récepteur nucléaire de l’acide rétinoïque RAR-α. Dans ce modèle, la norbixine inhibe partiellement la transactivation de RAR-α induite par l’A2E et réduit l’expression de molécules stimulées par l’A2E, qui sont impliquées dans l’angiogenèse et l’inflammation et qui sont critiques dans l’évolution de la DMLA [
27
].
Un modèle de choroïde obtenu par génie tissulaire a été conçu pour répliquer le stroma choroïdien dans la DMLA en employant des fibroblastes de choroïde humaine assemblés dans une matrice extracellulaire. Des cellules de l’épithélium pigmentaire rétinien, des cellules endothéliales de cordon ombilical humain et des mélanocytes choroïdiens ont ensuite été ensemencées à la surface de la matrice extracellulaire produite. Alors que les cellules de l’épithélium pigmentaire rétinien se développent en deux dimensions, les cellules de cordon ombilical sont en mesure de former des structures tubulaires qui génèrent un réseau vasculaire complexe, permettant potentiellement d’étudier les effets de différents agents anti-angiogéniques et anti-inflammatoires [
28
].
Un autre élément clé de la DMLA est représenté par les cellules microgliales, qui participent à l’inflammation et qui migrent dans les espaces sous-rétiniens. Les lignées de cellules de l’épithélium pigmentaire rétinien mises en culture avec du milieu conditionné par des cellules microgliales activées, montrent une accumulation de lipides, de l’autophagie et l’expression de gènes pro-inflammatoires, comme l’
IL-6
, l’
IL-8
, le
GM-CSF
(
granulocyte-macrophage colony-stimulating factor
), l’
IL-1β
et le
CCL-2
(
C-C motif chemokine ligand 2
) [
29
]. De plus, des cellules primaires de l’épithélium pigmentaire rétinien en coculture avec des cellules microgliales activées par des lipopolysaccharides bactériens pro-inflammatoires sécrètent plus de cytokines pro-inflammatoires, produisent moins de protéines de jonctions, de RPE65 (
retinal pigment epithelium-specific 65 kDa protein
) et présentent une altération de leur morphologie cellulaire [
30
].
Rétinopathie diabétique
La rétinopathie diabétique est une complication majeure du diabète et constitue la cause principale de déficience visuelle dans la population en âge de travailler dans le monde [
31
]. Parmi les complications microvasculaires du diabète, comme les néphropathies et les neuropathies, la rétinopathie diabétique demeure la plus fréquente. Cette maladie est catégorisée en fonction de la présence de lésions vasculaires visibles à l’ophtalmoscope. Le premier stade de la maladie est le stade non-prolifératif, caractérisé par une tortuosité vasculaire, des hémorragies rétiniennes, des microanévrismes et des exsudats lipidiques. Ce stade est suivi par un stade prolifératif, où de nouveaux vaisseaux fragiles et aberrants se développent (
Figure 3
) [
32
]. La prise en compte de l’œdème maculaire diabétique, caractérisé par une accumulation de liquide dans la rétine interne, entraînant un épaississement anormal de celle-ci, constitue un élément majeur dans la classification des rétinopathies diabétiques. Les œdèmes maculaires diabétiques peuvent survenir à tous les stades de sévérité des rétinopathies diabétiques, prolifératives ou non-prolifératives [
33
]. Les traitements actuels par injections intravitréennes de VEGF, parfois combinées à une thérapie par laser, sont seulement offerts pour les stades avancés de la maladie lorsque des dommages substantiels sont déjà survenus aux capillaires rétiniens.
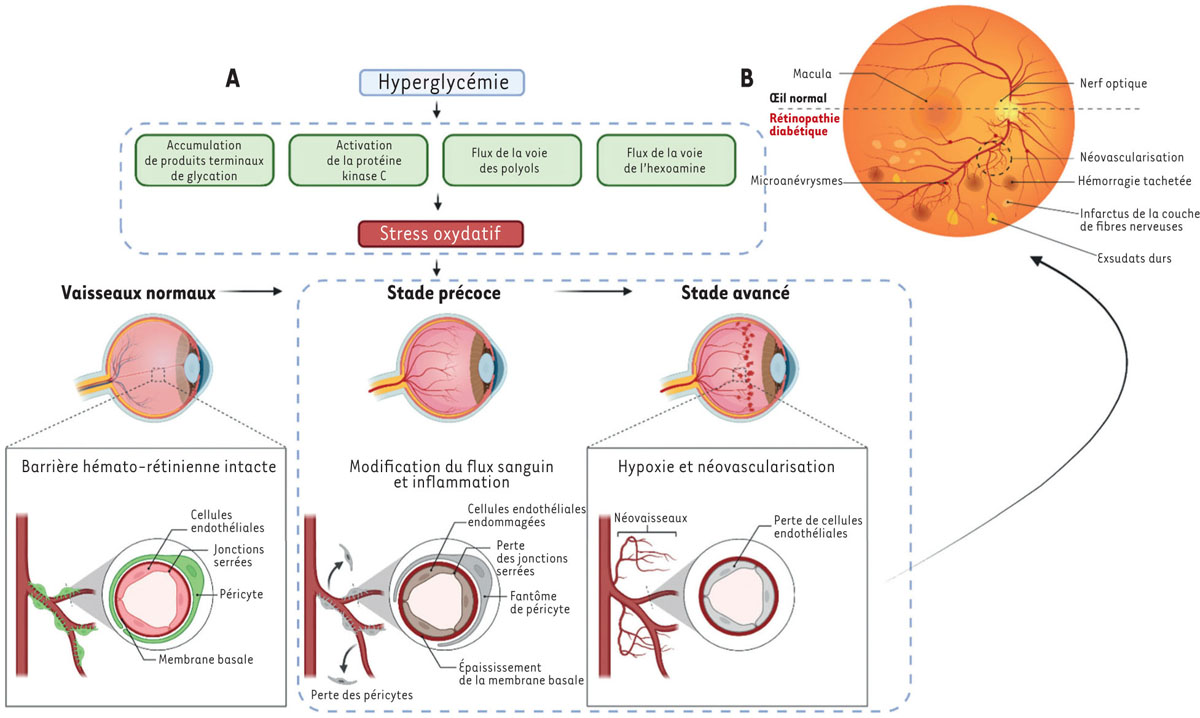
 | Figure 3.
A
.
L’hyperglycémie chronique dans le diabète entraîne une régulation positive de plusieurs voies de signalisation, dont la voie des polyols (
via
l’enzyme aldose réductase), la voie de la protéine kinase C (PKC, particulièrement l’isoforme PKC-β), la voie de biosynthèse de l’hexosamine, ainsi que l’activation de la production de produits terminaux de glycation avancée (AGEs). Ces AGEs interagissent avec leur récepteur (RAGE), activant des voies pro-inflammatoires et pro-oxydantes. Parallèlement, des enzymes telles que NADPH oxydase (NOX), iNOS (
inducible nitric oxide synthase
), et COX-2 (cyclo-oxygénase-2) sont activées, contribuant à un stress oxydant important. Celui-ci déclenche la pathogenèse de la rétinopathie diabétique, caractérisée par une perte de cellules endothéliales vasculaires, de jonctions serrées et de péricytes, avec un épaississement de la membrane basale, conduisant finalement à une hypoxie rétinienne, qui stimule la production de VEGF, favorisant la néovascularisation.
B
.
Il est possible d’observer des hémorragies, des exsudats secs dans la couche plexiforme externe, des infarctus de la couche de fibres nerveuses et des microanévrysmes chez un patient avec une rétinopathie diabétique [
55
] (figure traduite de l’anglais sous licence CC BY 4.0).
|
Le développement de thérapies pour le stade précoce, qui pourraient ralentir ou empêcher le développement de la maladie, constitue un objectif important. Démêler les aspects multifactoriels du diabète, notamment l’hyperglycémie chronique, la dérégulation métabolique et, à terme, l’hypoxie tissulaire, contribuera au développement de nouvelles cibles thérapeutiques [
34
]. Les capillaires rétiniens sont composés d’une couche interne de cellules endothéliales rétiniennes microvasculaires, avec des jonctions serrées, formant la barrière hémato-rétinienne interne, et de péricytes
12
rétiniens périvasculaires qui s’enroulent autour des cellules endothéliales, et qui ont un rôle structural et de signalisation [
35
]. Cette configuration permet le passage étroitement régulé de substances provenant du sang vers les tissus environnants métaboliquement très actifs, et inversement. La perte de contact entre les cellules endothéliales, assuré en conditions saines par des jonctions serrées, des jonctions adhérentes et des jonctions communicantes, joue un rôle majeur dans le dysfonctionnement capillaire rétinien et, finalement, dans la rupture de la barrière hémato-rétinienne. L’épaississement de la membrane basale et la perte des péricytes caractérisent le stade précoce de la rétinopathie diabétique. La perturbation structurale et fonctionnelle des péricytes rétiniens est impliquée dans le dysfonctionnement des cellules endothéliales et dans la progression de la maladie. Cependant, la chronologie des altérations des voies de signalisation, de la rupture de la barrière hémato-rétinienne, du remodelage de la matrice extracellulaire et de la mort cellulaire n’est pas encore totalement comprise. Le VEGF et l’angiopoïétine-2 (Ang-2) ont des implications majeures dans la progression de la rétinopathie diabétique (non-proliférative vers proliférative) [
35
]. Le profil de sécrétion du VEGF et d’Ang-2, ainsi que celui de plusieurs autres protéines impliquées dans le stress oxydant, l’angiogenèse, l’hyperglycémie et l’inflammation [
34
], est spécifique de chaque type cellulaire.
Puisque la raison principale pour laquelle la rétinopathie diabétique progresse est l’angiogenèse, plusieurs modèles cellulaires,
in vitro
, utilisent des cellules endothéliales pour imiter ce processus [
36
]. Les cellules endothéliales les plus utilisées sont les cellules endothéliales rétiniennes bovines [
37
], les cellules endothéliales rétiniennes humaines [
38
] et les cellules endothéliales rétiennes et choroïdiennes (RF/6a) de singes rhésus [
39
]. Cependant, des cellules endothéliales non-spécifiques à la rétine sont également utilisées afin de se concentrer davantage sur l’aspect angiogenèse de la rétinopathie. Les cellules endothéliales non-spécifiques à la rétine employées incluent des cellules endothéliales de la veine ombilicale humaines [
40
], des cellules endothéliales microvasculaires humaines [
41
] et des cellules endothéliales microvasculaires dermiques humaines [
42
]. Les cellules sont traitées avec de fortes doses de glucose de manière à imiter les conditions diabétiques. Le mécanisme ciblé dans ces études,
in vitro
, utilisant les cellules endothéliales est le processus d’angiogenèse. Ainsi, le biomarqueur souvent suivi au cours des expériences est le VEGF. Cependant, plusieurs autres marqueurs d’intérêt sont analysés : les protéines de la matrice extracellulaire et celles impliquées dans les voies de signalisation du stress oxydant, de l’inflammation et de l’apoptose [
43
].
D’autres types cellulaires utilisés dans les modèles
in vitro
sont spécifiques à la rétine, comme les péricytes, les fibroblastes, les macrophages, les cellules gliales et les cellules gliales de Müller [
44
]. Les cellules gliales sont d’importants soutiens du tissu neuronal, qui facilitent la communication entre les vaisseaux sanguins et les neurones. La relation entre les volets vasculaire et neuronal de la rétinopathie diabétique est généralement explorée lorsque des cellules gliales sont employées [
45
]. Parmi toutes les cellules gliales, les cellules gliales de Müller sont les plus couramment employées pour étudier la rétinopathie diabétique [
43
]. Il est donc essentiel d’analyser les profils de sécrétion des cellules en coculture lors de la modélisation in vitro de la rétinopathie diabétique. En particulier, des cellules microvasculaires endothéliales rétiniennes humaines ont été mises en coculture avec des péricytes de rétine humaine pendant plus de 21 jours dans l’objectif de pouvoir observer les différences dans le profil de sécrétion entre les conditions diabétiques et les conditions normales. Les conditions hypoxiques et hyperglycémiques ont généré des profils de sécrétion angiogéniques et inflammatoires différents pour les cellules en monoculture ou en coculture, mettant en évidence l’intérêt de ce dernier modèle [
46
]. Des cellules de l’épithélium pigmentaire rétinien ont aussi été mises en culture avec des cellules souches mésenchy-mateuses adipeuses présentant un phénotype différencié en péricytes, dans des conditions hyperglycémiques. Une augmentation des jonctions adhérentes et des jonctions serrées, ainsi qu’une réduction des niveaux d’ARNm des cytokines inflammatoires TNF-α, IL-1β et MMP-9 (métalloprotéinase matricielle 9) ont été observées dans les péricytes différenciés [
47
].
Il est aussi possible de modéliser les différentes étapes de l’angiogenèse, processus présent dans la rétinopathie diabétique proliférative, en intégrant : la prolifération des cellules endothéliales, leur migration, l’invasion de la matrice extracellulaire et l’angiogenèse. Ces modèles emploient des lignées cellulaires microvasculaires et macrovasculaires de l’endothélium [
48
]. Des cellules de cordon ombilical humain ont été largement employées afin d’étudier la capacité du VEGF-Trap
13
, et des anticorps monoclonaux bévacizumab et du ranibizumab d’inhiber la prolifération, la migration, l’activation des récepteurs, et la signalisation cellulaire des cellules endothéliales, induites par le VEGF [
49
].
Pour étudier les dysfonctions survenant dans la rétinopathie diabétique au niveau de la barrière hématorétinienne, cette structure a été modélisée avec des cellules de l’épithélium pigmentaire rétinien humain et des cellules vasculaires humaines, séparées par une membrane amniotique obtenue lors de césariennes chez des donneuses, dans le but de mimer la membrane de Bruch [
50
]. Une membrane de Bruch artificielle peut aussi être obtenue en utilisant de la fibroïne, une protéine de soie, qui pourrait être une bonne candidate comme support de culture de cellules de l’épithélium pigmentaire rétinien [
51
].
|
1.
Kaur
G
,
Singh
NK.
The role of inflammation in retinal neurodegeneration and degenerative diseases.
.
Int J Mol Sci
.
2022;
;
2022
:
:386.
.
2.
Kaur
G
,
Singh
NK.
Inflammation and retinal degenerative diseases.
.
Neural Regen Res
.
2023;
;
2023
:
:513.
–
8
.
3.
Ahmad
A
,
Ahsan
H.
Biomarkers of inflammation and oxidative stress in ophthalmic disorders.
.
J Immunoassay Immunochem
.
2020;
;
2020
:
:257.
–
71
.
4.
Tham
Y-C
,
Li
X
,
Wong
TY
,
et al.
.
Global prevalence of glaucoma and projections of glaucoma burden through 2040: a systematic review and meta-analysis.
.
Ophthalmology
.
2014;
;
2014
:
:2081.
–
90
.
5.
Weinreb
RN
,
Aung
T
,
Medeiros
FA.
The pathophysiology and treatment of glaucoma: a review.
.
JAMA
.
2014;
;
2014
:
:1901.
–
11
.
6.
Vohra
R
,
Tsai
JC
,
Kolko
M.
The role of inflammation in the pathogenesis of glaucoma.
.
Surv Ophthalmol
.
2013;
;
2013
:
:311.
–
20
.
7.
Killer
HE
,
Pircher
A.
Normal tension glaucoma: review of current understanding and mechanisms of the pathogenesis.
.
Eye
.
2018;
;
2018
:
:924.
–
30
.
8.
Vohra
R
,
Dalgaard
LM
,
Vibæk
J
,
et al.
.
Potential metabolic markers in glaucoma and their regulation in response to hypoxia.
.
Acta Ophthalmol
.
2019;
;
2019
:
:567.
–
76
.
9.
Sreekumar
PG
,
Hinton
DR
,
Kannan
R.
The emerging role of senescence in ocular disease.
.
Oxid Med Cellr Longev
.
2020;
;
2020
:
:2583601.
.
10.
Pinazo-Durán
MD
,
Gallego-Pinazo
R
,
García-Medina
JJ
,
et al.
.
Oxidative stress and its downstream signaling in aging eyes.
.
Clin Interv Aging
.
2014;
;
2014
:
:637.
–
52
.
11.
Liu
Q
,
Ju
W-K
,
Crowston
JG
,
et al.
.
Oxidative stress is an early event in hydrostatic pressure–induced retinal ganglion cell damage.
.
IOVS
.
2007;
;
2007
:
:4580.
–
9
.
12.
Yu
J
,
Zhong
Y
,
Cheng
Y
,
et al.
.
Effect of high hydrostatic pressure on the expression of glutamine synthetase in rat retinal Müller cells cultured in vitro.
.
Exp Ther Med
.
2011;
;
2011
:
:513.
–
6
.
13.
Tök
L
,
Nazıroğlu
M
,
Uğuz
AC
,
Tök
Ö.
Elevated hydrostatic pressures induce apoptosis and oxidative stress through mitochondrial membrane depolarization in PC12 neuronal cells: acell culture model of glaucoma.
.
J Recept Signal Transduct
.
2014;
;
2014
:
:410.
–
6
.
14.
Hernandez
MR
,
Pena
JDO
,
Selvidge
JA
,
et al.
.
Hydrostatic pressure stimulates synthesis of elastin in cultured optic nerve head astrocytes.
.
Glia
.
2000;
;
2000
:
:122.
–
36
.
15.
Saccà
SC
,
Tirendi
S
,
Scarfì
S
,
et al.
.
An advanced in vitro model to assess glaucoma onset.
.
ALTEX
.
2020;
;
2020
:
:265.
–
74
.
16.
Wang
Y
,
Zhong
Y
,
Zhang
L
,
et al.
.
Global incidence, progression, and risk factors of age-related macular degeneration and projection of disease statistics in 30 years: a modeling study.
.
Gerontology
.
2021;
;
2021
:
:721.
–
35
.
17.
Pierre
M
,
Lamaa
D
,
Fabre
M
,
et al.
.
Traitement topique de la dégénérescence maculaire liée à l’âge.
.
Med Sci (Paris)
.
2023;
;
2023
:
:958.
–
66
.
18.
Fleckenstein
M
,
Schmitz-Valckenberg
S
,
Chakravarthy
U.
Age-Related Macular Degeneration: A Review.
.
JAMA
.
2024;
;
2024
:
:147.
–
57
.
19.
Behar-Cohen
F
,
Sennlaub
F
,
Berdugo
M.
Espoirs thérapeutiques dans la dégénérescence maculaire liée à l’âge.
.
Med Sci (Paris)
.
2007;
;
2007
:
:127.
–
9
.
20.
Leveziel
N
,
Soubrane
G
,
Souied
EH.
Anti-VEGF : applications pratiques en ophtalmologie.
.
Med Sci (Paris)
.
2009;
;
2009
:
:1105.
–
7
.
21.
Roubeix
C
,
Sahel
J-A
,
Guillonneau
X
,
et al.
.
Sur les origines inflammatoires de la DMLA.
.
Med Sci (Paris)
.
2020;
;
2020
:
:886.
–
92
.
22.
Chan
N
,
He
S
,
Spee
CK
,
et al.
.
Attenuation of choroidal neovascularization by histone deacetylase inhibitor.
.
PLOS One
.
2015;
;
2015
:
:e0120587.
.
23.
Losso
JN
,
Truax
RE
,
Richard
G.
Trans-resveratrol inhibits hyperglycemia-induced inflammation and connexin downregulation in retinal pigment epithelial cells.
.
J Agric Food Chemi
.
2010;
;
2010
:
:8246.
–
52
.
24.
Izumi-Nagai
K
,
Nagai
N
,
Ohgami
K
,
et al.
.
Inhibition of choroidal neovascularization with an anti-inflammatory carotenoid astaxanthin.
.
IOVS
.
2008;
;
2008
:
:1679.
–
85
.
25.
Al Gwairi
O
,
Osman
N
,
Getachew
R
,
et al.
.
Multiple growth factors, but not VEGF, stimulate glycosaminoglycan hyperelongation in retinal choroidal endothelial cells.
.
Intl J Biol Sci
.
2016;
;
12
.
26.
Liu
X
,
Zhu
M
,
Yang
X
,
et al.
.
Inhibition of RACK1 ameliorates choroidal neovascularization formation in vitro and in vivo.
.
Exp Mol Pathol
.
2016;
;
2016
:
:451.
–
9
.
27.
Fontaine
V
,
Fournié
M
,
Monteiro
E
,
et al.
.
A2E-induced inflammation and angiogenesis in RPE cells in vitro are modulated by PPAR-α, -β/δ, -γ, and RXR antagonists and by norbixin.
.
Aging (Albany NY)
.
2021;
;
2021
:
:22040.
–
58
.
28.
Djigo
AD
,
Bérubé
J
,
Landreville
S
,
Proulx
S.
Characterization of a tissue-engineered choroid.
.
Acta Biomater
.
2019;
;
2019
:
:305.
–
16
.
29.
Nebel
C
,
Aslanidis
A
,
Rashid
K
,
Langmann
T.
Activated microglia trigger inflammasome activation and lysosomal destabilization in human RPE cells.
.
BBRC
.
2017;
;
2017
:
:681.
–
6
.
30.
Ma
W
,
Zhao
L
,
Fontainhas
AM
,
et al.
.
Microglia in the mouse retina alter the structure and function of retinal pigmented epithelial cells: a potential cellular interaction relevant to AMD.
.
PLOS One
.
2009;
;
2009
:
:e7945.
.
31.
Yau
JWY
,
Rogers
SL
,
Kawasaki
R
,
et al.
.
Global prevalence and major risk factors of diabetic retinopathy.
.
Diabetes care
.
2012;
;
2012
:
:556.
–
64
.
32.
Frey
T
,
Antonetti
DA.
Alterations to the blood-retinal barrier in diabetes: cytokines and reactive oxygen species.
.
Antioxid Redox Signal
.
2011;
;
2011
:
:1271.
–
84
.
33.
Zhang
X
,
Zeng
H
,
Bao
S
,
et al.
.
Diabetic macular edema: new concepts in patho-physiology and treatment.
.
Cell Biosci
.
2014;
;
2014
:
:1.
–
14
.
34.
Rübsam
A
,
Parikh
S
,
Fort
PE.
Role of inflammation in diabetic retinopathy.
.
Int J Mol Sci
.
2018;
;
2018
:
:942.
.
35.
Stitt
AW
,
Curtis
TM
,
Chen
M
,
et al.
.
The progress in understanding and treatment of diabetic retinopathy.
.
Prog Retin Eye Res
.
2016;
;
2016
:
:156.
–
86
.
36.
Kim
M-K
,
Kim
S-G
,
Lee
SK.
4-Hexylresorcinol induced angiogenesis potential in human endothelial cells.
.
Maxillofac Plast Reconstr Surg
.
2020;
;
2020
:
:23.
.
37.
Durham
JT
,
Dulmovits
BM
,
Cronk
SM
,
et al.
.
Pericyte chemomechanics and the angiogenic switch: insights into the pathogenesis of proliferative diabetic retinopathy?
IOVS
.
2015;
;
2015
:
:3441.
–
59
.
38.
Gong
Y
,
Fu
Z
,
Edin
ML
,
et al.
.
Cytochrome P450 oxidase 2C inhibition adds to ω-3 long-chain polyunsaturated fatty acids protection against retinal and choroidal neovascularization.
.
Arterioscler Thromb Vasc Biol
.
2016;
;
2016
:
:1919.
–
27
.
39.
Yu
Z
,
Zhang
T
,
Gong
C
,
et al.
.
Erianin inhibits high glucose-induced retinal angiogenesis via blocking ERK1/2-regulated HIF-1α-VEGF/VEGFR2 signaling pathway.
.
Sci Rep
.
2016;
;
2016
:
:34306.
.
40.
Johnen
S
,
Djalali-Talab
Y
,
Kazanskaya
O
,
et al.
.
Antiangiogenic and neurogenic activities of sleeping beauty-mediated PEDF-transfected RPE cells in vitro and in vivo.
.
BioMed Res Int
.
2015;
;
2015
:
:863845.
.
41.
Spuul
P
,
Daubon
T
,
Pitter
B
,
et al.
.
VEGF-A/Notch-induced podosomes proteolyse basement membrane collagen-IV during retinal sprouting angiogenesis.
.
Cell Rep
.
2016;
;
2016
:
:484.
–
500
.
42.
Siemerink
MJ
,
Hughes
MR
,
Dallinga
MG
,
et al.
.
CD34 promotes pathological epi-retinal neovascularization in a mouse model of oxygen-induced retinopathy.
.
PLOS One
.
2016;
;
2016
:
:e0157902.
.
43.
Sadikan
MZ
,
Abdul Nasir
NA
,
Lambuk
L
,
et al.
.
Diabetic retinopathy: a comprehensive update on in vivo, in vitro and ex vivo experimental models.
.
BMC Ophthalmol
.
2023;
;
2023
:
:421.
.
44.
Bergers
G
,
Song
S.
The role of pericytes in blood-vessel formation and maintenance.
.
Neuro-Oncol
.
2005;
;
2005
:
:452.
–
64
.
45.
Rungger–Brändle
E
,
Dosso
AA
,
Leuenberger
PM.
Glial reactivity, an early feature of diabetic retinopathy.
.
IOVS
.
2000;
;
2000
:
:1971.
–
80
.
46.
Eyre
JJ
,
Williams
RL
,
Levis
HJ.
A human retinal microvascular endothelial-pericyte co-culture model to study diabetic retinopathy in vitro.
.
Exp Eye Res
.
2020;
;
2020
:
:108293.
.
47.
Lupo
G
,
Agafonova
A
,
Cosentino
A
,
et al.
.
Protective effects of human pericyte-like adipose-derived mesenchymal stem cells on human retinal endothelial cells in an in vitro model of diabetic retinopathy: evidence for autologous cell therapy.
.
Int J Mol Sci
.
2023;
;
2023
:
:913.
.
48.
Stryker
ZI
,
Rajabi
M
,
Davis
PJ
,
Mousa
SA.
Evaluation of angiogenesis assays.
.
Biomedicines
.
2019;
;
2019
:
:37.
.
49.
Papadopoulos
N
,
Martin
J
,
Ruan
Q
,
et al.
.
Binding and neutralization of vascular endothelial growth factor (VEGF) and related ligands by VEGF Trap, ranibizumab and bevacizumab.
.
Angiogenesis
.
2012;
;
2012
:
:171.
–
85
.
50.
Hamilton
RD
,
Leach
L.
Isolation and properties of an in vitro human outer blood-retinal barrier model.
.
Methods Mol Biol
.
2011
:
:401.
–
16
.
51.
Galloway
CA
,
Dalvi
S
,
Shadforth
AMA
,
et al.
.
Characterization of human iPSC-RPE on a prosthetic Bruch’s membrane manufactured from silk fibroin.
.
IOVS
.
2018;
;
2018
:
:2792.
–
800
.
52.
Raîche-Marcoux
G
,
Guérin
S
,
Boisselier
É.
Modèles cellulaires des maladies inflammatoires du segment antérieur de l’œil.
.
Med Sci (Paris)
.
2025;
;
2025
:
:327.
–
35
.
53.
Jiang
S
,
Kametani
M
,
Chen
DF.
Adaptive Immunity: New Aspects of Pathogenesis Underlying Neurodegeneration in Glaucoma and Optic Neuropathy.
.
Front Immunol
.
2020;
;
11
:
:65.
.
54.
Fleckenstein
M
,
Keenan
TDL
,
Guymer
RH
,
et al.
.
Age-related macular degeneration.
.
Nat Rev Dis Primers
.
2021;
;
2021
:
:31.
.
55.
Chauhan
MZ
,
Rather
PA
,
Samarah
SM
,
et al.
.
Current and novel therapeutic approaches for treatment of diabetic macular edema.
.
Cells
.
2022;
;
2022
:
:1950.
.
|