Les myopathies inflammatoires autoimmunes sont caractérisées par la présence d’autoanticorps, qui définissent leur expression clinique et leur profil évolutif [ 1 – 4 ]. Comme pour les autres maladies auto-immunes, la plupart de ces autoanticorps ciblent des composants intracellulaires [ 1 , 5 ].
La pathogénicité de certains autoanti-corps présents dans des maladies auto-immunes comme le lupus érythémateux systémique, les vascularites à anticorps dirigés contre un antigène du cytoplasme des granulocytes neutrophiles ( anti-neutrophil cytoplasmic antigen , ANCA), ou certaines maladies neurologiques, néphrologiques ou endocrinologiques, a pu être établie par transfert de ces autoanticorps humains à la souris, lorsque ce transfert reproduit la maladie humaine, ou par l’efficacité d’un traitement visant à éliminer ces anticorps du sang des patients (par échange plasmatique) ou à empêcher leur production (en utilisant l’anticorps monoclonal rituximab dirigé contre les lymphocytes B) [ 6 ]. Dans le cas des myosites autoimmunes, la question de la pathogénicité des autoanticorps n’est pas résolue. Les résultats d’une étude récente ont cependant permis de préciser l’effet de certains de ces autoanticorps grâce à une analyse transcriptomique de cellules musculaires saines cultivées en leur présence [ 7 ].
L’identification des autoanticorps présents dans les myopathies inflammatoires autoimmunes, soit par la technique ELISA ( enzyme-linked immunosorbent assay ), soit par une technique d’ immunoblot (avec détection enzymatique ou par chimioluminescence) [ 8 ], permet un diagnostic non invasif de ces maladies, sans qu’une biopsie musculaire soit désormais nécessaire [ 1 , 5 , 6 ]. La détection de ces autoanticorps, qui appartiennent majoritairement à la classe des immunoglobulines G (IgG), permet de classer les myopathies inflammatoires autoimmunes en quatre groupes : myosite à inclusion, myosite de chevauchement avec le syndrome des anti-synthétases, dermatomyosites, et myosites nécrosantes auto-immunes [ 4 ].
Certains autoanticorps sont « spécifiques » des myosites : anti-SRP ( signal recognition particle ) et anti-HMGCR (3-hydroxy-3-méthylglutaryl-CoA réductase) pour les myosites nécrosantes auto-immunes ; anti-Mi-2 (Mi-2α et Mi-2β), anti-TIF1γ ( transcription intermediary factor 1γ ), anti-NXP2 (nucléoprotéine 2), anti-SAE1 ( SUMO-activating enzyme 1 ), et anti-MDA5 ( melanoma differentiation-associated protein 5 ) pour les dermatomyosites ; anti-Jo-1 (histidyl-tRNA synthétase), anti-PL-7 (thréonyl-tRNA synthétase), anti-PL-12 (alanyl-tRNA synthétase), anti-EJ (glycyl-tRNA synthétase), et anti-OJ (isoleucyl-tRNA synthétase) pour le syndrome des anti-synthétases appartenant aux myosites de chevauchement [ 1 , 5 ]. En revanche, d’autres autoanticorps sont simplement « associés » à une atteinte musculaire accompagnant l’atteinte auto-immunitaire d’autres organes (poumons, cœur, peau, etc.) : anti-PM/Scl (75 ou 100) pour la polymyosite/sclérodermie, anti-Ku pour les connectivites/myosite-sclérodermie, anti-Ro52/SSA-52 pour les maladies multi-organes [ 2 , 5 ].
Un autre intérêt de la détection des autoanticorps spécifiques dans le sang des personnes atteintes de myopathie auto-immune est de suivre l’évolution de la maladie, dont ils constitueraient un marqueur de l’activité (corrélation avec la force musculaire ou avec la concentration d’une enzyme musculaire spécifique dans le sang, la créatine kinase) [ 6 , 9 ]. Cependant, bien que la présence des signes cliniques de myosite soit corrélée à celle de ces autoanticorps, certains patients n’ayant pas d’autoanticorps identifiés ont pourtant des signes cliniques comparables à ceux des patients qui en produisent. L’effet pathogénique de ces autoanticorps n’est donc pas prouvé. D’autre part, leurs cibles sont majoritairement intracellulaires (cytoplasmiques ou nucléaires), ce qui pose la question de l’entrée de ces anticorps dans la cellule musculaire pour y exercer de possibles effets.
Les chercheurs ont d’abord analysé des biopsies musculaires issues de personnes atteintes de myopathie autoimmune, par microscopie confocale avec immunomarquage des IgG. Ils en ont conclu que les autoanticorps présents chez ces patients s’accumulaient dans le même compartiment subcellulaire que les molécules contre lesquelles ils étaient dirigés. Ils ont ensuite déterminé le profil transcriptomique des cellules musculaires de ces biopsies, par un séquençage nucléotidique de leurs ARN, à la recherche des gènes surexprimés ou sous-exprimés. Enfin et surtout, en cultivant des cellules musculaires saines en présence d’autoanticorps issus de certains de ces patients (anti-Mi2, anti-Pm/Scl, ou anti-ARN-t-synthétase), ils ont constaté que le profil transcriptomique de ces cellules était similaire à celui précédemment obtenu par l’analyse des biopsies musculaires. De plus, l’inhibition pharmacologique de la cible antigénique de l’anticorps anti-ARNt-synthétase dans les cellules en culture a provoqué la même altération du transcriptome que cet autoanticorps. À noter que l’entrée des anticorps dans les cellules en culture a été facilitée par une électroporation, et qu’aucun effet de ces autoanticorps sur le transcriptome n’a été constaté in vitro en l’absence d’électroporation ( Figure 1 ).
| Figure 1.
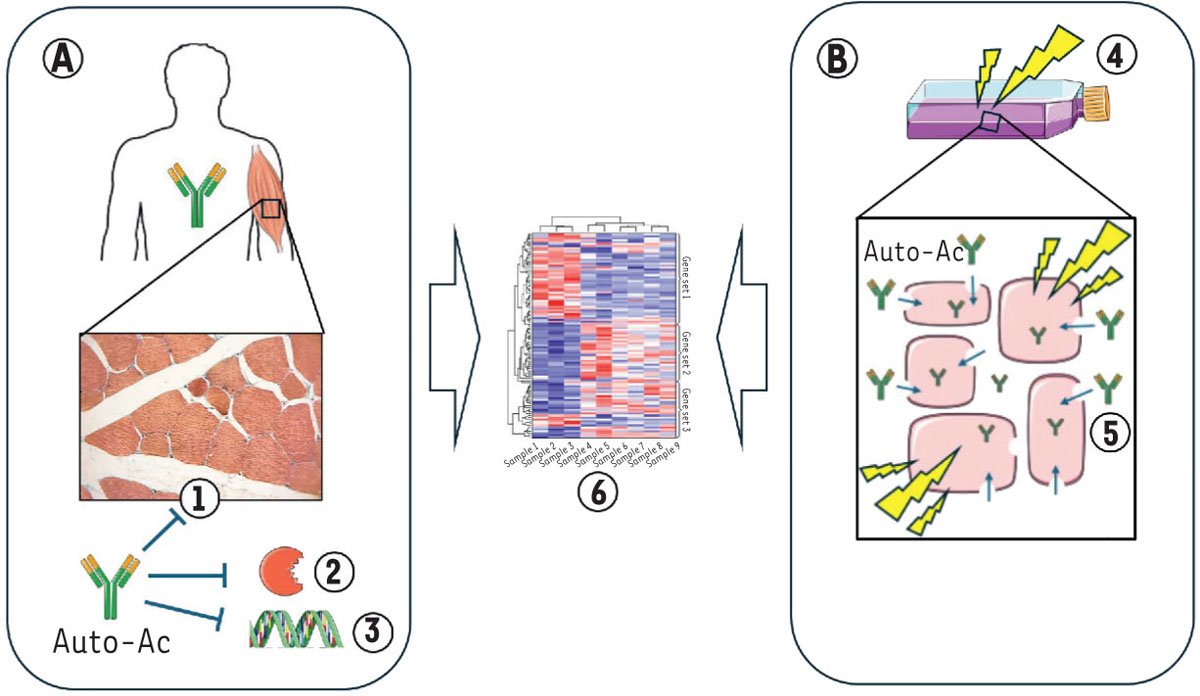
Schéma du protocole expérimental. A
.
Une analyse transcriptomique (6) de biopsies musculaires effectuées chez des personnes atteintes de myopathie inflammatoire autoimmune a permis de déterminer les conséquences transcriptomiques des effets supposés des auto-anti-corps (auto-Ac) présents sur leurs cellules musculaires : destruction « directe » de ces cellules et inhibition de leur régénération (1), inhibition enzymatique (2), ou action directe sur la transcription de certains gènes (3).
B
.
Les chercheurs ont cultivé des cellules musculaires saines en présence des auto-Ac (4). Lorsque la pénétration de ces auto-Ac dans les cellules a été favorisée par une électroporation (5), et seulement dans ce cas, l’expérience a produit des résultats transcriptomiques (6) similaires à ceux de l’analyse des biopsies musculaires des patients.
|
Il convient de relever de potentiels biais méthodologiques dans les expériences précédentes. Les conclusions de l’observation des biopsies musculaires par microscopie confocale sont limitées d’une part, par la technique d’immunofluorescence utilisée, qui ne permettait pas de s’assurer de la visualisation des autoanticorps spécifiques puisque les auteurs ont immunomarqué toutes les IgG, et d’autre part, par la structure-même des cellules musculaires, dont le cytoplasme est très mince et proche des parois membranaires, ce qui rend difficile la mise en évidence de la colocalisation des autoanticorps et des molécules contre lesquelles ils sont dirigés. Par ailleurs, pour tester l’effet des autoanticorps dans les cultures de cellules musculaires, les chercheurs ont utilisé les IgG totales extraites des sérums des patients, parmi lesquelles se trouvent peut-être d’autres anticorps, encore non identifiés, qui pourraient également participer à la dérégulation du transcriptome in vivo . Il conviendrait donc de répéter ces expériences in vitro après purification des autoanticorps spécifiques des myosites. De plus, l’hypothèse physiopathologique d’une cytotoxicité dépendante du système du complément, qui pourrait être activé par les autoanticorps pathogènes, n’a pas pu être testée avec les conditions expérimentales utilisées, en raison de l’électroporation des cellules pour y faire pénétrer les anticorps. Le recours à ce mode artificiel de pénétration des immunoglobulines dans les cellules musculaires ne fournit par ailleurs aucune indication sur le mécanisme par lequel les autoanticorps peuvent franchir la membrane plasmique de ces cellules in vivo . Malgré ces réserves, la reproduction in vitro , sur des cellules musculaires en culture mises en présence des autoanticorps des patients, d’un profil transcriptomique similaire à celui des biopsies musculaires de ces patients permet de faire l’hypothèse de certains mécanismes physiopathologiques communs.
Ces résultats ouvrent la voie à des thérapies ciblant directement les autoanticorps présents chez les patients : diminution de leur production par les plasmocytes en utilisant l’anticorps monoclonal anti-CD20 (rituximab), diminution de leur demi-vie en bloquant le récepteur néonatal du fragment Fc des IgG, FcRn [ 10 ] ( → ), par l’efgartigimod, ou épuration du sang par échanges plasmatiques [ 6 ]. On peut aussi envisager le développement de thérapies plus spécifiques, fondées sur les données transcriptomiques issues de la présente étude. Enfin, une future caractérisation des voies de signalisation activées ou réprimées par les autoanticorps pathogènes ( e.g ., voie de l’interféron, voie du complément) pourrait également permettre d’orienter les stratégies thérapeutiques dans les myopathies inflammatoires autoimmunes.
(→) Voir m/s n° 12, 2009, page 1 053