| |
| Med Sci (Paris). 41(8-9): 640–642. doi: 10.1051/medsci/2025085.MITD1 inhibe la réplication des flavivirus neurotropes dans les cellules microgliales Jim Zoladek,1 Marion Cannac,1 and Sébastien Nisole1* 1Institut de recherche en infectiologie de Montpellier (IRIM), Université de Montpellier, CNRS UMR9004
,
Montpellier
,
France |
Les flavivirus neurotropes
Parmi les virus capables d’infecter le système nerveux central figurent plusieurs flavivirus neurotropes, tels que le virus du Nil occidental (virus
West Nile
), le virus Usutu, le virus Zika, le virus de l’encéphalite japonaise et le virus de l’encéphalite à tiques. Transmis par des arthropodes hématophages, ces virus peuvent provoquer des maladies neurologiques graves chez l’homme, notamment des encéphalites et des méningites, associées à une mortalité élevée et à des séquelles neurologiques chez les survivants. Le virus de la dengue, le flavivirus le plus répandu dans le monde, peut lui aussi être associé à de graves complications neurologiques, bien qu’il ne soit pas considéré comme un virus neurotrope.
À la suite de la piqûre d’un moustique infecté ou d’une tique infectée, ces virus pénètrent dans l’organisme par la peau, dans laquelle ils commencent à se répliquer avant de se disséminer dans le reste du corps. Leur capacité à traverser la barrière hémato-encéphalique permet à ces flavivirus neurotropes d’accéder au système nerveux central et de s’y propager. L’infection des neurones perturbe leur fonctionnement et entraîne leur mort, ce qui déclenche une réponse immunitaire libérant des cytokines et d’autres médiateurs inflammatoires dans le cerveau. Ce mécanisme est à l’origine d’un cercle vicieux, dans lequel l’inflammation et la destruction des neurones s’entretiennent mutuellement, intensifiant ainsi les lésions cérébrales [
1
].
|
Caractéristiques et réplication des flavivirus Les flavivirus sont de petits virus enveloppés, dont le génome est constitué d’un ARN monocaténaire de polarité positive codant une unique polyprotéine. Après l’entrée du virus dans ses cellules cibles par endocytose, le génome viral est libéré dans le cytoplasme et directement traduit en polyprotéine, qui est ensuite clivée pour produire les protéines virales fonctionnelles. Celles-ci forment alors des invaginations au sein du réticulum endoplasmique, dans lesquelles l’ARN viral est répliqué et où les nouvelles particules virales sont assemblées. Enfin, les virions nouvellement formés sont libérés par exocytose après leur maturation dans l’appareil de Golgi. |
De la peau au cerveau, l’immunité antivirale innée joue un rôle crucial dans le contrôle de la dissémination des flavivirus au sein de l’organisme. Ce système de défense particulièrement efficace permet de limiter la propagation virale, ce qui explique pourquoi la grande majorité des infections sont asymptomatiques ou causent des symptômes pseudogrippaux bénins. Le chef d’orchestre de cette immunité antivirale innée est l’interféron, une famille de cytokines sécrétées par les cellules infectées, et qui déclenchent l’expression de centaines de gènes dans les cellules infectées et les cellules environnantes. Ces gènes induits par l’interféron produisent des protéines puissamment antivirales, qui bloquent la réplication de tous les virus connus [
2
]. Pour échapper à ce mécanisme de défense, les flavivirus ont développé de multiples stratégies pour contrecarrer la réponse interféron, et ainsi favoriser leur propagation [
3
].
|
Les cellules microgliales
Les cellules microgliales sont les principales cellules immunitaires résidentes du cerveau. Elles jouent un rôle essentiel dans la surveillance immunitaire et l’homéostasie du système nerveux central. Si un virus atteint le cerveau, ce sont les cellules microgliales qui assurent la protection des neurones en éliminant les particules virales et en coordonnant les réponses interféron et inflammatoire. Ainsi, des souris dépourvues de microglie sont plus sensibles à l’infection par les flavivirus neurotropes [
4
].
Si les cellules microgliales assurent notamment la protection des autres cellules cérébrales
via
la production d’interféron, leur propre intégrité dépend également de l’interféron. En effet, tandis que les neurones constituent les principales cellules cibles des flavivirus neurotropes dans le cerveau, ce sont les cellules microgliales qui sont préférentiellement infectées chez des souris dépourvues de réponse interféron [
5
]. Ce constat suggère que les cellules microgliales expriment des gènes stimulés par l’interféron qui assurent leur résistance aux infections flavivirales, préservant ainsi leur intégrité et, par conséquent, celle du cerveau.
|
MITD1
, un gène anti-flavivirus stimulé par l’interféron dans la microglie
Nous avons récemment réalisé un crible de plus de 1 000 gènes activés par l’interféron afin d’identifier lesquels inhibent la réplication des flavivirus neurotropes. Parmi les plus efficaces, nous avons identifié le gène codant MITD1 (
microtubule interacting and trafficking domain containing 1
), une protéine sans activité antivirale connue [
6
]. La seule fonction connue de MITD1 était son implication dans la mitose, au cours de laquelle MITD1 recrute les protéines du complexe ESCRT-III (
endosomal sorting complex required for transport
) dans les corps intermédiaires qui relient les deux cellules filles, permettant l’abscission [
7
]. Afin de déterminer comment MITD1 inhibe la réplication des flavivirus, dont le virus du Nil occidental, le virus Zika et le virus de la dengue, nous avons commencé par rechercher dans quelles cellules sa production était induite par l’interféron. Cependant, contrairement aux principaux gènes stimulés par l’interféron connus, nous ne sommes pas parvenus à identifier une lignée cellulaire répondant à ce critère. En éva
luant l’expression de
Mitd1
dans différents organes de souris infectées par le virus Usutu, nous avons découvert qu’elle n’était induite que dans le cerveau. La quantification de l’expression de
Mitd1
en réponse à l’interféron dans les neurones, astrocytes, oligodendrocytes et cellules microgliales, a ensuite montré que cette expression était induite exclusivement dans les cellules microgliales (
Figure 1A
). Enfin, l’inhibition de la production de MITD1 dans des cellules microgliales humaines traitées ou non par l’interféron, suivie de la mesure de la réplication du virus du Nil occidental dans ces cellules, a permis de confirmer que MITD1 constitue un effecteur clé de l’activité antivirale de l’interféron contre les flavivirus neurotropes dans la microglie.
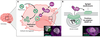 | Figure 1.
MITD1 bloque la réplication des flavivirus dans les cellules microgliales en séquestrant certaines protéines du complexe ESCRT-III. A
.
En réponse à l’interféron (IFN-I), l’expression de
MITD1
est induite dans les cellules microgliales, ce qui inhibe la réplication virale. Ce phénomène est observable par microscopie et se traduit par une diminution de la quantité d’ARN viral (en vert) dans les cellules exprimant
MITD1
(en rose).
B
.
Les flavivirus exploitent le complexe ESCRT-III pour former des usines virales au sein du réticulum endoplasmique. MITD1 interagit avec certaines protéines de ce complexe, comme CHM1B et CHMP4B, ce qui entraîne leur relocalisation au sein d’agrégats membranaires, limitant ainsi leur accessibilité au virus. La relocalisation de CHMP4B (en vert) induite par MITD1 (en rose) est particulièrement frappante, puisque l’on observe, par microscopie confocale, la formation d’agrégats circulaires de CHMP4B, qui encerclent des gouttelettes lipidiques.
|
|
Mécanisme d’inhibition des flavivirus par MITD1
En plus de leur rôle au cours de la mitose, les protéines ESCRT interviennent dans de multiples fonctions cellulaires impliquant des remodelages membranaires [
8
]. De nombreux virus exploitent la machinerie ESCRT à leur propre avantage, comme les virus enveloppés qui l’utilisent notamment pour assurer leur bourgeonnement [
9
]. Dans le cas des flavivirus, certaines protéines CHMP (
charged multivesicular body proteins
), membres du complexe ESCRT-III, sont relocalisées dans les invaginations du réticulum endoplasmique où se déroule la réplication de l’ARN viral, et participent directement à la biogenèse de ces usines de réplication virale [
10
]. Nous nous sommes donc demandé si, comme pendant la mitose, MITD1 était capable d’interagir avec des protéines ESCRT-III et de perturber la formation des usines virales. Nous avons choisi d’évaluer le rôle de CHMP1B, CHMP2A et CHMP4B, car ces trois protéines interagissent avec MITD1 [
7
] et sont impliquées dans la réplication des flavivirus [
10
]. Par des expériences de co-immunoprécipitation, nous avons d’abord pu confirmer que MITD1 est capable d’interagir avec ces trois protéines CHMP [
6
]. En revanche, en observant leur localisation subcellulaire, nous nous sommes aperçus que la surexpression de MITD1 entraînait une relocalisation spécifique de CHMP1B et CHMP4B, sans affecter celle de CHMP2A. Plus spécifiquement, MITD1 entraîne une agrégation de CHMP1B et CHMP4B dans des régions du cytoplasme riches en lipides. Cette relocalisation est particulièrement marquée dans le cas de CHMP4B, qui se retrouve agrégée autour de gouttelettes lipidiques [
6
] (
Figure 1B
). Nous avons ensuite évalué si ces trois protéines participent à la formation des usines virales, notamment dans les cellules microgliales. En utilisant des ARN interférents, nous avons montré que CHMP4B est essentielle à la biogenèse des sites de réplication virale, tandis que CHMP1B joue un rôle plus modeste et que CHMP2A n’est pas indispensable [
6
].
Les résultats de ces expériences suggéraient donc que MITD1 était capable d’empêcher la formation des usines virales en séquestrant CHMP4B et CHMP1B. Nous avons pu confirmer cette hypothèse en infectant des cellules microgliales humaines en culture primaire par le virus du Nil occidental, dans lesquelles nous avons montré que les protéines ESCRT-III étaient localisées à proximité des ARN viraux en cours de réplication, mais que la surexpression de
MITD1
entraînait la séquestration de CHMP4B et CHMP1B et leur relocalisation hors des sites de réplication [
6
] (
Figure 1B
).
|
Nous avons donc identifié un nouveau facteur antiviral, MITD1, capable d’inhiber la réplication des flavivirus neurotropes dans les cellules microgliales, les principales sentinelles antivirales du cerveau. Bien que les raisons exactes de cette spécificité cellulaire demeurent inconnues, il n’est pas surprenant que l’expression de
MITD1
, en raison de son rôle essentiel dans la division cellulaire, soit uniquement induite dans des cellules quiescentes, telles que les cellules microgliales.
Étant donné l’importance des protéines ESCRT-III dans la réplication de tous les virus, en particulier pour le bourgeonnement des virus enveloppés [
8
,
9
], MITD1 pourrait avoir une activité antivirale beaucoup plus large. Nous avons pu montrer que MITD1 inhibe également la réplication du virus Chikungunya [
6
], un arbovirus de la famille des
Togaviridae
qui peut également infiltrer le système nerveux central [
11
]. D’autres études seront nécessaires pour déterminer l’étendue de l’activité antivirale de MITD1.
|
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
1.
Chambers
TJ
,
Diamond
MS.
Pathogenesis of flavivirus encephalitis.
.
Adv Virus Res
.
2003;
;
60
:
:273.
–
342
.
2.
Schoggins
JW.
Interferon-stimulated genes: What do they all do?
Annu Rev Virol
.
2019;
;
6
:
:567.
–
84
.
3.
Zoladek
J
,
Nisole
S.
Mosquito-borne flaviviruses and type I interferon: catch me if you can!
Front Microbiol
.
2023;
;
14
:
:1257024.
.
4.
Seitz
S
,
Clarke
P
,
Tyler
KL.
Pharmacologic depletion of microglia increases viral load in the brain and enhances mortality in murine models of flavivirus-induced encephalitis.
.
J Virol
.
2018;
;
92
:
:e00525.
–
18
.
5.
Chotiwan
N
,
Rosendal
E
,
Willekens
SMA
,
et al.
.
Type I interferon shapes brain distribution and tropism of tick-borne flavivirus.
.
Nat Commun
.
2023;
;
14
:
:2007.
.
6.
Zoladek
J
,
Cannac
M
,
Seite
M
,
et al.
.
MITD1 is a brain-specific interferon-inducible factor that inhibits flavivirus replication.
.
Proc Natl Acad Sci USA
.
2025;
;
122
:
:e2502064122.
.
7.
Lee
S
,
Chang
J
,
Renvoisé
B
,
et al.
.
MITD1 is recruited to midbodies by ESCRT-III and participates in cytokinesis.
.
Mol Biol Cell
.
2012;
;
23
:
:4347.
–
61
.
8.
Vietri
M
,
Radulovic
M
,
Stenmark
H.
The many functions of ESCRTs.
.
Nat Rev Mol Cell Biol
.
2020;
;
21
:
:25.
–
42
.
9.
Calistri
A
,
Reale
A
,
Palù
G
,
et al.
.
Why cells and viruses cannot survive without an ESCRT.
.
Cells
.
2021;
;
10
:
:483.
.
10.
Tabata
K
,
Arimoto
M
,
Arakawa
M
,
et al.
.
Unique requirement for ESCRT factors inflavivirus particle formation on the endoplasmic reticulum.
.
Cell Rep
.
2016;
;
16
:
:2339.
–
47
.
11.
Arpino
C
,
Curatolo
P
,
Rezza
G.
Chikungunya and the nervous system: what we do and do not know.
.
Rev Med Virol
.
2009;
;
19
:
:121.
–
9
.
|