| |
| Med Sci (Paris). 41(8-9): 637–639. doi: 10.1051/medsci/2025104.Les cellules de Kupffer, un nouvel acteur de l’hypercholestérolémie et de l’athérosclérose Rebecca Fima1 and Thierry Huby2* 1Pre cure
, Hôpital
Hadassah ein karem
,
Jérusalem
,
Israël 2Sorbonne Université, Inserm UMRS1269, Nutrition et obésités : approches systémiques, Nutriomics
,
Paris
,
France |
Les accidents cardio-vasculaires et leurs complications représentent une cause majeure de mortalité dans le monde. L’hypercholestérolémie, caractérisée par une augmentation de la concentration sanguine des lipoprotéines de basse densité (
low-density lipoproteins
, LDL) riches en cholestérol, en est l’un des facteurs de risque les plus importants. Le foie, en tant qu’organe métabolique central, joue un rôle clé dans la régulation des concentrations plasmatiques des LDL et du cholestérol. Toutefois, il a été suggéré que les macrophages résidents des tissus pourraient également intervenir dans le contrôle de la cholestérolémie, notamment les macrophages résidents du foie, ou cellules de Kupffer [
1
,
2
].
Localisées dans la paroi des capillaires sinusoïdes hépatiques, les cellules de Kupffer sont en contact direct avec le sang et les lipoprotéines circulantes. Elles s’établissent au cours de l’embryogenèse et se maintiennent par prolifération, indépendamment des monocytes (cellules précurseurs de macrophages) à l’âge adulte. Leur homéostasie implique des facteurs sécrétés par les populations cellulaires hépatiques avec lesquelles elles interagissent, telles que les cellules étoilées et les cellules endothéliales des capillaires sinusoïdes [
3
,
4
]. Si le rôle des cellules de Kupffer dans la surveillance immunitaire est bien établi, notamment
via
la phagocytose des agents pathogènes intravasculaires, les résultats de récentes études ont orienté vers l’identification d’un rôle métabolique [
5
,
6
].
Nous avons évalué le rôle des cellules de Kupffer dans l’homéostasie du cholestérol en utilisant un modèle murin dépourvu du récepteur des LDL : les souris
Ldlr-/-
[
7
]. L’absence de ce récepteur à la surface des hépatocytes entraîne l’accumulation de ces lipoprotéines dans la circulation sanguine. Lorsque les souris
Ldlr-/-
sont nourries avec un régime enrichi en cholestérol, elles développent une hypercholestérolémie similaire à celle des patients atteints d’hypercholestérolémie familiale, une maladie due à des défauts monogéniques dans la voie de clairance hépatique des LDL et une cause d’accident coronarien précoce et de décès prématuré.
|
Phase aigüe : prolifération adaptative et formation de cellules de Kupffer spumeuses
Après seulement quatre jours d’un régime alimentaire enrichi en cholestérol, les cellules de Kupffer sont la seule population leucocytaire hépatique affectée par l’induction de l’hypercholestérolémie. Comparées aux cellules de Kupffer des souris
Ldlr-/-
nourries avec un régime standard sans cholestérol, elles présentent des changements majeurs dans leur profil d’expression génique, notamment une activation des voies de dégradation lysosomique, du métabolisme du cholestérol et du cycle cellulaire, suggérant une forte activité métabolique [
7
]. L’analyse de ces données, complétée par la cytométrie en flux et l’immunohistochimie, a permis de mettre en évidence une très forte augmentation du nombre de cellules de Kupffer, qui triple en seulement quelques jours. Cette augmentation est due à la prolifération des cellules induite par la cytokine CSF1 (
colony stimulating factor 1
) sécrétée par les cellules étoilées hépatiques [
7
]. Par ailleurs, nous avons montré, qu’en plus de proliférer, les cellules de Kupffer accumulent du cholestérol en grande quantité, principalement sous forme d’esters de cholestérol. Cette surcharge lipidique implique le récepteur CD36 (
cluster of differentiation
36), un récepteur « éboueur » (en anglais, «
scavenger
») connu pour jouer, dans les macrophages, un rôle important dans la reconnaissance et l’internalisation des lipoprotéines LDL modifiées ou oxydées. Une analyse transcriptomique a révélé l’existence d’une forte similitude entre ces cellules de Kupffer surchargées en cholestérol et les macrophages spumeux gorgés de gouttelettes lipidiques qui s’accumulent dans les plaques d’athérome [
7
].
|
Phase chronique : remplacement des cellules de Kupffer d’origine embryonnaire par des cellules de Kupffer d’origine monocytaire
Si, au début de l’hypercholestérolémie, les cellules de Kupffer semblent y répondre efficacement par leur prolifération, celle-ci ne parvient pas à compenser une surcharge lipidique prolongée : après trois semaines de régime riche en cholestérol, le nombre des cellules de Kupffer a fortement diminué, retrouvant quasiment son niveau basal. Étonnamment, plus de la moitié des cellules de Kupffer alors présentes sont d’origine monocytaire, suggérant une disparition progressive des cellules de Kupffer d’origine embryonnaire, qui constituaient auparavant la population exclusive [
7
].
L’analyse des mécanismes cellulaires impliqués dans ce changement a montré qu’au cours de l’hypercholestérolémie chronique, les cellules de Kupffer embryonnaires surchargées en cholestérol subissent un stress oxydant caractérisé par une augmentation de la production d’espèces réactives de l’oxygène par la mitochondrie, ce qui favoriserait leur mort et par conséquent leur remplacement. En effet, on constate un recrutement accru de monocytes circulants dans le foie, qui se différencient en cellules de Kupffer dans les capillaires sinusoïdes, permettant ainsi de maintenir la population de macrophages résidents et donc l’immunosurveillance hépatique. Cependant, ces nouvelles cellules de Kupffer d’origine monocytaire présentent des capacités fonctionnelles réduites par rapport à celles d’origine embryonnaire. L’expression de leurs récepteurs
scavenger
, tels que CD36, est plus faible, ce qui limite leur capacité à capter et éliminer les LDL oxydées de la circulation sanguine, et ainsi à se charger en cholestérol [
7
].
|
Conséquences pathologiques et perspectives thérapeutiques
Dans un modèle murin permettant de provoquer volontairement le remplacement des cellules de Kupffer embryonnaires par d’autres d’origine monocytaire chez des souris
Ldlr-/-
hypercholestérolémiques, nous avons constaté que cette substitution induit une augmentation du contenu en cholestérol des hépatocytes et de l’élimination fécale des acides biliaires (produits du catabolisme hépatique du cholestérol) [
7
]. L’analyse transcriptomique du foie de ces animaux suggère que ces effets sont la conséquence d’une diminution de l’activation hépatique des voies de signalisation impliquant les facteurs de transcription RXR (
retinoid X receptor
) et LXR (
liver X receptor
), des récepteurs nucléaires qui jouent un rôle clé dans l’homéostasie des lipides et des acides biliaires. Enfin, nous avons montré que cette substitution imparfaite des cellules de Kupffer aggrave l’hypercholestérolémie et accélère le développement de l’athérosclérose (
Figure 1
) [
7
].
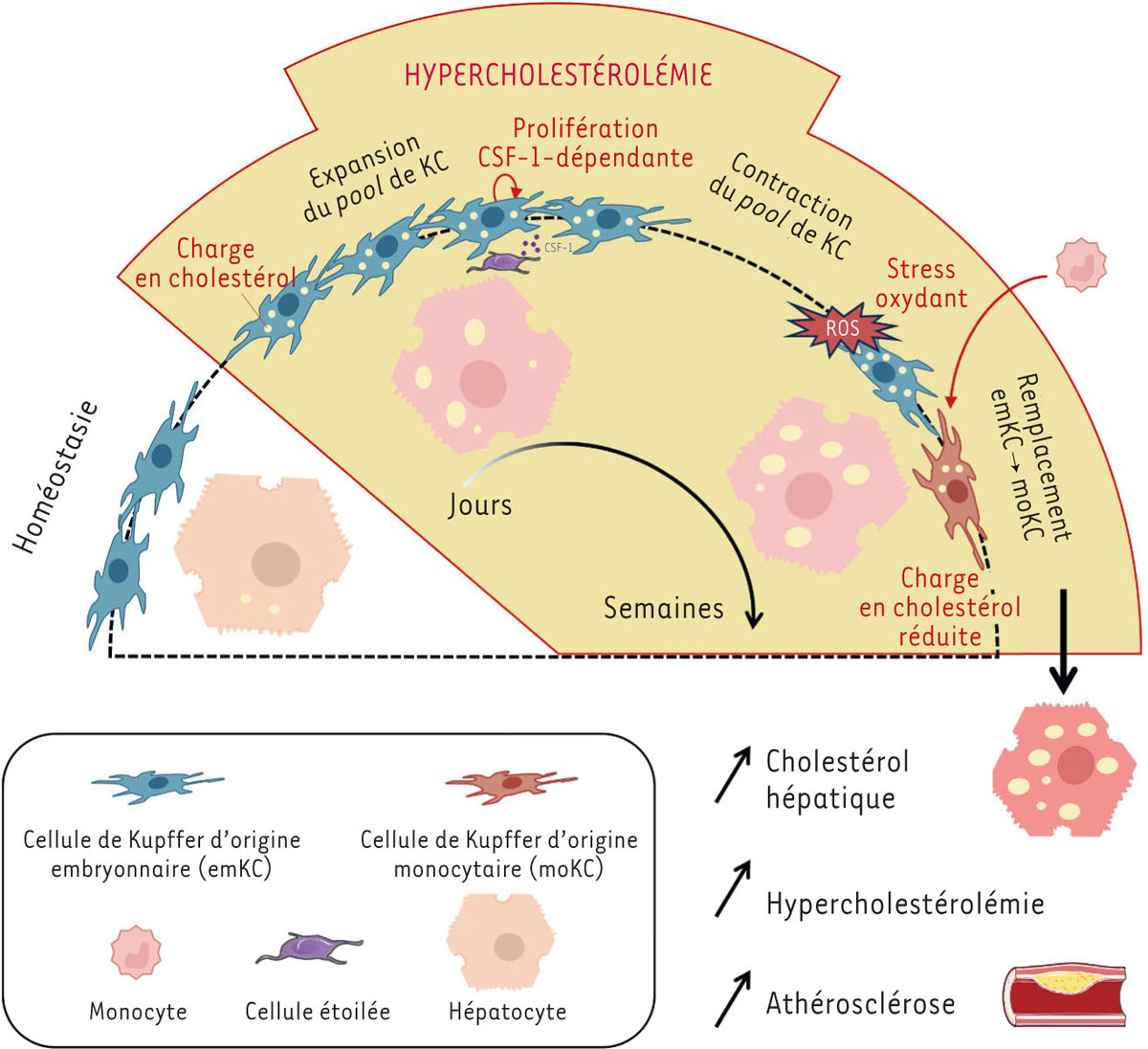
 | Figure 1.
Conséquences du remodelage de la population des macrophages résidents du foie au cours de l’hypercholestérolémie
.
À l’induction d’une hypercholestérolémie chez la souris, les macrophages résidents du foie, ou cellules de Kupffer (KC), se chargent en cholestérol et se multiplient en quelques jours. L’augmentation de leur nombre est induite par la cytokine CSF-1, produite par les cellules étoilées du foie. Avec le temps, ces cellules de Kupffer d’origine embryonnaire (emKC) subissent un stress oxydant lié à la production d’espèces réactives de l’oxygène (
reactive oxygen species
, ROS), et leur nombre diminue. Des monocytes sont alors recrutés et se différencient en cellules de Kupffer (moKC), dont la capacité à accumuler les lipides est cependant réduite. Cette substitution imparfaite des emKC par des moKC conduit à une accumulation du cholestérol dans les hépatocytes, aggrave l’hypercholestérolémie, et accélère le développement de l’athérosclérose.
|
La mise en évidence de l’importante contribution des cellules de Kupffer au métabolisme du cholestérol ouvre de nouvelles perspectives thérapeutiques. Il est désormais pertinent d’évaluer, dans des modèles précliniques, les effets bénéfiques de l’administration ciblée aux cellules de Kupffer, en utilisant des nanoparticules, de miARN fonctionnels [
8
] ou d’agonistes synthétiques des récepteurs LXR [
9
], qui ont montré leur capacité à favoriser l’efflux de cholestérol des macrophages spumeux. Une autre approche consisterait à utiliser des nanoparticules pour neutraliser les espèces réactives de l’oxygène et préserver ainsi la population des cellules de Kupffer d’origine embryonnaire [
10
]. Ces stratégies innovantes pour maintenir la fonction métabolique des cellules de Kupffer en cas d’hypercholestérolémie pourraient limiter le risque cardio-vasculaire associé.
|
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
1.
Bouchareychas
L
,
Pirault
J
,
Saint-Charles
F
,
et al.
.
Promoting macrophage survival delays progression of pre-existing atherosclerotic lesions through macrophage-derived apoE.
.
Cardiovasc Res
.
2015;
;
108
:
:111.
–
23
.
2.
Demetz
E
,
Tymoszuk
P
,
Hilbe
R
,
et al.
.
The haemochromatosis gene
Hfe
and Kupffer cells control LDL cholesterol homeostasis and impact on atherosclerosis development
.
.
Eur Heart J
.
2020;
;
41
:
:3949.
–
59
.
3.
Bonnardel
J
,
T’Jonck
W
,
Gaublomme
D
,
et al.
.
Stellate cells, hepatocytes, and endothelial cells imprint the Kupffer cell identity on monocytes colonizing the liver macrophage niche.
.
Immunity
.
2019;
;
51
:
:638.
–
54.e9
.
4.
Sakai
M
,
Troutman
TD
,
Seidman
JS
,
et al.
.
Liver-derived signals sequentially reprogram myeloid enhancers to initiate and maintain Kupffer cell identity.
.
Immunity
.
2019;
;
51
:
:655.
–
70.e8
.
5.
Tran
S
,
Baba
I
,
Poupel
L
,
et al.
.
Impaired Kupffer cell self-renewal alters the liver response to lipid overload during non-alcoholic steatohepatitis.
.
Immunity
.
2020;
;
53
:
:627.
–
40.e5
.
6.
Blériot
C
,
Barreby
E
,
Dunsmore
G
,
et al.
.
A subset of Kupffer cells regulates metabolism through the expression of CD36.
.
Immunity
.
2021;
;
54
:
:2101.
–
16.e6
.
7.
Fima
R
,
Dussaud
S
,
Benbida
C
,
et al.
.
Loss of embryonically-derived Kupffer cells during hypercholesterolemia accelerates atherosclerosis development.
.
Nat Commun
.
2024;
;
15
:
:8341.
.
8.
Nguyen
MA
,
Wyatt
H
,
Susser
L
,
et al.
.
Delivery of microRNAs by Chitosan nanoparticles to functionally alter macrophage cholesterol efflux
in vitro
and
in vivo
.
.
ACS Nano
.
2019;
;
13
:
:6491.
–
505
.
9.
Yu
M
,
Amengual
J
,
Menon
A
,
et al.
.
Targeted nanotherapeutics encapsulating liver X receptor agonist GW3965 enhance antiatherogenic effects without adverse effects on hepatic lipid metabolism in
Ldlr
-/-
mice
.
.
Adv Healthc Mater
.
2017;
;
6
:
:10.1002.
.
10.
Wang
Y
,
Li
L
,
Zhao
W
,
et al.
.
Targeted therapy of atherosclerosis by a broad-spectrum reactive oxygen species scavenging nanoparticle with intrinsic anti-inflammatory activity.
.
ACS Nano
.
2018;
;
12
:
:8943.
–
60
.
|