On connaît de nombreuses mutations somatiques ou germinales qui induisent une susceptibilité au cancer [ 1 ]. Cependant, certaines mutations peuvent aussi conférer une protection et pourraient constituer de nouvelles cibles thérapeutiques. Afin d’identifier des mutations associées à une résistance au cancer, une équipe de recherche a induit des mutations germinales aléatoires chez des souris C57BL/6J avec un agent mutagène chimique (N-nitroso-N-éthylurée), puis a évalué la croissance tumorale chez les souris de la troisième génération [ 2 ].
Dans un modèle de mélanome B16F10, associé ou non à une immunothérapie par anticorps anti-PD1, certaines souris contrôlaient mieux la croissance tumorale que les souris C57BL/6J de génotype « sauvage » ( i.e . non soumises à l’agent mutagène). Chez ces souris plus résistantes au mélanome, les chercheurs ont ensuite identifié une mutation du gène H2-Aa , qui code la chaîne a du complexe majeur d’histocompatibilité de classe II (CMH-II), orthologue de la molécule humaine HLA-DQ A1. Ces souris sont porteuses d’un allèle inactif du gène (absence de l’ARN messager), et leur phénotype a été nommé citation . Les souris hétérozygotes pour cet allèle ( H2-Aa cit/+ ) ont une inhibition significative de la croissance tumorale, tandis que les souris homozygotes ( H2-Aa cit/cit ) ont une quasi absence de développement tumoral, même sans immunothérapie anti-PD1. Ce résultat a été confirmé dans d’autres modèles tumoraux (mélanome YUMM1.G1, carcinome du côlon MC38), ou lorsque la délétion du gène H2-Aa a lieu après la greffe de la tumeur (souris H2-Aa flox/flox ; UBC-cre-ER T2 traitées avec du tamoxifène pour induire la synthèse de la recombinase cre) [ 2 ].
Les chercheurs ont ensuite montré que la protection anti-tumorale de ces souris était dépendante des lymphocytes T CD8 + puisque leur déplétion par un anticorps anti-CD8 restaure la croissance tumorale chez les souris H2-Aa cit/cit . Dans les tumeurs des souris H2-Aa cit/cit , l’infiltration des lymphocytes T CD8 + est forte, avec un phénotype mémoire et activé, et ces lymphocytes sont plus fonctionnels que ceux des souris de génotype « sauvage ». De plus, des réponses immunes spécifiques des antigènes tumoraux sont bien induites, puisque dans le modèle de mélanome B16F10-ovalbumine, les souris H2-Aa cit/cit ont une plus grande proportion de lymphocytes T CD8 + spécifiques de l’antigène ovalbumine [ 2 ]. Les chercheurs ont aussi montré que l’effet anti-tumoral implique en partie les lymphocytes T régulateurs, dont la proportion est plus faible dans les tumeurs des souris H2-Aa cit/cit que dans celles des souris de génotype « sauvage », ce qui contribue à un meilleur contrôle de la croissance tumorale [ 2 ].
Cette diminution du nombre des lymphocytes T régulateurs pourrait être due au défaut de l’expression du CMH-II par les thymocytes des souris H2-Aa cit/cit , ce qui altère le développement des lymphocytes T CD4 + , incluant les lymphocytes T régulateurs.
Il est classiquement décrit que les lymphocytes T CD8 + sont activés par les cellules dendritiques conventionnelles de type 1 (cDC1) via le CMH-I, et les lymphocytes T CD4 + par les cellules dendritiques conventionnelles de type 2 (cDC2) via le CMH-II [ 3 ]. Les cellules dendritiques, tout comme les macrophages et les lymphocytes B, peuvent présenter les antigènes et expriment les molécules du CMH-II. Afin d’identifier quelles populations de cellules présentatrices d’antigènes sont impliquées dans la résistance au cancer de ces souris, les chercheurs ont évalué la croissance tumorale chez des souris transgéniques qui ont une délétion spécifique du gène H2-Aa dans ces différentes populations : souris H2-Aaflox CD11c-cre (délétion dans toutes les cellules dendritiques), souris H2-AafloxCD19-cre (délétion dans les lymphocytes B), souris H2-Aaflox LysMcre (délétion dans toutes les cellules myéloïdes), et souris H2-AafloxXcr1-cre (délétion dans les cellules dendritiques cDC1). Ils ont montré que ce sont les cellules dendritiques, et étonnamment les cDC2, qui sont impliquées dans la résistance anti-tumorale des souris H2-Aa cit/+ ou H2-Aa cit/cit [ 2 ].
La comparaison des populations de cellules dendritiques chez les souris H2-Aa cit/cit et chez les souris témoins ( H2-Aa +/+ ) a montré une augmentation de la proportion des cellules cDC2 et une diminution de la proportion des cellules cDC1 dans la rate et dans la tumeur des souris H2-Aa cit/cit . La proportion des précurseurs de cellules dendritiques dans la moelle osseuse chez les souris mutantes étant similaire à celle chez les souris dépourvues de la mutation, les chercheurs en ont conclu que la délétion du gène H2-Aa affecte vraisemblablement la différenciation terminale des cellules dendritiques dans les tissus et organes. Au plan fonctionnel, les cellules dendritiques des souris H2-Aa cit/cit capturent l’antigène aussi efficacement que celles des souris témoins. En revanche, les cellules cDC2 des souris H2-Aa cit/cit activent plus efficacement les lymphocytes T CD8 + , in vitro et in vivo , que celles des souris témoins ou que les cellules cDC1 des souris H2- Aa cit/cit . En effet, les lymphocytes T CD8 + activés par les cellules cDC2 H2-Aa cit/cit prolifèrent davantage et produisent plus d’interféron γ. De plus, dans les organes lymphoïdes et dans la tumeur, les cellules cDC2 H2-Aa cit/cit expriment davantage les molécules d’activation et de costimulation CD80 et CMH-I. Une analyse transcriptomique de cellules dendritiques uniques a permis de confirmer et de compléter ces résultats en montrant, dans les cellules cDC2 H2-Aa cit/cit , un enrichissement en transcrits de gènes impliqués dans la prolifération ( Mki67) , dans les voies d’apprêtement et de présentation antigéniques ( Pdia3, Canx, Calr ) et plus particulièrement dans la présentation croisée 1, ( Sec61, Hsp90b1 ), et au contraire, un appauvrissement en transcrits de gènes associés à l’apoptose et à l’inhibition de la maturation cellulaire ( Erdr1, Zfp36 ) [ 2 ].
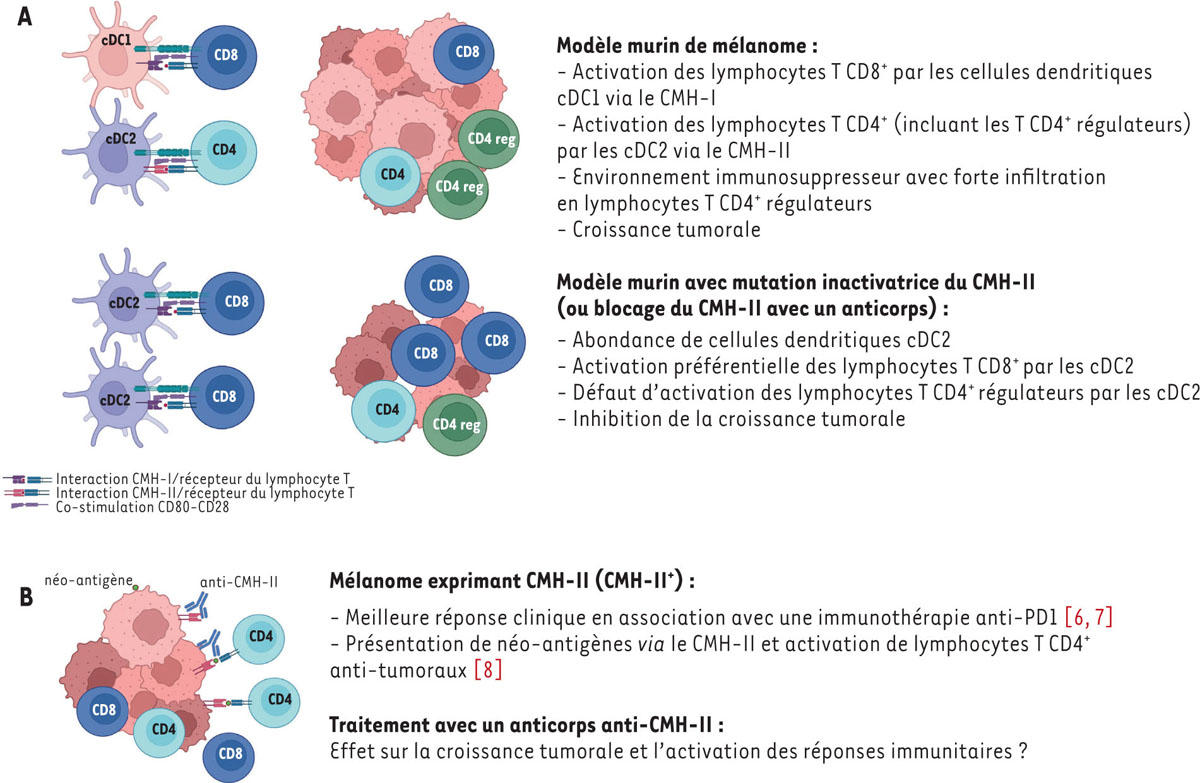
En résumé, la délétion du gène H2-Aa chez la souris entraîne une augmentation du nombre de cellules dendritiques cDC2 et de leur capacité de présentation antigénique et d’activation lymphocytaire, avec pour conséquence, d’une part, une activation plus efficace de la réponse antitumorale, caractérisée par des lymphocytes T CD8 + plus fonctionnels et cytotoxiques, et d’autre part, une diminution de la réponse immunosuppressive avec une réduction des lymphocytes T régulateurs. L’ensemble de ces mécanismes permet le contrôle de la croissance tumorale chez les souris H2-Aa cit/cit ( Figure 1A ).
| Figure 1.
Modèle d’activation des lymphocytes T dans le mélanome. A
.
En haut
: dans un modèle murin de mélanome, les cellules dendritiques conventionnelles de type 1 (cDC1) vont présenter les antigènes tumoraux aux lymphocytes T CD8
+
via
le CMH-I, et les cellules dendritiques conventionnelles de type 2 (cDC2) aux lymphocytes T CD4
+
via
le CMH-II. Un environnement immunosuppresseur se met en place, avec une infiltration importante de lymphocytes T CD4
+
régulateurs (CD4 reg), favorisant la croissance tumorale.
En bas
: l’inactivation génique du CMH-II ou son blocage par un anticorps induit une activation préférentielle des lymphocytes T CD8
+
, associée à une diminution des lymphocytes T CD4
+
régulateurs et à une inhibition de la croissance tumorale. Figure adaptée de [
2
].
B
.
Dans le mélanome, les cellules tumorales peuvent présenter des néo-antigènes
via
le CMH-II et activer les lymphocytes T CD8
+
et les lymphocytes T CD4
+
. Figure créée avec BioRender.
|
Les chercheurs ont ensuite développé, dans une perspective thérapeutique, un anticorps monoclonal dirigé contre le CMH-II. L’injection de cet anticorps aux souris favorise l’activation des lymphocytes T CD8 + via la présentation croisée par les cellules dendritiques, tout en bloquant l’activation des lymphocytes T CD4 + . Elle a inhibé la croissance de tumeurs B16F10 de manière dose dépendante, en synergie avec un traitement par des anticorps anti-PD1, et a induit une plus forte infiltration de ces tumeurs par des lymphocytes T CD8 + [ 2 ]. Le mécanisme anti-tumoral mis en évidence chez les souris porteuses de mutations inactivatrices du gène H2-Aa est dépendant des lymphocytes T CD8 + . Or, les lymphocytes T CD8 + induits expriment plus fortement PD-1, un marqueur généralement associé à l’épuisement des lymphocytes, et sont pourtant plus fonctionnels. Ce résultat est en accord avec ceux d’autres études qui ont montré que les lymphocytes T CD8 + PD-1 + induits après une vaccination ou infiltrant les tumeurs sont plus fonctionnels, et pourraient être les lymphocytes qui répondent le plus à une immunothérapie anti-PD1 [ 4 ]. Une meilleure caractérisation des lymphocytes T CD8 + (précurseurs mémoires, résidents mémoires…) pourrait compléter les résultats de la présente étude. D’autant que les lymphocytes T CD8 + qui se développent dans le contexte d’un déficit en CMH-II expriment un répertoire de récepteurs TCR ( T cell receptor ) modifié, et peuvent induire de l’auto-immunité et aussi avoir une fonction anti-tumorale [ 5 ].
Les chercheurs ont donc montré, chez la souris, que le blocage spécifique du CMH-II pourrait constituer une nouvelle piste thérapeutique contre le cancer. Cependant, la transposition en médecine humaine se révèle complexe, car contrairement à la souris qui n’exprime qu’un type de molécules du CMH-II (H2-A), le CMH-II humain est polymorphique (HLA-DQ, HLA-DR, HLA-DP). Le blocage de certaines molécules du CMH-II par un anticorps thérapeutique pourrait certes avoir un effet bénéfique partiel sur la croissance tumorale chez l’Homme, mais cet anticorps pourrait aussi bloquer les molécules du CMH-II présentes sur les cellules tumorales, ce qui aurait un effet pro-tumoral ( Figure 1B ). En effet, les cellules tumorales peuvent présenter des néo-antigènes tumoraux au système immunitaire via le CMH-II et induire une réponse anti-tumorale. Chez des patients atteints de mélanome traités avec un anticorps anti-PD1, l’expression des molécules CMH-II par les cellules tumorales est d’ailleurs associée à une meilleure réponse clinique [ 6 ]. Dans le cas du mélanome et du cancer du poumon, l’expression du CMH-II par les cellules tumorales et les néo-antigènes associés prédisent la réponse thérapeutique à l’anticorps anti-PD-1 [ 7 ]. D’autre part, dans un modèle pré-clinique murin de mélanome B16F10 pour lequel des néo-antigènes tumoraux restreints au CMH-II ont été identifiés, la vaccination avec ces néo-antigènes a inhibé la croissance tumorale et induit une forte infiltration de la tumeur par des lymphocytes T CD4 + et CD8 + [ 8 ].
Enfin, on ignore la raison pour laquelle dans certains modèles tumoraux, les cellules dendritiques capables d’induire une immunité antitumorale semblent être les cellules cDC1 [ 8 , 9 ], alors que dans d’autres modèles, ce sont les cellules cDC2 (en l’absence de lymphocytes T régulateurs) qui semblent nécessaires pour induire une immunité antitumorale impliquant les lymphocytes T CD4 + effecteurs [ 10 , 11 ], comme c’est le cas dans l’étude que nous avons présentée [ 2 ].