| |
| Med Sci (Paris). 41(8-9): 628–630. doi: 10.1051/medsci/2025101.Les dents au chevet de l’oreille Yassine Messat,1 Pierre-Yves Collart Dutilleul,1,2,3 and Azel Zine1* 1Laboratoire Bioingénierie et nanosciences (LBN), Université de Montpellier
,
Montpellier
,
France 2UFR d’odontologie, Université de Montpellier
,
Montpellier
,
France 3Centre de soins, d’enseignement et de recherche dentaires, CHU de Montpellier
,
Montpellier
,
France |
La pulpe dentaire désigne le tissu conjonctif fibreux, richement vascularisé et innervé, situé au centre de la dent et entouré par trois tissus minéralisés : l’émail, la dentine et le cément. Elle abrite un ensemble de cellules souches/ progénitrices, dont les cellules souches pulpaires (
dental pulp stem cells
, DPSC) [
1
]. Ces cellules sont localisées dans des niches périvasculaires, d’où elles peuvent être mobilisées en cas de lésion tissulaire [
2
]. Elles représentent une source très accessible de cellules souches, notamment dans les germes des dents de sagesse qui sont quotidiennement extraits dans les cabinets dentaires pour raison orthodontique, et jetés comme déchets opératoires.
Les cellules souches pulpaires sont des cellules multipotentes, auto-renouvelables, prolifératives et possédant des capacités de différenciation,
in vivo
ou
in vitro
, vers plusieurs types cellulaires de lignages différents : odontoblastes, ostéoblastes, cellules endothéliales, myoblastes, adipocytes, chondrocytes, hépatocytes, neurones, mélanocytes, et cellules pancréatiques [
3
]. Elles possèdent également des activités immunosuppressives et immunomodulatrices [
4
], ce qui augmente leur intérêt thérapeutique potentiel en médecine régé-nérative.
|
La neuropathie auditive est définie comme un déficit neurosensoriel dû à une absence, ou plus souvent au dysfonctionnement des neurones auditifs primaires, neurones bipolaires dont les corps cellulaires constituent le ganglion spiralé de l’oreille interne. Aucun traitement n’est actuellement disponible, et l’implant cochléaire prothétique, efficace pour pallier un dysfonctionnement des cellules de la cochlée quand ce dernier est responsable de la surdité, est en revanche inefficace sur les neuropathies auditives. De plus, la réduction de la densité de l’innervation des cellules sensorielles auditives dans la plupart des autres formes de surdité neurosensorielle restreint les performances de l’implant cochléaire prothétique pour la réhabilitation auditive.
La médecine régénérative représente un espoir thérapeutique dans diverses situations pathologiques : elle consiste à réparer une lésion ou à remplacer les parties endommagées d’un tissu ou d’un organe par une thérapie cellulaire ou par ingénierie tissulaire. La thérapie cellulaire nécessite une production et une maintenance
in vitro
de cellules souches/progénitrices, puis éventuellement leur modification afin de leur attribuer un statut de différenciation précis avant de les transplanter. Les cellules souches à fort potentiel thérapeutique peuvent être regroupées en deux catégories : 1) les cellules pluripotentes, généralement d’origine embryonnaire ou issues d’une reprogrammation cellulaire ; 2) les cellules multipotentes, isolées à partir de tissus d’individus adultes le plus souvent. Si les cellules souches pluripotentes, par leur capacité à générer pratiquement tous les types cellulaires, suscitent de grands espoirs, des problèmes éthiques et techniques ralentissent leur utilisation médicale [
5
]. Bien que plus limitées dans leur potentiel de différenciation, les cellules multipotentes, qui peuvent être isolées à partir de nombreuses sources tissulaires, représentent une alternative de choix [
6
].
|
Cellules souches de la pulpe dentaire : un fort potentiel thérapeutique
Durant ces dernières années, les cellules souches de la pulpe dentaire ont suscité un intérêt croissant dans différents modèles de différenciation
in vitro
: endothéliale, ostéogénique, chondrogénique, et neuronale [
7
]. En effet, la facilité d’obtention de ces cellules et leurs caractéristiques de cellules mésenchymateuses les rendent plus attrayantes que les cellules souches de la moelle osseuse. Les résultats de plusieurs travaux de recherche ont d’ailleurs confirmé qu’elles avaient un potentiel neurogénique plus important que les cellules souches de la moelle osseuse, et un « sécrétome » plus riche en cytokines et facteurs neurotrophiques [
8
,
9
]. Ces caractéristiques nous ont conduits à penser que l’utilisation des cellules souches pulpaires pouvait être pertinente pour obtenir un modèle humain de différenciation cellulaire en neurones auditifs primaires (neurones du ganglion spiralé), d’autant plus que la pulpe dentaire et le ganglion spiralé ont, en partie, une origine embryologique commune, mixte : ils dérivent à la fois de l’ectoderme non-neural et de la crête neurale [
10
,
11
].
|
Différenciation des cellules souches de la pulpe dentaire en neurones du ganglion spiralé : ultime étape vers la thérapie cellulaire de la neuropathie auditive ?
Nous avons mis au point une méthode de production de neurones du ganglion spiralé par différenciation
in vitro
progressive et dirigée des cellules souches pulpaires humaines. En modulant des voies de signalisation, des facteurs de transcription, des protéines de la matrice extracellulaire et des récepteurs neurotrophiques, nous avons montré que ces cellules peuvent se différencier
in vitro
en progéniteurs neuronaux otiques, puis en neurones dont la morphologie bipolaire est caractéristique des neurones du ganglion spiralé [
12
]. Des analyses de l’expression génique au cours de cette différenciation ont effectivement révélé l’induction de nombreux marqueurs connus des progéniteurs neuronaux otiques et des neurones du ganglion spiralé. De plus, en utilisant la microscopie à force atomique, nous avons montré que les neurones ainsi dérivés des cellules souches pulpaires
in vitro
présentent des propriétés nanomécaniques similaires à celles des neurones du ganglion spiralé
in vivo
[
12
]. Ainsi, les neurones différenciés
in vitro
à partir des cellules souches de la pulpe dentaire partagent des caractéristiques phénotypiques, transcriptomiques, et nanomécaniques avec les neurones du ganglion spiralé
in vivo
. De plus, dans des conditions de co-culture des progéniteurs neuro-naux otiques avec l’explant du ganglion spiralé du rat, nous avons observé des extensions neuronales provenant de l’explant et qui viennent au contact des ONP, ce qui suggère que ces cellules ont la capacité de se reconnecter au ganglion spiralé [
12
] (
Figure 1
).
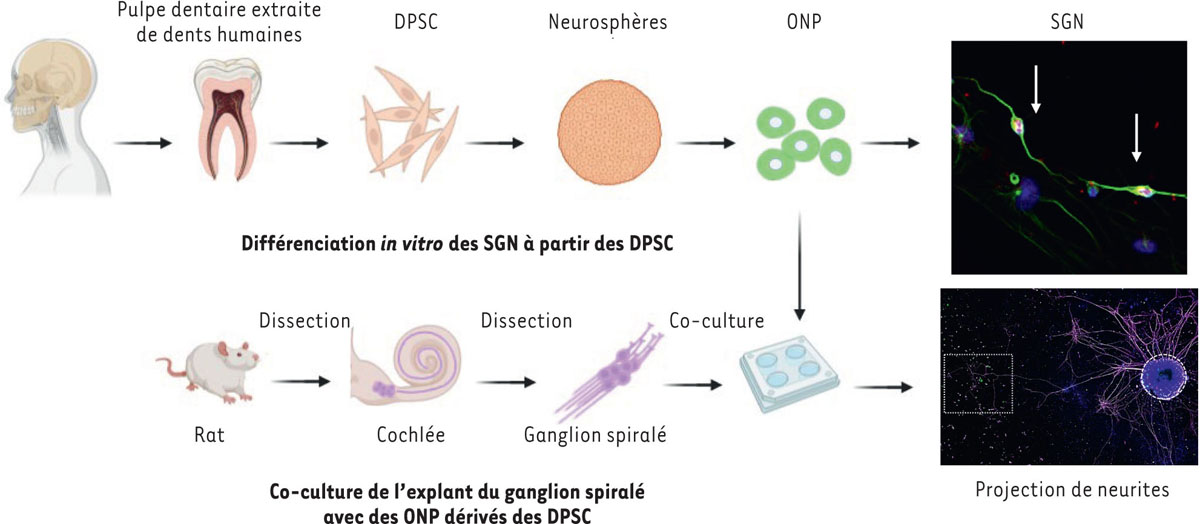
 | Figure 1.
Méthode de différenciation
in vitro
des cellules souches de la pulpe dentaire en progéniteurs neuronaux otiques et leur co-culture avec des explants du ganglion spiralé
.
Les cellules souches de la pulpe dentaire (
dental pulp stem cells
, DPSC) sont isolées à partir des dents humaines extraites. Après la propagation de ces cellules en culture, des neurosphères sont formées et différenciées en progéniteurs neuronaux otiques (
otic neuronal progenitors
, ONP), puis en neurones du ganglion spiralé (flèches blanches) (
spiral ganglion neurons
, SGN). La co-culture de ces ONP produits
in vitro
avec des explants du ganglion spiralé de ratons âgés de trois jours montre la projection de neurites (marqués en magenta) provenant de l’explant (indiqué par le cercle en trait pointillé) en direction des ONP (marqués en vert) (leur position est indiquée par le carré en trait pointillé).
|
Ces résultats ont permis d’élargir le spectre de différenciation des cellules souches de la pulpe dentaire, qui s’avère plus large que tous ceux des autres cellules souches provenant de tissus adultes décrits à ce jour, et qui témoigne d’une grande plasticité de ces cellules en réponse aux signaux externes (développementaux ou plus tardifs) dans un environnement propice.
Les cellules souches mésenchymateuses sont aujourd’hui utilisées dans de nombreux essais cliniques de transplantation cellulaire [
5
]. Les cellules souches de la pulpe dentaire, qui combinent certaines caractéristiques des cellules souches mésenchymateuses et des cellules souches neurales, ont révélé leur potentiel dans la perspective d’une thérapie cellulaire de la neuropathie auditive. Des études sont en cours afin d’établir les conditions requises pour pouvoir tester l’effet d’une greffe de cellules souches pulpaires différenciées en progéniteurs neuronaux otiques (ONP) dans des modèles animaux de neuropathie auditive [
13
].
|
Les données concernant les cellules souches de la pulpe dentaire convergent en faveur d’une future utilisation dans un cadre thérapeutique. Leur facilité d’accès chez l’ humain est un avantage considérable, qui permet d’envisager des transplantations autologues, évitant ainsi tout risque de rejet ou d’effets indésirables d’un traitement immunosuppresseur. De plus, lorsqu’elles sont maintenues
in vitro
dans des conditions propices, ces cellules ont un fort pouvoir de prolifération, ce qui permet d’en disposer en grand nombre dans un délai relativement court. Si la médecine régénératrice de demain s’inscrit toujours dans la recherche de produits cellulaires à fort potentiel thérapeutique, les cellules souches de la pulpe dentaire humaine doivent être considérées comme d’excellentes candidates pour la thérapie cellulaire de la neuropathie auditive (
Figure 2
). Ajoutons que leurs effets neuroprotecteur et immunomodulateur incitent à considérer la possibilité de les utiliser aussi dans d’autres maladies associées à des pertes ou des lésions de cellules neuronales [
14
].
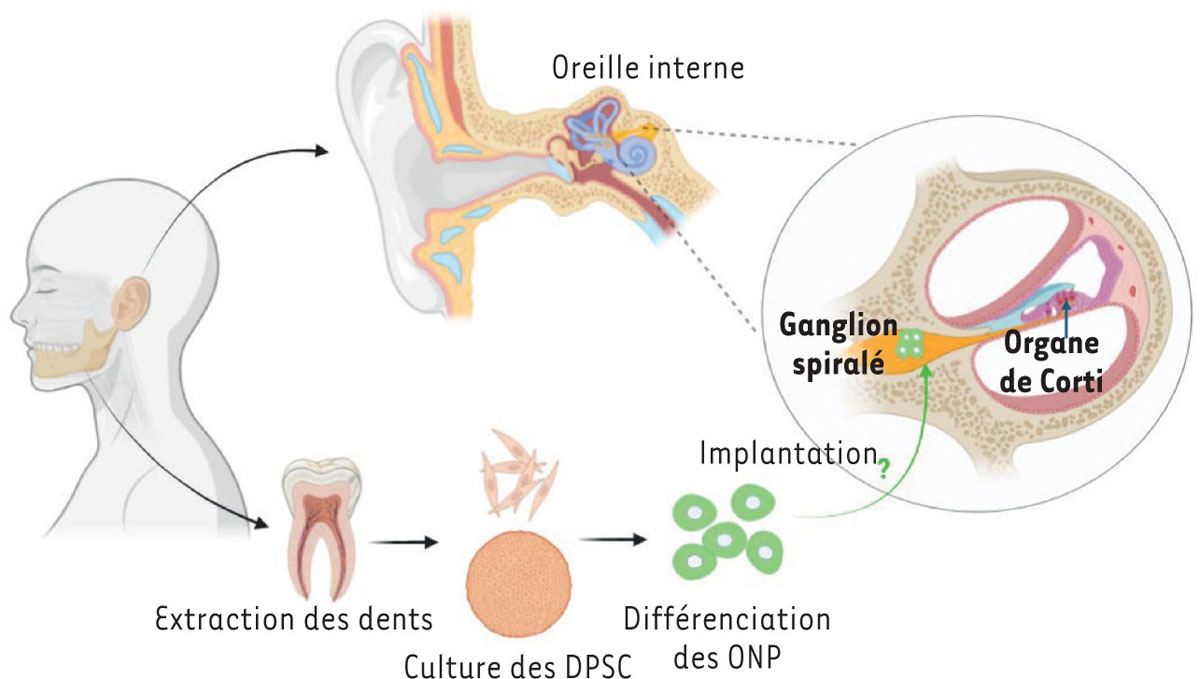
 | Figure 2.
Perspective d’une greffe des progéniteurs neuronaux otiques (ONP) dérivés des cellules souches de la pulpe dentaire dans le ganglion spiralé pour traiter la neuropathie auditive
.
|
|
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
1.
Gronthos
S
,
Mankani
M
,
Brahim
J
,
et al.
.
Postnatal human dental pulp stem cells (DPSCs)
in vitro
and
in vivo
.
.
Proc Natl Acad Sci USA
.
2000;
;
97
:
:13625.
–
30
.
2.
Sedgley
CM
,
Botero
TM.
Dental stem cells and their sources.
.
Dent Clin N Am
.
2012;
;
56
:
:549.
–
61
.
3.
Shi
X
,
Mao
J
,
Liu
Y.
Pulp stem cells derived from human permanent and deciduous teeth: Biological characteristics and therapeutic applications.
.
Stem Cells Transl Med
.
2020;
;
9
:
:445.
–
64
.
4.
Andrukhov
O
,
Behm
C
,
Blufstein
A
,
et al.
.
Immunomodulatory properties of dental tissue-derived mesenchymal stem cells: Implication in disease and tissue regeneration.
.
World J Stem Cells
.
2019;
;
11
:
:604.
–
17
.
5.
Moy
A
,
Kamath
A
,
Ternes
S
,
et al.
.
The challenges to advancing induced pluripotent stem cell-dependent cell replacement therapy.
.
Med Res Arch
.
2023;
;
2023
.
6.
Margiana
R
,
Markov
A
,
Zekiy
AO
,
et al.
.
Clinical application of mesenchymal stem cell in regenerative medicine: a narrative review.
.
Stem Cell Res Ther
.
2022;
;
13
:
:366.
.
7.
Nuti
N
,
Corallo
C
,
Chan
BMF
,
et al.
.
Multipotent differentiation of human dental pulp stem cells: a literature review.
.
Stem Cell Rev Rep
.
2016;
;
12
:
:511.
–
23
.
8.
Karaöz
E
,
Demircan
PC
,
Sağlam
Ö
,
et al.
.
Human dental pulp stem cells demonstrate better neural and epithelial stem cell properties than bone marrow-derived mesenchymal stem cells.
.
Histochem Cell Biol
.
2011;
;
136
:
:455.
.
9.
Chouaib
B
,
Collart-Dutilleul
P-Y
,
Blanc-Sylvestre
N
,
et al.
.
Identification of secreted factors in dental pulp cell-conditioned medium optimized for neuronal growth.
.
Neurochem Int
.
2021;
;
144
:
:104961.
.
10.
Kempfle
JS
,
Luu
N-NC
,
Petrillo
M
,
et al.
.
Lin28 reprograms inner ear glia to a neuronal fate.
.
Stem cells
.
2020;
;
38
:
:890.
–
903
.
11.
Chen
Z
,
Huang
Y
,
Yu
C
,
et al.
.
Cochlear Sox2
+
glial cells are potent progenitors for spiral ganglion neuron reprogramming induced by small molecules
.
.
Front Cell Dev Biol
.
2021;
;
9
:
:728352.
.
12.
Messat
Y
,
Martin-Fernandez
M
,
Assou
S
,
et al.
.
Differentiation of spiral ganglion neurons from human dental pulp stem cells: A further step towards autologous auditory nerve recovery.
.
Int J Mol Sci
.
2024;
;
25
:
:9115.
.
13.
Chen
W
,
Jongkamonwiwat
N
,
Abbas
L
,
et al.
.
Restoration of auditory evoked responses by human ES-cell-derived otic progenitors.
.
Nature
.
2012;
;
490
:
:278.
–
82
.
14.
Li
P
,
Ou
Q
,
Shi
S
,
et al.
.
Immunomodulatory properties of mesenchymal stem cells/dental stem cells and their therapeutic applications.
.
Cell Mol Immunol
.
2023;
;
20
:
:558.
–
69
.
|