Le virus de l’immunodéficience humaine de type 1 (VIH-1), isolé en 1983 [ 1 ], est l’agent pathogène responsable du syndrome de l’immunodéficience acquise (SIDA). Depuis sa découverte, il y a plus de 40 ans, son étude a permis le développement de traitements et prophylaxies efficaces. Malgré ces avancées, plus de 40 millions de personnes vivent avec le VIH-1 aujourd’hui dans le monde. De plus, les thérapies existantes ne permettent pas d’éliminer le virus, qui persiste à vie dans l’organisme des personnes infectées. Il est donc nécessaire de progresser dans la biologie de ce virus dans le but de découvrir de nouvelles cibles thérapeutiques.
Le VIH-1 est un virus enveloppé appartenant à la famille des rétrovirus, qui infecte les cellules immunitaires, principalement les lymphocytes T et les macrophages. Le cycle de réplication du virus peut être divisé en étapes précoces et étapes tardives. Les étapes précoces débutent par la fixation du VIH-1 à ses récepteurs et corécepteurs à la surface de la cellule cible. La particule virale fusionne ensuite avec la membrane plasmique cellulaire, ce qui permet l’entrée de la capside du virus dans le cytoplasme, puis dans le noyau de la cellule. Le génome viral, constitué de deux copies d’ARN simple brin, est rétrotranscrit en ADN, puis intégré dans le génome de la cellule hôte. Les étapes tardives du cycle de réplication du VIH-1 débutent par la production des protéines virales et des ARN viraux. Ces différents composants sont recrutés à la membrane plasmique de la cellule hôte, où ils s’assemblent pour former des particules virales, qui bourgeonnent, puis sont libérées dans le milieu extracellulaire. Pour réaliser ce cycle, le virus doit détourner à son profit des machineries cellulaires [ 2 ].
Le bourgeonnement et la libération des particules virales infectieuses est une étape clé pour la propagation du VIH-1 : une fois libéré, le virus peut infecter de nouvelles cellules et ainsi se propager dans l’organisme. Un acteur majeur du bourgeonnement du virus est la protéine virale Gag. Gag se lie à la membrane plasmique de la cellule, où elle s’assemble pour produire des particules sphériques [ 3 ]. Ensuite, Gag détourne la machinerie cellulaire de scission ESCRT-III ( endosomal sorting complex required for transport ), ce qui permet la coupure de la membrane déformée par l’assemblage de Gag, et ainsi la libération des particules virales dans le milieu extra-cellulaire [ 4 , 5 ]. Cependant, en comparaison à d’autres étapes du cycle viral (entrée du virus, rétrotranscription, intégration et réplication du génome viral), les mécanismes moléculaires impliqués dans le bourgeonnement et la libération du virus sont moins bien compris.
La membrane plasmique à partir de laquelle s’effectue le bourgeonnement du VIH-1 interagit avec un cortex d’actine sous-jacent. Ce cortex est constitué d’un réseau dense et épais (environ 200 nm) de filaments d’actine associés à la membrane via des protéines trans-membranaires. Cette association étroite représente un défi important pour la déformation et la scission de la membrane au cours du bourgeonnement des particules virales. En effet, le cortex d’actine joue certainement un rôle de barrière physique et influe sur la tension de la membrane plasmique, ce qui pourrait empêcher un recrutement efficace de la machinerie ESCRT-III [ 6 ]. Il est donc probable qu’un remodelage dynamique du cortex d’actine est nécessaire pour le bourgeonnement et la libération du VIH-1. Cependant, le rôle du cytosquelette d’actine dans ce processus ne fait pas l’objet d’un consensus [ 7 ].
Dans une étude récente, fruit de la collaboration entre chercheurs en biologie cellulaire, virologie et biochimie, un rôle clé de l’enzyme cellulaire MICAL1 ( molecule interacting with CasL protein 1 ) et de son activateur Rab35 a été identifié dans la dépolymérisation locale du cortex d’actine au moment du bourgeonnement du VIH-1 [ 8 ]. MICAL1 est une enzyme qui oxyde directement les filaments d’actine (sur deux résidus méthionine en positions 44 et 47), ce qui provoque leur dépolymérisation rapide [ 9 ]. Cette protéine est impliquée dans de nombreux mécanismes cellulaires faisant intervenir un remaniement du cytosquelette d’actine, comme la cytocinèse (la dernière étape de la division cellulaire conduisant à la séparation physique des cellules filles), la migration cellulaire, ou certains aspects du fonctionnement des neurones [ 9 , 10 ]. Cette étude montre que l’inhibition de l’expression de MICAL1 dans des cellules humaines infectées par le VIH-1 (cellules épithéliales et macrophages) réduit la libération des virus dans le milieu extracellulaire et provoque leur accumulation à la membrane plasmique, bien visible sur des images de microscopie électronique à balayage ( Figure 1 ). De plus, des expériences de microscopie électronique à transmission indiquent que les virus qui s’accumulent à la membrane plasmique en absence de MICAL1 sont bloqués à un stade précoce du processus de bourgeonnement, et sont incapables de déformer complètement la membrane. Cela perturbe le recrutement de la machinerie cellulaire ESCRT-III par le virus. En effet, des expériences de microscopie en fluorescence par réflexion totale interne ( total internal reflection fluoresence microscopy , TIRFM) ont révélé que l’inhibition de l’expression de MICAL1 provoque un retard dans le recrutement de la protéine ESCRT-III CHMP4B ( charged multivesicular body protein 4B ) au site de bourgeonnement du virus, ce qui contribue à expliquer les défauts de libération des particules virales.
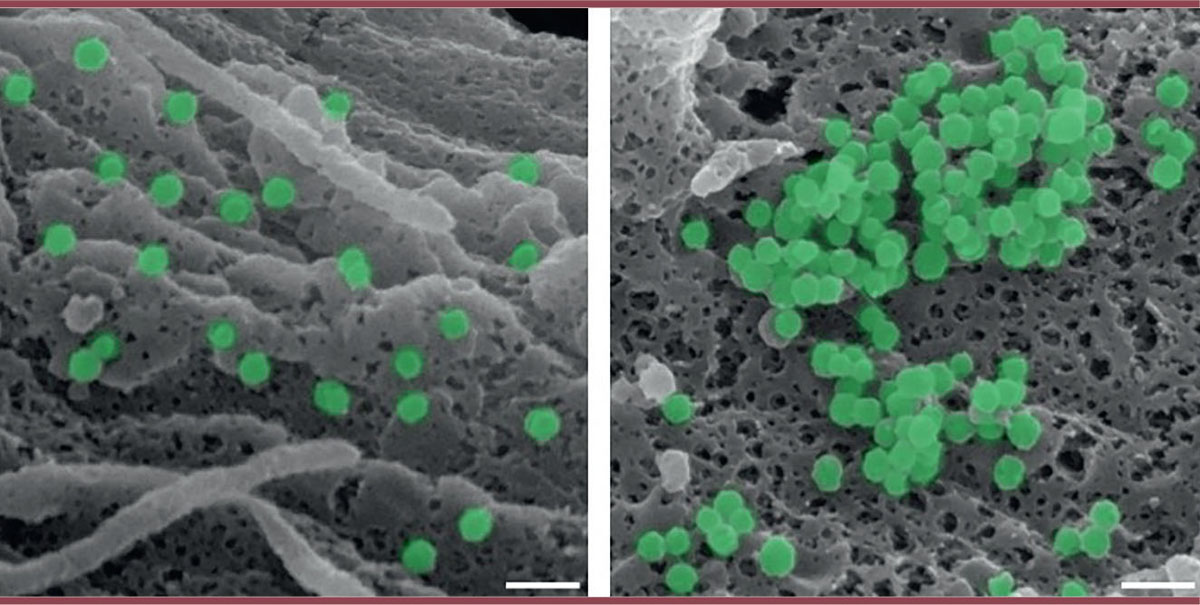
| Figure 1.
Images, par microscopie électronique à balayage, de cellules infectées par le VIH-1 après déplétion (à droite) ou non (à gauche) de l’oxydoréductase MICAL1
.
L’inhibition de l’expression de MICAL1 provoque une accumulation de particules virales (en vert) à la surface des cellules (barre d’échelle : 200 nm).
|
La protéine MICAL1 étant un régulateur majeur de la dynamique de l’actine dans la cellule, l’impact de l’inhibition de l’expression de MICAL1 sur le cortex d’actine aux sites de bourgeonnement du virus a ensuite été étudié. Dans les cellules infectées produisant normalement la protéine MICAL1, les virus bourgeonnent dans des zones de la membrane plasmique présentant peu d’actine corticale, ce qui est en accord avec les résultats d’une autre étude récente [ 11 ]. Au contraire, en l’absence de MICAL1, les filaments d’actine du cortex ne sont plus correctement désassemblés aux sites de bourgeonnement du virus. Pour montrer que cette présence anormale de filaments d’actine est responsable des défauts de bourgeonnement des particules virales, ces cellules ont été traitées par un composé chimique bloquant la polymérisation de l’actine, et ce traitement a suffi à corriger les défauts de bourgeonnement. La présence anormale de filaments d’actine au site du bourgeonnement du virus en absence de MICAL1 est donc responsable des défauts de bourgeonnement constatés.
Le composé chimique utilisé pour limiter la polymérisation de l’actine (CK666) inhibe la formation des réseaux d’actine branchée, qui coexistent dans la cellule avec des réseaux de filaments linéaires. Jusqu’alors, le rôle de MICAL1 sur la régulation de l’actine branchée n’avait pas été exploré. Grâce à des expériences in vitro sur des filaments uniques d’actine rendus fluorescents et observés dans des chambres microfluidiques, il a pu être montré que MICAL1 peut directement dissocier les branches des réseaux d’actine branchée, ce qui a révélé une nouvelle fonction de cette enzyme. Ainsi, MICAL1, vraisemblablement par son activité oxydase [ 12 ], assure le désassemblage des réseaux d’actine branchée localement aux sites de bourgeonnement du VIH-1.
L’activité de MICAL1 est finement contrôlée afin d’éviter la dépolymérisation complète du cytosquelette d’actine. L’enzyme est ainsi présente sous une forme auto-inhibée lorsque son domaine C-terminal, aussi appelé RBD ( Rab-binding domain ), est replié sur son domaine catalytique N-terminal. Son activation est donc dépendante de protéines activatrices, notamment la guanine triphosphatase (GTPase) Rab35. Cette étude montre que Rab35 est précisément localisée au niveau des sites du bourgeonnement du VIH-1, et l’inhibition de son expression dans les cellules infectées par le virus entraîne des effets similaires à ceux constatés en l’absence de MICAL1 : une réduction de la libération des virus dans le milieu extracellulaire et leur accumulation à la surface des cellules. La déplétion simultanée de MICAL1 et de Rab35 n’ayant pas d’effet additif, il a été conclu que ces deux protéines opèrent de concert lors du bourgeonnement du VIH-1.
En résumé, cette étude a fait progresser notre compréhension des mécanismes impliqués dans le contrôle de l’actine corticale lors du bourgeonnement du VIH-1 : le désassemblage local du cytosquelette d’actine par l’enzyme MICAL1 activée par Rab35 promeut la déformation membranaire induite par Gag et ainsi, la scission des virus par la machinerie ESCRT-III ( Figure 2 ). Plus généralement, l’oxydation de l’actine par MICAL1 pourrait jouer un rôle clé dans le bourgeonnement d’autres virus enveloppés. Ainsi, l’inhibition chimique de MICAL1 pourrait permettre de réduire la production d’autres virus enveloppés, comme les virus Ebola, de Marburg, et de Lassa, qui bourgeonnent, comme le VIH-1, à la membrane plasmique en recrutant la machinerie cellulaire ESCRT-III.
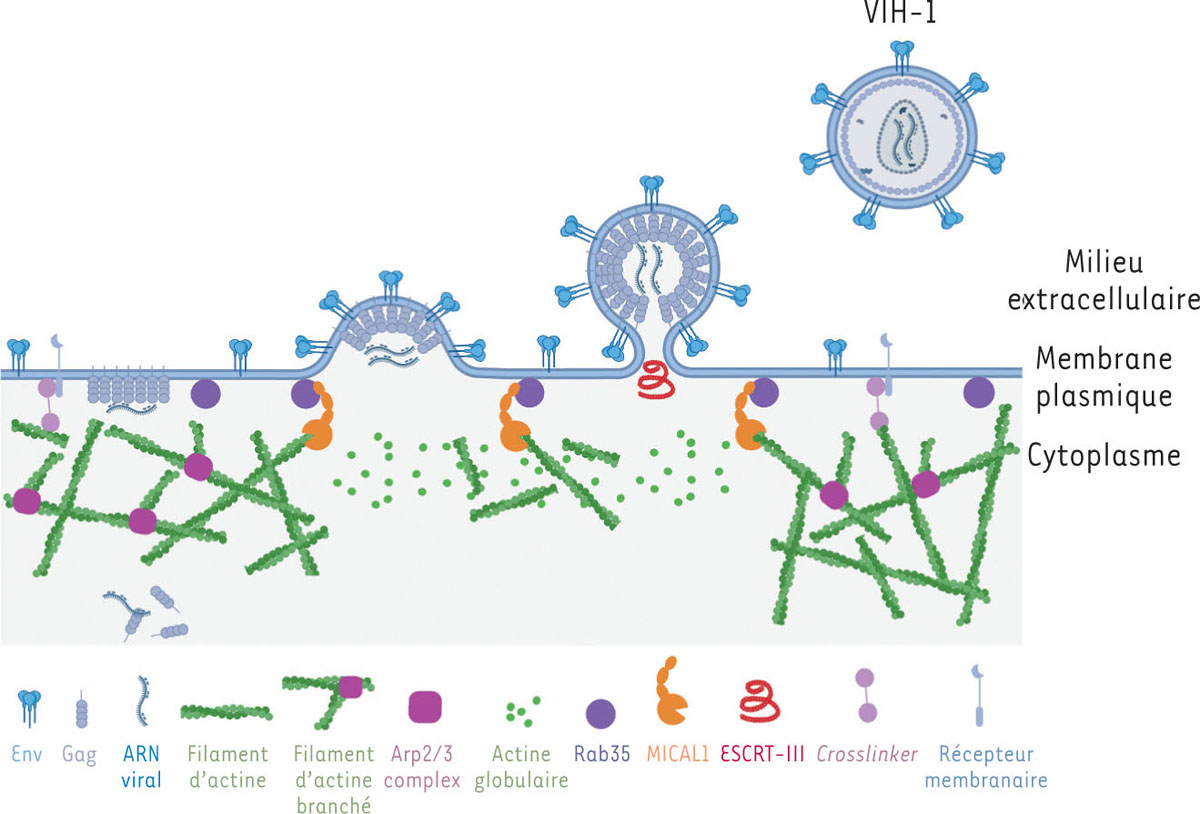
| Figure 2.
Modèle du rôle de Rab35 et MICAL1 dans le bourgeonnement du VIH-1
.
La protéine Rab35 est recrutée aux sites de bourgeonnement du VIH-1, où elle active l’enzyme MICAL1. MICAL1 désassemble localement les filaments d’actine, par dépolymérisation et débranchement, ce qui permet la déformation complète de la membrane plasmique par Gag, et le recrutement de la machinerie cellulaire ESCRT (
endosomal sorting complex required for transport
). Cela favorise le bourgeonnement du virus et sa libération par la cellule infectée. Figure réalisée avec BioRender.
|