| |
| Med Sci (Paris). 41(6-7): 551–554. doi: 10.1051/medsci/2025089.Plasticité épithéliale dans les maladies hépatiques chroniques Maïa Pesic,1,2a Ludovic Vallier,1,2b and Dylan Liabeuf1,2c 1Berlin institute of health (BIH), BIH centre for regenerative therapies (BCRT), Charité-Universitätsmedizin
,
Berlin
,
Allemagne 2Max Planck Institute for molecular genetics
,
Berlin
,
Allemagne |
Ce que l’on sait de la physiopathologie…
Les maladies hépatiques chroniques sont des affections progressives caractérisées par des lésions répétitives et la régénération graduelle du tissu hépatique, conduisant à une fibrose, et finalement à la cirrhose [
1
]. Leurs origines diverses incluent des causes métaboliques, comme pour la maladie stéatosique du foie associée à un dysfonctionnement métabolique (MASLD) et son stade ultérieur, la stéatohépatite associée à un dysfonctionnement métabolique (MASH), toxiques (maladie alcoolique du foie, hépatotoxicité médicamenteuse chronique), virales (hépatites B et C), et auto-immunes.
La prévalence des maladies hépatiques chroniques a considérablement augmenté au cours des dernières décennies, provoquant une crise de santé publique mondiale [
2
,
3
]. De plus, le fardeau économique sociétal ne peut être ignoré car ces maladies nécessitent un traitement et une surveillance à long terme. Ces deux aspects soulignent le besoin urgent d’améliorer les stratégies préventives, diagnostiques et thérapeutiques, ce qui rend nécessaire d’approfondir notre compréhension des mécanismes moléculaires impliqués dans l’apparition de la maladie et dans sa progression.
La physiopathologie des maladies hépatiques chroniques doit prendre en compte l’interaction complexe de facteurs génétiques, environnementaux et métaboliques. Malgré leurs causes hétérogènes, ces maladies ont une progression commune. Les lésions hépatiques persistantes déclenchent un processus de cicatrisation caractérisé par une réaction pro-inflammatoire, qui active les cellules stellaires hépatiques et leur fait produire de manière excessive de la matrice extracellulaire, ce qui entraîne une fibrose. Au fur et à mesure de la progression fibrotique, l’architecture du foie est perdue, et le fonctionnement hépatique se détériore. Ce changement implique directement les cellules épithéliales constituant le parenchyme hépatique : les hépatocytes et les cholangiocytes [
4
]. Or, le renouvellement des hépatocytes joue un rôle homéostatique essentiel pour cet organe à fort potentiel de régénération [
5
–
7
], et est également impliqué dans le processus de réparation après une lésion hépatique. Contrairement aux lésions hépatiques aigües, où la prolifération des cellules épithéliales (hépatocytes et, dans une moindre mesure, cholangiocytes) aide à la régénération, en cas de lésion chronique, la prolifération des hépatocytes est bloquée, ce qui empêche le retour à un foie sain. Ainsi, à des stades avancés des maladies chroniques hépatiques, la présence de « nodules régénératifs » contenant principalement des hépatocytes altérés signale des tentatives infructueuses de restauration tissulaire, entraînant une instabilité génomique qui favorise le développement d’un cancer. Notre compréhension des processus régénératifs au cours des maladies hépatiques chroniques, qu’ils soient efficaces ou fonctionnellement inadaptés, reste incomplète. Notamment, on ignore dans quelle mesure des processus régénératifs alternatifs à la prolifération des cellules épithéliales sont impliqués dans la réparation tissulaire, mais aussi dans la pathogenèse. Répondre à cette question pourrait aider à découvrir des leviers moléculaires exploitables pour développer des thérapies limitant la progression des maladies hépatiques chroniques et favorisant la réparation des tissus affectés. Cependant, l’étude de ces processus régénératifs chez l’homme représente un véritable défi technique. Les modèles d’étude traditionnels, tels que les modèles animaux (rongeurs, poisson zèbre) et les systèmes de culture cellulaire
in vitro
, ont fourni des informations précieuses, mais ne peuvent reproduire la complexité des maladies hépatiques humaines. Il existe donc un besoin pressant de développer d’autres modèles capables d’imiter l’environnement du foie humain et de faciliter l’étude de processus dynamiques tels que la fibrose, la régénération et la carcinogenèse qui en découle [
8
].
|
Comment en savoir plus pour soigner…
Les mécanismes qui sous-tendent la régénération de l’organe durant la progression des maladies chroniques du foie humain restent mal compris. Les modèles traditionnels,
in vivo
(animaux) ou
in vitro
(cultures de lignées cellulaires souvent transformées ou cancéreuses), ont parfois fourni des informations contradictoires, et différents mécanismes ont été identifiés en fonction du modèle et du type de lésion. Certains modèles ont révélé des processus de dédifférenciation et re-différenciation des cellules hépatiques, d’autres, l’activation d’une population de cellules progénitrices assimilées aux cellules souches. Cette population s’avère être associée aux dysfonctionnements métaboliques, et apparaît lorsque les hépatocytes sont endommagés et incapables de proliférer. Il convient de préciser que ces différents mécanismes, les voies métaboliques et inflammatoires impliquées, et notamment la présence de cellules souches, n’ont pas encore été validés dans l’espèce humaine.
Dans ce contexte, une récente étude propose pour la première fois une description de la plasticité cellulaire dans les processus régénératifs de la phase de stéatose hépatique associée à un dysfonctionnement métabolique (MASLD) [
9
]. Les auteurs ont utilisé une technique de séquençage de l’ARN des noyaux cellulaires (
single-nucleus RNA sequencing
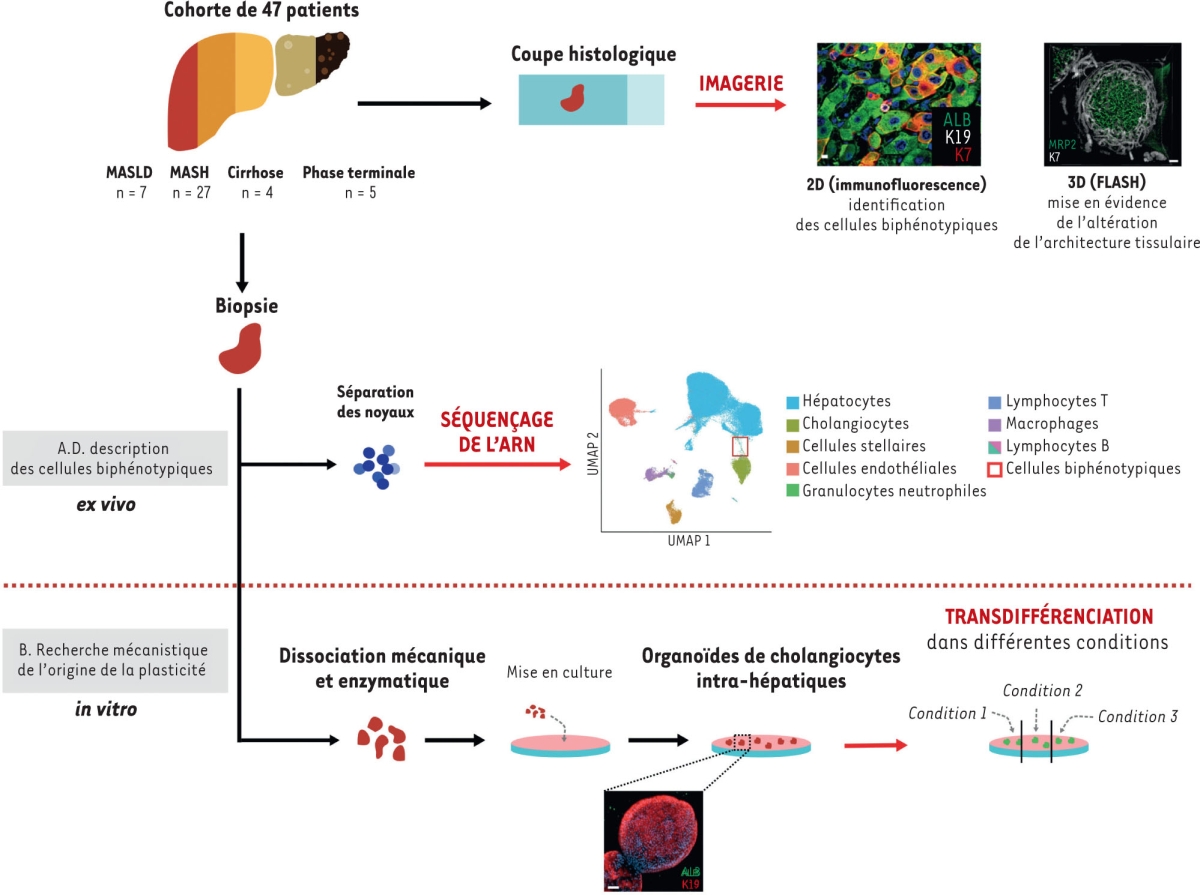
, snRNA-seq), qui leur a permis de définir le transcriptome de cellules individuelles chez 47 personnes atteintes ou non d’une maladie hépatique chronique à différents stades (MASLD, MASH, cirrhose, et phase terminale). Grâce à cela, la composition multicellulaire de chaque foie a pu être étudiée, et notamment les caractéristiques des hépatocytes et des cholangiocytes au cours de la progression de la maladie.
Cet atlas cellulaire a pu être couplé à une vision spatiale détaillée, grâce à des techniques d’imagerie en 3D, de l’architecture hépatique durant la progression de la maladie. Après un processus de clarification optique, les biopsies de foie ont été colorées avec des anticorps dirigés contre des marqueurs tels que MRP2 (
multidrug resistance protein 2
) pour les hépatocytes, et KRT7 (kératine 7), KRT19 (kératine 19) pour les cholangiocytes. Les échantillons ont ensuite été imagés par des techniques de microscopie avancées, notamment l’analyse microscopique rapide d’organes entiers colorés par anticorps (
fast light-microscopic analysis of antibody-stained whole organs
, FLASH) [
10
,
11
] et la microscopie fondée sur l’immunofluorescence à haute résolution (
Figure 1
).
 | Figure 1
Représentation graphique du plan expérimental
.
MASLD :
metabolic dysfunction-associated steatotic liver disease
(maladie stéatosique du foie associée à un dysfonctionnement métabolique) ; MASH :
metabolic dysfunction-associated steatohepatitis
(stéatohépatite associée à un dysfonctionnement métabolique) ; FLASH : f
ast light-microscopic analysis of antibody-stained whole organs
(analyse microscopique rapide d’organes entiers colorés par anticorps). Avec la permission de Nature [
9
].
|
|
Ce faisant, cette équipe a constaté que le foie malade peut contenir des cellules biphénotypiques combinant l’expression de gènes caractérisant les hépatocytes et les cholangiocytes. Le nombre de ces cellules augmente durant la progression de la maladie jusqu’aux stades terminaux. Ces cellules biphénotypiques sont produites aussi bien par les hépatocytes que par les cholangiocytes [
9
]. Les résultats suggèrent que sous la pression répétée des blessures associées à la MASLD et à sa progression, les cellules épithéliales hépatiques acquièrent une plasticité conduisant à un processus de transdifférenciation visant à remplacer les hépatocytes détruits par la maladie. En revanche, ils n’ont pas mis en évidence l’activation de cellules souches ou le processus de dédifférenciation qui avaient été constatés chez les rongeurs. Par conséquent, l’augmentation de la plasticité cellulaire pourrait représenter la réponse régénérative principale dans le contexte des maladies chroniques hépatiques humaines (
Figure 2
).
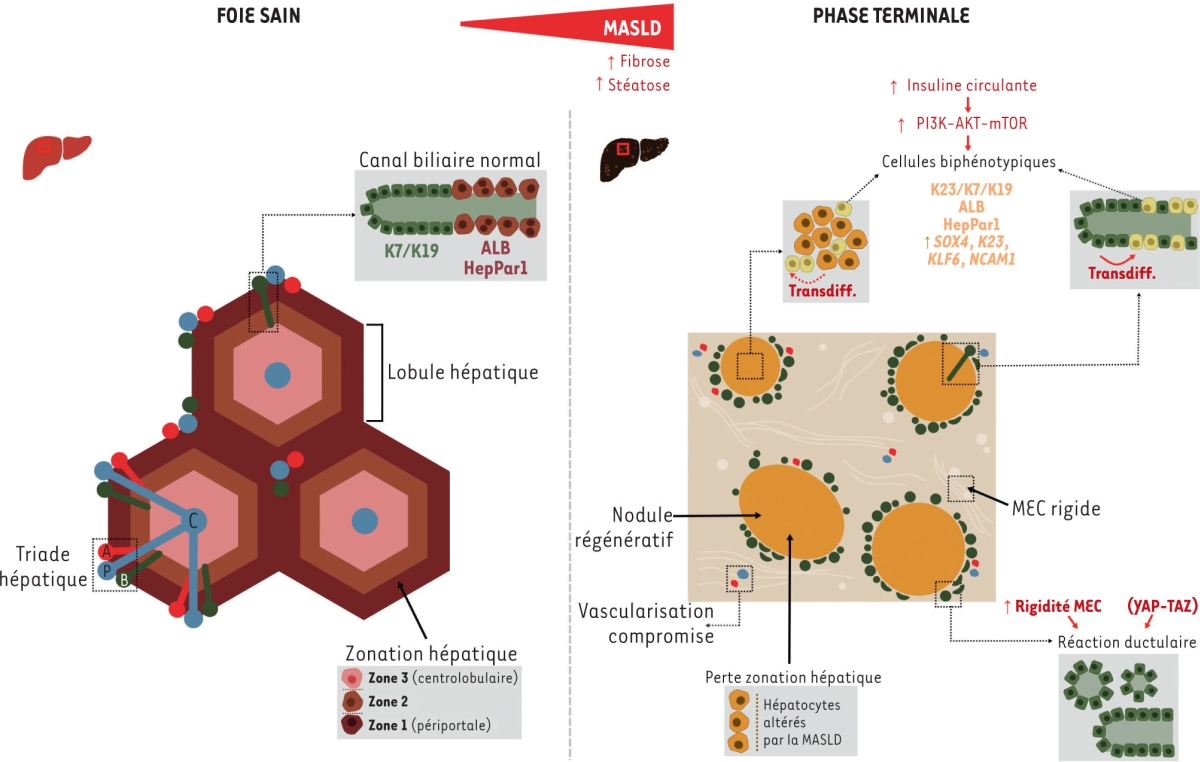
 | Figure 2
Représentation schématique des altérations structurelles du foie d’un individu atteint de MASLD en phase terminale par rapport à un foie sain. À gauche :
le foie sain est organisé en lobules hépatiques, centrés autour d’une branche de la veine hépatique (veine centrale, C), et alimentés en périphérie par la triade hépatique : artère hépatique (A), canal biliaire (B), veine porte (P).
À droite :
lors de l’évolution de la maladie, la structure lobulaire caractéristique du foie, avec sa zonation, est remplacée par des nodules régénératifs ayant perdu la zonation et entourés de nombreuses structures ductulaires, dans une matrice extracellulaire (MEC) fibrotique. AKT (PKB) : protéine kinase B ; ALB : albumine ; HepPar1 :
hepatocyte paraffin 1
; KLF6 :
Kruppel-like factor 6
; K7, K19, K23 : kératines 7, 19, 23 ; MRP2 :
multidrug resistance protein 2
; mTOR :
mammalian target of rapamycin
; NCAM1 :
neural cell adhesion molecule 1
; PI3K : phosphoinositide 3-kinase ; SOX4 :
SRY-box transcription factor 4
; TAZ :
tafazzin
; TGF-β :
transforming growth factor β
; YAP :
Yes-associated protein
.
|
La carte cellulaire obtenue par ces investigations a aussi permis une analyse approfondie des changements structurels au cours de la progression de la maladie. En effet, les dysfonctionnements hépatiques de la MASLD sont associés à une perte de zonation des hépatocytes et à un remodelage profond de l’arbre biliaire. L’apparition de cellules biphénotypiques semble donc liée à un changement profond de la niche cellulaire entourant les hépatocytes et cholangiocytes [
9
] (
Figure 2
).
Cette étude a aussi révélé des facteurs potentiellement impliqués dans ce processus de plasticité-transdifférenciation. Les gènes codant les facteurs de transcription SOX4 (
SRY-related HMG-box 4
) et KLF6 (
Krüppel-like factor 6
) sont par exemple fortement exprimés dans les cellules biphénotypiques [
9
]. Il convient de noter que la plupart de ces facteurs avaient précédemment été associés aux cancers hépatiques. La tumorigenèse qui peut survenir dans l’évolution de la MASLD pourrait donc provenir d’un processus régénératif dysfonctionnel. Afin de modéliser les mécanismes sous-jacents, l’équipe a tiré parti des organoïdes de cholangiocytes humains cultivés
in vitro
, qui ont permis de montrer l’importance de la voie de signalisation de l’insuline pour la production des cellules biphénotypiques [
9
] (
Figure 1
). Or l’obésité, cause principale de la MASLD et qui est souvent accompagnée d’un diabète de type 2, entraîne une surproduction d’insuline. Celle-ci pourrait donc être un inducteur majeur du processus régénératif et potentiellement cancéreux dans le foie MASLD (
Figure 2
). L’ensemble de ces résultats montre que la combinaison de nouveaux outils comme le séquençage de l’ARN de cellules individuelles et des organoïdes dérivés de patients permet d’étudier des mécanismes biologiques dont l’analyse était jusqu’à maintenant réservée aux modèles animaux. Néanmoins, plusieurs aspects des mécanismes de la régénération hépatique restent à élucider. En particulier, les interactions entre les mécanismes régénératifs et les mécanismes pro-inflammatoires et fibrotiques n’ont pas été éclaircies. La réaction ductulaire, définie comme une prolifération excessive des cholangiocytes et considérée comme une étape initiale de la régénération hépatique, reste elle aussi à caractériser quant à ses implications régénératrice ou délétère [
12
,
13
](
→
).
(→) Voir
m/s
n° 11, 2012, page 958
Des études complémentaires sont donc nécessaires pour tenter de comprendre comment les différents types cellulaires du foie interagissent pour stimuler ou inhiber la réparation tissulaire. |
Les résultats de ces travaux de recherche représentent une avancée significative dans la compréhension des maladies chroniques du foie et de la dégénérescence hépatique progressive qu’elles entraînent. Ils ont mis en lumière le rôle crucial de la plasticité épithéliale dans la pathogenèse et la régénération hépatique. L’identification des mécanismes sous-jacents au processus de régénération tissulaire dans le foie pourrait d’ailleurs être mise à profit pour d’autres organes tels que le poumon ou le rein, où l’on constate également des processus inflammatoires et fibrosants en cas de maladie chronique. Ces résultats fournissent également des bases prometteuses pour le développement de biomarqueurs spécifiques et de stratégies visant à moduler la plasticité épithéliale afin de prévenir la progression des maladies chroniques. Enfin, ils soulignent les liens étroits entre régénération tissulaire et tumorigenèse hépatique, avec là encore de possibles implications diagnostiques et thérapeutiques. La modulation ciblée des voies impliquées dans la plasticité cellulaire chez les personnes atteintes de maladies hépatiques chroniques pourrait en effet permettre de renforcer la réponse réparatrice du foie tout en atténuant le risque oncogénique. |
|
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
.
|
1.
Eslam
M
,
Newsome
PN
,
Sarin
SK
,
et al.
.
A new definition for metabolic dysfunction-associated fatty liver disease: An international expert consensus statement.
.
J Hepatol
.
2020;
;
73
:
:202.
–
9
.
2.
Devarbhavi
H
,
Asrani
SK
,
Arab
JP
,
et al.
.
Global burden of liver disease: 2023 update.
.
J Hepatol
.
2023;
;
79
:
:516.
–
37
.
3.
Riazi
K
,
Azhari
H
,
Charette
JH
,
et al.
.
The prevalence and incidence of NAFLD worldwide: a systematic review and meta-analysis.
.
Lancet Gastroenterol Hepatol
.
2022;
;
7
:
:851.
–
861
.
4.
Mu
X
,
Español-Suñer
R
,
Mederacke
I
,
et al.
.
Hepatocellular carcinoma originates from hepatocytes and not from the progenitor/biliary compartment.
.
J Clin Invest
.
2015;
;
125
:
:3891.
–
903
.
5.
Raven
A
,
Lu
W-Y
,
Man
TY
,
et al.
.
Cholangiocytes act as facultative liver stem cells during impaired hepatocyte regeneration.
.
Nature
.
2017;
;
547
:
:350.
–
4
.
6.
Wang
B
,
Zhao
L
,
Fish
M
,
et al.
.
Self-renewing diploid Axin2
+
cells fuel homeostatic renewal of the liver
.
.
Nature
.
2015;
;
524
:
:180.
–
85
.
7.
Michalopoulos
GK
,
Bhushan
B
.
Liver regeneration: biological and pathological mechanisms and implications.
.
Nat Rev Gastroenterol Hepatol
.
2021;
;
18
:
:40.
–
55
.
8.
Segovia-Miranda
F
,
Morales-Navarrete
H
,
Kücken
M
,
et al.
.
Three-dimensional spatially resolved geometrical and functional models of human liver tissue reveal new aspects of NAFLD progression.
.
Nat Med
.
2019;
;
25
:
:1885.
–
93
.
9.
Gribben
C
,
Galanakis
V
,
Calderwood
A
,
et al.
.
Acquisition of epithelial plasticity in human chronic liver disease.
.
Nature
.
2024;
;
630
:
:166.
–
73
.
10.
Messal
HA
,
Almagro
J
,
Zaw Thin
M
,
et al.
.
Antigen retrieval and clearing for whole-organ immunofluorescence by FLASH.
.
Nat Protoc
.
2021;
;
16
:
:239.
–
62
.
11.
Messal
HA
,
Alt
S
,
Ferreira
RMM
,
et al.
.
Tissue curvature and apicobasal mechanical tension imbalance instruct cancer morphogenesis.
.
Nature
.
2019;
;
566
:
:126.
–
30
.
12.
Lemaigre
F.
Le développement des lignages hépatiques dans le foie normal et durant la régénération.
.
Med Sci (Paris)
.
2012;
;
28
:
:958.
–
62
.
13.
Sato
K
,
Marzioni
M
,
Meng
F
,
et al.
.
Ductular reaction in liver diseases: Pathological mechanisms and translational significances.
.
Hepatology
.
2019;
;
69
:
:420.
.
|