| |
| Med Sci (Paris). 41(4): 312–315. doi: 10.1051/medsci/2025052.L’horloge circadienne, cible thérapeutique contre la fibrose hépatique Quand l’horloge circadienne remet le foie au diapason Émilie Crouchet,1a Catherine Schuster,1b and Thomas F. Baumert1,2,3c 1Université de Strasbourg, Inserm, Institut de médecine translationnelle et des maladies du foie (ITM)
,
UMR_S1110
,
Strasbourg
,
France 2Pôle des pathologies hépatiques et digestives, Hôpitaux universitaires de Strasbourg
,
Strasbourg
,
France 3Institut universitaire de France (IUF)
,
Paris
,
France MeSH keywords: |
L’horloge circadienne : orchestre symphonique de notre organisme
Les routines quotidiennes de la vie sur Terre sont rythmées par les cycles lumière/obscurité induits par la rotation de notre planète. Nous sommes des êtres diurnes : nous menons la plupart de nos activités pendant la journée, et nous nous reposons pendant la nuit. Comme tous les organismes sensibles à la lumière, nous avons développé différents mécanismes d’adaptation à ces changements, et en particulier les rythmes circadiens, qui désignent toutes les variations rythmiques internes sur une période de 24 heures. Sous le contrôle de notre horloge interne, ces cycles quotidiens coordonnent nos fonctions biologiques et préparent le corps aux activités récurrentes telles que les cycles veille/sommeil et alimentation/jeûne, ou la régulation de la température corporelle, du rythme cardiaque, et du métabolisme [
1
].
Dans les années 1950, Franz Halberg, l’un des pionniers de la chronobiologie moderne, propose le terme « circadien », dérivé du latin
circa diem
(« environ un jour »), pour décrire les oscillations d’environ 24 heures de notre horloge interne [
2
]. L’horloge circadienne des mammifères est structurée de manière hiérarchique. L’horloge centrale est située dans le noyau suprachiasmatique du cerveau, et est principalement stimulée par la lumière perçue par la rétine et transmise par l’axe rétino-hypothalamique (
Figure 1
). Le noyau suprachiasmatique, tel un chef d’orchestre, synchronise les oscillateurs secondaires situés dans les tissus périphériques, qui répondent en jouant leur partition cellulaire et en régulant l’expression de milliers de gènes (
Figure 1
). De plus, la plupart de nos cellules, si ce n’est toutes, possèdent une horloge moléculaire autonome, qu’elles conservent en culture
ex vivo
[
3
]. La luminosité régule principalement l’horloge centrale, mais d’autres signaux temporels additionnels permettent de maintenir cette harmonie entre les différents oscillateurs. Ils peuvent être d’origine neuronale, hormonale ou métabolique. Tous ces signaux répondent au nom allemand «
Zeitgeber »
, qui signifie « donneur de temps ». En plus de la lumière, les principaux
Zeitgeber
incluent l’alimentation, le sommeil, l’exercice physique et la température (
Figure 1
) [
1
].
 | Figure 1
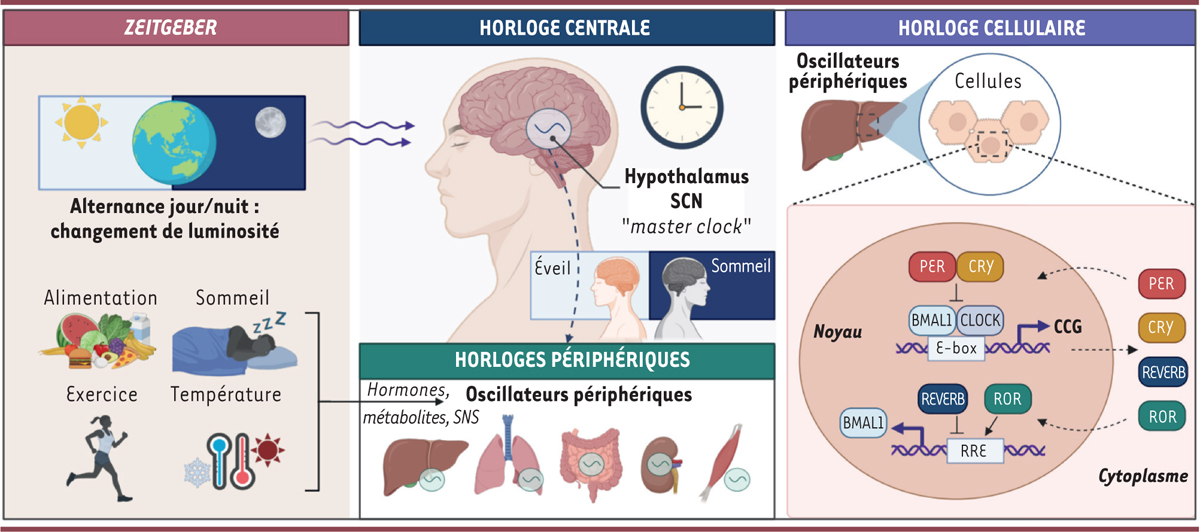
Hiérarchie et régulation de l’horloge circadienne
.
L’horloge centrale se situe dans le noyau suprachiasmatique (
suprachiasmatic nucleus
, SCN) du cerveau. Elle est principalement influencée par les changements de luminosité. Elle contrôle et synchronise les horloges périphériques dans différents organes. D’autres
Zeitgeber
(« donneurs de temps ») participent à la régulation des horloges périphériques, comme les hormones circulantes, les métabolites, le système nerveux sympathique (SNS), qui peuvent être modulés par l’alimentation, le sommeil, l’exercice physique, et la température corporelle. Chaque cellule des organes ou tissus périphériques contient de plus une horloge cellulaire autonome. Elle consiste en deux boucles de rétroaction transcriptionnelle régulant l’expression oscillatoire de milliers de gènes dits CCG (
clock-controlled genes
). Ces derniers régissent de très nombreux processus physiologiques. Protéines impliquées dans les boucles de régulation transcriptionnelle de l’horloge circadienne : BMAL1 (
basic helix-loop-helix ARNT-like 1
) et CLOCK (
clock circadian regulator
), PER (
period
), CRY (
cryptochrome
), NR1D1 et NR1D2 (
nuclear receptor subfamily 1 group D members 1 and 2
) aussi appelés REV-ERBα et REV-ERBβ, ROR (
retinoic acid receptor-related orphan receptor
). RRE :
ROR and REV-ERB-response element
. Figure réalisée avec BioRender.
|
|
Dérégulation des rythmes circadiens : de la symphonie à la cacophonie
Dans nos sociétés modernes, les individus sont moins contraints par les cycles jour/nuit et autres
Zeitgeber
. En effet, la lumière artificielle, la disponibilité continue de nourriture, les exigences professionnelles (exemple des travailleurs de nuit) et la privation de sommeil perturbent nos rythmes circadiens. De nombreuses études scientifiques ont montré que la perturbation des rythmes circadiens peut être à l’origine de diverses maladies [
1
]. Pour filer la métaphore, lorsque la communication entre le chef et son orchestre est perturbée, il en résulte une cacophonie cellulaire pouvant mener à des troubles neurologiques, cardiaques, ou métaboliques, incluant l’obésité et le diabète de type 2 [
1
].
Le foie est un organe métaboliquement très actif et fortement influencé par les cycles alimentation/jeûne. La disponibilité des nutriments pendant la phase d’éveil permet le stockage d’énergie, tandis que pendant la phase de repos ou en cas de demande accrue (exercice physique), cette réserve d’énergie est réquisitionnée. Plusieurs mécanismes fonctionnent ici de concert. D’une part, les niveaux d’énergie et de métabolites sont signalés aux oscillateurs moléculaires par différents capteurs métaboliques (
e.g
., les facteurs de transcription SIRT1 et SREBP, ou les protéine-kinases AMPK et AKT
1,
). D’autre part, ces capteurs de l’état énergétique de la cellule interagissent avec les protéines de l’horloge circadienne et modulent leur activité. Ces mécanismes se traduisent par une rythmicité générale du transcriptome, du métabolome et du lipidome hépatiques. Une relation orchestrée entre l’horloge circadienne et le métabolisme est donc indispensable au bon fonctionnement du foie [
3
,
4
].
L’apport de nutriments en excès, notamment de sucres, couplé à une mauvaise hygiène de vie, de sommeil, et à la sédentarité perturbent cet équilibre. La perte des rythmes peut entraîner des maladies telles que la stéatose hépatique métabolique (
metabolic dysfunction-associated fatty liver disease
, MAFLD). Cette maladie comprend un large spectre de lésions hépatiques allant de la stéatose simple à la stéatohépatite (
metabolic dysfunction-associated steatohepatitis
, MASH), sa forme la plus sévère, pouvant entraîner de graves complications telles qu’une fibrose avancée, une cirrhose, ou un cancer du foie [
3
–
5
]. Au vu des changements de mode de vie actuels, les épidémiologistes prévoient un fort accroissement des cas de MASH au cours de la prochaine décennie [
6
]. Récemment, un traitement contre la MASH réduisant la stéatose a été mis sur le marché. Cependant, son effet sur la fibrose hépatique avancée et ses complications doit encore être évalué. Rétablir les rythmes circadiens hépatiques dérégulés par les troubles métaboliques pourrait ainsi constituer une nouvelle stratégie thérapeutique.
|
Rétablir les rythmes circadiens contre la fibrose hépatique : bien connaître la partition
Notre équipe de recherche s’est donc penchée sur cette question [
7
]. Les fibroblastes hépatiques, ou cellules étoilées, sont des acteurs majeurs de la fibrose. En cas de dommages chroniques, ces cellules sont surstimulées pour réparer les tissus. La voie de signalisation du TGF-β (
tumor necrosis factor
β) permet notamment de différencier les cellules étoilées en myofibroblastes, qui produisent en excès une matrice extracellulaire anormale [
8
]. En analysant les variations circadiennes du transcriptome hépatique de souris, mais également de patients, nous avons découvert que l’induction de la voie du TGF-β et les réponses des cellules étoilées sont cycliques, et donc sous contrôle de l’horloge circadienne. Une expérience dans un modèle murin de MASH a permis de montrer que les cellules étoilées possèdent leur propre horloge moléculaire contrôlant leur activation, leur métabolisme, et la production de matrice extracellulaire. De plus, les troubles métaboliques associés à la MASH perturbent l’expression rythmique de différents gènes et l’expression des gènes pro-fibrotiques dans les cellules étoilées, et contribuent ainsi au développement de la fibrose (
Figure 2
) [
7
]. Une analyse réalisée sur des cellules isolées de foie humain a également mis en évidence un mécanisme complexe de communication entre les hépatocytes et les cellules étoilées : la perturbation des rythmes circadiens dans les hépatocytes induit une perte de synchronicité dans les cellules étoilées. Ainsi, l’installation progressive d’une diaphonie
2,
entre ces deux types cellulaires, due à la perturbation de leurs rythmes circadiens respectifs et aux troubles métaboliques, contribuerait à la progression de la maladie (
Figure 2
) [
7
].
 | Figure 2
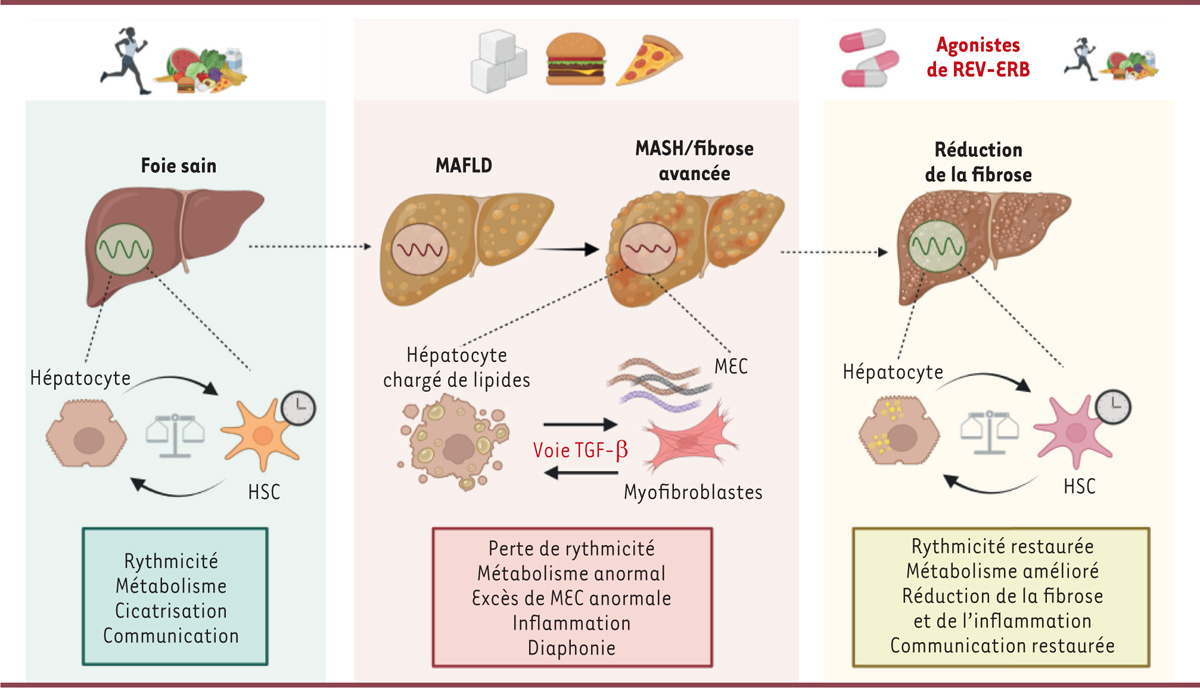
Rétablir les rythmes circadiens réduit la fibrose hépatique
.
Dans le foie sain, les rythmes circadiens contrôlent l’expression de nombreux gènes, dont les gènes du métabolisme et les gènes impliqués dans la production de matrice extracellulaire (MEC) (processus de cicatrisation). Ils permettent également une communication optimale entre les cellules étoilées (
hepatic stellate cells
, HSC) et les hépatocytes. Dans la fibrose hépatique induite par la MASH, la perturbation des rythmes circadiens entraîne un métabolisme hépatique anormal et une inflammation du foie. De plus, une stimulation persistante de la voie de signalisation par TGFβ induit une activation des HSC en myofibroblastes, qui produisent en excès une MEC anormale. Ce phénomène perturbe fortement la communication entre les hépatocytes et les myofibroblastes. Le ciblage pharmacologique de l’horloge circadienne par un agoniste des protéines REV-ERB réduit la fibrose hépatique et rétablit la communication intercellulaire et la production physiologique de MEC. Figure réalisée avec BioRender.
|
À la lumière de ces résultats, nous avons alors cherché à apporter une « preuve de concept » à visée thérapeutique en modulant les rythmes circadiens dans des modèles murins de fibrose hépatique induite par la MASH. Nous avons montré que l’activation des récepteurs nucléaires REV-ERB, impliqués dans la régulation du rythme circadien (
Figure 1
), par l’agoniste SR9009 réduit significativement la fibrose hépatique en diminuant la production de TGF-β et de son récepteur, l’activation des cellules étoilées et l’accumulation de matrice extracellulaire, ainsi que l’inflammation hépatique (
Figure 2
) [
7
]. Nous avons également obtenu des résultats en faveur d’une amélioration des voies métaboliques dans les hépatocytes. Enfin, nous avons confirmé le potentiel thérapeutique de SR9009 sur la fibrose induite dans un modèle de sphéroïdes multicellulaires humains
3
.
|
La fibrose hépatique due aux maladies métaboliques comme la MASH, en constante augmentation, constitue un problème mondial de santé publique. Nous avons montré que la régulation des rythmes circadiens est perturbée en cas de maladie hépatique chronique, et que cette perturbation contribue à la progression de la fibrose. En ayant montré qu’un composé ciblant l’horloge circadienne améliore la fibrose hépatique dans des modèles murins ou dérivés de tissu humain, nous proposons une nouvelle stratégie thérapeutique contre la fibrose. Des études complémentaires sont en cours pour transférer ces résultats vers la pratique médicale.
La portée de ces découvertes dépasse le cadre de la MASH. En effet, l’infection chronique par le virus de l’hépatite C, une autre cause majeure de la fibrose hépatique et du cancer du foie, perturbe fortement le transcriptome et l’épigénome hépatique, ainsi que la rythmicité cellulaire, en modifiant l’expression des gènes de l’horloge moléculaire. Ces perturbations conduisent à l’activation de voies métaboliques anormales et au développement de la fibrose, et perdurent partiellement même après l’élimination du virus [
10
]. Pour ces patients, le risque de développer un cancer du foie à long terme reste donc élevé. Une stratégie thérapeutique ciblant l’horloge circadienne pourrait améliorer la fibrose et prévenir le développement du cancer du foie chez les personnes souffrant d’une fibrose avancée induite par une infection chronique par le virus de l’hépatite C, ou par le virus de l’hépatite B [
11
].
|
Footnotes |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
.
|
1.
Schrader
LA
,
Ronnekleiv-Kelly
SM
,
Hogenesch
JB
,
et al.
.
Circadian disruption, clock genes, and metabolic health.
.
J Clin Invest
.
2024;
;
134
:
:e170998.
.
2.
Halberg
F.
The 24-hour scale: a time dimension of adaptive functional organization.
.
Perspect Biol Med
.
1960;
;
3
:
:491.
–
527
.
3.
Bolshette
N
,
Ibrahim
H
,
Reinke
H
,
et al.
.
Circadian regulation of liver function: from molecular mechanisms to disease pathophysiology.
.
Nat Rev Gastroenterol Hepatol
.
2023;
;
20
:
:695.
–
707
.
4.
Mukherji
A
,
Dachraoui
M
,
Baumert
TF.
Perturbation of the circadian clock and pathogenesis of NAFLD.
.
Metabolism
.
2020;
;
111S
:
:154337.
.
5.
Mukherji
A
,
Bailey
SM
,
Staels
B
,
et al.
.
The circadian clock and liver function in health and disease.
.
J Hepatol
.
2019;
;
71
:
:200.
–
11
.
6.
Kalligeros
M
,
Henry
L
,
Younossi
ZM.
Metabolic dysfunction-associated steatotic liver disease and its link to cancer.
.
Metabolism
.
2024;
;
160
:
:156004.
.
7.
Crouchet
E
,
Dachraoui
M
,
Jühling
F
,
et al.
.
Targeting the liver clock improves fibrosis by restoring TGF-α signaling.
.
J Hepatol
.
2024;
;
S0168-8278
(
(24)
)
:02480.
–
2
.
8.
Parola
M
,
Pinzani
M.
Liver fibrosis in NAFLD/NASH: from pathophysiology towards diagnostic and therapeutic strategies.
.
Mol Aspects Med
.
2024;
;
95
:
:101231.
.
9.
Roehlen
N
,
Saviano
A
,
El Saghire
H
,
et al.
.
A monoclonal antibody targeting nonjunctional claudin-1 inhibits fibrosis in patient-derived models by modulating cell plasticity.
.
Sci Transl Med
.
2022;
;
14
:
:eabj4221.
.
10.
Mukherji
A
,
Jühling
F
,
Simanjuntak
Y
,
et al.
.
An atlas of the human liver diurnal transcriptome and its perturbation by hepatitis C virus infection.
.
Nat Commun
.
2024;
;
15
:
:7486.
.
11.
Zhuang
X
,
Forde
D
,
Tsukuda
S
,
et al.
.
Circadian control of hepatitis B virus replication.
.
Nat Commun
.
2021;
;
12
:
:1658.
.
|