| |
| Med Sci (Paris). 40(8-9): 643–652. doi: 10.1051/medsci/2024100.Des organoïdes cérébraux pour la compréhension et la thérapie des maladies génétiques rares avec troubles neurodéveloppementaux Fatima El It,1,2 Laurence Faivre,1,2,3 Christel Thauvin-Robinet,1,2,3 Antonio Vitobello,1,2,4 and Laurence Duplomb1,2* 1UMR1231 Inserm, Génétique des anomalies du développement (GAD), université de Bourgogne Franche-Comté
,
Dijon
,
France 2FHU TRANSLAD, CHU Dijon
,
Dijon
,
France 3Centre de référence des anomalies du développement et syndromes malformatifs, CHU Dijon
,
Dijon
,
France 4Unité fonctionnelle innovation en diagnostic génomique des maladies rares, CHU Dijon
,
Dijon
,
France |
Vignette (© Laurence Duplomb).
Souvent d’origine génétique et affectant plus de 3 % des enfants dans le monde, les troubles neurodéveloppementaux (TND) forment un groupe hétérogène de maladies comprenant les troubles du spectre autistique (TSA), les troubles du développement intellectuel (TDI), les troubles du déficit de l’attention avec ou sans hyperactivité (TDAH), les troubles spécifiques du langage et des apprentissages (TSLA), l’épilepsie, etc. On estime aujourd’hui à plus de 1 700 le nombre de gènes dont des variations sont responsables de TND. Beaucoup de gènes, mais aussi de nouveaux mécanismes moléculaires à l’origine d’anomalies chromosomiques et génétiques restent à découvrir, de nombreux patients n’ayant pas reçu, à ce jour, de diagnostic moléculaire de leur maladie [
1
].
Au cours du développement du cerveau, de l’embryon au jeune enfant, des variations génétiques peuvent entraîner divers défauts cellulaires : altérations de l’axe de division des progéniteurs neuronaux, de la migration cellulaire, des connexions synaptiques, de la régulation transcriptionnelle/épigénétique de l’ADN, de la synthèse, de la localisation et de la fonction des protéines ou des voies de signalisation, entraînant des dysfonctionnements cérébraux associés ou non à des anomalies de la structure cérébrale.
Le déploiement des techniques de séquençage à haut débit du génome et des explorations du type -omique associées représente une réelle révolution dans la médecine des maladies rares. De plus en plus de variations génétiques pathogènes sont identifiées, apportant des réponses à des patients restés longtemps en errance diagnostique. Ces découvertes sont à l’origine de projets de recherche fondamentale qui ont permis de comprendre les mécanismes cellulaires impliqués dans les maladies, et qui ont contribué aux connaissances en biologie des cellules et des tissus. Cependant, dans le cas des TND, ces projets sont confrontés à plusieurs difficultés liées au nombre réduit de patients et à la complexité des mécanismes qui contrôlent le neurodéveloppement. L’accès à des échantillons de cerveau humain vivant n’étant pas envisageable, les études cellulaires et moléculaires sur le tissu altéré restent limitées. Pour pallier ce manque, des modèles animaux sont souvent utilisés, tels que la souris (
Mus musculus
), le poisson zèbre (
Danio rerio
), ou la drosophile (
Drosophila melanogaster
), mais des différences existent entre les phénotypes de ces animaux et de l’être humain. La production d’organoïdes cérébraux à partir de cellules souches pluripotentes induites (iPSC) constitue une approche complémentaire de ces modèles animaux, en reproduisant
in vitro
les étapes fondamentales du développement cérébral. Cette approche innovante est porteuse d’espoir pour accélérer la recherche et le développement de traitements des TND.
|
Les cellules souches pluripotentes induites
La reprogrammation de cellules somatiques (fibroblastes ou cellules mononucléées du sang) en cellules souches pluripotentes induites (iPSC,
induced pluripotent stem cells
) repose sur l’expression de quatre facteurs de transcription de pluripotence,
OCT3/4, SOX2, KLF4
, et
c-MYC
(ou
OSKM
), appelés facteurs de Yamanaka en hommage au découvreur de l’effet de cette combinaison de facteurs [
2
]. Différentes méthodes de vectorisation, virales ou non virales, sont utilisées pour introduire les gènes codant ces facteurs dans les cellules [
3
], et ainsi générer des iPSC définies par une morphologie typique, la capacité d’auto-renouvellement et la pluripotence [
4
] (→).
(→) Voir la Synthèse de E. Kieffer
et al
.,
m/s
n° 10, octobre 2010, page 848
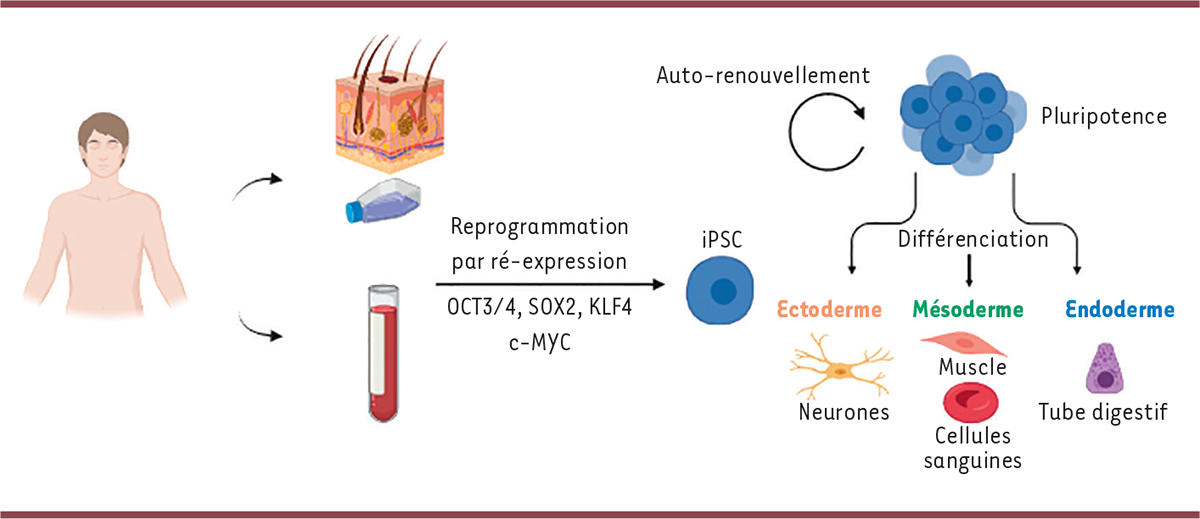
Les iPSC sont des cellules très compactes, avec un ratio noyau/cytoplasme élevé, qui forment des colonies aux bords réguliers. Les termes « capacité d’auto-renouvellement » et « pluripotence » signifient respectivement que ces cellules sont capables de se multiplier à l’infini et qu’elles peuvent se différencier dans tous les types de cellules qui composent un organisme. Pour valider leur reprogrammation, un test de différenciation des iPSC dans des cellules composant les trois feuillets embryonnaires (mésoderme, endoderme et ectoderme) est requis. C’est en effet de ces trois feuillets que proviennent les différents types cellulaires de l’organisme : par exemple, les neurones dérivent de l’ectoderme, les cellules musculaires et les vaisseaux sanguins du mésoderme, et le tube digestif de l’endoderme (
Figure 1
).
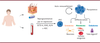 | Figure 1.
La reprogrammation des iPSC est réalisée à partir de cellules somatiques du donneur, soit de fibroblastes issus d’une biopsie de peau, soit de cellules mononucléées sanguines
. Ces cellules, reprogrammées par expression des facteurs de Yamanaka (OCT3/4, SOX2, KLF4 et c-MYC), ont un pouvoir d’autorenouvellement et de pluripotence, et peuvent se différencier en cellules constitutives des trois feuillets embryonnaires que sont l’ectoderme, le mésoderme et l’endoderme, pour donner ensuite naissance à toutes les cellules qui composeront l’organisme humain adulte (Figure créée avec BioRender.com).
|
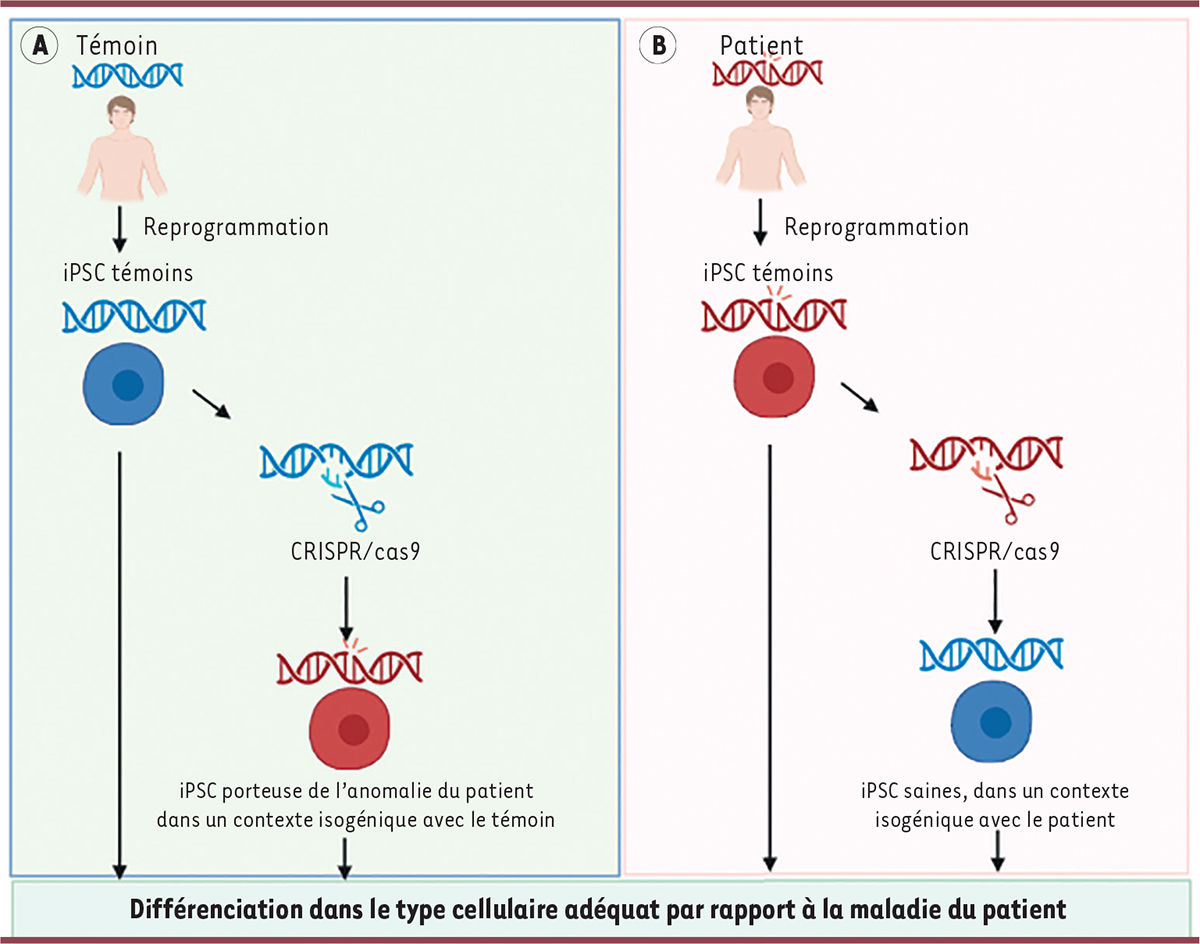
L’un des intérêts majeurs des iPSC réside dans le fait qu’elles conservent les mêmes informations génétiques que celles de la personne dont les cellules utilisées pour les produire (fibroblastes ou cellules sanguines) sont issues. Les cellules d’un patient atteint d’une maladie génétique, et qui a accepté
1,
une biopsie de peau ou une prise de sang, pourront donc être reprogrammées en iPSC qui seront porteuses de la variation génétique responsable de sa maladie. S’il s’agit d’une variation létale pour le fœtus
2,
, des iPSC porteuses de l’anomalie peuvent, dans certains cas, être obtenues à partir de cellules saines, qui ne sont pas porteuses de la variation génétique, celle-ci étant alors introduite en utilisant la technique d’édition de gène CRISPR/Cas9 (
Figure 2A
)
3
. La technique CRISPR/Cas9 peut également être utilisée afin de corriger ou d’empêcher l’expression de l’allèle porteur de la mutation dans les cellules du patient (
Figure 2B
). Dans ce cas, le fonds génétique étant le même, seuls les effets pathogènes de l’anomalie seront révélés.
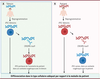 | Figure 2.
A
.
L’obtention des iPSC de patients nécessite un consentement. En cas de refus ou d’impossibilité d’obtenir des cellules somatiques, la mutation pathogène peut être éditée par la technique CRISPR/Cas9 dans des iPSC issues de cellules saines.
B
.
La correction de la mutation pathogène peut également être obtenue par la technique CRIPSR/Cas9. Dans les conditions A et B, les cellules mutées et les cellules saines sont en contexte isogénique. Le choix de la différenciation des iPSC dans un ou plusieurs types cellulaires est réalisé en fonction des atteintes cliniques du patient (Figure créée avec BioRender.com).
|
Indépendamment de la technique utilisée pour les produire, reprogrammation avec ou sans édition de gène par CRISPR/Cas9, les iPSC porteuses de la variation génétique pourront ensuite être différenciées dans le type cellulaire affecté par la maladie, ce qui permettra l’étude des mécanismes cellulaires et moléculaires impliqués. Un défi persiste néanmoins car certaines variations pathogènes, comme les anomalies complexes (remaniement chromosomique par exemple), sont difficilement modélisables. |
Des organoïdes aux assembloïdes
Au début des années 2000, Itskovitz-Eldor
et al
. ont montré la capacité des cellules souches embryonnaires humaines (hESC,
human embryonic stem cells
), cultivées en suspension, à s’agréger en corps embryoïdes, puis à acquérir des marqueurs spécifiques des trois couches germinales embryonnaires [
5
]. Ces observations ouvraient ainsi la voie à de nombreuses études sur le développement embryonnaire humain, puis au développement d’un système de culture cellulaire en trois dimensions, les organoïdes, possédant des caractéristiques structurelles et fonctionnelles de l’organe en développement qu’ils représentent. Les iPSC furent ensuite utilisées afin de produire des organoïdes représentatifs de différents organes : la peau, le poumon, le foie, ou le cerveau [
6
] (→).
(→) Voir la Synthèse de H. Chneiweiss
et al
.,
m/s
n° 11, novembre 2023 et voir la série
Organoïdes
Le premier modèle d’organoïde cérébral doté d’une formation auto-organisée, avec une polarité apico-basale, et représentant les aspects spatio-temporels de la corticogenèse précoce, a été obtenu par Eiraku
et al
., en 2008, à partir de hESC [
7
]. Peu après, en 2013, Lancaster
et al
. décrivirent un protocole permettant la génération d’organoïdes cérébraux à partir d’iPSC [
8
]. Ces organoïdes reproduisaient le développement cérébral humain fœtal, avec une auto-organisation qui débute par une prolifération des progéniteurs neuronaux, suivie de leur différenciation en différents types de neurones fonctionnels, en oligodentrocytes et en astrocytes [
9
].
Deux types d’organoïdes cérébraux peuvent être produits. Il est en effet possible de produire des organoïdes cérébraux dits « entiers », composés de plusieurs régions du cerveau (régions corticales, ventricules, hippocampe, plexus choroïde), ou des organoïdes guidés vers une région spécifique (région cérébrale postérieure ou antérieure, cervelet, hypothalamus, cortex) [
10
]. Techniquement, l’approche guidée est la plus robuste et elle permet une meilleure reproductibilité, mais elle est restreinte à la partie cérébrale ciblée, qui se trouve ainsi dépourvue de connexions avec les autres régions du cerveau.
Grâce à des systèmes de co-culture, apportant une contrainte de forte proximité, il est désormais possible de produire des assembloïdes, qui résultent de la fusion d’au moins deux organoïdes guidés, chacun étant representatif d’une région spécifique d’un tissu, ou de tissus différents. Les premiers assembloïdes cérébraux ont été produits en 2017, par l’équipe de Sergiu P Pas¸ca (
Stanford University School of Medicine
, Stanford, États-Unis) [
11
] puis par celle de Juergen A Knoblich (
Institute of Molecular Biotechnology
, Vienne, Autriche) [
12
], en produisant des organoïdes correspondant aux zones ventrale et dorsale du cerveau antérieur, puis en les co-cultivant pour qu’ils fusionnent. Cette approche a permis d’étudier les dynamiques inter-régions, reflétant les migrations se produisant au cours du développement cérébral embryonnaire, comme la migration des interneurones (principalement GABAergiques) nés dans la zone ventrale et devant migrer dans la zone dorsale. Grâce à cette approche, l’équipe de Sergiu Pas¸ca a pu montrer l’utilité des assembloïdes en pathologie cérébrale pour comprendre les mécanismes cellulaires impliqués. Utilisant des assembloïdes produits à partir d’iPSC de patients, ils ont en effet modélisé le syndrome de Thimoty, causé par des variations gain-defonction dans le gène
CACNA1C
(
calcium voltage-gated channel subunit alpha1 C
) qui code les canaux calciques de type L, responsables, entre autres, d’épilepsie, de TSA, de retard de développement, et ont mis en évidence une altération de la migration des interneurones, celle-ci pouvant être restaurée en bloquant l’activité des canaux calciques de type L par des molécules pharmacologiques spécifiques. Toujours dans l’équipe de Sergiu Pas¸ca, Andersen
et al
., ont produit des assembloïdes constitués d’organoïdes de cortex cérébral, de cerveau postérieur avec moelle spinale, et de muscle squelettique, et recréé ainsi
in vitro
un axe fonctionnel dans lequel l’activation des neurones corticaux contrôle la contraction musculaire
via
les motoneurones, un modèle qui ouvre de nouvelles perspectives pour l’étude et le traitement des maladies associées à des troubles moteurs [
13
].
Les applications des organoïdes cérébraux
L’utilisation d’organoïdes cérébraux a permis de comprendre les mécanismes impliqués dans le développement normal du cerveau, et de les confronter à ceux observés en conditions pathologiques, dans le but de trouver de nouvelles cibles thérapeutiques et d’élaborer des traitements personnalisés. Différentes maladies, d’origine génétique ou pas, sont étudiées grâce aux organoïdes cérébraux, notamment :
-
des défauts cérébraux résultant d’une infection virale, due au virus Zika [
14
], au SARS-CoV-2 (
severe acute respiratory syndrome coronavirus 2
) [
15
], au virus Herpès simplex [
14
], etc. Dans le cas du virus Zika, les organoïdes ont permis de comprendre comment le virus pénètre dans les progéniteurs neuraux et entraîne leur apoptose, avec pour conséquence une microcéphalie. Ces études ont également montré l’existence de mécanismes pathogènes communs aux microcéphalies induites par plusieurs virus et de tester des stratégies antivirales.
-
des maladies génétiques neurodéveloppementales, comme la trisomie 21 [
16
], le syndrome de l’X-fragile [
17
], le syndrome de DiGeorge [
18
], le syndrome de Pitt-Hopkins [
19
], mais également des troubles du spectre autistique pour lesquels les causes génétiques ont été identifiées, comme des mutations des gènes
KMT5B
(
lysine methyltransferase 5B
),
CHD8
(
chromodomain helicase DNA binding protein 8
) et
CNTNAP2
(
contactin-associated protein 2
) [
20
]. Ces études ont permis de consolider les connaissances acquises à partir des modèles animaux ou des cultures cellulaires en deux dimensions. Elles ont aussi permis de caractériser de nouveaux mécanismes clés impliqués dans la pathogénèse de ces maladies, et de tester des stratégies pour corriger les phénotypes pathologiques.
-
Même si les organoïdes cérébraux sont surtout reconnus comme des outils de choix pour les études du neurodéveloppement, ils sont aussi d’un intérêt majeur pour les maladies neurodégénératives, avec des études réalisées sur des organoïdes issus de cellules de patients présentant une maladie de Parkinson, avec ou sans cause génétique connue (par exemple, impliquant les gènes
LRRK2
[
leucine-rich repeat kinase 2
] [
21
] et
SNCA
[
synuclein alpha
] [
22
]), ou une maladie d’Alzheimer (impliquant
PSEN1
[
presenilin 1
] [
23
]). Pour la maladie d’Alzheimer, le modèle d’organoïde cérébral reproduit les défauts caractéristiques de la maladie, comme l’agrégation de la protéine amyloïde et l’hyperphosphorylation de la protéine Tau. Le succès de l’utilisation de molécules pharmacologiques dont les effets sur la réduction des agrégats amyloïdes sont connus (telles que les inhibiteurs des sécrétases J et E) suggère que les organoïdes cérébraux représentent un bon modèle pour l’identification de nouvelles molécules thérapeutiques dans cette maladie. Des tests de criblage de molécules à haut débit ont déjà été réalisés, et sont en cours d’optimisation pour proposer une médecine personnalisée de précision [
24
].
-
les tumeurs cérébrales, comme le glioblastome ou le médulloblastome [
25
,
26
].
-
les maladies mentales, comme la schizophrénie (avec les mutations du gène
DISC1
[
disrupted-in-schizophrenia 1
] [
27
])
-
les maladies résultant d’expositions à des toxines [
9
,
28
], ou l’impact, sur le développement cérébral fœtal, d’une exposition
in utero
à des antidépresseurs [
29
], à l’alcool, à la cocaïne, à la méthamphétamine, pris par la mère au cours de la grossesse [
30
]. Plus spécifiques que les tests classiques d’embryotoxicité réalisés
in vitro
, les organoïdes cérébraux permettent de tester la neurotoxicité embryonnaire de médicaments, de substances chimiques ou illicites, avec des temps d’exposition prolongés, ou à des temps précis du développement de l’organoïde, et de compléter cette étude par des analyses morphologiques, transcriptionnelles et fonctionnelles.
Les limites des organoïdes cérébraux
La modélisation d’un tissu reposant sur des organoïdes présente plusieurs avantages : les organoïdes permettent d’obtenir une complexité et une maturité cellulaire plus importante que celles obtenues dans un modèle en 2D ; ils permettent de pallier les limites des modèles animaux, qui ne reproduisent pas toujours fidèlement certaines caractéristiques des cerveaux humains, en raison de différences de régulation du cycle cellulaire des progéniteurs neuronaux, des voies de signalisation ou de migration cellulaire [
31
]. L’approche par organoïdes cérébraux possède néanmoins ses limites. Le cerveau humain se caractérise par une taille et une architecture spécifiques. Il contient un nombre important de neurones, de différents types, qui établissent des connexions pour former un réseau complexe et mature capable d’intégrer les modifications de l’environnement. L’organoïde cérébral est un outil qui reste limité à l’échelle du millimètre, correspondant au cerveau d’un insecte, et qui est constitué d’un nombre réduit de neurones. Loin de recréer les six couches du néocortex humain, il possède une architecture globale bien différente, mais qui, à l’échelle microscopique, reproduit le développement cérébral, avec plusieurs couches de neurones de différentes identités. Des cellules microgliales, capables de réponses immunitaires, peuvent ainsi être observées dans des organoïdes cérébraux [
32
]. Mais bien que ses neurones soient actifs, l’organoïde reste très immature, et son réseau neuronal est loin d’avoir la complexité de celui du cerveau humain.
L’absence de vascularisation est l’un des défis importants qu’il est nécessaire de relever : sans vascularisation, l’oxygène et les nutriments sont apportés aux cellules directement par diffusion. Au cours de la croissance de l’organoïde, l’efficacité de cette diffusion vers son centre diminue, le mettant en hypoxie et lui apportant moins de nutriments. Inévitablement, un stress, puis une mort cellulaire par nécrose sont donc observés au centre de l’organoïde, rendant toute exploitation impossible. Durant ces cinq dernières années, plusieurs équipes ont cherché à produire des organoïdes vascularisés : en les transplantant dans des cerveaux de souris pour « capter » leur vascularisation ; en réalisant des co-cultures en présence de cellules endothéliales de veines ombilicales humaines, puis en les transplantant dans des cerveaux de souris ; ou en les cultivant avec des organoïdes de vaisseaux sanguins [
33
]. Une approche différente, récemment décrite par Qian
et al
. [
34
], consiste à réaliser des coupes d’organoïdes corticaux épaisses de 500 μm, qui peuvent être répétées toutes les 4 semaines, afin de faciliter le contact du centre de l’organoïde avec le milieu de culture et ses nutriments, prévenant ainsi la mort des cellules et maintenant la neurogénèse et le développement du cortex à un stade du développement équivalent à celui du troisième trimestre de grossesse dans l’espèce humaine. La culture de coupes d’organoïdes dans un système d’interface air-liquide permet également de prolonger la vie de l’organoïde, avec une amélioration de la survie des neurones et une croissance des axones efficace et fonctionnelle [
35
]. Très récemment, Dao
et al
. ont produit des assembloïdes en associant des organoïdes cérébraux et des organoïdes de vaisseaux sanguins, créant ainsi des organoïdes vascularisés qui acquièrent des fonctions biologiques spécifiques de la barrière hémato-encéphalique [
36
].
Des questions éthiques présentes et à venir
Outre les limites et les défis expérimentaux, l’utilisation des organoïdes cérébraux pose des questions éthiques[
37
–
40
]. Les premiers questionnements éthiques sont classiques en recherche sur l’homme : ils concernent l’utilisation de matériel humain, le consentement des patients pour la production d’iPSC à partir d’une biopsie de peau ou d’une prise de sang, le consentement sur le devenir de leurs iPSC en organoïdes cérébraux pour la recherche fondamentale, la médecine personnalisée, etc. Plus spécifiquement, les organoïdes cérébraux issus de ces prélèvements peuvent être transférés dans des modèles animaux chimériques, ou assemblés avec d’autres organoïdes en complexes de statut moral ou juridique mal défini. Bien que non envisageable aujourd’hui, la possibilité que, grâce aux évolutions techniques, les organoïdes cérébraux puissent, un jour, être dotés d’une conscience est une question qui est néanmoins débattue
4
[
47
] (→)
(→) Voir l’Éditorial de H. Chneiweiss,
m/s
n° 2, février 2020, page 99
En effet, la présence, par exemple, de l’hippocampe, structure cérébrale impliquée dans la mémoire, et celle de connections neuronales actives, détectées par des enregistrements d’activités électriques et ressemblant à celles d’un cerveau fœtal en développement, ont conduit les scientifiques, les philosophes, mais aussi le grand public, à débattre de cette question de la « conscience des organoïdes cérébraux ». Quel statut moral doit-on donc leur accorder ? Quelles seront les capacités cognitives dont seront dotées les prochaines générations d’organoïdes cérébraux, alors probablement couplés à l’intelligence artificielle ? |
Les organoïdes cérébraux comme modèle cellulaire
Déjà utilisés dans plusieurs laboratoires, les organoïdes cérébraux ont montré leur intérêt pour la recherche sur les troubles neurodéveloppementaux. Certaines études ont en effet ouvert de nouvelles perspectives thérapeutiques, comme la découverte de la protéine HSF2 (
heat shock transcription factor 2
) une cible potentielle dans le syndrome de Rubinstein-Taybi, une maladie génétique associant des anomalies morphologiques et une déficience intellectuelle [
41
]. D’autres études sont à des stades plus avancés, avec le développement de tests de molécules à potentiel thérapeutique. Trujillo
et al
. ont, par exemple, testé 14 molécules pharmacologiques dans le syndrome de Rett
5
, parmi lesquelles deux se sont révélées capables d’améliorer de façon partielle certaines fonctions neuronales d’un organoïde, ouvrant un espoir pour les patientes, mais suggérant également la nécessité de combiner plusieurs molécules pour cibler toutes les anomalies [
42
].
|
Les organoïdes cérébraux comme modèle cellulaire de TDN
L’utilisation des organoïdes cérébraux représente un atout important pour décrypter les mécanismes cellulaires impliqués dans la pathogénèse des TDN et découvrir de potentielles cibles thérapeutiques en testant
in vitro
des molécules pharmacologiques, dans l’espoir de développer des essais précliniques pour une médecine personnalisée (projet MIND [
modelisation of neurodevelopmental disorders
],
Figure 3
). L’identification de nouveaux gènes candidats, dont les variations sont responsables de TND, ou de variations de signification incertaine, est la première étape du projet. Des iPSC obtenues à partir du sang ou d’une biopsie de peau de patient, ou les iPSC obtenues par la technique CRIPSR/Cas9, sont utilisées pour produire des organoïdes cérébraux pour lesquels les étapes du développement, la morphologie, la structure, et la fonction sont étudiées et comparées à des organoïdes produits à partir d’iPSC issues de cellules de donneurs sains.
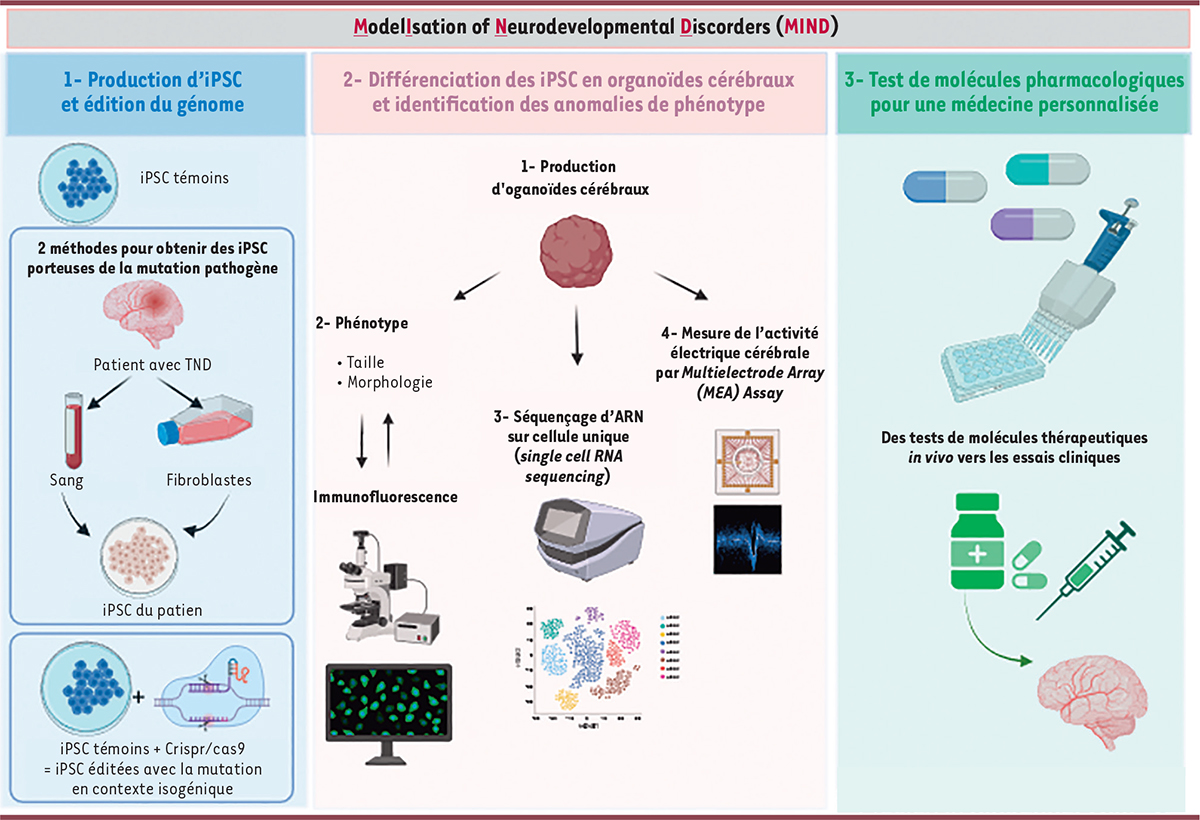
 | Figure 3.
Le projet MIND
(modelisation of neurodevelopmental disorders)
et la modélisation des maladies neurodéveloppementales par production d’organoïdes cérébraux
.
Les iPSC porteuses de la variation pathogène sont utilisées pour produire des organoïdes cérébraux dont la morphologie, le génotype et la fonction sont étudiés et comparés à des organoïdes provenant d’iPSC saines (témoins). Le but de ce projet est de caractériser les mécanismes cellulaires responsables de la maladie dans l’espoir d’identifier de nouvelles cibles thérapeutiques et de développer des tests de molécules pharmaceutiques
in vitro
(Figure créée avec BioRender.com).
|
Étudier le développement de l’organoïde
La taille de l’organoïde au cours de son développement (
Figure 4A
) est un critère important qui peut permettre de confirmer l’implication d’un variant génétique dans le cas de l’étude d’anomalies de taille du cerveau, comme la microcéphalie [
43
] ou la mégalencéphalie [
44
]. Des immunomarquages, réalisés sur des coupes d’organoïdes, peuvent ensuite révéler des pistes pour comprendre les mécanismes impliqués. Il est ainsi possible d’observer, avec les différents marqueurs, un nombre important de rosettes avec une zone ventriculaire (exprimant PAX6 [
paired box 6
]) et des zones corticales (
Figure 4B
). La prolifération des progéniteurs (révélée par le marqueur Ki67) et leur axe de division (visualisé par HTA28 [
histone H3 phospho Ser28
] et Tpx2 [
targeting protein for Xklp2
]), ainsi que la mise en place des différentes structures à identité neuronale spécifique (PAX6 pour les progéniteurs, TBR1 [
T-brain transcription factor 1
] / TUJ1 [
class III beta-tubulin
] / SATB2 [
special AT-rich sequence-binding protein 2
] / CTIP2 [
coup-TFI interacting protein 2
] pour les neurones à apparition précoce ou tardive, ou GFAP [
glial fibrillary acidic protein
] pour les astrocytes) peuvent également être visualisées (
Figure 4C, D
). Les résultats de ces immunomarquages permettent d’élaborer des hypothèses quant aux mécanismes impliqués dans ces maladies. Ainsi, une diminution de la prolifération des progéniteurs neuronaux, associée à leur différenciation accélérée en neurones, peut être le reflet
in vitro
d’une microcéphalie. À l’inverse, une prolifération exagérée des progéniteurs associée à un retard de la différenciation neuronale orientera vers une mégalencéphalie.
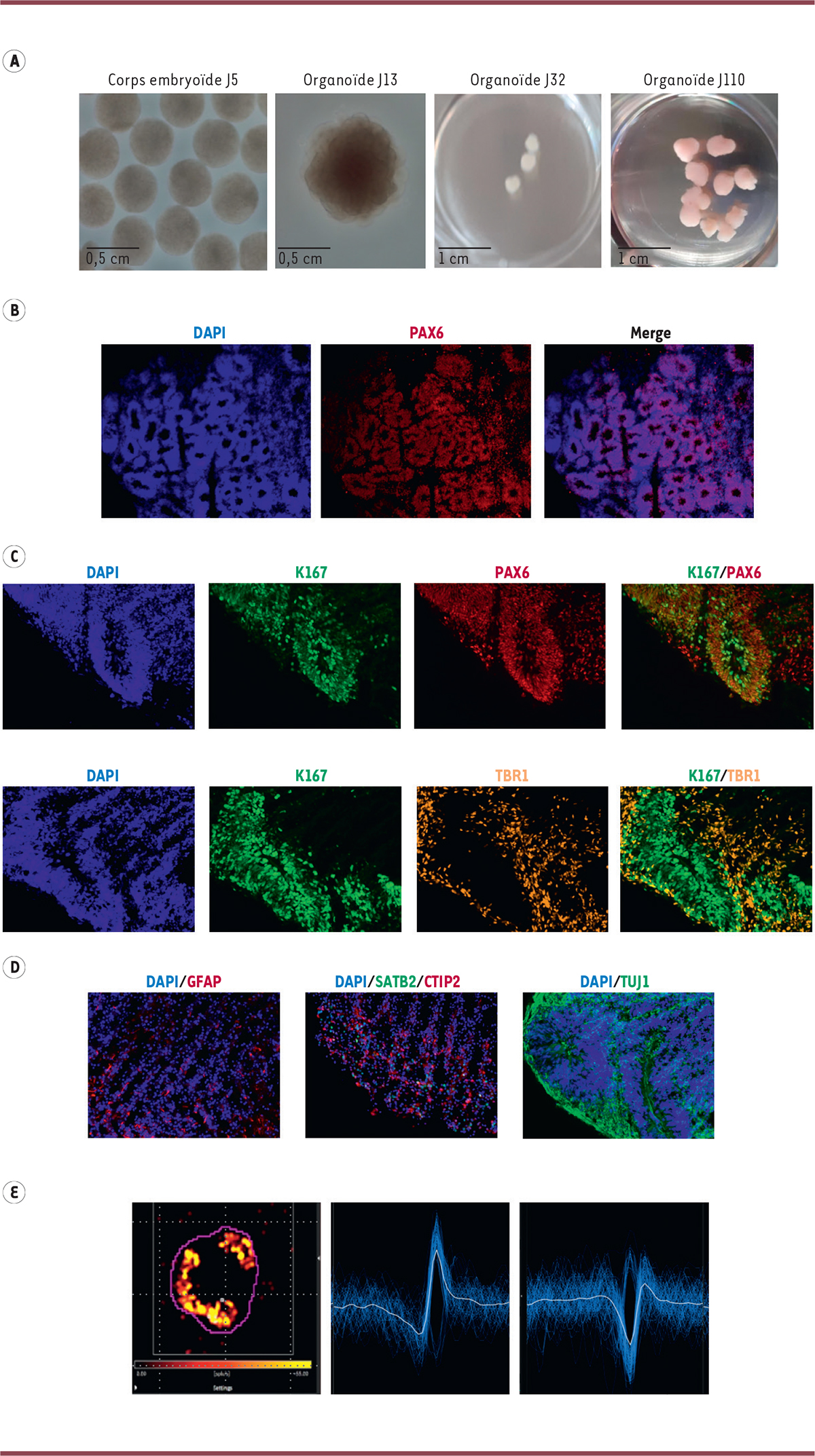
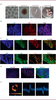 | Figure 4.
Analyses morphologiques et fonctionnelles des organoïdes cérébraux. A.
Évolution des organoïdes cérébraux en culture, du stade « corps embryoïde », à 5 jours de culture, jusqu’à 110 jours de culture. Les deux images de gauche montrent des observations d’organoïdes à la loupe (x 4,5), les deux autres à l’œil nu. Les organoïdes cérébraux ont été produits en utilisant le kit
STEMdiffTMCerebral Organoid
de
STEMCELLTMTechnology
.
B
.
Visualisation des rosettes d’un organoïde cérébral après 25 jours de culture (J25) avec un marquage par un anticorps anti-PAX6 spécifiques des progéniteurs neuronaux. Les noyaux cellulaires sont marqués au DAPI (grossissement x10).
C
.
marquage d’un organoïde à J25 montrant la colocalisation du marqueur de prolifération Ki67 (en vert) avec les progéniteurs neuronaux exprimant PAX6 (PAX6+) (en rouge), mais pas avec le marqueur neuronal TBR1 (en orange) (grossissement x 20).
D
.
Immunomarquages d’un organoïde à J115 montrant la présence de cellules GFAP
+
(en rouge), SATB2
+
(en vert), CTIP2
+
(en rouge) et TUJ1
+
(en vert) (grossissement x 20).
E
.
Capture d’écran de la «
heat map
», réalisée à l’aide du logiciel
3Brain
, montrant l’enregistrement avec une puce de 4 096 microélectrodes, de l’activité électrique d’un organoïde cérébral (délimité par le contour violet). À droite, exemples de signaux d’activité neuronale enregistrés sur deux microélectrodes de la puce. PAX6 :
paired box 6
; TBR1 :
T-box brain transcription factor 1
; GFAP :
glial fibrillary acidic protein
; SATB2 :
special AT-rich sequence-binding protein 2
CTIP2 :
coup-TFI interacting protein 2 ;
TUJ1 :
class III beta-tubulin
.
|
Étudier l’activité électrique de l’organoïde
Après 12 semaines de culture, l’organoïde cérébral est doté d’activité électrique spontanée. Cette activité peut être mesurée par la technique de puces à microélectrodes (MEA) : l’organoïde est déposé sur une micropuce (
3Brain
)
6
permettant l’enregistrement des pics d’activité électrique produite par les neurones qui le constituent (
Figure 4E
). La fréquence et l’intensité de ces pics survenant spontanément ou après stimulation électrique ou chimique sont enregistrées. Ce système permet ainsi de tester l’effet de molécules à potentiel pharmacologique sur l’activité des cellules.
Étudier le transcriptome Des analyses transcriptomiques, réalisées par séquençage de l’ARN sur cellule unique (scRNA-seq), permettent d’évaluer l’expression des gènes dans chaque type cellulaire composant l’organoïde. Il est ainsi possible de définir l’identité de chacune des cellules, les voies de différenciation qui sont activées, et le devenir des cellules, et ainsi d’appréhender l’impact possible d’une variation génétique sur le développement du cerveau. Les résultats de ces analyses permettent de définir des groupes de cellules composant l’organoïde, selon leur profil transcriptomique, et ainsi d’identifier les divergences à l’échelle de la cellule et à l’échelle de l’organoïde. |
Dans le cadre du projet MIND, différents gènes candidats, dont des variants seraient à l’origine de TND, sont explorés. Nous présentons les études portant sur deux de ces gènes.
Le gène
PTBP1
La protéine PTBP1 (
polypyrimidine tract-binding protein 1
) est une protéine de liaison à l’ARN qui participe à la régulation de l’epissage alternatif. Ce facteur d’épissage navigue entre le noyau et le cytoplasme grâce à la présence, à son extrémité N-terminale, d’une séquence de localisation nucléaire (NLS) et d’une séquence d’exportation nucléaire (NES). Des variations pathogènes, apparues
de novo
ou héritées, et affectant la localisation de cette protéine, ont été trouvées chez 23 individus présentant un nouveau syndrome caractérisé par différents troubles du neurodéveloppement. Les études
in vivo
, réalisées chez le poisson zèbre, et
in vitro
sur des fibroblastes de patients ou de souris (cellules NIH-3T3) dans lesquels les variations pathogènes ont été introduites, ont mis en évidence plusieurs défauts cellulaires. Les études actuelles consistent à produire des organoïdes cérébraux à partir d’iPSC de patients afin d’en définir la morphologie, et de les caractériser histologiquement et fonctionnellement. La technique de séquençage de l’ARN sur cellule unique, réalisée au cours du développement de l’organoïde, apporte des informations quant aux trajectoires développementales qui sont affectées par la mutation. Un modèle murin dans lequel la mutation humaine la plus fréquente est introduite (
knock-in
) complète cette analyse avec l’étude du développement embryonnaire du cerveau. Ce modèle permet en outre de comparer les effets des variations génétiques d’intérêt entre espèces (homme/souris). Ce type d’étude, associant plusieurs méthodes et modèles complémentaires, est essentiel pour accroître les connaissances sur la fonction de la protéine étudiée et sur le développement sain et pathologique du cerveau, et ainsi comprendre la cause des symptômes des patients, avec à long terme, la perspective de thérapies ciblées.
Le gène
PIK3CA
Le gène
PIK3CA
(
phosphatidylinositol-4,5-bisphosphate 3-kinase, catalytic subunit alpha
) code la sousunité catalytique p110D de la PI3K (
phosphatidylinositol 3-kinase
), une protéine kinase impliquée dans les premières étapes de phosphorylation de la voie de signalisation PI3K/AKT (protéine kinase B)/mTOR (
mammalian target of rapamycin
), une voie très importante dans la prolifération et le métabolisme cellulaires. Cette voie est souvent ciblée par les thérapies utilisées dans de nombreux cancers. Elle est également l’objet d’essais cliniques réalisés dans le cadre de maladies rares, comme les syndromes avec hypercroissance découlant de variations dans
PIK3CA
(syndromes PROS, pour PIK3CA
-related overgrowth syndromes
) [
45
]. Parmi ces syndromes, le syndrome MCAP (
megalencephaly-capillary malformation-polymicrogyria
, MIM
7,
# 602501) est caractérisé par une mégalencéphalie
8,
et une polymicrogyrie
9
, associées ou non à des retards cognitifs et moteurs, des malformations vasculaires des parties molles, et des anomalies distales des membres. Les variations de
PIK3CA
sont principalement post-zygotiques, mais elles peuvent être constitutives dans de très rares cas. Grâce à l’engagement de notre équipe auprès des patients PROS (collaborations nationales et internationales pour le diagnostic, le suivi, les essais cliniques et les études fonctionnelles
in vitro
), des iPSC, issues d’une patiente de 3 ans souffrant du syndrome MCAP résultant d’une mutation constitutive de
PIK3CA
, ont été obtenues par reprogrammation des cellules sanguines mononucléées de la patiente. Une des hypothèses pour expliquer l’apparition de ce syndrome est l’existence d’une prolifération exagérée des progéniteurs neuraux, due à l’activation constitutive de PIK3CA et, par conséquent, à celle permanente de la voie PI3K/AKT/mTOR. Cette prolifération exagérée associée à un retard de différenciation pourrait être l’explication de la mégalencéphalie. Cette étude constitue une preuve de concept pour l’utilisation des organoïdes cérébraux dans l’avancée de la recherche de thérapies pour les TND et comme modèles précliniques pertinents. Elle est liée à l’essai clinique SESAM (dont le promoteur est le CHU de Dijon). Il s’agit d’un essai multicentrique de phase II, en double aveugle, contrôlé par placebo, visant à évaluer la sécurité et l’efficacité de l’alpelisib (BYL719), inhibiteur de la phosphatidylinositol-3-kinase, chez les patients pédiatriques et adultes atteints du syndrome MCAP. Cette molécule, ou d’autres molécules non encore testées chez l’homme mais connues pour leur efficacité
in vitro
, comme le triptolide [
46
], seront testées sur les organoïdes cérébraux produits, dans l’espoir d’en corriger le phénotype.
|
Décrypter les mécanismes moléculaires impliqués dans les maladies associant des anomalies cérébrales est crucial pour le développement de stratégies thérapeutiques ciblées. En plus d’être une nouvelle source de connaissances des bases moléculaires et cellulaires du développement cérébral humain, les organoïdes cérébraux représentent un puissant outil pour modéliser et comprendre l’impact de variants génétiques dans les TND ou toutes autres maladies affectant le développement ou les fonctions du cerveau. Ils offrent une opportunité sans précédent pour tester des molécules pharmacologiques dans l’espoir de découvrir de nouveaux traitements, voire d’envisager une médecine personnalisée. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
.
|
Nous remercions les patients et leur famille pour leurs consentements pour les biopsies de peau ou les prises de sang. La production des iPSC, la production des organoïdes et les analyses qui en découlent sont financés par les projets PERSONALISE (ISITE-FEDER), MIND (amorçage CHU Région Bourgogne-Franche Comté), et MultiomixCare : cette étude a reçu le soutien financier du « Programme Prioritaire de Recherche Maladies Rares » du Programme français d’Investissements d’Avenir
.
|
Footnotes |
1.
Schule
R
,
Timmann
D
,
Erasmus
CE
et al.
Solving unsolved rare neurological diseases-a Solve-RD viewpoint.
.
Eur J Hum Genet
.
2021;
;
29
:
:1332.
–
6
.
2.
Takahashi
K
,
Tanabe
K
,
Ohnuki
M
et al.
Induction of pluripotent stem cells from adult human fibroblasts by defined factors.
.
Cell
.
2007;
;
131
:
:861.
–
72
.
3.
Malik
N
,
Rao
MS
.
A review of the methods for human iPSC derivation.
.
Methods Mol Biol
.
2013;
;
997
:
:23.
–
33
.
4.
Kieffer
E
,
Kuntz
S
,
Viville
S
.
Tour d’horizon des lignées de cellules souches pluripotentes.
Med Sci (Paris)
.
2010;
;
26
:
:848.
–
54
.
5.
Itskovitz-Eldor
J
,
Schuldiner
M
,
Karsenti
D
et al.
Differentiation of human embryonic stem cells into embryoid bodies compromising the three embryonic germ layers.
.
Mol Med
.
2000;
;
6
:
:88.
–
95
.
6.
Chneiweiss
H
,
Dubart-Kupperschmitt
A
,
Duclos-Vallee
JC
,
et al.
Pour une bonne compréhension et un bon usage du terme « organoïdes ».
.
Med Sci (Paris)
.
2023;
;
39
:
:876.
–
8
.
7.
Eiraku
M
,
Watanabe
K
,
Matsuo-Takasaki
M
,
et al.
Self-organized formation of polarized cortical tissues from ESCs and its active manipulation by extrinsic signals.
.
Cell Stem Cell
.
2008;
;
3
:
:519.
–
32
.
8.
Lancaster
MA
,
Knoblich
JA
.
Generation of cerebral organoids from human pluripotent stem cells.
.
Nat Protoc
.
2014;
;
9
:
:2329.
–
40
.
9.
Eichmuller
OL
,
Knoblich
JA
.
Human cerebral organoids – a new tool for clinical neurology research.
.
Nat Rev Neurol
.
2022;
;
18
:
:661.
–
80
.
10.
Acharya
P
,
Choi
NY
,
Shrestha
S
,
et al.
Brain organoids: A revolutionary tool for modeling neurological disorders and development of therapeutics.
.
Biotechnol Bioeng
.
2024;
;
121
:
:489.
–
506
.
11.
Birey
F
,
Andersen
J
,
Makinson
CD
,
et al.
Assembly of functionally integrated human forebrain spheroids.
.
Nature
.
2017;
;
545
:
:54.
–
9
.
12.
Bagley
JA
,
Reumann
D
,
Bian
S
,
et al.
Fused cerebral organoids model interactions between brain regions.
.
Nat Methods
.
2017;
;
14
:
:743.
–
51
.
13.
Andersen
J
,
Revah
O
,
Miura
Y
,
et al.
Generation of Functional Human 3D Cortico-Motor Assembloids.
.
Cell
.
2020;
;
183
:
:1913-29 e26.
.
14.
Krenn
V
,
Bosone
C
,
Burkard
TR
,
et al.
Organoid modeling of Zika and herpes simplex virus 1 infections reveals virus-specific responses leading to microcephaly.
.
Cell Stem Cell
.
2021;
;
28
:
:1362.
-
79 e7
.
15.
Ramani
A
,
Muller
L
,
Ostermann
PN
,
et al.
SARS-CoV-2 targets neurons of 3D human brain organoids.
.
EMBO J
.
2020;
;
39
:
:e106230.
.
16.
Xu
R
,
Brawner
AT
,
Li
S
,
et al.
OLIG2 Drives Abnormal Neurodevelopmental Phenotypes in Human iPSC-Based Organoid and Chimeric Mouse Models of Down Syndrome.
.
Cell Stem Cell
.
2019;
;
24
:
:908.
-
26 e8
.
17.
Kang
Y
,
Zhou
Y
,
Li
Y
,
et al.
A human forebrain organoid model of fragile X syndrome exhibits altered neurogenesis and highlights new treatment strategies.
.
Nat Neurosci
.
2021;
;
24
:
:1377.
–
91
.
18.
Khan
TA
,
Revah
O
,
Gordon
A
,
et al.
Neuronal defects in a human cellular model of 22q11.2 deletion syndrome.
.
Nat Med
.
2020;
;
26
:
:1888.
–
98
.
19.
Papes
F
,
Camargo
AP
,
de Souza
JS
,
et al.
Transcription Factor 4 loss-of-function is associated with deficits in progenitor proliferation and cortical neuron content.
.
Nat Commun
.
2022;
;
13
:
:2387.
.
20.
Paulsen
B
,
Velasco
S
,
Kedaigle
AJ
,
et al.
Autism genes converge on asynchronous development of shared neuron classes.
.
Nature
.
2022;
;
602
:
:268.
–
73
.
21.
Kim
H
,
Park
HJ
,
Choi
H
,
et al.
Modeling G2019S-LRRK2 Sporadic Parkinson’s Disease in 3D Midbrain Organoids.
.
Stem Cell Reports
.
2019;
;
12
:
:518.
–
31
.
22.
Jo
J
,
Yang
L
,
Tran
HD
,
et al.
Lewy Body-like Inclusions in Human Midbrain Organoids Carrying Glucocerebrosidase and alpha-Synuclein Mutations.
.
Ann Neurol
.
2021;
;
90
:
:490.
–
505
.
23.
Raja
WK
,
Mungenast
AE
,
Lin
YT
,
et al.
Self-Organizing 3D Human Neural Tissue Derived from Induced Pluripotent Stem Cells Recapitulate Alzheimer’s Disease Phenotypes.
.
PLoS One
.
2016;
;
11
:
:e0161969.
.
24.
Park
JC
,
Jang
SY
,
Lee
D
,
et al.
A logical network-based drug-screening platform for Alzheimer’s disease representing pathological features of human brain organoids.
.
Nat Commun
.
2021;
;
12
:
:280.
.
25.
Krieger
TG
,
Tirier
SM
,
Park
J
,
et al.
Modeling glioblastoma invasion using human brain organoids and single-cell transcriptomics.
.
Neuro Oncol
.
2020;
;
22
:
:1138.
–
49
.
26.
Ogawa
J
,
Pao
GM
,
Shokhirev
MN
,
et al.
Glioblastoma Model Using Human Cerebral Organoids.
.
Cell Rep
.
2018;
;
23
:
:1220.
–
9
.
27.
Srikanth
P
,
Lagomarsino
VN
,
Muratore
CR
,
et al.
Shared effects of DISC1 disruption and elevated WNT signaling in human cerebral organoids.
.
Transl Psychiatry
.
2018;
;
8
:
:77.
.
28.
Shou
Y
,
Liang
F
,
Xu
S
,
et al.
The Application of Brain Organoids: From Neuronal Development to Neurological Diseases.
.
Front Cell Dev Biol
.
2020;
;
8
:
:579659.
.
29.
Marinho
LSR
,
Chiarantin
GMD
,
Ikebara
JM
,
et al.
The impact of antidepressants on human neurodevelopment: Brain organoids as experimental tools.
.
Semin Cell Dev Biol
.
2023;
;
144
:
:67.
–
76
.
30.
Fan
P
,
Wang
Y
,
Xu
M
,
et al.
The Application of Brain Organoids in Assessing Neural Toxicity.
.
Front Mol Neurosci
.
2022;
;
15
:
:799397.
.
31.
Zhou
Y
,
Song
H
,
Ming
GL
.
Genetics of human brain development.
.
Nat Rev Genet
.
2024;
;
25
:
:26.
–
45
.
32.
Ormel
PR
,
Vieira de Sa
R
,
van Bodegraven
EJ
,
et al.
Microglia innately develop within cerebral organoids.
.
Nat Commun
.
2018;
;
9
:
:4167.
.
33.
Ye
B.
Approaches to vascularizing human brain organoids.
.
PLoS Biol
.
2023;
,
21
(
(5)
):
:e3002141.
.
34.
Qian
X
,
Su
Y
,
Adam
CD
,
et al.
Sliced Human Cortical Organoids for Modeling Distinct Cortical Layer Formation.
.
Cell Stem Cell
.
2020;
;
26
:
:766.
-
81 e9
.
35.
Giandomenico
SL
,
Mierau
SB
,
Gibbons
GM
,
et al.
Cerebral organoids at the air-liquid interface generate diverse nerve tracts with functional output.
.
Nat Neurosci
.
2019;
;
22
:
:669.
–
79
.
36.
Dao
L
,
You
Z
,
Lu
L
,
et al.
Modeling blood-brain barrier formation and cerebral cavernous malformations in human PSC-derived organoids.
.
Cell Stem Cell
.
2024;
;
31
:
:818.
–
33
.
37.
Lavazza
A
,
Massimini
M
.
Cerebral organoids: ethical issues and consciousness assessment.
.
J Med Ethics
.
2018;
;
44
:
:606.
–
10
.
38.
Koplin
JJ
,
Savulescu
J
.
Moral Limits of Brain Organoid Research.
.
J Law Med Ethics
.
2019;
;
47
:
:760.
–
7
.
39.
Hyun
I
,
Scharf-Deering
JC
,
Lunshof
JE
.
Ethical issues related to brain organoid research.
.
Brain Res
.
2020;
;
1732
:
:146653.
.
40.
Boyd
JL
.
Moral considerability of brain organoids from the perspective of computational architecture.
.
Oxf Open Neurosci
.
2024;
;
3
:
:kvae004.
.
41.
de Thonel
A
,
Ahlskog
JK
,
Daupin
K
,
et al.
CBP-HSF2 structural and functional interplay in Rubinstein-Taybi neurodevelopmental disorder.
.
Nat Commun
.
2022;
;
13
:
:7002.
.
42.
Trujillo
CA
,
Adams
JW
,
Negraes
PD
,
et al.
Pharmacological reversal of synaptic and network pathology in human MECP2-KO neurons and cortical organoids.
.
EMBO Mol Med
.
2021;
;
13
:
:e12523.
.
43.
Lancaster
MA
,
Renner
M
,
Martin
CA
,
et al.
Cerebral organoids model human brain development and microcephaly.
.
Nature
.
2013;
;
501
:
:373.
–
9
.
44.
Li
Y
,
Muffat
J
,
Omer
A
,
et al.
Induction of Expansion and Folding in Human Cerebral Organoids.
.
Cell Stem Cell
.
2017;
;
20
:
:385.
-
96 e3
.
45.
Hillmann
P
,
Fabbro
D
.
PI3K/mTOR Pathway Inhibition: Opportunities in Oncology and Rare Genetic Diseases.
.
Int J Mol Sci
.
2019;
;
20
:
:5792.
.
46.
Da Costa
R
,
De Almeida
S
,
Chevarin
M
,
et al.
Neutralization of HSF1 in cells from PIK3CA-related overgrowth spectrum patients blocks abnormal proliferation.
.
Biochem Biophys Res Commun
.
2020;
;
530
:
:520.
–
6
.
47.
Chneiweiss
H.
Organoïdes : nouvelles perspectives et nouvelles questions éthiques.
.
Med Sci (Paris)
.
2020;
;
36
:
:99.
–
100
.
|