© médecine/sciences
Le muscle strié squelettique adulte est l’organe central impliqué dans les mouvements volontaires, la respiration, la locomotion ou encore le maintien de la posture. Il est composé de milliers de fibres musculaires possédant la capacité unique de se contracter. De façon remarquable, les fibres musculaires endommagées peuvent se réparer en cas de lésion du muscle. Ce processus appelé régénération musculaire ou myogénèse est le fait de plusieurs acteurs cellulaires qui vont interagir entre eux, comme les cellules endothéliales, les cellules fibroblastiques ou encore les cellules de l’inflammation. Mais cette capacité régénérative n’est rendue possible que grâce aux cellules souches musculaires, également appelées cellules satellites. Localisées autour des fibres musculaires et initialement quiescentes, c’est-à-dire sans activité de prolifération, et métaboliquement ralenties, les cellules satellites ont le potentiel de s’activer rapidement après l’induction d’une lésion de la membrane de la fibre musculaire. Une fois activées, elles prolifèrent, se différencient en cellules musculaires (myocytes) puis fusionnent entre elles afin de former de nouvelles fibres musculaires multinucléées (myofibres) [ 1 ]. Dans le même temps, un petit pool de cellules activées retourne à l’état quiescent autour des fibres afin de repeupler le réservoir de cellules souches musculaires. Ce processus biologique de formation de myotubes à partir de cellules souches musculaires et le maintien du nombre de cellules souches musculaires définit la myogenèse adulte (ou myogenèse régénérative).
Ce processus myogénique est en rapport direct avec l’expression de facteurs de transcription spécifiques, tels que Pax7, MyoD et Myogénine. L’expression spatio-temporelle de ces facteurs de transcription doit être précisément orchestrée grâce à l’action de facteurs épigénétiques agissant sur l’ouverture et la fermeture de la chromatine, et donc sur le remodelage de celle-ci. Ces facteurs épigénétiques sont cruciaux pour certains types de cellules souches (comme les cellules souches embryonnaires murines (mESC pour murine-embryonic stem cells ) en régulant la structure de la chromatine à l’origine de la modulation de l’expression génique dont dépend le devenir des cellules souches. Des dérégulations épigénétiques ont été observées dans de nombreuses pathologies telles que la maladie d’Alzheimer, les maladies d’Alzheimer, de Parkinson et de Huntington, ainsi que la sclérose latérale amyotrophique. Cette dernière, également appelée maladie de Charcot, est une maladie du motoneurone. La disparition des motoneurones entraîne une faiblesse musculaire et une amyotrophie importante. Il est donc nécessaire de comprendre le fonctionnement de ces facteurs épigénétiques afin de pouvoir in fine mettre en place des nouvelles stratégies thérapeutiques dans ces maladies.
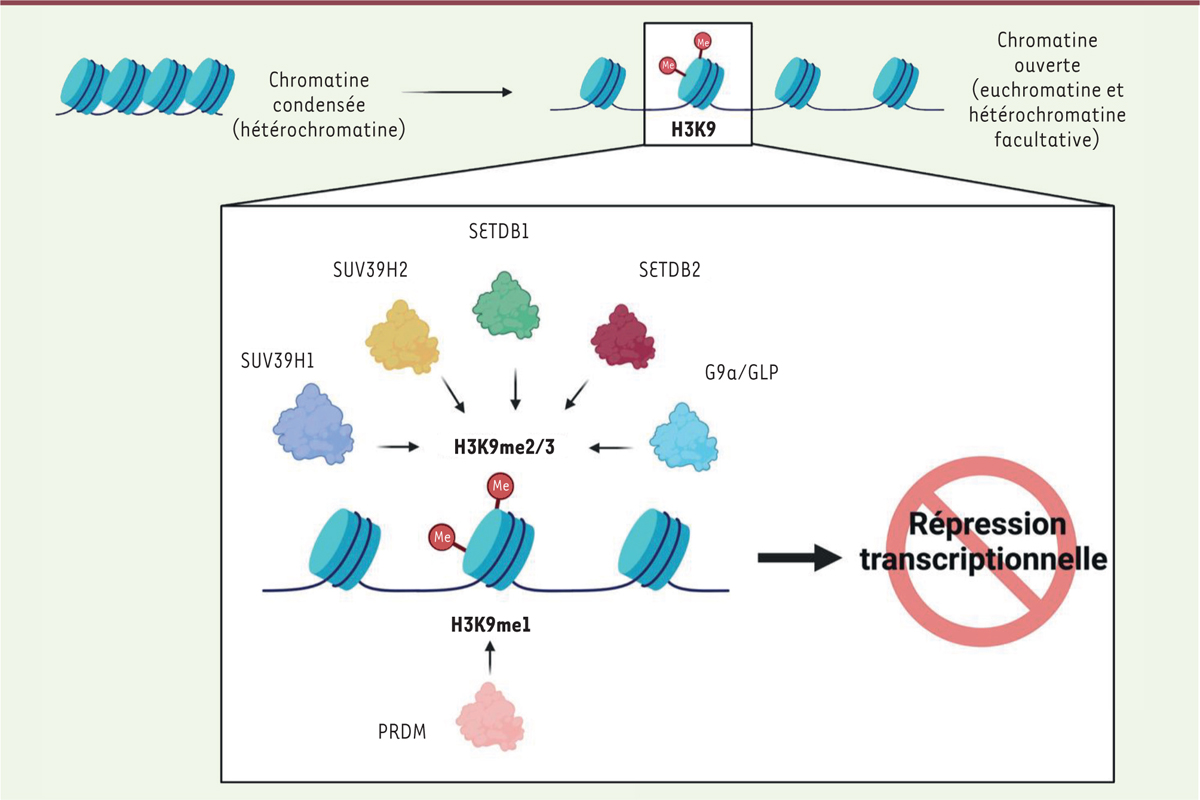
Les régulateurs clés de la chromatine sont les histones lysines méthyltransférases (KMT) et les déméthylases. Les histones méthyltransférases ont pour fonction de déposer des marques méthyles sur deux types d’acides aminés (les lysines et les arginines) présents sur les histones. Les déméthylases ont la capacité d’enlever ces marques. Parmi les KMT, la famille SUV39 dépose des marques méthyles répressives sur la lysine 9 de l’histone H3. La méthylation de la lysine 9 de l’histone H3 (H3K9) joue un rôle majeur dans l’extinction des gènes, terme désignant la répression transcriptionnelle qui s’exerce sur les zones majoritairement ouvertes de la chromatine, appelées euchromatine et hétérochromatine facultative. Cependant, son rôle reste à approfondir au cours de la myogenèse adulte. Cette famille est composée de six différents acteurs : SUV39H1, SUV39H2, SETDB1, SETDB2, G9a/GLP and PRDM ( Figure 1 ). Tous ne vont pas agir de la même façon ; PRDM, par exemple, a la capacité de poser une marque méthyle sur H3K9. Les quatre autres ont la capacité de di-méthyler ou tri- méthyler H3K9.
SUV39H1 est la KMT la plus explorée à ce jour. Elle participe à la répression de gènes impliqués dans la prolifération des cellules musculaires lorsque celles-ci se différencient et sortent du cycle cellulaire [ 2 ]. A l’inverse, dans les progéniteurs musculaires (myoblastes), SUV39H1 entraîne la répression génique du facteur de transcription myogénine en agissant directement sur son promoteur. La répression de myogénine se fait via la voie de signalisation p38-γ qui va ensuite agir sur SUV39H1, mettant ainsi en lumière les acteurs pouvant agir en amont des KMT. Cette répression permet d’éviter une entrée en différenciation trop précoce des myoblastes [ 3 ]. A l’inverse, dans des contextes de régénération musculaire in vivo , G9a ne semble pas avoir d’effet sur la myogenèse régénérative [ 4 ]. Un travail récent a cependant montré le rôle de HAIRLESS, une déméthylase antagoniste agissant sur la lysine 9 de l’histone 3. HAIRLESS est exprimée spécifiquement dans les cellules satellites quiescentes et sa perte induit une accélération de la perte des cellules souches musculaires avec l’âge [ 5 ]. Ces découvertes mettent en évidence le rôle crucial des KMT au cours de plusieurs étapes clés de la myogenèse adulte et pointent la nécessité d’explorer le rôle que peuvent avoir les autres KMT tout au long de ce processus.
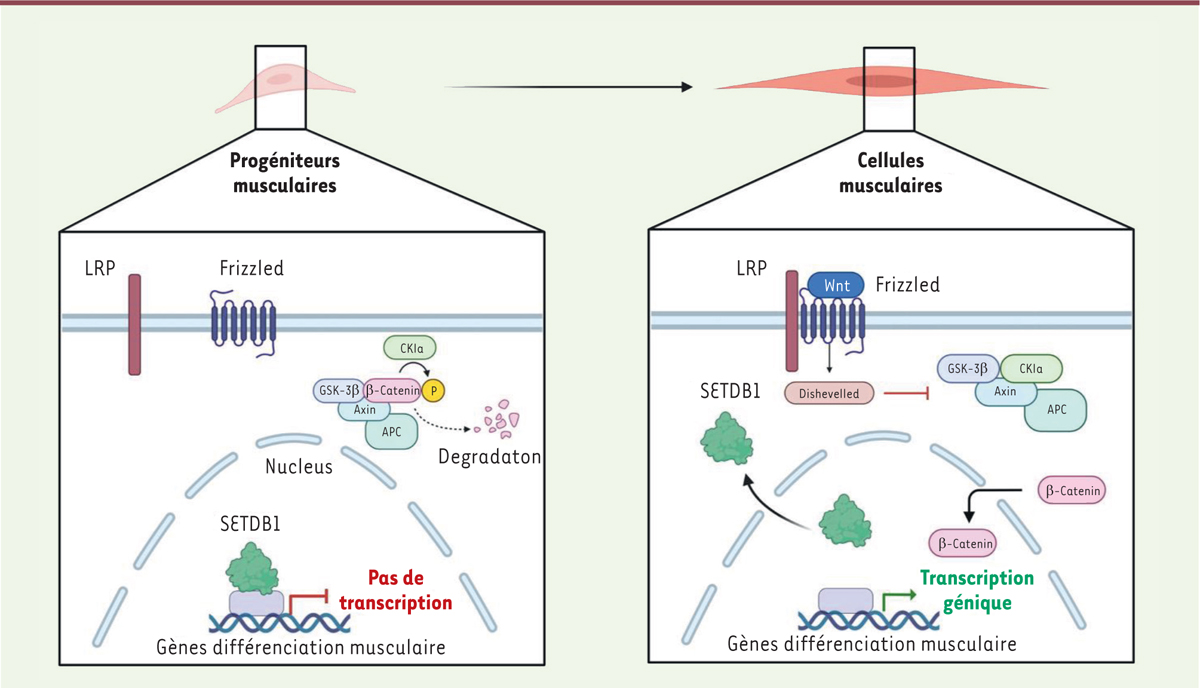
Actuellement, notre équipe s’intéresse à SETDB1, (pour SET domain bifurcated 1 ), également appelé ESET ou KMT1E [ 6 ]. SETDB1 est crucial pour la régulation de la pluripotence et l’auto-renouvellement des cellules souches embryonnaires chez la souris [ 7 ], et également pour la différenciation de divers progéniteurs comme, par exemple, les cellules souches pluripotentes humaines durant le développement [ 8 ]. SETDB1 est impliqué dans la triméthylation de la H3K9, au niveau de l’euchromatine et de l’hétérochromatine facultative, deux zones compactées [ 6 ]. Ces zones non compactées étant les plus à même d’être transcrites, il est nécessaire d’avoir des processus capables de réprimer la transcription de certaines de ces zones à découvert. L’équipe a montré qu’au sein des myoblastes, la localisation de SETDB1 est principalement nucléaire où il réprime spécifiquement certains gènes impliqués dans leur différenciation [ 9 ]. Lorsque le mécanisme de différenciation et de sortie du cycle cellulaire se met en place, SETDB1 est exporté hors du noyau et se retrouve au sein du cytoplasme. Ce transfert est contrôlé par la voie de signalisation Wnt/b-Caténine canonique ( Figure 2 ). L’accumulation de SETDB1 dans le cytoplasme est corrélée à une diminution de la protéine b-Caténine dans le cytoplasme. A l’inverse, l’absence de SETDB1 au sein du cytoplasme de la cellule est reliée à la présence de b-Caténine. Cette étude a également démontré que l’activation de la voie canonique Wnt3A/b-Caténine entraîne moins de dépôts de marques répressives H3K9 sur la chromatine au niveau de loci cibles comprenant Ankrd1 et Atxn10 , ceux-ci étant impliqués dans la différenciation des myoblastes. Cette diminution des marques répressives va entraîner un remodelage de la chromatine et son ouverture, induisant la transcription de gènes tels que ceux impliqués dans la différenciation des myoblastes, et ainsi induire leur différenciation précoce.
Notre travail actuel se focalise sur le rôle de SETDB1 dans les cellules souches musculaires lors de la régénération musculaire adulte. Pour ce faire, nous avons développé un modèle murin conditionnel permettant d’invalider l’expression du gène Setdb1 au sein des cellules souches musculaires de manière spécifique et temporellement contrôlée. Grâce à cet outil, nous pouvons caractériser au niveau histologique et moléculaire in vivo les conséquences de la perte de SETDB1 dans les cellules souches musculaires au cours de la myogenèse régénérative. Ces résultats permettront de mieux appréhender l’impact de SETDB1 sur le devenir des cellules souches musculaires murines et d’apporter de nouvelles pièces au puzzle du rôle des KMT au sein du muscle strié squelettique.