| |
| Med Sci (Paris). 38(11): 955–959. doi: 10.1051/medsci/2022141.Les génomes viraux défectueux du virus Chikungunya: Vers une nouvelle approche d’antiviraux à large spectre ? Sandra Khau1* and Cassandra Lopatynski1** 1M2 Infectiologie, Immunité, Vaccinologie et Biomédicaments, université de Tours
,
37000Tours
,
France |
L’actualité scientifique vue par les étudiants du Master 2 Infectiologie, Immunologie, Vaccinologie et Biomédicaments de la faculté de Pharmacie de l’université de Tours
Série coordonnée par Sophie Sibéril. La modification des habitats naturels des insectes vecteurs de maladies infectieuses est liée à l’urbanisation et à la déforestation. La perte de zones de biodiversité animale et le déplacement des vecteurs en zones urbaines favorisent ainsi l’émergence de maladies infectieuses telles que les arboviroses.
Le virus Chikungunya (CHIKV) est un arbovirus appartenant au genre Alphavirus transmis par les moustiques
Aedes spp
. L’infection par le virus peut provoquer, dans certains cas, une fièvre et des douleurs articulaires. CHIKV représente ainsi une menace importante puisque les moustiques vecteurs colonisent de nouveaux territoires, augmentant la prévalence de l’infection. Au cours des 15 dernières années, plusieurs épidémies ont émergé, dont celle de 2005-2006 dans l’Océan Indien, due à la souche CHIKV-IOL, et celle de 2013-2014, dans les îles des Caraïbes, due à la souche CHIKV-Carib [
1
–
3
]. En absence de traitement et de vaccin, la stratégie de contrôle du moustique vecteur reste actuellement l’axe de prévention principal contre l’infection. Une étude récente du groupe de Marco Vignuzzi, publiée dans
PLOS Pathogens
en 2021, a décrit une nouvelle stratégie pour sélectionner des particules virales défectueuses, aussi appelées génomes viraux défectueux (DVG,
defective viral genomes
), dans le but de lutter contre la multiplication virale et la dissémination de CHIKV parmi les insectes vecteurs. Les DVG sont naturellement produits au cours d’une infection à CHIKV
in vitro
dans des cellules de vertébrés et d’invertébrés, et
in vivo
chez le moustique [
4
,
5
]. Ces DVG se caractérisent par des délétions de bases génomiques compensées par le détournement des ressources cellulaires de l’hôte et/ou de protéines codées par le virus sauvage. Les DVG entrent ainsi en compétition avec le virus sauvage et se retrouvent en plus grand nombre, ce qui entraîne l’inhibition de la propragation du virus sauvage [
6
–
8
]. Dans l’article de Levi
et al.
[
5
], les auteurs ont développé une stratégie innovante permettant de caractériser les DVG produits ayant le meilleur potentiel antiviral contre le virus CHIKV sauvage. À l’issue de cette caractérisation, la capacité de ces DVG à inhiber la propagation du virus sauvage a ainsi été démontrée
in vivo
chez le moustique.
|
Génération de génomes viraux défectueux (DVG) par passages successifs
in vitro
et
in vivo
en condition de forte multiplicité d’infection
In vitro
, les auteurs ont obtenu des DVG en infectant des cellules de mammifères (Vero, Huh7) ou de moustiques (Aag2, U4.4) à une forte multiplicité d’infection (MOI pour
multiplicity of infection
) avec les souches parentales CHIKV-IOL ou CHIK-Carib
via
dix passages successifs (
Figure 1A
). L’ARN a été extrait du surnageant à chaque passage et un séquençage ARN à haut débit (RNAseq) a été effectué pour identifier les DVG des deux souches. La quantification des DVG a été réalisée par des analyses bio-informatiques (
Figure 1B
). Comme attendu, la quantité de DVG a augmenté au fur et à mesure des passages, et ce, quel que soit le type cellulaire. Afin de vérifier que les DVG pouvaient être également générés
in vivo
chez le moustique, les auteurs ont fait ingérer quotidiennement aux moustiques
Aedes aegypti
du sang infecté par la souche CHIKV-Carib. Après sept jours d’infection, les moustiques ont été sacrifiés et les organes ont été recueillis (intestin moyen, paroi abdominale, thorax, tête, pattes, ailes). L’analyse bio-informatique des ARN extraits a montré des profils de DVG similaires à ceux obtenus
in vitro
. Ces résultats indiquent que les DVG sont facilement générés lors d’une infection chez le moustique hôte et qu’ils partagent des profils de délétion semblables à ceux observés dans les cultures cellulaires.
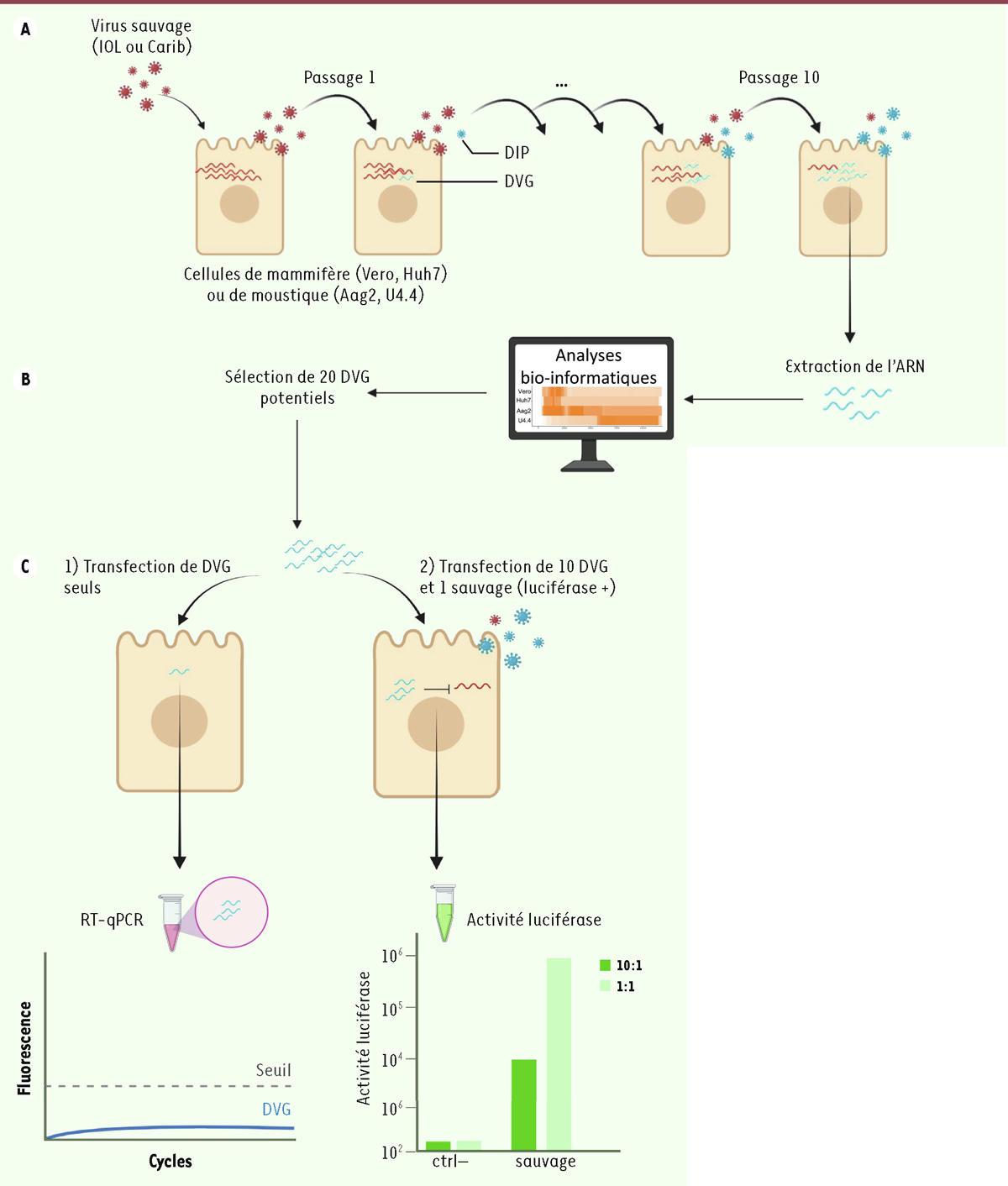
 | Figure 1.
Stratégie globale allant de la génération des DVG (pour Defective Viral Genome)
in vitro
et
in vivo
à leur caractérisation par analyse bio-informatique. A. Génération des DVG par passages successifs in vitro et in vivo en condition de forte infection.
Dix passages en série des souches parentales CHIKV-Carib et CHIKV-IOL ont été réalisés en condition de forte multiplicité d’infection (MOI pour
Multiplicity of infection
) dans des cellules de mammifère (Vero, Huh7) ou de moustique (Aag2, U4.4). Les DVG sont ainsi produits et sont assemblés sous forme de DIP (pour
Defective interfering particle
).
B. Les DVG produits
in vitro
et
in vivo
sont quantifiés et caractérisés par des analyses bio-informatiques.
Les ARNs sont extraits des surnageants à chaque passage puis séquencés (RNAseq) dans le but de quantifier les DVG des souches Carib et IOL. A l’aide d’une carte thermique, les « points chauds » potentiels de délétion du génome viral dans les différents types de cellules (de mammifère et de moustique) sont identifiés. Parmi les centaines de DVG caractérisés, 20 DVG potentiels sont sélectionnés à partir de deux critères : présence à une fréquence élevée et maintien dans tous les passages (1 à 10).
C. Les DVG sélectionnés sont incapables de s’auto-répliquer en absence de virus sauvage et interfèrent avec la réplication des virus sauvages CHIKV-Carib et CHIKV-IOL. (1)
Une RT-qPCR réalisée après transfection des DVG seuls a permis de mettre en évidence que les DVG candidats ne peuvent pas s’auto-répliquer en absence du virus parental.
(2)
La transfection des DVG en grand nombre (ratio 10:1) conduit à une inhibition de la réplication du virus sauvage CHIKV-Carib-Gluc (dans lequel a été cloné le gène rapporteur de la luciférase ; luciférase +), révélée par une diminution de l’activité luciférase. Cela aboutit à l’accumulation des DVG et à la libération de particules interférentes défectueuses. En rouge sont représentés les génomes et particules de virus sauvages (IOL ou Carib), en bleu les DVG et les particules interférentes défectueuses. Ratio 10:1 ou ratio 1:1 : mélange contenant dix fois plus ou autant d’ARN de DVG que d’ARN de virus sauvage CHIKV-Carib-Gluc.(figure réalisée avec Biorender)
|
L’analyse bio-informatique a permis d’identifier chez les DVG les plus fréquents et persistants générés
in vitro
et
in vivo
, des « points chauds » de délétion du génome viral dans les différents types de cellules hôtes (
Figure 1B
). En effet, lors de l’infection des cellules de mammifères Vero et Huh7 par la souche CHIKV-Carib, les délétions de l’ARN étaient circonscrites à la région couvrant les protéines non structurales NSP1-NSP2 (
Figure 2A
) alors que, lorsque les cellules de moustiques Aag2 étaient infectées, les délétions étaient plus largement répandues dans le génome. Les cellules de moustique U4.4 présentaient quant à elles des délétions de leur ARN dans la seconde moitié du génome (de la région NSP3 à la région 3’UTR) (
Figure 2A
). La même expérience a été réalisée avec la souche CHIKV-IOL (
Figure 2B
) et les profils de délétion d’ARN trouvés étaient similaires à ceux de la souche CHIKV-Carib dans les cellules de mammifère Vero et de moustique Aag2 mais différents dans les cellules de mammifère Huh7 et de moustiques U4.4. Ces variations, observées aussi bien lors d’infections
in vitro
qu’
in vivo
, suggèrent que les profils de délétion dans les DVG sont influencés par la souche virale et le type cellulaire hôte.
 | Figure 2.
Représentation graphique des génomes viraux défectueux produits
in vitro
et
in vivo
et caractérisés par analyse bio-informatique.
Schéma des DVG candidats en fonction du type cellulaire (mammifère ou moustique) et de la souche à partir desquels ils ont été purifiés (CHIKV-Carib (
A
), CHIKV-IOL (
B
)). Les pointillés représentent les zones de délétion potentielles.
|
|
Les DVG inhibent la réplication du virus sauvage
in vitro
dans les cellules de mammifères et de moustiques
Dans le but de choisir la particule défectueuse potentiellement la plus interférente parmi les centaines de DVG produits, les auteurs ont sélectionné 20 DVG les plus fréquemment retrouvés et maintenus au cours des différents passages dans les cultures de cellules de mammifère ou de moustique (
Figure 1B
). Après transfection des DVG seuls (sans virus sauvage) dans des cellules de mammifère, une RT-qPCR (
quantitative reverse transcription polymerase chain reaction
) réalisée à différents temps post-infection a montré que le nombre de copies d’ARN des DVG diminuait au fil du temps, ce qui reflète leur dégradation progressive. Ainsi, aucun DVG candidat ne peut s’auto-répliquer en l’absence du virus parental (
Figure 1C
.1
). Lorsque les cellules ont été transfectées avec un mélange contenant dix fois plus d’ARN de DVG que d’ARN de virus sauvage CHIKV-Carib-Gluc, dans lequel a été cloné le gène rapporteur codant la luciférase, une diminution significative de l’activité luciférase était observable (
Figure 1C
.2
). Ces résultats indiquent que les DVG dérivant de cultures de cellules de mammifère ou de moustique peuvent inhiber la réplication virale des virus sauvages dans des cellules de mammifère lorsque ces DVG sont introduits de manière exogène en quantités importantes.
Pour déterminer si ces DVG peuvent aussi inhiber la réplication virale dans les cellules de moustique, la même expérience a été réalisée dans des cellules d’un autre moustique,
Aedes albopictus
(U4.4). De façon similaire à ce qui a été observé précédemment, une inhibition de la réplication du virus sauvage a été induite en présence des ARN de DVG.
Il est intéressant de noter que les auteurs ont également montré que les DVG dérivant d’un Alphavirus peuvent avoir une activité inhibitrice
in vitro
sur différentes souches. En effet les DVG dérivés de la souche CHIKV-IOL (possédant 7 % de divergence nucléotidique avec la souche CHIKV-Carib [
9
]) sont capables d’inhiber la souche sauvage CHIKV-Carib et réciproquement. Les DVG peuvent donc avoir une action à large spectre au sein d’une même espèce virale [
9
]. Afin de savoir si l’inhibition peut s’effectuer de manière plus large au sein des différents virus du genre Alphavirus, la même expérience d’interférence des DVG a été réalisée mais en présence soit du virus O’nyong-nyong (proche de CHIKV) soit du virus Sindbis (très éloigné de CHIKV) en tant que souche sauvage cible. Les résultats ont indiqué que certains DVG maintenaient une activité inhibitrice contre les virus O’nyong-nyong et Sindbis. Ainsi, les DVG dérivant d’un Alphavirus peuvent avoir une activité inhibitrice sur différentes souches virales proches mais également sur des souches plus éloignées appartenant au même genre.
|
Les DVG bloquent la dissémination virale
in vivo
dans les moustiques
Aedes aegypti
Pour déterminer la capacité des DVG à bloquer l’infection ou la dissémination dans le moustique hôte, des ARN purifiés de DVG avec le meilleur potentiel antiviral ont été injectés dans des moustiques
Aedes aegypti
. Deux jours plus tard, les moustiques ont été nourris de sang contenant du virus CHIKV-Carib-Gluc. Cinq jours après l’infection, les niveaux de réplication virale dans les intestins moyens étaient identiques en absence ou en présence de DVG tandis que la réplication virale dans le reste du corps du moustique diminuait significativement en présence des DVG. Ces résultats renforcent donc l’idée que les DVG n’auraient pas d’effet direct sur le degré d’infectiosité mais exerceraient un rétrocontrôle négatif sur la réplication virale et la dissémination dans le moustique hôte.
|
En conclusion, il a été mis en évidence qu’il existe différents types de génomes viraux défectueux (DVG) générés lors de l’infection à CHIKV qui se caractérisent par divers profils de délétions, et cela
in vitro
chez les vertébrés et les invertébrés, mais également
in vivo
chez le moustique. Les DVG ayant la meilleure activité inhibitrice contre la souche sauvage CHIKV
in vitro
à la fois chez les vertébrés et les invertébrés peuvent avoir une activité antivirale à large spectre en agissant sur différents virus du genre Alphavirus. De plus, une pré-exposition aux DVG peut moduler la dissémination virale dans le moustique.
Les travaux réalisés par cette équipe constituent donc une base solide pour l’application des DVG dans le contexte de la lutte contre les arbovirus. En effet, les DVG peuvent être un outil thérapeutique utile contre l’infection des organismes cibles (moustiques, mammifères) par le CHIKV mais également par d’autres Alphavirus. Ces DVG peuvent de ce fait représenter également une stratégie de contrôle de la dissémination virale au sein de la population des moustiques qui deviennent ainsi incompétents pour la propagation du virus. Un autre article publié par cette même équipe en 2021 s’intéresse à d’autres points tels que l’éventuel rôle immunostimulant de ces DVG et leur mode d’administration [
8
]. L’injection de
Virus-Like Particles
contenant les DVG a montré des résultats prometteurs
in vivo
dans un modèle murin. Cette stratégie permet de délivrer les DVG au site d’injection et de les disséminer aux organes ciblés par les virus, permettant ainsi de diminuer l’infectiosité et la dissémination virale chez la souris [
8
]. Dans l’ensemble, les résultats obtenus par l’équipe de Marco Vignuzzi représentent aujourd’hui une avancée majeure et prometteuse dans la prévention et l’élaboration de traitements contre les arboviroses.
|
1.
Vignuzzi
M
,
Higgs
S
.
The Bridges and Blockades to Evolutionary Convergence on the Road to Predicting Chikungunya Virus Evolution.
.
Annu Rev Virol.
2017;
;
4
:
:181.
–
200
.
2.
Levi
LI
,
Vignuzzi
M
.
Arthritogenic Alphaviruses: A Worldwide Emerging Threat?
.
Microorganisms.
2019;
;
7
:
:133.
.
3.
Chretien
J-P
,
Anyamba
A
,
Bedno
SA
,
et al.
Drought-associated chikungunya emergence along coastal East Africa.
.
Am J Trop Med Hyg.
2007;
;
76
:
:405.
–
407
.
4.
Poirier
EZ
,
Goic
B
,
Tomé-Poderti
L
,
et al.
Dicer-2-Dependent Generation of Viral DNA from Defective Genomes of RNA Viruses Modulates Antiviral Immunity in Insects.
.
Cell Host Microbe.
2018;
;
23
:
:353.
–
65.e8
.
5.
Levi
LI
,
Rezelj
VV
,
Henrion-Lacritick
A
,
et al.
Defective viral genomes from chikungunya virus are broad-spectrum antivirals and prevent virus dissemination in mosquitoes.
.
PLoS Pathog.
2021;
;
17
:
:e1009110.
.
6.
Tapia
K
,
Kim
W
,
Sun
Y
,
et al.
Defective Viral Genomes Arising In Vivo Provide Critical Danger Signals for the Triggering of Lung Antiviral Immunity.
.
PLoS Pathog.
2013;
;
9
:
:e1003703.
.
7.
Shirogane
Y
,
Rousseau
E
,
Voznica
J
,
et al.
Experimental and mathematical insights on the competition between poliovirus and a defective interfering genome.
.
PLoS Pathog.
2021;
;
17
:
:e1009277.
.
8.
Rezelj
VV
,
Carrau
L
,
Merwaiss
F
,
et al.
Defective viral genomes as therapeutic interfering particles against flavivirus infection in mammalian and mosquito hosts.
.
Nat Commun.
2021;
;
12
:
:2290.
.
9.
Zhang
X
,
Huang
Y
,
Wang
M
,
et al.
Differences in genome characters and cell tropisms between two chikungunya isolates of Asian lineage and Indian Ocean lineage.
.
Virology J.
2018;
;
15
:
:130.
.
|