Le cancer du sein est le cancer le plus fréquent et la deuxième cause de mortalité par cancer chez les femmes [ 1 ]. Chaque année, près de 1,3 million de cas de cancer du sein sont diagnostiqués dans le monde, dont 20 % correspondent au sous-type triple-négatif (TN) [ 2 ] ( → ).
(→) Voir la Nouvelle de M. M-Rabet et al ., m/s n° 11, novembre 2017, page 936
Ce sous-type est défini par l’absence d’expression du récepteur des œstrogènes (ER), du récepteur de la progestérone (PR), et du récepteur 2 du facteur de croissance épidermique humain (HER2) par les cellules tumorales. Il est considéré comme la forme la plus agressive du cancer du sein, pour laquelle aucune thérapie spécifique efficace n’est disponible. Le traitement habituel repose sur une chimiothérapie à base de doxorubicine, une anthracycline certes efficace, mais aux nombreux effets indésirables, dus notamment à sa cardiotoxicité [ 3 ]. Dans ce contexte, plusieurs études précliniques sont actuellement en cours pour concevoir de nouvelles molécules ayant un réel potentiel thérapeutique et moins d’effets secondaires.
Les statines sont des inhibiteurs de la 3-hydroxy-3-méthyl-glutaryl coenzyme A réductase largement utilisés pour traiter l’hypercholestérolémie et réduire ainsi la mortalité par accident cardiovasculaire. La simvastatine, l’une des statines les plus lipophiles, serait la meilleure candidate pour le traitement du cancer du sein [ 4 ] pour plusieurs raisons : 1) elle inhibe préférentiellement la croissance des cellules tumorales du cancer du sein TN par rapport aux cellules tumorales non TN [ 5 ], 2) son utilisation est associée à une réduction significative de la croissance des cellules cancéreuses in vitro et in vivo , et 3) des études précliniques ont montré qu’elle pourrait supprimer la tumeur et réduire le potentiel métastatique du cancer du sein [ 6 ]. Ces études plaident en faveur d’un effet bénéfique de l’utilisation de simvastatine sur la survie des patientes atteintes d’un cancer du sein. Sur le plan fonctionnel, la sensibilité des cellules tumorales du cancer du sein à la simvastatine a été associée à une réduction de la prolifération et de la survie ( in vitro et in vivo ) de ces cellules, et à une réduction de la croissance tumorale. Cependant, les mécanismes moléculaires impliqués dans ces effets de la simvastatine ne sont pas entièrement compris. Or, nous avons récemment identifié le signal calcique comme un acteur central de la réponse des cellules cancéreuses TN à la simvastatine [ 7 ].
Un rôle critique de la perturbation de l’homéostasie calcique dans l’apoptose cellulaire a été proposé [ 8 ]. Les propriétés antitumorales de la simvastatine ont été associées à un dérèglement de l’homéostasie du calcium, dont le mécanisme reste inconnu. Nous avons montré que la signalisation par l’ion Ca 2+ est nécessaire pour ces propriétés antitumorales, et que les flux de Ca 2+ provenant des réserves intracellulaires sont impliqués au même titre que ceux provenant du milieu extracellulaire à travers les canaux calciques membranaires TRPC1 et TRPC3 contrôlés par le senseur calcique du réticulum endoplasmique STIM1 ( stromal interaction molecule 1 ) [ 7 ]. Cette augmentation de la concentration intracellulaire des ions Ca 2+ entraîne une accumulation de molécules impliquées dans la mort cellulaire, telles que BIM ( Bcl-2-like protein 11 ), et une surcharge mitochondriale en ions Ca 2+ induisant la diminution du potentiel membranaire de la mitochondrie (ΔΨ m ), la surproduction d’espèces réactives de l’oxygène (ROS), avec pour conséquence la libération de facteurs pro-apoptotiques, tels que le cytochrome c, qui active la caspase-3, ce qui conduit à l’apoptose cellulaire. L’analyse de la croissance tumorale dans un modèle de xénogreffe de tumeur chez la souris a confirmé le rôle central du Ca 2+ dans la capacité de la simvastatine à réduire le volume de la tumeur ( Figure 1 ) . Dans des expériences in vitro , l’augmentation de la concentration intracellulaire des ions Ca 2+ dans les cellules tumorales mammaires par l’ajout de simvastatine diminue leurs capacités invasives et tumorigènes, en accord avec l’impact thérapeutique favorable de cette molécule suggéré par les résultats des études précliniques. Ces résultats lèvent le voile sur le mécanisme moléculaire de l’activité de la simvastatine et fournissent un nouveau support expérimental pour de futurs essais cliniques utilisant ce médicament pour traiter le cancer du sein.
| Figure 1.
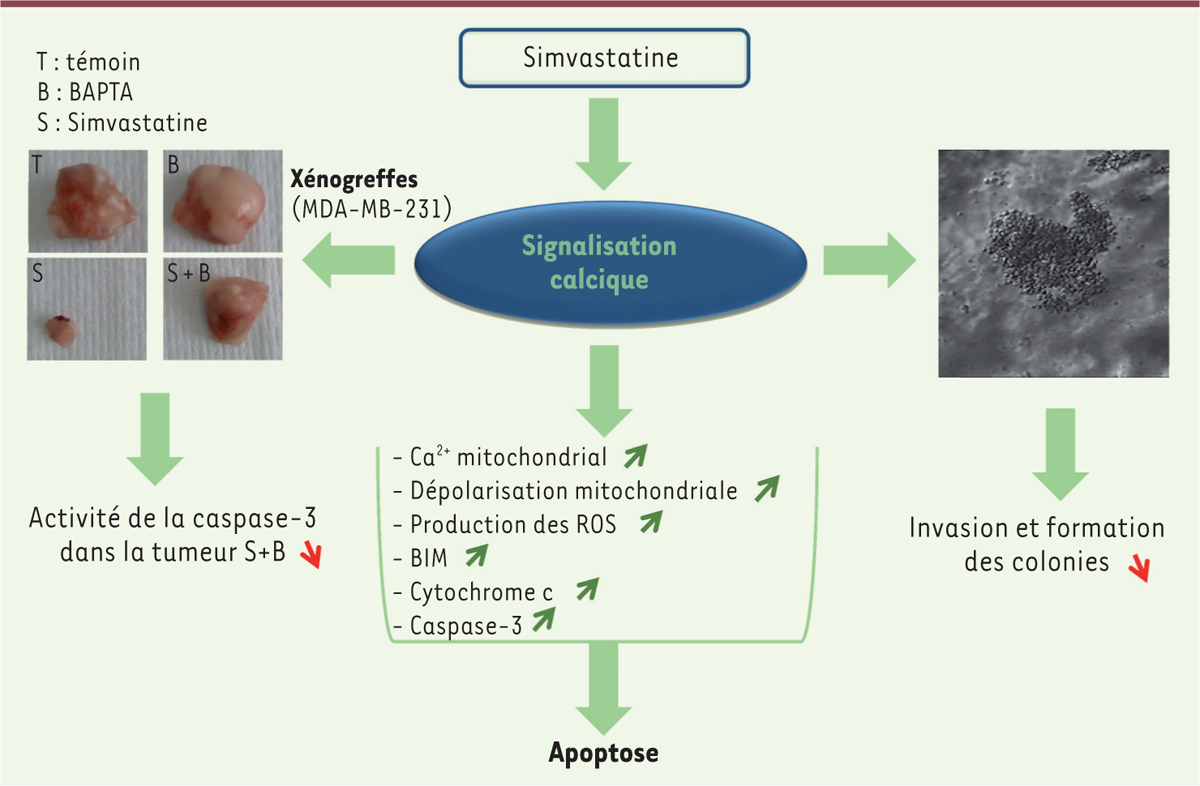
Représentation schématique du mode d’action de la simvastatine dans les cellules tumorales du cancer du sein.
Le traitement des cellules tumorales du cancer du sein par la simvastatine provoque une élévation de la concentration cytoplasmique de l’ion Ca
2+
via
la libération des réserves intracellulaires, à laquelle s’ajoute une entrée de Ca
2+
provenant de l’espace extracellulaire impliquant les canaux calciques TRPC1 et TRPC3 [
7
]. L’augmentation de la concentration cytosolique de Ca
2+
induit l’activation de la protéine BIM, une augmentation de la concentration mitochondriale de Ca
2+
, suivie par une dépolarisation de la membrane mitochondriale et la surproduction de dérivés réactifs de l’oxygène (
reactive oxygen species
, ROS), qui permet notamment la libération du cytochrome c et l’activation de la caspase-3. L’activation de ces voies de signalisation contrôlées par la concentration cytosolique de Ca
2+
est impliquée dans l’apoptose, l’invasion tumorale et la formation des colonies de cellules cancéreuses. Chez les souris porteuses de xénogreffes tumorales, la chélation du Ca
2+
intracellulaire par le BAPTA diminue considérablement la capacité de la simvastatine à réduire le volume tumoral. BAPTA : acide aminopolycarboxylique qui fixe le calcium ; MDA-MB-231 : cellules de cancer du sein établies en lignée.
|
Par ailleurs, notre étude [ 7 ] a permis de montrer que les effets pro-apoptotiques de la simvastatine et de la doxorubicine impliquent, dans les deux cas, une augmentation de la concentration intracellulaire des ions Ca 2+ . Nous avons analysé l’impact de l’association simvastatine plus doxorubicine sur les cellules cancéreuses mammaires. Nous avons d’abord constaté que la cytotoxicité de la simvastatine était bien supérieure à celle de la doxorubicine, avec une différence d’un facteur 30 dans les valeurs de la concentration inhibitrice médiane après 48 heures de traitement. En outre, la combinaison de la simvastatine et de la doxorubicine à faibles doses augmentait l’apoptose des cellules cancéreuses TN de façon synergique et pas seulement additive (l’indice de combinaison entre les deux médicaments était nettement inférieur à 1 1, ) [ 7 ]. Ces résultats indiquent que la combinaison de simvastatine et de doxorubicine pourrait être efficace pour traiter le cancer du sein, notamment son sous-type triple-négatif.