| |
| Med Sci (Paris). 37(8-9): 820–822. doi: 10.1051/medsci/2021129.L’interaction HMGB1/tétranectine Une cible thérapeutique dans les états septiques ? Yasmine Adimi,1a Mathieu Esposito,1b Rayan Braik,1c and Jonathan Pol2d 1Master 2 Immunologie intégrative et systémique (I2S), Parcours Immunologie, mention BMC, Sorbonne Université
,
Paris
,
France
.
2Inserm U1138, Université de Paris, Sorbonne Université
,
Paris
,
France
.
MeSH keywords: Animaux, Modèles animaux de maladie humaine, Protéine HMGB1, Humains, Sepsie, traitement médicamenteux |
Le sepsis est un syndrome, caractérisé par un dysfonctionnement d’organes secondaire à une réponse inflammatoire générale dérégulée et induit par une infection [
1
]. Chaque année, dans le monde, la mortalité liée au sepsis est estimée à environ 11 millions de personnes – soit près d’un décès sur cinq [
2
]. La prise en charge des états septiques représente donc actuellement l’un des plus grands enjeux de la médecine. D’un point de vue physiopathologique, le sepsis est caractérisé, dans sa phase aiguë, par une décharge massive de cytokines pro- et anti-inflammatoires libérées secondairement à la présence de signaux de dangers constitutifs des pathogènes incriminés. Cette libération massive de cytokines - appelée tempête cytokinique - peut aboutir, par des mécanismes complexes, à un syndrome de défaillance multi-viscéral (SDMV) et au décès [
1
]. En dépit des possibilités thérapeutiques nouvelles apparues depuis l’avènement des anticorps monoclonaux, largement utilisés dans les maladies auto-immunes et inflammatoires, aucune étude clinique n’a montré de résultats encourageants dans le sepsis [
3
]. Une des hypothèses avancées à cette absence de résultats serait que le blocage d’une cytokine - intégrée dans un processus complexe de signalisation - serait insuffisant pour moduler efficacement le processus physiopathologique dans son ensemble.
Peu d’études se sont intéressées aux médiateurs terminaux du sepsis, dont la régulation par des traitements pharmacologiques pourrait améliorer la prise en charge clinique de cette maladie. Parmi ces médiateurs, les protéines HMGB1 (
high mobility group box 1)
et tétranectine (TN) suscitent désormais un intérêt croissant pour leur rôle dans les mécanismes sous-jacents aux états septiques.
|
HMGB1 : une cible potentielle pour le contrôle de l’inflammation et du sepsis
HMGB1 est une protéine constitutive de la chromatine. En condition de stress, elle est détectée dans le milieu extracellulaire et joue le rôle d’alarmine pour le système immunitaire, participant ainsi au processus inflammatoire [
4
]. En présence d’endotoxines bactériennes (lipopolysaccharides, LPS), les macrophages produisent non seulement des cytokines pro-inflammatoires, comme les facteurs de nécrose tumorale TNF-α et β, mais peuvent aussi libérer dans le milieu HMGB1. Chez les souris traitées avec du LPS, la production transitoire mais massive de ces cytokines ainsi que la libération plus tardive de HMGB1 s’accompagnent de dommages tissulaires et conduit au choc septique. En clinique, la survie des sujets présentant une septicémie est corrélée aux concentrations sériques de HMGB1 ; les patients présentant des concentrations moindres ont plus de chance de survie. Dans le modèle murin de sepsis induit par le LPS, l’injection d’un anticorps (Ac) neutralisant anti-HMGB1 améliore la survie, alors que, inversement, l’administration de HMGB1, en plus du LPS, est létale [
5
]. La protéine HMGB1 semble aussi impliquée dans l’immunosuppression qui succède au sepsis. En effet, sa présence inhibe l’explosion oxydante des neutrophiles et empêche ainsi l’élimination des pathogènes dans les modèles murins de choc septique. Chez les patients ayant survécu à un choc septique, le dysfonctionnement des neutrophiles est persistant tant qu’HMGB1 est détectable dans le sérum. Comme précédemment, l’activité oxydante des neutrophiles peut être rétablie en présence d’un Ac anti-HMGB1 [
6
]. Enfin, l’HMGB1 circulante peut être capturée par certains macrophages par endocytose, et pourrait induire leur mort cellulaire par pyroptose [
7
]. La pyroptose est une mort cellulaire programmée dépendant de la caspase 1 et contrôlée par l’assemblage d’un complexe protéique nommé « pyroptosome ». Elle aboutit à la perte d’intégrité de la membrane plasmique, à la libération de cytokines pro-inflammatoires et de signaux de danger [
8
]. La libération et l’internalisation de HMGB1 jouent donc un rôle majeur dans l’évolution de l’inflammation lors d’un choc septique.
|
La tétranectine : un régulateur de l’inflammation et du sepsis
La tétranectine (TN) est une protéine oligomérique liant le plasminogène et appartenant à la famille des C-lectines, des protéines reconnaissant les glycoconjugués de façon calcium-dépendante [
9
]. Son rôle physiologique reste à ce jour indéterminé. Les études concernant la TN suggèrent qu’elle jouerait un rôle dans la régulation de la fibrinolyse ainsi que dans le développement des tissus musculaires et osseux. Ainsi, sa dérégulation est impliquée dans la genèse de certaines maladies osseuses (telle que l’ostéogenèse imparfaite) et coronariennes [
10
,
11
].
Dans une étude récemment publiée dans
Science Translational Medicine
, Chen
et al.
[
12
] ont observé, dans le sérum de patients septiques ayant un taux élevé de HMGB1, une diminution de la TN. Cette diminution était également plus marquée chez les patients décédés d’un choc septique. Afin d’évaluer le rôle physiologique de la TN, les auteurs ont alors utilisé des souris dans lesquelles le gène codant la TN avait été invalidé (souris TN KO). Après induction d’un choc septique par ponction-ligature cæcale (LCP), les souris TN KO présentaient une atteinte d’organes plus sévère (notamment des poumons et du foie), une production de facteurs pro-inflammatoires augmentée dans les poumons (IL[interleukine]-1β, IL-6 et cyclooxygénase-2], ainsi qu’une mortalité plus élevée en comparaison avec des souris de phénotype sauvage. Dans un autre modèle murin de choc septique par LCP de souris, l’administration sanguine de TN murine à une dose subphysiologique (0,1 mg/kg) était associée à une survie prolongée. Au contraire, ce bénéfice n’était pas observé à une dose supraphysiologique (1 mg/kg) [
12
]. Ainsi, en fonction de sa concentration circulante, la TN présenterait une activité anti-inflammatoire bénéfique dans le cadre du sepsis.
|
Certains anticorps ciblant la tétranectine peuvent prévenir la mortalité dans le choc septique
Afin d’évaluer plus précisément le rôle de la TN dans le sepsis, Chen
et al.
ont, dans un premier temps, immunisé quatre lapins avec de la TN murine pour produire des anticorps polyclonaux (pAb1 à 4) anti-TN [
12
]. Ces Ac anti-TN ont ensuite été administrés par voie intrapéritonéale à des souris présentant une septicémie induite par LCP et leur impact sur la létalité a été analysé. Remarquablement, deux de ces préparations d’anticorps polyclonaux (pAb2 et pAb3) ont amélioré le taux de survie des animaux. Dans un premier temps, les auteurs ont alors recherché dans la TN humaine, la séquence en acides aminés de la protéine qui était reconnue par les anticorps montrant un bénéfice thérapeutique chez la souris. L’épitope ainsi défini, noté p5, correspond aux résidus 86 à 109 de la protéine et adopte une forme d’hélice α stable [
12
]. Dans un second temps, les chercheurs ont généré des anticorps monoclonaux par immunisation de souris avec la TN humaine. L’analyse des épitopes reconnus a permis d’identifier une séquence immunodominante au sein de p5, correspondant aux résidus 93 à 102 (NDALYEYLRQ). Cet épitope, étiqueté p5-5, est également retrouvé dans la séquence de la protéine d’autres mammifères, comme la souris, le lapin, et le singe. Ainsi, ces anticorps pourraient être utilisés à la fois dans des modèles animaux précliniques et en clinique chez l’homme [
12
].
Afin d’évaluer l’intérêt thérapeutique des anticorps anti-TN, Chen
et al
. ont administré à des souris ayant une septicémie (dans le modèle LCP) des anticorps monoclonaux dirigés contre les domaines p5 (anti-TN-p5 : IgG2a mAb2, IgG1 mAb6, IgG2b mAb8) ou contre un autre domaine de la TN, le domaine p2 (anti-TN-p2 : IgG1 mAb9). L’injection du mAb9 anti-TN-p2 induisait une mortalité précoce. À l’inverse, les souris septiques injectées avec les Ac anti-TN-p5 présentaient un meilleur taux de survie que les souris non traitées. En particulier, l’administration du mAb8 anti-TN-p5 limitait la diminution de la TN circulante et réduisait le taux sanguin des cytokines associées à la gravité du sepsis (IL-6, CXCL1 [
chemokine C-X-C motif ligand 1
]). Cet Ac réduisait la charge bactérienne, mesurée 28 heures après l’induction de l’état de choc, et atténuait notablement les défaillances pulmonaires et hépatiques [
12
]. Ainsi, les anti-TN-p5 semblent faciliter l’élimination des pathogènes et prévenir l’inflammation pathologique conduisant au choc septique.
|
TN interagit avec HMGB1 et facilite son endocytose par les macrophages
En utilisant la technique de résonance plasmonique de surface (OpenSPR), qui permet d’évaluer les constantes d’interaction entre deux molécules, les auteurs ont mis en évidence une interaction directe de forte affinité entre HMGB1 et TN, qui était bloquée en présence de l’Ac anti-TN-p5 mAb8. Afin de préciser ces mécanismes, des macrophages ont été cultivés en présence de HMGB1 et de TN, couplés ou non à des fluorochromes, en présence ou non d’un inhibiteur d’endocytose ; le contenu intracellulaire a été analysé par des techniques de
western blot
et de microscopie à fluorescence. Ces expériences ont révélé que l’interaction de TN avec HMGB1 favorise l’endocytose du complexe HMGB1/TN par les macrophages [
12
].
|
L’internalisation du complexe TN/HMBG1 est impliquée dans la pyroptose des macrophages
La protéine HMGB1 avait été décrite comme un déclencheur de la pyroptose des macrophages, évènement qui participe à la phase hyperinflammatoire, potentiellement mortelle, du sepsis. Pour cette raison, Chen
et al.
ont évalué le rôle de la TN sur cette mort cellulaire induite par HMGB1. Ils ont ainsi montré que l’addition de HMGB1
in vitro
dans un modèle de culture de macrophages humains, n’est pas suffisante pour provoquer la pyroptose, détectée par l’analyse de la perte d’intégrité de la membrane cellulaire. À l’inverse, l’ajout simultané de TN et de HMGB1 provoquait la pyroptose, celle-ci étant inhibée par l’adjonction d’un Ac anti-TN-p5. L’action conjointe de la TN et de HMGB1 serait donc nécessaire à l’induction de la pyroptose des macrophages. Ainsi, l’action bénéfique des Ac anti-TN-p5 dans les modèles murins de choc septique peut être expliquée par deux hypothèses non exclusives : 1) l’injection d’Ac anti-TN-p5 empêche l’endocytose de la TN et d’HMGB1, limitant ainsi la pyropoptose et donc la décharge de cytokines pro-inflammatoires néfaste durant la phase aiguë du sepsis ; 2) l’inhibition de l’endocytose du complexe TN/HMGB1 induit une augmentation des concentrations plasmatiques de la TN qui pourrait avoir une action immuno-régulatrice bénéfique.
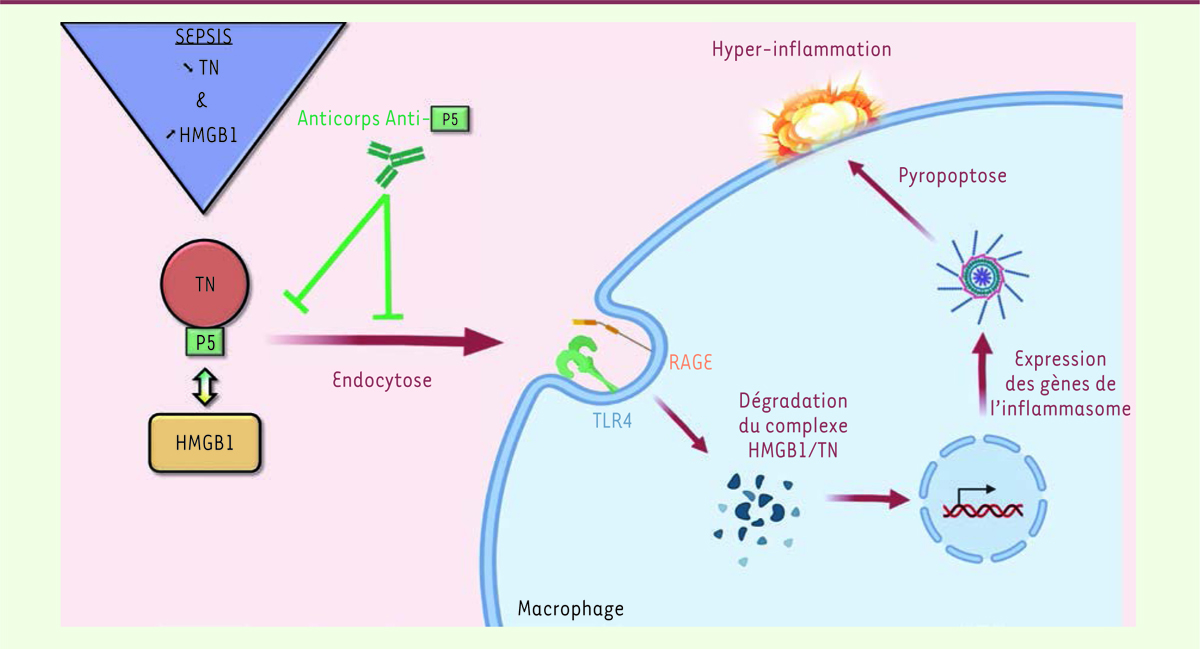
 | Figure 1.
L’endocytose du complexe TN/HMGB1 participe à la pyroptose des macrophages.
Le sepsis entraîne une diminution de la concentration sérique de la protéine TN et une augmentation de HMGB1. La TN interagit avec HMGB1 probablement via son domaine P5, induisant l’endocytose du complexe HMGB1/TN par les macrophages, ces derniers présentant des récepteurs détectant l’HMGB1 extracellulaire comme TLR4 et RAGE. La dégradation du complexe HMGB1/TN induit une cascade de signalisation responsable de l’activation de l’inflammasome puis de la pyroptose des macrophages. L’ensemble de ces mécanismes entraine une hyper-inflammation. Les anticorps monoclonaux spécifiques du domaine P5 de la TN empêchent l’interaction TN/HMGB1 et leur endocytose, évite la pyroptose et l’hyper-inflammation. HMGB1 :
high-mobility group box 1
; RAGE :
receptor for advanced glycation end products
; TLR4 :
Toll-like receptor 4
; TN : tétranectine.
|
|
Les résultats de cette étude suggèrent que la TN facilite l’endocytose du complexe TN/HMGB1 par les macrophages et précipite leur mort cellulaire par pyroptose, ainsi que la décharge de cytokines pro-inflammatoires. La pyroptose est un mécanisme protecteur de l’hôte qui peut cependant avoir des effets délétères lorsqu’elle est mal régulée, en particulier dans les états septiques, au cours desquels elle entraîne la libération excessive de cytokines pro-inflammatoires. L’utilisation d’anticorps monoclonaux dirigés contre un domaine peptidique particulier de la TN empêche sa liaison avec HMGB1, et donc son internalisation par les macrophages. L’effet bénéfique potentiel des Ac anti-TNp5 reposerait donc sur leur contrôle indirect de la pyroptose. D’autres études seront nécessaires pour mieux caractériser les mécanismes immunorégulateurs des TN et HMGB1. Enfin, compte tenu de l’hétérogénéité des patients septiques, une approche individualisée sera probablement le prérequis indispensable à l’utilisation de ce type de thérapies ciblées.
Tempora mutantur et nos mutamur in illis !
1
‡
|
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
Footnotes |
1.
Hotchkiss
RS
Moldawer
LL
Opal
SM
et al.
Sepsis and septic shock.
.
Nat Rev Dis Primers.
2016;
;
2
:
:16045.
.
3.
Cavaillon
J
,
Singer
M
,
Skirecki
T
.
Sepsis therapies: learning from 30 years of failure of translational research to propose new leads.
.
EMBO Mol Med.
2020;
;
12
:
:e10128.
.
4.
Deng
M
Scott
MJ
Fan
J
Billiar
TR
Location is the key to function: HMGB1 in sepsis and trauma-induced inflammation.
.
J Leukoc Biol.
2019;
;
106
:
:161.
–
169
.
5.
Wang
H
Bloom
O
Zhang
M
et al.
HMG-1 as a late mediator of endotoxin lethality in mice.
.
Science.
1999;
;
285
:
:248.
–
251
.
6.
Grégoire
M
Tadié
JM
Uhel
F
et al.
Frontline science: HMGB1 induces neutrophil dysfunction in experimental sepsis and in patients who survive septic shock.
.
J Leukoc Biol.
2017;
;
101
:
:1281.
–
1287
.
7.
Xu
J
Jiang
Y
Wang
J
et al.
Macrophage endocytosis of high-mobility group box 1 triggers pyroptosis.
.
Cell Death Differ.
2014;
;
21
:
:1229.
–
1239
.
8.
Man
SM
Karki
R
Kanneganti
TD
Molecular mechanisms and functions of pyroptosis, inflammatory caspases and inflammasomes in infectious diseases.
.
Immunol Rev.
2017;
;
277
:
:61.
–
75
.
9.
Berglund
L
Petersen
TE
The gene structure of tetranectin, a plasminogen binding protein.
.
FEBS Lett.
1992;
;
309
:
:15.
–
19
.
10.
Wewer
UM
Ibaraki
K
Schjørring
P
et al.
A potential role for tetranectin in mineralization during osteogenesis.
.
J Cell Biol.
1994;
;
127
:
:1767.
–
1775
.
11.
McDonald
K
,
Glezeva
N
,
Collier
P
, et al.
Tetranectin, a potential novel diagnostic biomarker of heart failure, is expressed within the myocardium and associates with cardiac fibrosis.
.
Sci Rep.
2020;
;
10
:
:7507.
.
12.
Chen
W
,
Qiang
X
,
Wang
Y
, et al.
Identification of tetranectin-targeting monoclonal antibodies to treat potentially lethal sepsis.
.
Sci Transl Med.
2020;
;
12
:
:3833.
.
|