| |
| Med Sci (Paris). 36(11): 1085–1087. doi: 10.1051/medsci/2020217.
La bactérie
Vibrio cholerae
lyse les bactéries environnantes et assimile leur ADN qu’elle intègre dans son propre génome
Marion Cannac1* and Thomas Petit1** 1École normale supérieure de Lyon, Département de biologie, Master biologie
,
Lyon
,
France MeSH keywords: Antibiose, Bactéries, Bactériolyse, Conjugaison génétique, Compétence pour la transformation par l'ADN, ADN bactérien, Génome bactérien, Transformation bactérienne, Vibrio cholerae, physiologie, génétique, métabolisme, pathogénicité |
Pour survivre dans une niche écologique ou en coloniser une nouvelle, les bactéries doivent acquérir des caractéristiques qui leur confèrent des avantages dans cette niche. Chez les bactéries, ces caractéristiques peuvent être acquises de façon horizontale, entre individus non apparentés co-existants dans le même environnement, par ce que l’on nomme des transferts horizontaux de gènes (THG) [
1
]. Les THG sont cependant peu stables en général, car l’ADN n’est pas toujours intégré dans le génome bactérien ou conservé sous forme de plasmide de façon pérenne. De plus, leur bénéfice est variable selon la qualité de l’ADN incorporé, l’information portée et le locus d’insertion dans le génome : si l’ADN est dénaturé, qu’il ne porte pas une information utile pour la bactérie ou qu’il s’insère dans un gène vital pour la bactérie, le THG peut être délétère, voire non viable.
La transformation naturelle est un type de THG. Elle consiste, pour une bactérie compétente, à incorporer dans son génome de l’ADN capté dans le milieu [
2
].
Vibrio cholerae
est une bactérie Gram-négative qui peut être pathogène pour l’Homme, mais qui vit en milieu naturel sur les exosquelettes chitineux du zooplancton d’eau douce [
3
]. La compétence de
V. cholerae,
c’est-à-dire sa capacité à acquérir une molécule d’ADN exogène par ses caractéristiques naturelles, est sous le contrôle de la chitine et de ses produits de dégradation, ainsi que sous celui de la densité cellulaire
via
le
quorum sensing
. Ces facteurs externes modulent l’activité du régulon
com
de compétence de la bactérie, qui correspond à un ensemble de gènes contrôlant la compétence, régulés par un gène commun. Ce gène régulateur commun est
qstR,
codant un facteur de transcription du même nom qui agit directement sur le régulon
com
pour permettre à la bactérie d’intégrer naturellement de l’ADN du milieu. QstR est régulé conjointement par
tfox
, gène régulateur directement activé par la chitine et ses produits de dégradation [
4
], et par
hapR
, gène maître du
quorum sensing
[
5
].
Pourtant, l’activation du régulon
com
ne suffit pas à expliquer la transformation naturelle efficace de
V. cholerae
. Borgeaud
et al.
se sont alors questionnés sur l’implication d’autres acteurs dans la transformation de
V. cholerae
[
6
]. Cette bactérie présente un système de sécrétion de type 6 (SST6), une machinerie protéique largement répandue au sein des bactéries Gram-négatives, qui permet d’injecter des protéines, appelées effecteurs, à la fois dans des hôtes eucaryotes et procaryotes. Ce système s’apparente à une seringue et est équipé d’un fourreau contractile qui, lorsqu’il est activé, propulse un tube protéique qui vient transpercer la membrane de l’hôte, induisant la libération des effecteurs dans la cellule cible [
7
]. Les auteurs ont alors exploré un potentiel rôle du SST6 de
V. cholerae
dans le processus d’assimilation de l’ADN en vue d’une transformation naturelle.
|
Le cluster de gènes du SST6 est activé par les mêmes voies que celui des gènes de compétence
Les auteurs ont voulu vérifier si les facteurs influençant le régulon de compétence contrôlaient également l’expression des gènes du SST6. Pour cela, ils ont utilisé une souche de
V. cholerae
modifiée de manière à ce que
tfox
soit artificiellement induit en présence d’arabinose dans le milieu de croissance, ce qui permet d’étudier l’expression de différents gènes en fonction de l’activation artificielle ou non de
tfox
. Comme décrit précédemment, l’activation de
tfox
permet l’expression des gènes de compétence. De même, en accord avec l’hypothèse des auteurs, les résultats de ces expériences montrent que les gènes du cluster codant le SST6 (
vipA, vipB, vasD
et
vasK
) ne sont activés qu’en présence d’arabinose, leur expression est donc sous la dépendance de Tfox.
Par ailleurs, les auteurs ont voulu tester l’importance des gènes
hapR
et
qstR
dans l’activation du cluster de gènes codant le SST6. Les auteurs ont donc évalué l’expression des gènes du SST6 lorsque
tfox
était activé mais que
hapR
et
qstR
étaient inactivés. Ils ont alors mis en évidence la nécessité de l’activation de
tfox
mais également d’
hapR
et de
qstR
pour l’expression des gènes du cluster codant le SST6. Ainsi, comme pour le régulon
com,
le cluster codant le SST6 est activé par Tfox et HapR
via
l’activation du facteur de transcription QstR.
|
Le SST6 est induit par la croissance de la bactérie sur une surface de chitine semblable à son environnement naturel
On sait donc d’une part que
tfox
est induit après croissance de
V. cholerae
sur la chitine et d’autre part que l’activation de
tfox
, avec le concours de
hapR
, permet l’induction
via
QstR des gènes du cluster codant le SST6. Afin de lier définitivement la chitine à l’expression du SST6, les auteurs ont ensemencé des bactéries exprimant VipA (une des protéines du SST6) fusionnée à la GFP sur un milieu chitineux ou non. En présence de chitine, ils ont alors observé l’expression de la GFP, sous forme de foci allongés, témoignant de l’expression des gènes codant pour le SST6. La bactérie
V. cholerae
assemble donc son SST6 lors de sa croissance sur un milieu chitineux naturel, environnement dans lequel la bactérie acquiert une compétence naturelle efficace. Ces résultats suggèrent que le SST6 pourrait jouer un rôle dans la compétence de la bactérie.
|
L’expression du SST6 en parallèle des gènes de compétence mène à la lyse des bactéries voisines et à la transformation naturelle de V. cholerae
Les auteurs ont alors émis l’hypothèse que le SST6 pourrait contribuer à la transformation naturelle de
V. cholerae
, certainement en facilitant la récupération d’ADN. Ils ont d’abord observé, par des essais de compétition, que l’activation de Tfox menait à une lyse significative des bactéries entourant
V. cholerae
, de manière dépendante des gènes
hapR
,
qstR
, et ceux codant pour le SST6. Ces résultats suggèrent donc que le SST6 pourrait être impliqué dans la transformation en lysant les bactéries voisines de
V. cholerae
. Afin de tester cette hypothèse, des essais de transformation ont été menés entre deux souches de
V. cholerae
sensibles à l’action du SST6. La première, désignée comme la souche proie, contenait dans son génome une cassette de résistance à la kanamycine et avait subi une inactivation de son SST6, l’empêchant de se comporter en « attaquante ». La deuxième, la souche prédatrice, jouissait d’un SST6 totalement fonctionnel et contenait une cassette de résistance à la rifampicine. La combinaison de ces deux résistances permettait de sélectionner uniquement les souches prédatrices ayant récupéré par transformation la cassette de résistance à la kanamycine de la souche proie. Les seuls essais dans lesquels était observée l’apparition de colonies bactériennes sur les milieux de double sélection, c’est-à-dire de colonies transformées, étaient ceux où Tfox était activé par l’arabinose et où à la fois le gène maître du quorum sensing
hapR
, le gène régulateur
qstR
, les gènes de compétence et ceux du cluster codant le SST6 étaient fonctionnels. Le SST6 de
V. cholerae
est donc bien nécessaire à la transformation naturelle de la bactérie, lorsque celle-ci croît sur un milieu chitineux à une densité bactérienne importante, par son action de lyse des bactéries voisines suivie d’une récupération de leur ADN.
|
Pour résumer, dans son environnement naturel,
V. cholerae
croît sur des surfaces chitineuses qui induisent l’expression de
tfox
. De plus, elle forme facilement des communautés de microorganismes appelées biofilms qui se composent de plusieurs espèces de bactéries. Dans ces biofilms,
V. cholerae
se trouve à haute densité cellulaire, ce qui induit l’expression du gène
hapR
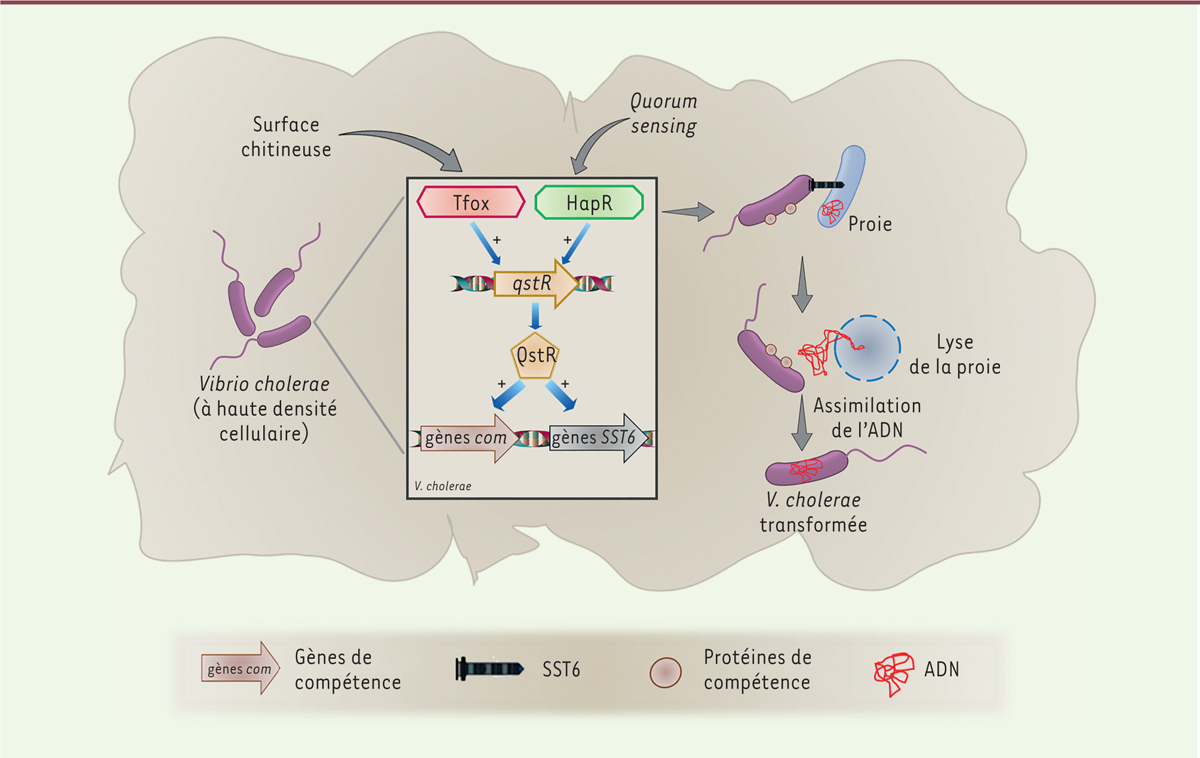
. Les résultats exposés ici montrent que les protéines Tfox et HapR activent l’expression du facteur de transcription QstR qui, à son tour, active non seulement le programme de compétence, mais aussi les gènes codant le SST6
(
Figure 1
)
. Ainsi,
V. cholerae
peut induire la lyse de bactéries compétitrices via son SST6, provoquant la libération d’ADN dans le milieu. Puisque la bactérie exprime des protéines de compétence, elle peut facilement assimiler l’ADN environnant, ce qui permet sa transformation. Les bactéries appartenant à la même souche ne sont pas affectées par l’effet toxique du SST6 et des effecteurs qu’il permet d’injecter, car elles expriment des protéines inactivant ces effecteurs [
8
].
 | Figure 1.
Le transfert horizontal de gènes est favorisé par le SST6 chez
Vibrio cholerae
. Le transfert horizontal de gènes est favorisé par la co-régulation du régulon
com
des gènes de compétence et du SST6, contrôlée par le facteur de transcription QstR. Ce dernier est lui-même régulé conjointement par
tfox
, gène régulateur de la transformation, activé par le milieu chitineux, et
hapR
, gène maître du
quorum sensing
, activé à haute densité cellulaire.
|
Les transferts horizontaux de gènes sont primordiaux pour l’évolution des bactéries. En effet, en assimilant l’ADN de microorganismes présents dans l’environnement, les bactéries peuvent acquérir de nouveaux gènes leur conférant un avantage sélectif. Le système décrit chez
V. cholerae
est en ce sens très efficace. En effet, suite à la lyse par le SST6 de bactéries avoisinantes, l’ADN récupéré par
V. cholerae
a une probabilité plus forte de porter des gènes permettant de mieux survivre dans les conditions spécifiques du milieu, puisqu’il provient de bactéries qui y sont adaptées. Par ailleurs, le fait que l’ADN provienne de bactéries dont la lyse a été déclenchée par
V. cholerae
limite le délai pendant lequel l’ADN reste libre dans le milieu, ce qui augmente sa qualité et sa probabilité d’intégration au sein du génome de
V. cholerae
.
Les avantages acquis par transformation naturelle peuvent favoriser la réplication de la bactérie chez des hôtes comme l’homme, à son détriment. En effet, l’acquisition d’îlots de pathogénicité et de résistance aux antibiotiques contribue à la virulence de la bactérie, qui provoque chaque année des épidémies souvent mortelles. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
|
1.
Thomas
CM
,
Nielsen
KM
.
Mechanisms of, and barriers to, horizontal gene transfer between bacteria.
.
Nat Rev Microbiol.
2005;
;
3
:
:711.
–
721
.
2.
Chen
I
,
Dubnau
D
.
DNA uptake during bacterial transformation.
.
Nat Rev Microbiol.
2004;
;
2
:
:241.
–
249
.
3.
Finkelstein
RA
,
Baron
S
.
Cholera, Vibrio cholerae O1 and O139, and other pathogenic vibrios.
.
Medical microbiology.
1996
;
Galveston (TX):
:
University of Texas Medical Branch at Galveston;
4.
Meibom
KL
,
Blokesch
M
,
Dolganov
NA
,
et al.
Chitin induces natural competence in Vibrio cholerae.
.
Science.
2005;
;
310
:
:1824.
–
1827
.
5.
Lo Scrudato
M
,
Blokesch
M
.
A transcriptional regulator linking quorum sensing and chitin induction to render Vibrio cholerae naturally transformable.
.
Nucleic Acids Res.
2013;
;
41
:
:3644.
–
58
.
6.
Borgeaud
S
,
Metzger
LC
,
Scrignari
T
,
et al.
The type VI secretion system of Vibrio cholerae fosters horizontal gene transfer.
.
Science.
2015;
;
347
:
:63.
–
67
.
7.
Ho
BT
,
Dong
TG
,
Mekalanos
JJ
.
A view to a kill: the bacterial type 6 secretion system.
.
Cell Host Microbe.
2014;
;
15
:
:9.
–
21
.
8.
Dong
TG
,
Ho
BT
,
Yoder-Himes
DR
,
et al.
Identification of T6SS-dependent effector and immunity proteins by Tn-seq in Vibrio cholerae.
.
Proc Natl Acad Sci USA.
2013;
;
110
:
:2623.
–
2628
.
|