| |
| Med Sci (Paris). 36(4): 348–357. doi: 10.1051/medsci/2020061.Antiplaquettaires actuels, en cours de développement et
cibles thérapeutiques Mustapha Zine El Alaoui,1* Alexandre Guy,1* Loubna Khalki,4 Youness Limami,5 Ali Benomar,5 Nabil Zaid,6 Yahia Cherrah,5 Hassan Mekhfi,7 Rachida Cadi,1 and Younes Zaid5,6** 1Department of Biology, Faculty of Sciences, Hassan II
University, Casablanca, Maroc 2Laboratoire d’hématologie, Hôpital universitaire de
Bordeaux, Pessac, France 3Univ. Bordeaux, Inserm, UMR1034, Biologie des maladies
cardiovasculaires, F-33600Pessac,
France 4Research Center of Mohammed VI University of Health
Sciences, Casablanca, Maroc 5Research Center of Abulcasis University of Health
Sciences, Rabat, Maroc 6Faculty of Sciences, Department of Biology, Mohammed V
University, Rabat, Maroc 7Laboratory of Physiology, Genetic and Ethnopharmacology,
Faculty of Sciences, Mohammed the First University,
Oujda,
Maroc |

Vignette (Photo © Inserm U949). Les maladies cardiovasculaires (MCV) constituent un ensemble d’affections qui touchent le
système cardiovasculaire et représentent la première cause de mortalité dans le monde.
L’Organisation mondiale de la santé (OMS) estime que, d’ici à 2030, près de
23,6 millions de personnes décèderont de maladies cardiovasculaires, principalement de
cardiopathies et d’accidents vasculaires cérébraux. La survenue d’évènements
cardiovasculaires (ECV) résulte le plus souvent de la présence d’athérosclérose au
niveau vasculaire. Ces plaques d’athérosclérose se constituent au niveau des vaisseaux,
secondairement à des facteurs de risque tels que tabagisme, dyslipidémie, obésité, ou
hypertension artérielle. Ces plaques sont à l’origine d’une sténose ou d’une obstruction
complète du vaisseau, conduisant à une ischémie chronique ou aiguë des tissus qui sont
situés dans le territoire de vascularisation atteint. Les plaquettes sont des cellules sanguines dont le rôle principal est de participer aux
mécanismes d’hémostase primaire et de coagulation. En effet, en cas de lésion
vasculaire, leur activation et leur agrégation permettent la mise en place d’un thrombus
prévenant ainsi la survenue d’une hémorragie. La membrane des plaquettes,
via l’exposition de phospholipides, constitue un élément majeur qui
contribue à l’activation des voies de la coagulation. Elle représente ainsi une surface
catalytique pour les principaux facteurs de la coagulation. Mais l’activation
plaquettaire joue également un rôle primordial dans les mécanismes de mise en place
d’athérosclérose au niveau artériel, et en cas de rupture de plaques d’athérome, en
étant les principaux constituants du thrombus à l’origine de la survenue d’un ECV. Il
est donc légitime que les plaquettes soient devenues les cibles privilégiées de
médicaments indiqués dans la prévention et le traitement de ces évènements. Les voies
d’activation plaquettaire étant multiples, de nombreux médicaments ont été développés
dans le but d’interférer avec l’activation plaquettaire via
l’inhibition de ces différentes voies. Dans cette revue, nous ferons un état des lieux
des médicaments antiplaquettaires disponibles à la prescription, mais également des
nouveaux antiplaquettaires en cours de développement. La Figure 1 résume toutes les cibles moléculaires des
agents antiplaquettaires identifiées jusqu’à présent et le Tableau I résume les caractéristiques
principales des agents antiplaquettaires actuels.
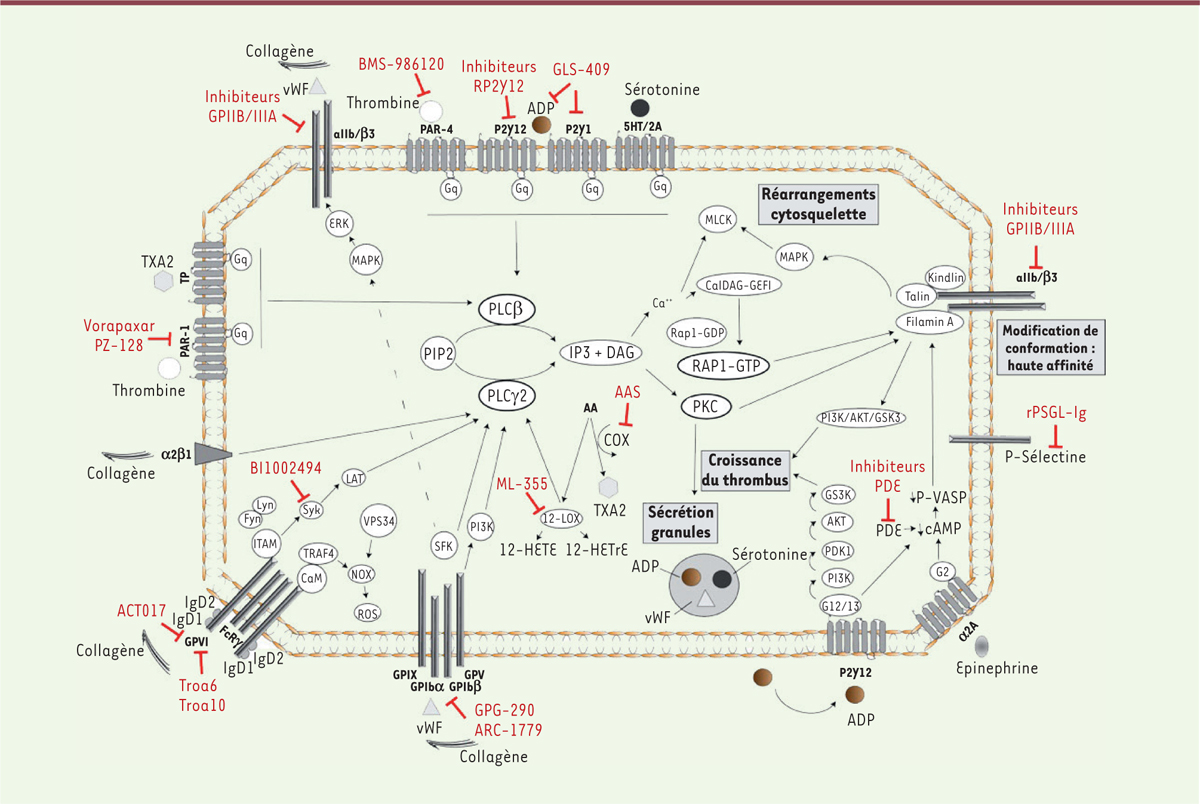
 | Figure 1. Mécanismes d’activation plaquettaire et molécules
anti-plaquettaires. L’interaction du collagène avec
le complexe GPIb-IX-V et le complexe GPVI-RFcγ déclenche l’activation de la
PLC-γ2 (voir Glossaire). La liaison d’agonistes solubles
(ADP, thrombine, TXA2) au niveau des récepteurs couplés aux protéines Gq
déclenche l’activation de la PLCβ. L’activation des PLC-γ2 et PLCβ entraîne
l’augmentation de la concentration en calcium intra-cellulaire, puis
l’activation de la PKC et de RAP1. L’activation de PKC et RAP1 mène à la
réorganisation du cytosquelette, à la sécrétion granulaire, et à la
modification conformationnelle de l’intégrine αIIbβ3. La liaison du
fibrinogène à l’intégrine αIIbβ3 permet d’initier l’agrégation plaquettaire,
et déclenche la signalisation « outside-in » permettant la réorganisation du
cytosquelette puis la croissance et la stabilisation du thrombus. |
Tableau I.
| Antiagrégant |
Cible |
Demi-vie |
Avantages |
Inconvénients |
Réf |
| Aspirine |
COX-1
COX-2 |
13 à 31 min |
Prévention secondaire à long terme contre les MCV, coût
réduit |
Résistance possible, toxicité gastro-intestinale,
complications hémorragiques, variabilité potentielle de réponse
individuelle |
[42] |
| Clopidogrel |
P2Y12 |
0,5 à 1 h |
Possibilité d’utilisation en cas d’intolérance à
l’aspirine, risque hémorragique inférieur à celui de l’aspirine (2 %
versus 2,66 %). |
Prurit, éruption cutanée, risque de résistance,
rarement purpura thrombocytopénique |
[43] |
| Prasugrel |
P2Y12 |
2 à 15 h |
Inhibition plaquettaire plus importante que le
clopidogrel, meilleure efficacité que le clopidogrel dans la prise
en charge du SCA. |
Risque hémorragique majoré, coût supérieur au
clopidogrel |
[44] |
| Ticagrelor |
P2Y12 |
6 à 12 h |
Efficace chez les patients résistants au clopidogrel,
inhibition forte et rapide versus le clopidogrel,
cliniquement supérieur au clopidogrel quand administré aux patients
souffrant d’un SCA. |
Risque hémorragique important, effets secondaires
(dyspnée, céphalées, toux, syndrome de réponse inflammatoire
systémique), coût mensuel important versus le
clopidogrel (75 € vs 18 €). |
[45] |
| Cangrelor |
P2Y12 |
5 min |
Action très rapide
Efficacité inhibitrice plaquettaire
importante |
Risque hémorragique majoré par rapport au
clopidogrel |
[46] |
| Dipyridamole |
PDE |
24 h |
Risque hémorragique moindre versus
l’aspirine, effet couplé anti-inflammatoire et antiplaquettaire,
propriétés anti-oxydantes. |
Céphalées (>1/3 des patients traités) |
[47] |
| Cilostazol |
PDE3 |
11 à 13 h |
Efficacité en prévention secondaire lors des AVC,
risque hémorragique moindre versus l’aspirine |
Non encore approuvé par la FDA dans la prise en charge
de l’AVC |
[48] |
| Iloprost |
IP |
30 min |
Effet vasodilatateur pulmonaire, amélioration de
l’oxygénation vasculaire chez les patients atteints d’hypertension
artérielle pulmonaire. |
Effets secondaires (toux, céphalées, douleurs de
mâchoire) |
[49] |
| Abciximab |
GPIIb/IIIa |
10 min |
Réduction de risque d’évènements ischémiques et
réduction de mortalité chez les patients avec IDM |
Risque de thrombopénie, risque hémorragique
important |
[50] |
| Tirofiban |
GPIIb/IIIa |
2 h |
Réduction de risque d’évènements ischémiques et
réduction de mortalité chez les patients avec IDM, immunogénicité
limitée, |
Risque hémorragique important |
|
| Eptifibatide |
GPIIb/IIIa |
2.5 h |
Immunogénicité limitée, innocuité supérieure au
tirofiban chez les patients avec SCA. |
Risque hémorragique important |
|
| Vorapaxar (SCH 530348) |
PAR-1 |
159 à 311 h |
Forme orale disponible, longue demi-vie |
Contre-indiqué chez les patients avec antécédents d’AVC
du fait d’un risque d’hémorragie intracrânienne |
|
Caractéristiques des agents antiplaquettaires
actuels. MCV : Maladie cardiovasculaire ; SCA : Syndrome
coronarien aigu ; SRIS : Syndrome de réponse inflammatoire systémique ;
AVC : Accident vasculaire cérébral. |
|
Les mécanismes de l’activation plaquettaire Le premier évènement qui mène à l’activation plaquettaire est l’exposition du
collagène sous-endothélial au niveau de la circulation sanguine, lors d’une blessure
vasculaire. Le collagène ainsi exposé entraîne l’adhérence des plaquettes en
interagissant avec de nombreux récepteurs exprimés par ces cellules. Les plaquettes
se lient en effet au facteur von Willebrand (vWF), lui-même associé au collagène,
via le complexe (GP)Ib-IX-V. Ce complexe est constitué de
quatre protéines trans-membranaires de type I : GPIbα, GPIbβ, GPIX et GPV. Cette
liaison entre le complexe (GP)Ib-IX-V et le facteur vWF est renforcée par une
seconde interaction qui s’établit entre le collagène et le complexe GPVI-RFcγ,
composé de la glycoprotéine GPVI associée au récepteur pour la région Fc des IgG de
type IIa (RFcgIIa). L’engagement de ces deux récepteurs plaquettaires a un rôle
primordial dans l’activation plaquettaire : il déclenche les signaux dits
« inside-out » qui vont provoquer l’activation des intégrines
α2β1 (ou GPIa-IIa) et αIIbβ3 (ou GPIIb/IIIa). Cette activation va également
renforcer l’adhérence plaquettaire via la liaison de l’α2β1 au
collagène et de l’αIIbβ3 au facteur vWF (Figure 1). |
Les signaux « inside-out » Le premier mécanisme initiant les signaux « inside-out » est
déclenché par la liaison du domaine A1 du facteur vWF, lié au collagène, à la
sous-unité GPIb, entraînant l’activation du complexe (GP)Ib-IX-V [1]. Cette activation provoque la
mobilisation des protéine kinases de la famille Src (SFK), l’activation de la
phospholipase Cγ2 (PLCγ2), la formation de diacylglycérol (DAG) et l’activation de
la protéine kinase C (PKC). Le second mécanisme, qui repose sur l’activation du
complexe GPVI-RFcγ par le collagène, conduit au recrutement des kinases de la
famille Src, Fyn et Lyn, au niveau d’un domaine spécifique du RFcγ (le domaine ITAM,
pour immune receptor tyrosine-based activation motif), puis,
via la voie de signalisation Syk/LAT (linker for T-cell
activation), à l’activation de la PLCγ2 [2]. L’activation de la GPVI est également à
l’origine d’une augmentation de la production intracellulaire de dérivés réactifs de
l’oxygène (ROS) par les plaquettes, via la liaison de TRAF4
(tumour-necrosis factor receptor associated factor 4) à la
GPVI, participant à leur activation. Même si le collagène est le ligand principal de
la GPVI, d’autres protéines, comme la laminine, les D-Dimères, le fibrinogène ou la
fibrine peuvent interagir avec la GPVI [3]. La PLCγ2 est donc une protéine « pivot » dans les voies de
signalisation « inside-out » plaquettaires mais une autre
phospholipase, la PLCβ, activée par des récepteurs liés à la protéine Gq
(Gq-protein-coupled receptors, ou GPCR) est également
impliquée. Les GPCR comprennent notamment le récepteur P2Y12 (récepteur de
l’adénosine diphosphate), les récepteurs de la thrombine (protease-activated
receptor, PAR), le récepteur du thromboxane A2 (thromboxane
receptor, TP), le récepteur de l’épinéphrine (récepteur adrénergique
α2A) et le récepteur de la sérotonine (récepteur du 5-hydroxytryptamine 2A). La
liaison de ces récepteurs à leurs ligands respectifs entraîne l’activation de la
PLCβ, responsable de l’activation plaquettaire précoce. Celle-ci aura pour résultat
la libération extra-cellulaire des granules denses (contenant de l’ADP et de la
sérotonine) et des granules α (contenant du facteur vWF et du fibrinogène), qui
entretiendront l’activation plaquettaire. La surface plaquettaire va également
constituer une surface catalytique pour le complexe pro-thrombinase, générant la
formation, à partir de pro-thrombine, de thrombine qui participe aussi à
l’activation plaquettaire précoce, via son interaction avec les
récepteurs PAR-1 et PAR-4 [4]. L’ensemble de ces signaux conduiront donc à l’activation des PLCγ2 et
PLCβ et à la production de seconds messages, inositol-triphosphate (ITP) et
diacylglycérol (DAG), augmentant les taux de calcium (Ca++)
intra-plaquettaire, l’activation de la PKC et de la protéine CalDAG-GefI
(calcium- and DAG- regulated guanine nucleotide exchange factor
1), provoquant l’activation d’une GTPase, Rap1 (Ras-related
protein 1), cruciale pour la fonction de l’intégrine αIIbβ3 et pour
induire les modifications conformationnelles du cytosquelette plaquettaire et la
génération de thromboxane A2 [5]. L’intégrine αIIbβ3 activée subit une modification conformationnelle
qui favorise sa liaison au fibrinogène, qui est le point de départ d’une deuxième
vague de signaux, dits signaux « outside-in », cruciale pour la
croissance et la stabilisation du thrombus. |
Les signaux « outside-in » La modification conformationnelle de l’intégrine αIIbβ3 lui permet d’acquérir une
haute affinité pour le fibrinogène, avec, pour conséquence, l’établissement de ponts
entre plaquettes (ou agrégation plaquettaire) augmentant ainsi la taille du
thrombus. L’activation de l’αIIbβ3 entraîne également une vague de signaux
intra-cellulaires concourant à la stabilisation et à la croissance du thrombus. On
retrouve, notamment, la voie de signalisation de la phosphoinositide-3-kinase (PI3K)
et d’Akt (protéine kinase B) impliquant PDK1 (phosphoinositide-dependent
protein kinase 1) et GSK3 (glycogen synthase
kinase-3). La voie des MAPK (mitogen-activated protein
kinases) participe, elle, au réarrangement du cytosquelette [6]. À noter que la PI3K est
activée en aval de nombreux récepteurs, dont le complexe GpIb-IX-V, le complexe
GpVI-RFcg, les GPCR ou la GPIIb-IIIa [7]. Son activation active également la GPIIb-IIIa
(« inside-out ») via la voie PLC-Rap1 [5]. |
Les antiplaquettaires disponibles Les inhibiteurs de cyclo-oxygénases L’aspirine ou acide acétylsalicylique (AAS) appartient à la famille des
anti-inflammatoires non stéroïdiens (AINS) salicylés. À fortes doses, cette
molécule est utilisée à visée anti-inflammatoire. À des doses plus faibles, elle
est prescrite comme anti-plaquettaire. L’aspirine agit en inhibant de manière
irréversible les cyclo-oxygénases (COX) 1 et 2, via
l’acétylation de résidus sérine, respectivement aux positions 529 et 516, de ces
molécules [ 8]. Dans les
plaquettes, COX1 (principale COX présente dans les plaquettes humaines) est
responsable du métabolisme de l’acide arachidonique (AA) en TXA2 qui sera
sécrété par la plaquette et stimulera, par effet autocrine, les récepteurs
plaquettaires participant à l’activation de ces cellules. L’AAS inhibe la
synthèse de TXA2 par les plaquettes. En raison d’une synthèse protéique
de novo faible par les plaquettes, et d’un effet sur les
plaquettes mais aussi sur leurs progéniteurs, l’aspirine a une action dans la
durée, bien que sa demi-vie soit courte. Sur le plan thérapeutique, l’aspirine
est indiquée à forte posologie, en phase aiguë de la survenue d’ECV (infarctus
du myocarde, accident vasculaire cérébral), puis en prévention secondaire, à des
posologies plus faibles. L’aspirine est également indiquée en prévention
primaire en cas de risque cardio-vasculaires. Les inhibiteurs du récepteur P2Y12 Le récepteur de l’ADP P2Y12 peut être inhibé par cinq molécules : deux
appartiennent à la famille des thiénopyridines (clopidogrel -
Plavix ®, prasugrel Efient ®) et deux aux
cyclopentyl-triazolo-pyrimidines (CPTP) : le ticagrelor (Brilique ®)
et le cangrelor. Ces molécules permettent l’inhibition de la voie impliquant
l’ADP à l’origine de l’activation de GPIIb-IIIa. Le clopidogrel est la molécule la plus anciennement utilisée. Il est prescrit en
phase aiguë d’un syndrome coronarien aigu (SCA), notamment après la réalisation
d’une angioplastie coronarienne pour prévenir la récidive d’évènement ischémique
et la thrombose de stent. Le clopidogrel est inactif in
vitro : il s’agit d’une prodrogue qui, pour être efficace, doit
être métabolisée dans le foie par différents cytochromes, notamment le
cytochrome hépatique P450. Le métabolite actif du clopidogrel se fixe sur les
récepteurs de l’ADP des plaquettes sanguines pour exercer son effet
antiagrégant. Le récepteur P2Y1 n’est, lui, pas inhibé par le clopidogrel et
conserve sa capacité à initier l’activation plaquettaire. Le clopidogrel est
prescrit en association avec l’aspirine pendant 3 mois en cas d’implantation de
stents nus, et pendant 6 mois à 1 an après implantation de
stents à élution (stents dits « actifs »).
Un des inconvénients du clopidogrel est la résistance de certains patients à ce
traitement. En effet, le clopidogrel est le substrat de la P-glycoprotéine
(P-gp) (transporteur d’efflux) qui est activé par de nombreuses isozymes du
CYP450 (1A2, 2B6, 2C9, 2C19, 3A4). Des polymorphismes de CYP450 ou de la P-gp
vont ainsi modifier les concentrations de clopidogrel et son efficacité
clinique. Tout comme le clopidogrel, le prasugrel est une prodrogue hydrolysée puis
métabolisée par le cytochrome P450 dans sa forme active. Son action sur le
récepteur P2Y12 est irréversible. Sa biotransformation ne nécessite qu’une seule
étape, en comparaison des deux étapes du clopidogrel, rendant son action
beaucoup plus rapide, (de l’ordre de 30 minutes), et permettant de limiter la
variabilité d’efficacité et les interactions médicamenteuses. Cette molécule est
beaucoup moins sensible aux variations d’activité du cytochrome que le
clopidogrel. Sa demi-vie est courte, entraînant, comme avec le clopidogrel, un
risque d’augmentation de réactivité plaquettaire et donc de résistance au
traitement. Cependant, il a été montré que le prasugrel avait une efficacité
plus importante et plus rapide, rendant son utilisation intéressante chez les
patients à haut risque dans un contexte de SCA [9]. Son utilisation en association avec
l’aspirine est indiquée en 1e ligne (par rapport à l’association
aspirine-clopidogrel) chez les patients atteints de SCA, en vue d’une
angioplastie coronaire. Le ticagrelor fait partie d’une nouvelle classe d’antiagrégants plaquettaires,
les cyclopentyl-triazolo-pyrimidines (CPTP) [10], des analogues de l’adénosine
tri-phosphate (ATP). Ce médicament, qui n’est pas une prodrogue, a la propriété
d’être un antagoniste direct des récepteurs P2Y12 de l’ADP, mais de façon
réversible du fait d’une demi-vie relativement courte (6 à 12 heures). Son
action est rapide, de l’ordre de 30 minutes. Le métabolisme du ticagrelor dépend
du CYP3A4/3A5 ; les polymorphismes de la p-gp ou du CYP2C19 n’affectant donc pas
sa biodisponibilité, contrairement aux inhibiteurs ou aux inducteurs du CYP3A4,
qui sont donc contre-indiqués. Le ticagrelor est responsable d’une inhibition
plaquettaire profonde, et expose de manière moins importante que le clopidogrel
et le prasugrel à une augmentation de réactivité plaquettaire. Comme pour le
prasugrel, il a été montré que le ticagrelor avait une efficacité supérieure au
clopidogrel au cours du traitement du SCA, indiquant ce traitement en première
ligne chez les patients atteints de SCA, en association avec l’aspirine [11]. Une des limitations à l’utilisation des antagonistes du récepteur P2Y12 est leur
délai d’action, de plusieurs heures, nécessitant la mise au point de nouvelles
molécules avec un délai d’action plus rapide, nécessaires dans un contexte
d’urgence, comme le SCA. Parmi ces molécules, le cangrelor, médicament de la
famille des CPTP, un analogue réversible de l’adénosine triphosphate (ATP), a
une action très rapide, de l’ordre de 1 à 3 minutes. Sa demi-vie est très
courte, de l’ordre de 5 minutes, permettant de minimiser le risque de saignement
et d’exercer un effet inhibiteur plaquettaire de l’ordre de 50 à 70 minutes
après arrêt du traitement [12]. Plusieurs essais cliniques randomisés ont montré une efficacité
supérieure du cangrelor par rapport au clopidogrel, concernant notamment
l’efficacité de revascularisation en cas de SCA, ou le risque de re-thrombose de
stent. À noter que le cangrelor peut bloquer de manière
compétitive l’accès du clopidogrel au récepteur P2Y12, diminuant l’efficacité
inhibitrice du clopidogrel. Une étude, parue en 2014, rapportait le développement d’un nouvel antagoniste du
récepteur P2Y12, le SAR216471, qui offrait l’avantage d’une administration à la
fois intra-veineuse et orale [13]. |
Les inhibiteurs de la glycoprotéine IIb/IIIa Le progrès le plus révolutionnaire de la thérapie antiplaquettaire au cours de ces
dernières années a été le développement des antagonistes des récepteurs GPIIb/IIIa
administrés par voie intraveineuse. Les anti-GPIIb/IIIa sont les seuls à mériter le
terme d’« antiagrégant », puisqu’ils inhibent l’interaction des résidus Arginine
(R), Glycine (G), Acide aspartique (D), en position γ400-411 du fibrinogène, avec
son récepteur plaquettaire, la glycoprotéine IIb/IIIa, exprimée sur les plaquettes
activées. L’agrégation est donc inhibée quel que soit l’activateur. Trois molécules sont actuellement disponibles : l’abciximab (Reopro®), le
tirofiban (Agrastat®) et l’eptifibatide (Integrilin®) [14]. L’abciximab est un
fragment chimérique Fab d’un anticorps monoclonal murin bloquant la GpIIb/IIIa de
manière non compétitive. La majorité des récepteurs (80 %) sont liés à l’anticorps
après deux heures, et l’agrégation plaquettaire est totalement inhibée ; la fonction
plaquettaire se rétablit partiellement après environ 48 heures. Le tirofiban est le
deuxième inhibiteur de la GpIIb/IIIa développé après l’abciximab. C’est un
inhibiteur non peptidique dérivé de la tyrosine, avec une action rapide et courte
due à sa demi-vie plasmatique d’environ 2 heures, contrairement à l’abciximab qui a
une plus longue durée de vie. Le tirofiban est un inhibiteur compétitif de la
GpIIb/IIIa avec une spécificité élevée mais une affinité relativement faible. Après
l’arrêt du traitement, le tirofiban est éliminé par voie rénale et la fonction
plaquettaire revient à la normale en 4 à 8 heures. L’eptifibatide a des propriétés
similaires au tirofiban [15]. Cette molécule, dérivée d’une protéine contenue dans le venin d’une
espèce de serpent Sistrurus miliarus barbouri, est un heptapeptide
cyclique composé de six acides aminés et d’un résidu de mercaptopropionyl [15]. Contrairement à l’abciximab,
l’eptifibatide se lie à la GpIIb/IIIa avec une grande spécificité et une faible
affinité. Étant donné la rapide dissociation de l’eptifibatide de son récepteur,
l’agrégation plaquettaire normale est restaurée environ 4 heures après l’arrêt de la
perfusion. L’eptifibatide et le tirofiban sont recommandés en cas d’ischémie
continue, de biomarqueurs cardiaques positifs ou quand le patient présente de grands
facteurs de risque [15]. |
Les molécules vasodilatatrices à action antiplaquettaire Les inhibiteurs de la phosphodiestérase Le dipyridamole (Persantine ®) appartient à la famille des inhibiteurs
de la phosphodiestérase (PDE), une enzyme impliquée dans la dégradation de
l’AMPc, ce qui a pour conséquence une augmentation de la concentration locale
d’adénosine, une stimulation de l’adénylate-cyclase et une augmentation de la
concentration intra-plaquettaire d’AMPc. Cette dernière empêche la mobilisation
du calcium libre qui est essentielle à l’activation plaquettaire. L’activité
antiplaquettaire du dipyridamole est cependant moindre que celle de l’aspirine
et des antagonistes des récepteurs de l’ADP. Son action sur la PDE, qui dure
environ 24 heures, est réversible. Une combinaison d’aspirine et de dipyridamole
est utilisée en pratique clinique en prévention secondaire lors de la survenue
d’AVC. Cette molécule peut être utilisée comme agent vasodilatateur coronarien
au cours de l’angine de poitrine. Le cilostazol (Pletal ®) fait
également partie de la famille des inhibiteurs de la PDE, inhibant la PDE-3,
avec une activité inhibitrice plaquettaire. Cette molécule est métabolisée par
le système des cytochromes microsomaux hépatiques P450 (CYP3A4, CYP2C9), et ses
métabolites sont excrétés par les urines. L’effet antiagrégant du cilostazol se
manifeste par une augmentation des concentrations de nucléotides cycliques
intra-plaquettaires, secondaire au blocage de l’externalisation de la
P-sélectine membranaire. Le cilostazol a démontré son efficacité après
angioplastie coronaire, en association à l’aspirine et au clopidogrel [ 16]. Les analogues de la prostacycline L’iloprost (Ilomedine ®) est un analogue de la prostacycline (ou
prostaglandine I2, PGI2) indiqué dans l’ischémie sévère des membres inférieurs.
Ses propriétés pharmacodynamiques incluent l’inhibition de l’agrégation
plaquettaire, de l’adhérence et de la sécrétion plaquettaires, la vasodilatation
et la diminution de la libération de radicaux libres d’oxygène [ 17]. Cette molécule a une demi-vie
très brève, d’environ 30 minutes, et est le plus souvent administrée par voie
intra-veineuse en continu. |
Les nouvelles voies de recherche L’inhibition des protease-activated receptors Au moins deux récepteurs de la thrombine (PAR1 et PAR4) sont exprimés à la
surface des plaquettes humaines. Si l’activation de PAR1 entraîne un signal
rapide et transitoire des cellules, celle de PAR4 est à l’origine d’une
activation prolongée, requise pour la stabilisation du thrombus [ 18]. PAR1 a l’affinité la
plus importante pour la thrombine. Il potentialise le clivage de PAR4 par la
thrombine via la mise en place d’hétérodimères PAR1-PAR4. Le
RWJ-58259 a été l’un des premiers antagonistes sélectifs du récepteur PAR-1 qui
a été développé, avec une action puissante et suffisante pour concurrencer le
mécanisme d’activation intramoléculaire du récepteur [ 19]. Malgré sa bonne efficacité, il n’a pas
progressé dans les essais cliniques en raison d’une biodisponibilité faible et
d’une demi-vie très courte : dans un essai réalisé à partir de microsomes
hépatiques, il a été rapporté avoir une demi-vie de 9,2 minutes chez l’homme, la
demi-vie chez la souris après administration étant de 19,2 minutes [ 20]. Une étude récente a
néanmoins identifié un métabolite actif de la molécule présentant une activité
significative in vivo alors que la majeure partie du RWJ-58259
a été consommée, ouvrant la voie à la synthèse d’analogues afin d’améliorer sa
stabilité [ 21]. Deux
autres antagonistes de PAR1 ont été développés : le vorapaxar (anciennement SCH
530348) et l’atopaxar. Le vorapaxar a une action compétitive avec le ligand de
PAR1, produit de la thrombine par protéolyse. Son administration, en association
avec un traitement par clopidogrel et aspirine, entraîne une réduction de la
mortalité cardiovasculaire, mais avec un risque d’hémorragie intracrânienne
majoré [ 23]. Son
indication est limitée, avec une possibilité de prescription chez les patients
présentant une athérosclérose (particulièrement les patients avec atteinte
artérielle périphérique) sans antécédents d’AVC. Plusieurs inconvénients sont
associés à cette molécule : son délai d’action important, sa demi-vie longue (5
à 11 heures), ainsi que sa réversibilité d’action également très longue, de
l’ordre de 4 à 8 semaines [ 24]. De fait, des recherches sur des molécules avec de meilleures
caractéristiques pharmacocinétiques ont été conduites. Un peptide inhibiteur de
PAR-1, qui se lie à l’extrêmité C-terminale intracellulaire de PAR1, le PZ-128,
a récemment été développé. PZ-128 inhibe l’agrégation plaquettaire et la
formation de thrombus [ 25] et, dans une étude de phase I, il entraîne une diminution de
l’activation plaquettaire [ 26]. Un inhibiteur de PAR4 est également en cours de développement,
le BMS-986120. Celui-ci a inhibé la formation de thrombose artérielle dans un
modèle de primate [ 27]
et, dans un essai de phase I, cette molécule a inhibé l’agrégation plaquettaire
et la thrombose ex vivo [ 28]. Sa sécurité d’administration est
actuellement en cours d’évaluation dans un essai de phase II chez des patients
nécessitant une coronaroplastie percutanée L’inhibition du complexe GpVI-RFCg Une des voies d’activation plaquettaire repose sur l’activation du complexe
GpVI-RFcγ via la liaison du collagène à ce complexe. Des
molécules inhibitrices de ce complexe ont donc été développées : anticorps
dirigés contre la GpVI, ou protéine de fusion dirigée contre le complexe soluble
GpVI-Fc (Revacept). Ces molécules diminuent la taille de l’infarctus dans un
modèle murin d’ischémie-reperfusion [ 29]. Des protéines à activité lectin-like,
modulant la GpVI, ont également été identifiées dans le venin du serpent
Tropidolaemus wagleri : un hexa- (Troα6) et un décapeptide
(Troα10), tous deux dérivés de la protéine Tro ( trowaglerix)
purifiée à partir du venin de ce serpent. Ces peptides inhibent l’agrégation
plaquettaire impliquant le collagène et la formation de thrombus chez la souris
[ 30]. Un anticorps
dirigé contre la GPVI, l’ACT017, a, enfin, montré des résultats prometteurs dans
un modèle de primate et, récemment chez l’homme, dans un essai de phase I [ 31]. La voie initiée par
la GPVI peut également être inhibée, en aval, et le rôle de Syk, activée en
amont du complexe GpVI-RFcγ, a notamment été étudié. À noter que des souris dont
le gène codant Syk a été invalidé sont protégées dans un modèle de thrombose
artérielle, sans déficit majeur d’hémostase. Des résultats similaires ont été
retrouvés, également chez la souris, avec l’utilisation d’un inhibiteur de Syk,
BI1002494 [ 32]. Inhibition du facteur calcium- and DAG-regulated guanine nucleotide exchange
Factor-1 CalDAG-GEFI ( calcium- and DAG-regulated guanine nucleotide exchange
Factor-1) est un activateur des GTPases de la sous-famille Rap1
( Ras-related protein 1) qui stimule l’adhérence des
plaquettes, notamment via l’activation de la GpIIb/IIIa.
L’activation de Rap1 est également requise pour d’autres processus
plaquettaires : la sécrétion granulaire, la génération de TXA2 ou la rétraction
du caillot [ 5]. L’activation de Rap1 par
CalDAG-GEFI est un processus important parmi les mécanismes d’activation
plaquettaire, en aval de nombreuses voies de signalisation, notamment des
récepteurs PAR, P2Y12 et GpVI. Des données montrent que des souris transgéniques
exprimant un niveau réduit de CalDAG-GEFI présentent une réponse plaquettaire
réduite en présence de plusieurs agonistes [ 33], et sont protégées vis-à-vis du risque
thrombotique. Cette voie d’inhibition semble donc prometteuse dans le
développement de molécules antiplaquettaires. Régulation du métabolisme oxydatif plaquettaire Les lipooxygénases (LOX) sont des enzymes qui catalysent l’oxydation des acides
gras insaturés les transformant en molécules importantes dans différentes voies
de signalisation. La 12-LOX (qui oxyde l’acide arachidonique au niveau du
carbone situé en position 12) est présente dans les mégacaryocytes et les
plaquettes humaines. Cette oxydation génère l’acide
12(S)-hydroperoxyicosa-5,8,10,14 tétraénoique (12(S)HETrE) qui est ensuite
réduit en acide 12(S)-hyroxy-5,8,10,14 eicosatétraénoique (12(S)HETE).
L’inhibition de la 12-LOX a pour conséquence une diminution de l’agrégation
plaquettaire en réponse à des agonistes de PAR1, PAR4, GPVI ou RFcγIIa et le
MLL-355, inhibiteur de la 12-LOX, réduit l’activation plaquettaire et la
survenue de thrombose artérielle chez la souris [ 34]. NOX2 ( nicotinamide adenine
dinucleotide phosphate oxydase 2) est une enzyme qui catalyse la
génération de l’ion superoxyde à partir du NADPH. C’est l’enzyme principale de
génération de superoxyde dans les plaquettes humaines. Les dérivés réactifs de
l’oxygène (ROS) produits à partir du superoxyde augmentent la réactivité
plaquettaire. Les plaquettes de souris déficientes en NOX2 présentent un défaut
de réponse à une stimulation par le collagène, une diminution de la production
de ROS et une diminution de la phosphorylation de PLCγ2 et de Syk. Ces souris
ont, de plus, une propension diminuée à la thrombose. L’activité de NOX2 est
régulée par une PI3K de classe III, la VPS34 ( vacuolar protein sorting
34) [ 35]
et il a été montré que les plaquettes déficientes en VPS34 avaient une capacité
réduite de génération du complexe NOX2 et donc une capacité réduite de
production de ROS, menant à une hypoagrégabilité plaquettaire et une diminution
de la survenue de thrombus [ 35]. L’inhibition du récepteur P2Y1 Outre le récepteur P2Y12, les plaquettes expriment également le récepteur P2Y1
impliqué dans la régulation calcique et les modifications conformationnelles.
Une molécule inhibitrice des récepteurs P2Y12 et P2Y1 a été développée
récemment : le GLS-409. Dans un modèle canin, le GLS-409 inhibe l’agrégation
plaquettaire et la survenue de thrombose [ 36], sans saignement majeur constaté. Une
molécule inhibant uniquement le récepteur P2Y1 (MRS2179) est également en cours
de développement. L’inhibition des kinases plaquettaires L’activation de différentes voies de signalisation plaquettaire conduit à la
génération de phosphatidylinositol-3-phosphate (PI3P) via
l’action de PI3K. La PDK1 ( phosphoinositide-dependent kinase 1)
est activée à la suite de sa liaison à la PI3P et la phosphorylation de
protéines appartenant la famille Akt. Or, un déficit plaquettaire en PDK1
entraîne une diminution de l’activation plaquettaire, en raison de la diminution
de signal « outside-in » initié par GpIIb/IIIa. Chez l’homme,
un inhibiteur de PDK1 inhibe l’activation plaquettaire [ 37] et des souris déficientes en PDK1
plaquettaire présentent une diminution de la formation de thrombus artériels
[ 38]. L’inhibition de la liaison du facteur von Willebrand au complexe
GPIb/IX/V La liaison du facteur von Willebrand (FvW) à la GPIbα plaquettaire est une autre
voie qui suscite l’intérêt de plusieurs équipes de chercheurs. Le FvW joue un
rôle important dans l’hémostase en participant à l’adhérence, à l’activation et
à l’agrégation plaquettaire. Un antagoniste de cette voie a été développé, le
GPG-290. Il s’agit d’une protéine recombinante formée des 290 acides aminés de
la partie N-terminale de la GPIbα fusionnés à la région Fc d’une immunoglobuline
(Ig) G1 humaine mutée. Le blocage de l’interaction entre la GPIbα et le FvW par
le GPG-290 représente une stratégie efficace pour prévenir la formation du
thrombus occlusif sans pour autant induire une augmentation du temps de
saignement [ 39].
L’étude des effets de cette inhibition a également été réalisée en utilisant
l’ARC-1779 , un aptamère capable de se lier au domaine A1 du
facteur vWF et d’inhiber sa liaison à la GpIB. Il a été notamment montré, au
cours de la maladie de Willebrand de type 2B, que l’administration d’ARC-1779
entraînait une correction de la thrombopénie et une augmentation des niveaux du
FvW [ 40]. L’inhibition de la P-sélectine La liaison entre la P-sélectine et son ligand, P-Selectine glycoprotein
ligand-1 (PSGL-1), favorise l’interaction entre plaquettes et
leucocytes au cours de la formation du thrombus et permet de stabiliser
l’interaction entre la GPIIb/IIIa et le fibrinogène, renforçant ainsi
l’agrégation plaquettaire. Le rPSGL-Ig ( recombinant p-selectin
glycoprotein ligand-immunoglobulin), antagoniste de la P-sélectine,
a été étudié : cette molécule diminue l’agrégation plaquettaire reposant sur la
thrombine, et diminue l’afflux calcique intra-plaquettaire impliquant le
récepteur RFcγIIA [ 41]. |
Dans le but de réduire la mortalité associée aux maladies cardiovasculaires,
plusieurs agents antiplaquettaires, avec des propriétés différentes, ont été
développés au cours de ces dernières années. Une molécule peut être efficace dans le
traitement d’un ECV, sans l’être au cours d’un autre évènement, rendant difficile la
mise au point d’une molécule ayant une efficacité globale dans la prise en charge de
toutes les MCV. La résistance possible à certains agents antiplaquettaires et les
complications hémorragiques variables, selon chaque molécule, constituent une
difficulté importante pour les chercheurs. Il apparaît donc nécessaire de mettre au
point de nouvelles stratégies de traitement fondées sur une compréhension plus fine
des voies de signalisation impliquées dans l’activation plaquettaire. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données
publiées dans cet article.
|
|
5HT/2A
|
5-hydroxytyptamine 2A receptors
|
|
12-LOX
|
12-lypoxygénase |
|
12-HETE
|
acide 12(S)-hyroxy-5,8,10,14 eicosatétraénoïque |
|
12-HETrE
|
acide 12(S)-hydroperoxyicosa-5,8,10,14 tétraénoïque |
|
AA
|
acide arachidonique |
|
AAS
|
acide acétylsalicylique |
|
ADP
|
adénosine diphosphate |
|
Akt
|
protéine kinase B |
|
AMPc
|
adénosine monophosphate cyclique |
|
CalDAG-GEFI
|
calcium DAG-regulated guanine nucleotide exchange factor
I
|
|
CaM
|
calmoduline |
|
DAG
|
diacylglycérol |
|
COX
|
cyclooxygénase |
|
ERK
|
extracellular signal-regulated kinase
|
|
GP
|
glycoprotéine |
|
GDP
|
guanosine diphosphate |
|
GTP
|
guanosine triphosphate |
|
GPCR
|
G-protein coupled receptors
|
|
GSK3
|
glycogen synthase kinase 3
|
|
IP3
|
inositol trisphosphate |
|
ITAM
|
immune receptor tyrosine-based activation motif
|
|
MAPK
|
mitogen-activated protein kinase
|
|
MLCK
|
myosin light-chain kinase
|
|
NOX
|
nicotinamide adénine dinucléotide phosphate |
|
P2Y12 et P2Y1
|
récepteurs de l’ADP |
|
PAR
|
protease-activated receptor
|
|
PDK1
|
phosphoinositide-dependent protein kinase 1
|
|
PIP3
|
phosphatidylinositol 3,4,5 trisphosphate |
|
PIP2
|
phosphatidylinositol 4,5 diphosphate |
|
PI3K
|
phosphoinositide 3 kinase |
|
PLC
|
phospholipase C |
|
PKC
|
protéine kinase C |
|
Rap1
|
Ras-related protein 1
|
|
RFcγ
|
chaîne g des récepteurs pour la région Fc des IgG |
|
ROS
|
reactive oxygen species
|
|
SFK
|
Src family protein kinases
|
|
TNF
|
tumor necrosis factor
|
|
TRAF-4
|
TNF receptor-associated factor 4
|
|
TXA2
|
thromboxane A2 |
|
TP
|
récepteur du TXA2 |
|
VASP
|
vasodilator stimulated phosphoprotein
|
|
VSP34
|
vacuolar sorting protein 34
|
|
FvW
|
facteur von Willebrand |
|
1.
Maurer
E
,
Tang
C
,
Schaff
M
et al.
Targeting platelet GPIbβ reduces platelet adhesion, GPIb
signaling and thrombin generation and prevents arterial
thrombosis . Arterioscler Thromb Vasc Biol.
2013; ; 33 :
:1221.–1229. 2.
Manne
BK
,
Badolia
R
,
Dangelmaier
C
et al.
Distinct pathways regulate Syk protein activation downstream of
immune tyrosine activation motif (ITAM) and hemITAM receptors in
platelets . J Biol Chem.
2015; ; 290 :
:11557.–11568. 3.
Onselaer
MB
,
Hardy
AT
,
Wilson
C
et al.
Fibrin and D-dimer bind to monomeric GPVI .
Blood Adv.
2017; ; 1 :
:1495.–1504. 4.
Badimon
L
,
Padró
T
,
Vilahur
G
. Atherosclerosis, platelets and thrombosis in
acute ischaemic heart disease . Eur Heart J Acute
Cardiovasc Care.
2012; ; 1 :
:60.–74. 5.
Stefanini
L
,
Bergmeier
W
. RAP1-GTPase signaling and platelet
function . J Mol Med.
2016; ; 94 :
:13.–19. 6.
Flevaris
P
,
Li
Z
,
Zhang
G
et al.
Two distinct roles of mitogen-activated protein kinases in
platelets and a novel Rac1-MAPK-dependent integrin outside-in retractile
signaling pathway . Blood.
2009; ; 113 :
:893.–901. 7.
Valet
C
,
Severin
S
,
Chicanne
G
et al.
The role of class I, II and III PI 3-kinases in platelet
production and activation and their implication in
thrombosis . Adv Biol Regul.
2016; ; 61 :
:33.–41. 8.
Ricciotti
E
,
FitzGerald
GA
. Prostaglandins and inflammation .
Arterioscler Thromb Vasc Biol.
2011; ; 31 :
:986.–1000. 9.
Verdoia
M
,
Schaffer
A
,
Barbieri
L
et al.
Benefits from nnew ADP antagonists as compared with clopidogrel
in patients with stable angina or acute coronary syndrome undergoing
invasive management: a meta-analysis of randomized trials .
J Cardiovasc Pharmaco.
2014; ; 63 :
:339.–350. 10.
Teng
R
,
Butler
K
. Pharmacokinetics, pharmacodynamics, tolerability
and safety of single ascending doses of ticagrelor, a reversibly binding
oral P2Y12 receptor antagonist, in healthy subjects .
Eur J Clin Pharmacol.
2010; ; 66 :
:487.–496. 11.
Roffi
M
,
Patrono
C
,
Collet
JP
et al.
2015 ESC Guidelines for the management of acute coronary
syndromes in patients presenting without persistent ST-segment elevation:
task force for the management of acute coronary syndromes in patients
presenting without persistent ST-segment elevation of the European society
of cardiology (ESC) . Eur Heart J.
2016; ; 37 :
:267.–315. 12.
Angiolillo
DJ
. ADP receptor antagonism: what’s in the
pipeline? . Am J Cardiovasc Drugs Drugs Devices
Interv.
2007; ; 7 :
:423.–432. 13.
Boldron
C
,
Besse
A
,
Bordes
MF
et al.
N-[6-(4-butanoyl-5-methyl-1H-pyrazol-1-yl)pyridazin-3-yl]-5-chloro-1-[2-(4-methylpiperazin-1-yl)-2-oxoethyl]-1H-indole-3-carboxamide
(SAR216471), a novel intravenous and oral, reversible, and directly acting
P2Y12 antagonist . J Med Chem.
2014; ; 57 :
:7293.–7316. 14.
Coller
BS
. αIIbβ3: structure and function .
J Thromb Haemost.
2015; ; 13 : (suppl 1)
:S17.–S25. 15.
Shah
I
,
Khan
SO
,
Malhotra
S
et al.
Eptifibatide: the evidence for its role in the management of
acute coronary syndromes . Core Evid.
2009; ; 4 :
:49.–65. 16.
Jeong
YH
,
Tantry
US
,
Park
Y
et al.
Pharmacodynamic effect of cilostazol plus standard clopidogrel
versus double-dose clopidogrel in patients with type 2 diabetes undergoing
percutaneous coronary intervention . Diabetes
Care.
2012; ; 35 :
:2194.–2197. 17.
Ozat
M
,
Gungor
T
,
Barun
S
et al.
The effects of iloprost, a prostacyclin analogue, in experimental
ischaemia/reperfusion injury in rat ovaries . Exp
Toxicol Pathol.
2009; ; 61 :
:519.–527. 18.
Han
X
,
Nieman
MT
. PAR4 (protease-activated receptor 4):
particularly important 4 antiplatelet therapy .
Arterioscler Thromb Vasc Biol.
2018; ; 38 :
:287.–289. 19.
Zhang
HC
,
Derian
CK
,
Andrade-Gordon
P
et al.
Discovery and optimization of a novel series of thrombin receptor
(par-1) antagonists: potent, selective peptide mimetics based on indole and
indazole templates . J Med Chem.
2001; ; 44 :
:1021.–1024. 20.
Damiano
BP
,
Derian
CK
,
Maryanoff
BE
et al.
RWJ-58259: a selective antagonist of protease activated
receptor-1 . Cardiovasc Drug Rev.
2003; ; 21 :
:313.–326. 21.
Robinson
E
,
Knight
E
,
Smoktunowicz
N
et al.
Identification of an active metabolite of PAR-1 antagonist
RWJ-58259 and synthesis of analogues to enhance its metabolic
stability . Org Biomol Chem.
2016; ; 14 :
:3198.–3201. 22.
Morrow
DA
,
Braunwald
E
,
Bonaca
MP
et al.
Vorapaxar in the secondary prevention of atherothrombotic
events . N Engl J Med.
2012; ; 366 :
:1404.–1413. 23.
Tricoci
P
,
Huang
Z
,
Held
C
et al.
Thrombin-receptor antagonist vorapaxar in acute coronary
syndromes . N Engl J Med.
2012; ; 366 :
:20.–33. 24.
Kosoglou
T
,
Reyderman
L
,
Tiessen
RG
et al.
Pharmacodynamics and pharmacokinetics of the novel PAR-1
antagonist vorapaxar (formerly SCH 530348) in healthy
subjects . Eur J Clin Pharmacol.
2012; ; 68 :
:249.–258. 25.
Zhang
P
,
Gruber
A
,
Kasuda
S
et al.
Suppression of arterial thrombosis without affecting hemostatic
parameters with a cell-penetrating PAR1 pepducin .
Circulation.
2012; ; 126 :
:83.–91. 26.
Gurbel
PA
,
Bliden
KP
,
Turner
SE
et al.
Cell-penetrating pepducin therapy targeting PAR1 in subjects with
coronary artery disease . Arterioscler Thromb Vasc
Biol.
2016; ; 36 :
:189.–197. 27.
Wong
PC,
Seiffert
D,
Bird
JE, et al.
Blockade of protease-activated receptor-4 (PAR4) provides robust
antithrombotic activity with low bleeding . Sci
Transl Med.
2017;; 9 : :eaaf5294..
28.
Wilson
SJ
,
Ismat
FA
,
Wang
Z
et al.
PAR4 (protease-activated receptor 4) antagonism with BMS-986120
inhibits human ex vivo thrombus formation .
Arterioscler Thromb Vasc Biol.
2018; ; 38 :
:448.–456. 29.
Pachel
C
,
Mathes
D
,
Arias-Loza
AP
et al.
Inhibition of platelet GPVI protects against myocardial
ischemia-reperfusion injury . Arterioscler Thromb
Vasc Biol.
2016; ; 36 :
:629.–635. 30.
Chang
CH
,
Chung
CH
,
Tu
YS
et al.
Trowaglerix venom polypeptides as a novel antithrombotic agent by
targeting immunoglobulin-like domains of glycoprotein VI in
platelet . Arterioscler Thromb Vasc Biol.
2017; ; 37 :
:1307.–1314. 31.
Voors-Pette
C
,
Lebozec
K
,
Dogterom
P
et al.
Safety and tolerability, pharmacokinetics, and pharmacodynamics
of ACT017, an antiplatelet GPVI (glycoprotein VI) Fab: first-in-human
healthy volunteer trial . Arterioscler Thromb Vasc
Biol.
2019; ; 39 :
:956.–964. 32.
van Eeuwijk
JMM
,
Stegner
D
,
Lamb
DJ
et al.
The novel oral Syk inhibitor, Bl1002494, protects mice from
arterial thrombosis and thromboinflammatory brain
infarction . Arterioscler Thromb Vasc Biol.
2016; ; 36 :
:1247.–1253. 33.
Piatt
R
,
Paul
DS
,
Lee
RH
et al.
Mice Expressing low levels of CalDAG-GEFI exhibit markedly
impaired platelet activation with minor impact on
hemostasis . Arterioscler Thromb Vasc Biol.
2016; ; 36 :
:1838.–1846. 34.
Adili
R
,
Tourdot
BE
,
Mast
K
et al.
First selective 12-LOX inhibitor, ML355, impairs thrombus
formation and vessel occlusion in vivo with minimal effects on
hemostasis . Arterioscler Thromb Vasc Biol.
2017; ; 37 :
:1828.–1839. 35.
Liu
Y
,
Hu
M
,
Luo
D
et al.
Class III PI3K positively regulates platelet activation and
thrombosis via PI(3)P-directed function of NADPH oxidase .
Arterioscler Thromb Vasc Biol.
2017; ; 37 :
:2075.–2086. 36.
Gremmel
T
,
Yanachkov
IB
,
Yanachkova
MI
et al.
Synergistic inhibition of both P2Y1 and
P2Y12 adenosine diphosphate receptors as novel approach to
rapidly attenuate platelet-mediated thrombosis .
Arterioscler Thromb Vasc Biol.
2016; ; 36 :
:501.–509. 37.
Dangelmaier
C
,
Manne
BK
,
Liverani
E
et al.
PDK1 selectively phosphorylates Thr(308) on Akt and contributes
to human platelet functional responses . Thromb
Haemost.
2014; ; 111 :
:508.–517. 38.
Münzer
P
,
Walker-Allgaier
B
,
Geue
S
et al.
PDK1 determines collagen-dependent platelet Ca2+
signaling and is critical to development of ischemic stroke in
vivo . Arterioscle Thromb Vasc Biol.
2016; ; 36 :
:1507.–1516. 39.
Wadanoli
M
,
Sako
D
,
Shaw
GD
et al.
The von Willebrand factor antagonist (GPG-290) prevents coronary
thrombosis without prolongation of bleeding time .
Thromb Haemost.
2007; ; 98 :
:397.–405. 40.
Jilma-Stohlawetz
P
,
Knöbl
P
,
Gilbert
JC
et al.
The anti-von Willebrand factor aptamer ARC1779 increases von
Willebrand factor levels and platelet counts in patients with type 2B von
Willebrand disease . Thromb Haemost.
2012; ; 108 :
:284.–290. 41.
Sathish
J
,
Falati
S
,
Croce
K
et al.
Antibody cross-linking of human platelet P-selectin induces
calcium entry by a mechanism dependent upon Fcγ receptor
IIA . Thromb Haemost.
2004; ; 92 :
:598.–605. 42.
Tanasescu
S
,
Lkvesque
H
,
Thuillez’
C
. Pharmacology of aspirine .
Rev Med Interne.
2000; ; 21 : (suppl 1)
:s18.–s26. 43.
Bennett
CL
,
Connors
JM
,
Carwile
JM
et al.
Thrombotic thrombocytopenic purpura associated with
clopidogrel . N Engl J Med.
2000; ; 342 :
:1773.–1777. 44.
Schnapf
A.
. Prasugrel versus clopidogrel: new management
strategies for acute coronary syndrome . J Cardiovasc
Nurs.
2013; ; 28 :
:483.–494. 45.
Wallentin
L
,
Becker
RC
,
Budaj
A
et al.
Ticagrelor versus clopidogrel in patients with acute coronary
syndromes . N Engl J Med.
2009; ; 361 :
:1045.–1057. 46.
Cada
DJ
,
Baker
DE
,
Ingram
KT
. Cangrelor . Hosp
Pharm.
2015; ; 50 :
:922.–929. 47.
Kim
HH
,
Sawada
N
,
Soydan
G
et al.
Additive effects of statin and dipyridamole on cerebral blood
flow and stroke protection . J Cereb Blood Flow
Metab.
2008; ; 28 :
:1285.–1293. 48.
DiNicolantonio
JJ
,
Lavie
CJ
,
Fares
H
et al.
Meta-analysis of cilostazol versus aspirin for the secondary
prevention of stroke . Am J Cardiol.
2013; ; 112 :
:1230.–1234. 49.
Gessler
T
,
Ghofrani
HA
,
Held
M
et al.
The safety and pharmacokinetics of rapid iloprost aerosol
delivery via the BREELIB nebulizer in pulmonary arterial
hypertension . Pulm Circ.
2017; ; 7 :
:505.–513. 50.
De Luca
G
,
Navarese
E
,
Marino
P
. Risk profile and benefits from Gp IIb-IIIa
inhibitors among patients with ST-segment elevation myocardial infarction
treated with primary angioplasty: a meta-regression analysis of randomized
trials . Eur Heart J.
2009; ; 30 :
:2705.–2713. |