| |
| Med Sci (Paris). 35(2): 97–99. doi: 10.1051/medsci/2019017.Le récepteur P2X7, une nouvelle cible thérapeutique
dans la maladie d’Alzheimer Elodie Martin,1 Jean Kanellopoulos,2 Bertrand Fontaine,3 Benoît Delatour,1 and Cécile Delarasse4* 1Sorbonne Université, Inserm, CNRS, Institut du cerveau et la
moelle épinière, 105,
boulevard de l’Hôpital, 75013Paris,
France 2Université Paris-Saclay, CNRS, I2BC,
rue du Doyen Georges
Poitou, 91400Orsay,
France 3Sorbonne Université, AP-HP, Hôpital Pitié-Salpêtrière,
Inserm, CNRS, Institut de myologie, 105, boulevard de l’Hôpital,
75013Paris,
France 4Sorbonne Université, Inserm, CNRS, Institut de la
Vision, 17, rue
Moreau, 75012Paris,
France MeSH keywords: Maladie d'Alzheimer, Animaux, Modèles animaux de maladie humaine, Humains, Souris, Souris transgéniques, Thérapie moléculaire ciblée, Récepteurs purinergiques P2X7, Traitements en cours d'évaluation, génétique, thérapie, méthodes, tendances, physiologie |
La maladie d’Alzheimer (MA) est une pathologie neurodégénérative liée à l’âge qui se
caractérise par des pertes des fonctions cognitives avec au premier plan une
atteinte mnésique. Actuellement, il n’y a aucun traitement qui retarde ou arrête la
progression de la maladie. La plupart des approches thérapeutiques pour traiter la
MA ciblent les mécanismes conduisant à la formation des deux lésions
caractéristiques de la pathologie : les plaques séniles composées d’agrégats
extracellulaires de peptides amyloïdes β (Aβ) et les dégénérescences
neurofibrillaires constituées d’agrégats intracellulaires de protéines Tau
hyperphosphorylées. Plusieurs études ont révélé que des processus inflammatoires et immunologiques
participaient à la progression de la MA et des études génétiques ont identifié
plusieurs gènes de susceptibilité à la maladie impliqués dans la réponse immunitaire
innée associée [1]. Au cours
de la progression de la maladie, les cellules gliales (astrocytes1, et cellules microgliales2) sont activées autour des lésions composées de peptides Aβ, et
produisent des quantités excessives de cytokines pro-inflammatoires [2, 3]. Les cellules gliales activées et les
neurones endommagés peuvent également libérer de l’ATP en réponse à des particules
extracellulaires, comme les peptides Aβ. Des taux élevés d’ATP extracellulaire
agissent comme un signal de danger qui active les récepteurs purinergiques. Ces
récepteurs ont diverses propriétés dans le système nerveux central (SNC) : ils
contribuent non seulement au fonctionnement des neurones mais également aux lésions
neuronales en fonction de l’environnement physiologique ou pathologique. |
Le récepteur purinergique P2X7 Parmi les récepteurs purinergiques, le récepteur P2X7 (P2X7R) pourrait être impliqué
dans le développement et la progression de la MA. Son expression est augmentée dans
les cellules gliales qui entourent les plaques d’Aβ dans des modèles animaux et chez
les patients atteints de MA. P2X7R est à l’origine de l’activation de l’inflammasome
NLRP3 (NOD-like receptor family, pyrin domain containing 3) qui
conduit, notamment, à la libération de la cytokine pro-inflammatoire interleukine-1β
(IL-1β) [4]. Des expériences
réalisées in vitro et in vivo ont montré que
l’activation de NLRP3 contribuait à la réponse inflammatoire pathogène au cours de
la MA [1]. P2X7R peut cependant présenter des
effets neuroprotecteurs. Nous avons en effet montré qu’une stimulation brève du
récepteur activait la coupure protéolytique non-amyloïdogénique de la protéine
précurseur du peptide amyloïde (APP) [5, 6] :
une α-sécrétase coupe l’APP au sein de la séquence peptidique Aβ, ce qui empêche la
formation de peptides Aβ neurotoxiques et produit un fragment soluble, le sAPPα, qui
est neurotrophique et neuroprotecteur. P2X7R joue également un rôle dans la
phagocytose des peptides Aβ. Il contribuerait ainsi à la clairance de ces peptides.
Ces fonctions multiples de P2X7R nous ont conduits à émettre l’hypothèse que sa
stimulation pourrait avoir un effet double dans la MA : activer la voie
non-amyloïdogénique neuroprotectrice et/ou entraîner une suractivation des cellules
gliales, à l’origine d’une réponse pro-inflammatoire excessive. |
Effet/impact de l’invalidation de P2X7R sur le développement de la MA Nous avons tout d’abord mis en évidence que, dans le cerveau de patients atteints de
MA et dans un modèle murin développant des lésions amyloïdes (les souris
transgéniques TgAPP/PS13), les cellules qui
expriment fortement P2X7R étaient principalement les astrocytes et les cellules
microgliales. Afin de déterminer le rôle de P2X7R dans la MA, nous avons donc évalué
l’effet de l’invalidation génétique de P2X7R chez ces souris TgAPP/PS1 [7]. Nous avons montré dans ce
modèle que la déficience en P2X7R diminuait la pathologie amyloïde, améliorait la
plasticité synaptique au niveau de l’hippocampe et normalisait les déficits de
mémoire. Ces effets ne sont cependant pas transduits via la
modulation de la coupure de l’APP, l’activation des astrocytes et des cellules
microgliales, les processus de phagocytose ou encore la libération d’IL-1β, comme
cela avait été décrit in vitro et dans d’autres modèles
pathologiques. Nos travaux mettent donc en évidence un autre mécanisme : le déficit
en P2X7R affecte en effet principalement la libération des chimiokines
pro-inflammatoires CCL(C-C motif chemokine ligand) 3, 4 et 5,
surexprimées dans le modèle murin TgAPP/PS1 [2], qui sont impliquées dans le recrutement de cellules immunitaires dans le
SNC. En utilisant des cellules microgliales et des astrocytes de souris déficientes
pour P2X7R, nous avons montré le rôle spécifique du récepteur dans la production de
CCL3 en réponse aux peptides Aβ. Nous avons également montré que l’absence de P2X7R
réduisait le recrutement des lymphocytes T cytotoxiques CD8+, cette
réduction étant corrélée à la diminution du taux de CCL3 produit. Nos travaux ont ainsi mis en évidence l’implication particulière de P2X7R dans les
processus neurodégénératifs via la production de chimiokines et le
recrutement de lymphocytes T pathogéniques, à l’origine d’une altération des
fonctions neuronales. |
Les résultats que nous avons obtenus nous conduisent à proposer un nouveau modèle
permettant d’expliquer les effets délétères de l’inflammation au cours de la MA.
Dans ce modèle, les niveaux chroniquement élevés de peptide Aβ induiraient la
libération d’ATP par les cellules gliales, qui serait ensuite amplifiée par les
astrocytes via les récepteurs purinergiques. P2X7R détecterait
l’ATP ainsi produit, entraînant la libération de chimiokines à l’origine d’une
cascade de processus pathologiques (Figure
1).
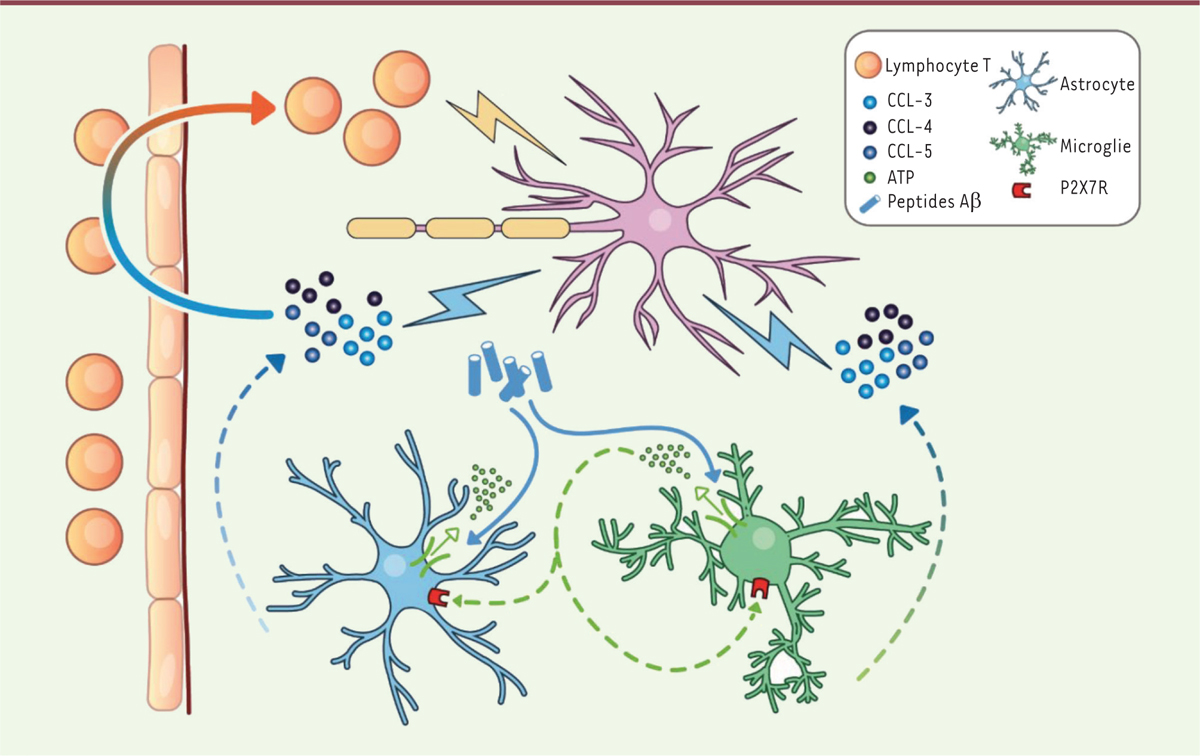
 | Figure 1. Rôle du récepteur purinergique P2X7R dans la pathologie
amyloïde Aß. 1. Les peptides amyloïdes β (Aβ)
induisent la libération d’ATP par les cellules gliales.
2. Les astrocytes et la microglie
activés peuvent à leur tour libérer de l’ATP via
l’activation de récepteurs purinergiques.
3. L’augmentation des niveaux d’ATP
active P2X7R, entraînant la libération des chimiokines CCL(C-C
motif chemokine ligand) 3, 4 et 5 par la microglie et les
astrocytes. 4. La production de ces
chimiokines pourrait entraîner directement une altération des fonctions
neuronales et endommager les neurites, et
(5) conduirait au recrutement de
lymphocytes T dans le système nerveux central, en particulier les
lymphocytes T CD8+, qui (6)
contribueraient également à la toxicité neuronale. |
La production de chimiokines dépendantes de P2X7R pourrait en effet altérer
directement les fonctions cognitives. L’expression de CCL3 et de son récepteur CCR5
sont augmentées dans le cerveau des patients atteints de MA et chez les souris
modèle de MA [3]. Chez ces souris, la
surexpression de CCR5 entraîne des déficits cognitifs. Inversement, son inhibition
dans l’hippocampe améliore la mémoire. Le traitement de tranches d’hippocampe par
CCL3 et son injection intra-cérébroventriculaire chez des souris altèrent la
plasticité synaptique à long terme et les capacités de mémoire spatiale ; ces effets
délétères étant bloqués par un antagoniste du récepteur de la chimiokine, CCR5
[8]. De même, chez les
souris déficientes en CCL3 ou CCR5, l’injection intracérébrale de peptides Aβ
entraîne des déficits cognitifs et un dysfonctionnement synaptique qui sont réduits
par rapport à des souris sauvages. Ainsi, la libération de CCL3 dépendante de P2X7R
pourrait directement entraîner des altérations synaptiques et des atteintes de
mémoire. Les chimiokines pourraient également contribuer aux processus pathologiques dans la
MA par le biais d’interactions entre neurones et lymphocytes T. Nous avons montré
que le nombre de lymphocytes T CD8+ était diminué dans le cerveau des
souris TgAPP/PS1 déficientes pour P2X7R, ce qui est corrélé à une diminution des
taux de CCL3 produits. Ces résultats sont en accord avec des travaux qui suggèrent
que CCL3 est impliquée dans l’infiltration de lymphocytes T dans le cerveau des
patients atteints de MA [9].
Le recrutement des lymphocytes T CD8+ dans le SNC peut entraîner des
dommages neuronaux. Dans des souris modèle de tauopathie, on observe ainsi une
infiltration anormale de lymphocyte T CD8+, et la déplétion de ces
lymphocytes améliore les atteintes cognitives [10, 11] (→).
(→) Voir la Synthèse de C. Laurent et al.,
m/s n° 10, octobre 2017, page 817
Le recrutement des lymphocytes T est également associé à la production de CCL3. Ces
données suggèrent donc que l’inhibition de P2X7R pourrait avoir un impact bénéfique
sur la pathologie Tau. Des études complémentaires d’inhibition du récepteur de la chimiokine, CCR5, sont
cependant nécessaires pour distinguer les deux mécanismes potentiellement impliqués
ou montrer qu’ils agissent en synergie, menant à la progression de la MA. |
Notre analyse détaillée des fonctions du P2X7R dans un modèle murin de MA a révélé un
rôle inattendu de ce récepteur dans cette maladie neurodégénérative. Elle a mis en
évidence un nouveau mécanisme pathologique impliquant la libération de chimiokines.
Nous avons montré que l’absence de P2X7R réduit non seulement les lésions Aβ, mais
également les déficits cognitifs associés. Ces dernières années, plusieurs
antagonistes de P2X7R ont été développés [4].
Nos résultats suggèrent que des traitements pharmacologiques ciblant spécifiquement
P2X7R pourraient constituer une nouvelle voie de recherche pour le traitement de la
MA. |
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les
données publiées dans cet article.
|
Notre laboratoire est financé par l’agence nationale pour la recherche
(ANR-12-MALZ-0003-02-P2X7RAD) and Bpifrance. Nous sommes également financés par
l’Inserm, le CNRS, l’université Sorbonne Université et le programme
d’investissements d’avenir (programme ANR-10-IAIHU-06 [IHU-A-ICM]).
|
Footnotes |
1. Heneka
MT,
Carson
MJ, El
Khoury
J, et al.
Neuroinflammation in Alzheimer’s disease .
Lancet Neurol.
2015; ; 14 :
:388.–405. 2. Martin
E,
Boucher
C,
Fontaine
B,
Delarasse
C. Distinct
inflammatory phenotypes of microglia and monocyte-derived macrophages in
Alzheimer’s disease models: effects of aging and amyloid
pathology . Aging Cell.
2017; ; 16 :
:27.–38. 3. Martin
E,
Delarasse
C. Complex role of
chemokine mediators in animal models of Alzheimer’s disease .
Biomed J.
2018; ; 41 :
:34.–40. 4. Di
Virgilio
F, Dal
Ben
D,
Sarti
AC, et al.
The P2X7 Receptor in Infection and Inflammation .
Immunity.
2017; ; 47 :
:15.–31. 5. Delarasse
C,
Auger
R,
Gonnord
P, et al.
The purinergic receptor P2X7 triggers alpha-secretase-dependent
processing of the amyloid precursor protein . J Biol
Chem.
2011; ; 286 :
:2596.–2606. 6. Darmellah
A,
Rayah
A,
Auger
R, et al.
Ezrin/radixin/moesin are required for the purinergic P2X7
receptor (P2X7R)-dependent processing of the amyloid precursor
protein . J Biol Chem.
2012; ; 287 :
:34583.–34595. 7. Martin
E,
Amar
M,
Dalle
C, et al.
New role of P2X7 receptor in an Alzheimer’s disease mouse
model . Mol Psychiatry. 2018 June 22. doi:
10.1038/s41380-018-0108-38. Marciniak
E,
Faivre
E,
Dutar
P, et al.
The chemokine MIP-1alpha/CCL3 impairs mouse hippocampal synaptic
transmission, plasticity and memory . Sci
Rep.
2015; ; 5 : :15862.. 9. Man
SM,
Ma
YR,
Shang
DS, et al.
Peripheral T cells overexpress MIP-1alpha to enhance its
transendothelial migration in Alzheimer’s disease .
Neurobiol Aging.
2007; ; 28 :
:485.–496. 10. Laurent
C,
Dorothee
G,
Hunot
S, et al.
Hippocampal T cell infiltration promotes neuroinflammation and
cognitive decline in a mouse model of tauopathy .
Brain.
2017; ; 140 :
:184.–200. 11. Laurent
C,
Dorothée
G,
Hunot
S, et al.
Tau et troubles cognitifs : un rôle pour les lymphocytes
T . Med Sci (Paris).
2017; ; 33 :
:817.–819. |