| |
| Med Sci (Paris). 35: 32–34. doi: 10.1051/medsci/2019023.Expériences et réflexions chez l’enfant De l’AMM à l’utilisation d’un traitement innovant : quel
parcours ! (1) Claude Cancès1* 1Coordonnateur pédiatrique du Centre de référence des
maladies neuromusculaires de Toulouse, Hôpital Pierre-Paul
Riquet, place du Docteur
Baylac, 31059Toulouse Cedex 9,
France |

Tout clinicien que nous sommes, et quel que soit le type de médicament innovant, nous
avons le droit si ce n’est le devoir de réfléchir à la pertinence même d’un nouveau
traitement. Cela signifie à l’évidence bien connaître au préalable la pathologie
neuromusculaire, son histoire naturelle et les éventuels traitements existants. Il faut
également avoir une connaissance la plus optimale possible des essais thérapeutiques
antérieurs finalisés, en cours ou à venir, et dans l’idéal partager ces informations le
plus tôt possible, avant que ne se concrétise la possibilité de prescrire la nouvelle
molécule. Il convient aussi d’évaluer, esprit critique en éveil, la pertinence de la ou
des indications proposées, des objectifs du traitement innovant et des modalités
d’évaluation choisies pour juger de son efficacité en vie réelle. Avant de commencer à
prescrire, il convient également de discuter du ou des critères à privilégier pour
valider la poursuite ou au contraire l’arrêt du traitement, et du moment opportun pour
prendre ce type de décision. Nous pouvons enfin dès ce premier stade réfléchir à une
potentielle évolution future des indications, ou en tout cas avoir conscience qu’elles
pourront évoluer au fur et à mesure de l’enrichissement de nos connaissances sur la
nouvelle thérapie. |
La mise à disposition d’un traitement innovant connait différents temps possibles.
L’avant autorisation de mise sur le marché (AMM) est l’étape des essais cliniques et
de leurs résultats. Elle nous concerne tous. Il est important pour ceux parmi nous
qui le peuvent et qui le souhaitent de participer à ces essais thérapeutiques.
Autour de l’AMM, le traitement est prescrit au travers des divers types
d’autorisation temporaire d’utilisation (ATU). L’obtention de l’AMM et la phase de
post-AMM se traduisent par la mise en place des traitements ou la poursuite de ceux
initiés sous ATU. A toutes ces phases se pose la question de l’accessibilité du
traitement innovant. Pour l’optimiser, une réflexion préparatoire partagée par tous les Centres de
référence est essentielle. Nous la menons en neuropédiatrie avant la mise en place
des traitements innovants. Nous continuons à la mener après, au travers de
discussions lors de réunions de concertation pluridisciplinaires (RCP). A l’échelle
locale cette fois, chaque centre doit également s’interroger sur la faisabilité de
la mise en œuvre du traitement. Avons-nous le plateau technique, les compétences
médicales et paramédicales et les infrastructures nécessaires ? Si la réponse est
non, notre rôle est d’adresser le patient à un centre plus expert ou doté d’un
plateau technique adapté. Si la réponse est oui, un travail préparatoire avec toutes
les équipes du centre, et notamment avec nos collègues pharmaciens, est
indispensable. |
Quand s’annonce l’heure de la prescription, il est important de délivrer une
information la plus objective possible au patient et à ses accompagnants. Elle
portera sur les bénéfices espérés et sur les risques connus. Elle portera également
sur les inconnus à ce stade, c’est-à-dire les bénéfices réels du traitement
innovant, potentiellement variables selon les malades, et sur ses effets secondaires
à court terme (en général déjà révélés par les essais thérapeutiques) mais surtout à
moyen et à long terme. C’est une donnée dont les patients doivent être informés,
comme ils doivent l’être des critères qui pourront permettre de décider de la
poursuite ou de l’arrêt du traitement. L’information concerne également les
modalités concrètes de mise en place du traitement. Il ne s’agit pas de rester vague
mais au contraire de détailler avec précision le mode de prise en charge
(hospitalisation ou non), les modalités d’administration (intraveineuse,
sous-cutanée ou orale), la surveillance requise et le calendrier de soins. Se mettre en capacité de délivrer le traitement nécessite une bonne coordination
entre les professionnels, tant pour la mise à disposition des équipes médicales,
paramédicales et de pharmacie, que pour la disponibilité d’une unité de lieu. Dans
l’idéal, ce lieu dispose d’une capacité d’accueil des patients constante, mais qui
doit pouvoir aussi être modulable puisque le traitement de certains patients peut
être décalé en raison d’une pathologie intercurrente transitoire. En pratique, cette
unité de lieu est extrêmement variable d’un hôpital à l’autre. Certains services ne
peuvent pas ou difficilement augmenter leur capacité d’accueil. Il faut savoir
proposer un schéma le plus bienveillant possible, c’est-à-dire adapté au malade et
non à la structure hospitalière. Cela signifie notamment s’efforcer de réaliser dans
la mesure du possible tous les actes nécessaires en une journée ou une journée et
demie, ce qui peut impliquer de changer nos propres habitudes. Il faut aussi
rappeler au patient qu’il convient de poursuivre le suivi et la prise en charge
multidisciplinaire, réajustés en intégrant les besoins liés au traitement innovant
et aux autres évaluations requises. C’est fondamental. |
Ces considérations théoriques sont issues de notre expérience du nusinersen, un
médicament indiqué pour les patients symptomatiques atteints d’amyotrophie spinale
(SMA) 5q et qui n’ont jamais atteint un stade de marche autonome. Le schéma
thérapeutique débute par quatre doses de charge, sur près de deux mois, puis des
doses d’entretien tous les quatre mois. Chaque injection a lieu dans le cadre de ce
que nous appelons la « journée nusinersen ». à son arrivée, le patient a très vite
un bilan biologique, préalable au lancement du conditionnement du produit. Il
bénéficie d’évaluations cliniques et fonctionnelles, mais aussi du bilan nécessaire
à son suivi pluridisciplinaire, avant de recevoir l’injection requise puis d’être
surveillé durant quelques heures. À chaque nouvelle journée « nusinersen », nous
réalisons une surveillance clinique et biologique de la tolérance, des effets
indésirables et des bénéfices du traitement. Nous recueillons aussi des données à
visée de recherche clinique ultérieure (recueil national), avec composition d’une
Biobanque pour des projets de recherche plus fondamentale. Une problématique inhérente au traitement par nusinersen, mais également à d’autres
thérapies innovantes est la décision de le poursuivre ou non, après une période
minimale nécessaire pour juger de son efficacité. Nous avons longuement discuté de
la durée de traitement nécessaire pour prendre cette décision, avant de conclure que
nous pourrions probablement évaluer si le traitement est efficace ou non entre 12 et
24 mois après son initiation. Pour ma part, j’évalue la plupart des patients sur le
plan clinique et fonctionnel à M18. C’est l’étape la plus compliquée, notamment à
aborder avec les familles, même si chacun la comprend parfaitement lorsqu’une
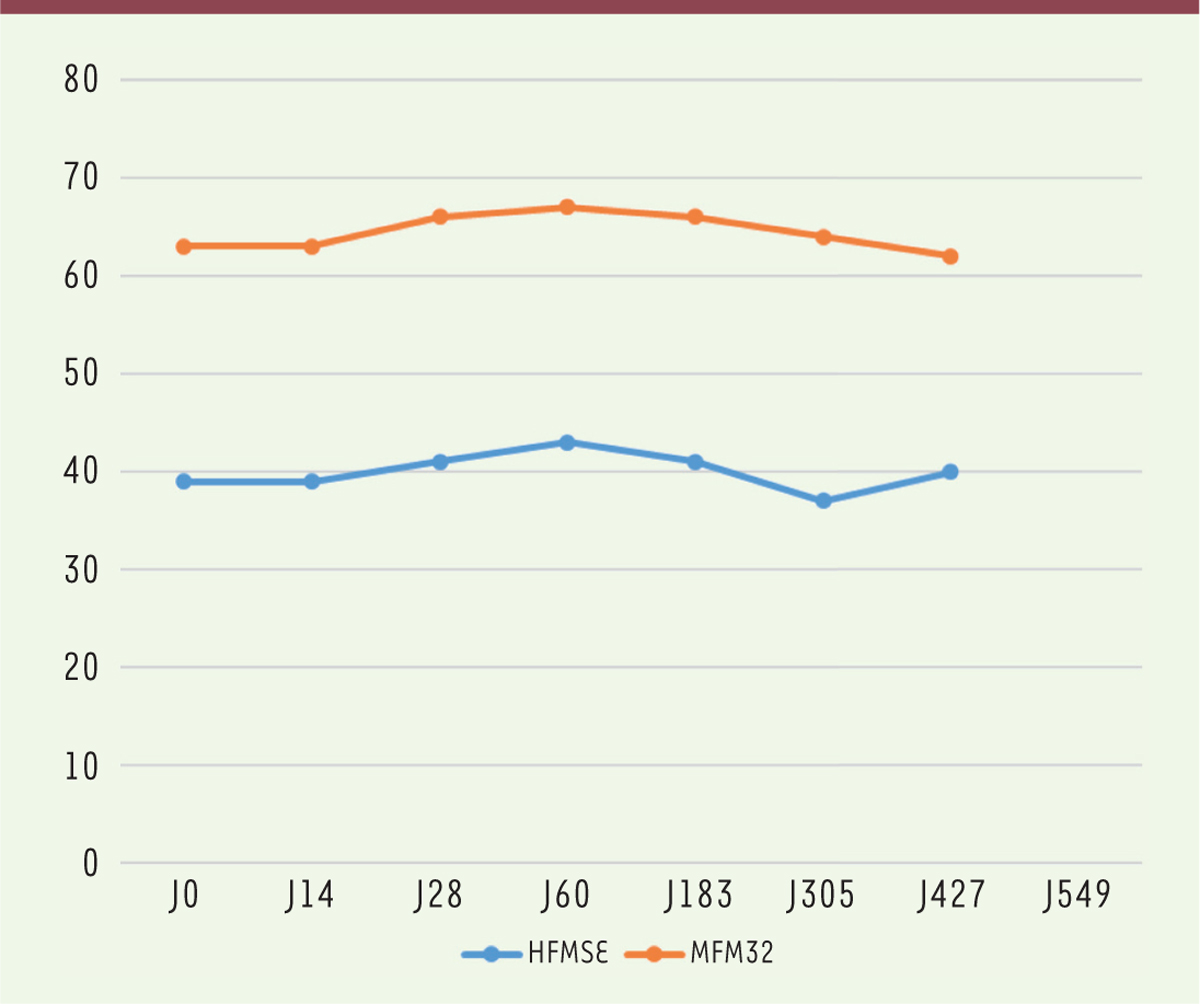
information adéquate a été donnée avant de débuter le traitement. Le cas de ce garçon suivi par notre centre illustre la difficulté de cette décision.
Agé de neuf ans, il est évalué par deux tests fonctionnels, HFMSE et Mesure de
Fonction Motrice (MFM), depuis plusieurs années (Figures 1 et 2). Nous sommes à 14 mois du début du traitement par nusinersen
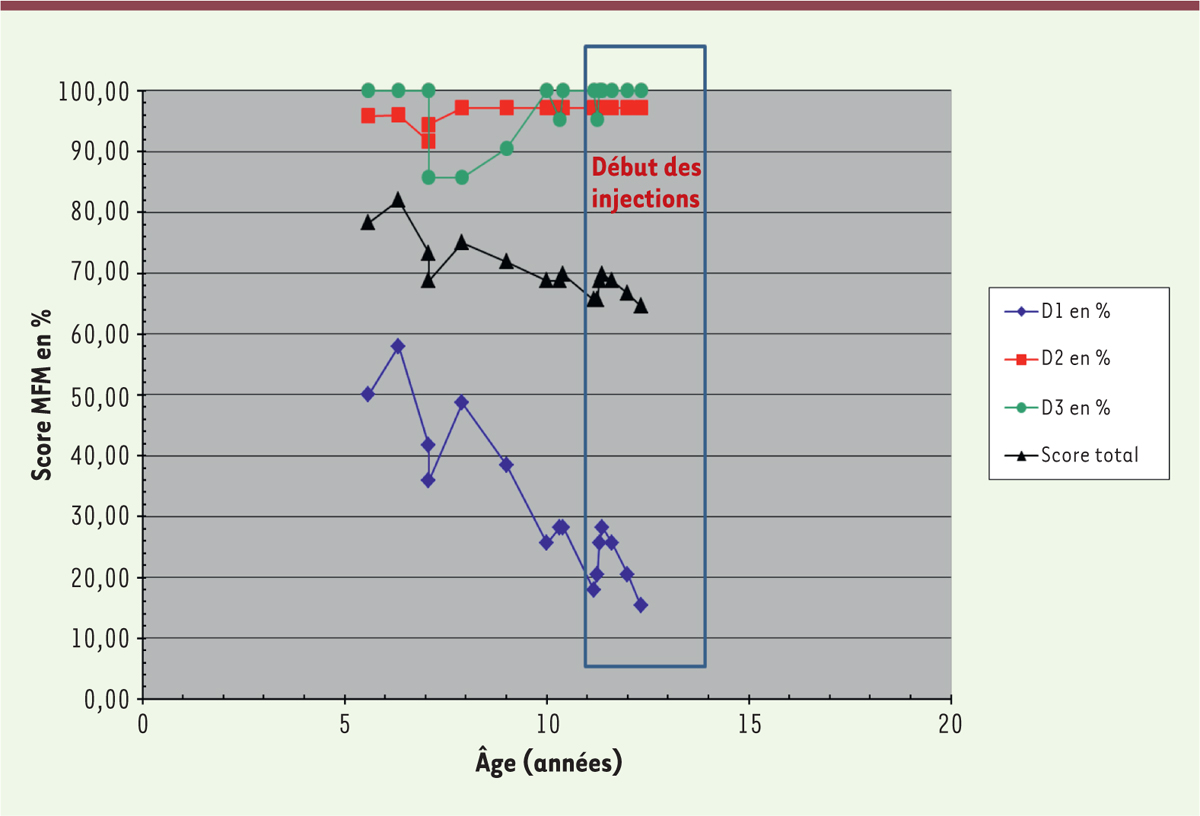
et sur les trois dimensions de la MFM (D1, D2 et D3), l’impression globale est qu’il
ne progresse pas, voire qu’il régresse (Figure
2). C’est aussi le ressenti de la famille. Nous ferons une
nouvelle évaluation dans quatre mois. Si la situation n’a pas évolué, nous pourrions
envisager d’arrêter le traitement.
 | Figure 1. Évaluation fonctionnelle HFMSE et MFM32 (score total) du patient sous
nusinersen. |
 | Figure 2. Évaluation fonctionnelle MFM32 du patient avant et sous nusinersen. |
|
Disposer d’une structure adaptée Notre unité a traité par nusinersen un nombre croissant d’enfants atteints de SMA, au
fur et à mesure des étapes successives de sa mise sur le marché. La possibilité
d’une ATU nominative a été ouverte en octobre 2016. Nous en avons dès lors fait
bénéficier trois patients atteints d’une SMA de type I bis, venus s’ajouter au
patient (type I) traité dans le cadre de l’essai clinique de phase 3 ENDEAR
(NCT02193074). L’ATU nominative a fait place à une ATU de cohorte le 12 mai 2017,
puis à une AMM en juin 2017. Entre fin avril et fin juin 2017, cinq patients
supplémentaires atteints d’une SMA de type II ont commencé un traitement par
nusinersen dans notre unité. Depuis août 2017, trois nouveaux patients, atteints de
SMA de type II, les ont rejoints. Toutes ces prises en charge ont été possibles
parce que notre unité est à géométrie variable, mutualisée avec d’autres
spécialités. Nous avons pu ainsi cibler les équipes paramédicales nécessaires, puis
choisir les jours les plus opportuns, quitte à décaler si nécessaire le traitement
de certains patients. Nous n’avons pas rencontré de difficultés particulières sur le
plan technique (préparation du produit notamment) ni en termes de possibilité
d’accueil. Notre expérience de la mise en œuvre du nusinersen nous conduit à deux réflexions
plus générales sur l’arrivée des traitements innovants. La première, pragmatique,
porte sur la nécessité de disposer de structures d’accueil adaptées aux pathologies
chroniques et/ou aux biothérapies de type hôpital de jour ou hospitalisation à
domicile, mutualisées, avec des jours dédiés par pathologie. De tels dispositifs
permettent de bénéficier d’un partage de compétences (médicales, paramédicales…) et
de capacités d’accueil modulables. Ils supposent en revanche une coordination
paramédicale et un secrétariat renforcé. |
La recherche ne s’arrête pas La seconde réflexion porte non pas sur la forme qu’adopte la mise à disposition des
innovations thérapeutiques, mais sur le fond. Elle consiste à garder en tête que ce
n’est pas parce qu’un traitement innovant est proposé qu’il doit être prescrit. Ce
n’est pas non plus parce qu’il est prescrit qu’il faut arrêter tout travail de
recherche. Les études doivent se poursuivre en post-AMM (phase IV). Nous avons là un
rôle très important à jouer, dans la collecte de données sur l’efficacité en
population et les effets secondaires, l’ajustement ou le réajustement progressif des
indications, et la poursuite d’acquisition de connaissances biocliniques
(biomarqueurs, outils d’évaluation…) en lien renforcé avec nos unités de recherche
clinique. |
L’auteur déclare n’avoir aucun lien d’intérêt concernant les données
publiées dans cet article.
|