La réhabilitation auditive des enfants atteints de surdité congénitale sévère ou profonde repose actuellement sur la pose chirurgicale d’un implant cochléaire prothétique [11] (→) de préférence avant l’âge de 18 mois, permettant alors une bonne acquisition du langage oral et une scolarité normale [1]. Cette réhabilitation auditive est cependant loin d’être optimale, en particulier à cause des performances insuffisantes de l’implant pour la perception de la parole dans un environnement bruyant, et plus encore, de la musique. Dans plus de la moitié des cas, la surdité a une cause génétique. Il s’agit en fait de plus de cent formes monogéniques, transmises pour la plupart sur le mode autosomique récessif1 [12] (→).
(→) Voir le Dossier technique de D. Bouccara et al., m/s n° 2, février 2005, page 190
(→) Voir la Synthèse de J.P. Hardelin et al., m/s n° 3, mars 2004, page 311
Avec l’identification de la plupart des gènes responsables, et grâce aux progrès dans la compréhension des divers mécanismes physiopathologiques impliqués, la recherche de thérapies alternatives, adaptées à chaque forme génétique de surdité, devient possible [2, 3]. Parmi elles, la thérapie génique, dont l’objectif est de rétablir la production de la protéine défectueuse dans les cellules où sa présence est indispensable, fait actuellement l’objet de nombreux travaux de recherche qui utilisent des modèles de souris génétiquement modifiées afin de reproduire la forme correspondante de surdité humaine [13] (→).
(→) Voir la Synthèse de A. Meyer et al., m/s n° 10, octobre 2013, page 883
La stratégie testée jusqu’à présent consistait à injecter dans l’oreille interne des souriceaux mutés, peu après leur naissance, donc à un stade où la cochlée est encore immature2, une copie fonctionnelle de la séquence codante du gène défectueux, insérée dans un vecteur viral inoffensif appartenant à la famille des adeno-associated virus (AAV) [4]. Quelques résultats encourageants ont déjà été rapportés dans des formes rares de surdité, pour lesquelles cette stratégie a permis, chez les souriceaux traités, de prévenir la survenue de la surdité ou, plus souvent, d’en limiter la sévérité [14] (→).
(→) Voir la Synthèse de C. Calvet et al., m/s n° 10, octobre 2018, page 842
Cependant, pour de nombreuses autres formes de surdité, cette approche se heurte à de réelles difficultés [5]: trouver une variété d’AAV qui infecte efficacement (et, de préférence, assez spécifiquement) les cellules dysfonctionnelles par lesquelles on souhaite faire synthétiser la protéine manquante, apporter à ces cellules la copie fonctionnelle du gène défectueux à un stade précédant leur éventuelle dégénérescence irréversible, et pouvoir transférer aux cellules la séquence codante entière du gène lorsqu’elle est longue, sachant que la capacité « d’empaquetage » des vecteurs AAV est limitée à des fragments d’ADN « étranger » de taille inférieure à 5 000 nucléotides (5 kb). Par ailleurs, au moins une question supplémentaire doit être résolue chez l’animal avant d’envisager de tester cette stratégie thérapeutique chez l’homme. Elle découle du fait que la surdité congénitale est actuellement dépistée par un examen systématique des nouveau-nés, donc plusieurs mois après l’apparition physiologique de l’audition durant la vie fœtale3 [6]. Il est donc nécessaire de tester préalablement chez la souris l’efficacité de la thérapie génique après le début de l’audition dans cette espèce, ce qui n’avait encore jamais été réalisé. Une étape importante vient d’être franchie dans le modèle murin de la forme de surdité congénitale par mutation du gène de l’otoferline, une protéine impliquée dans la libération du neurotransmetteur par les cellules sensorielles auditives [7, 8]. Chez ces souris, dont la surdité est profonde, une récupération durable – pendant au moins 20 semaines – des seuils de perception auditive a été obtenue après une injection intracochléaire unique délivrant les fragments d’ADN thérapeutiques à l’âge de 1 mois (Figure 1) [9]. Cette étude a également permis de résoudre le problème posé par le transfert de fragments d’ADN de grande taille aux cellules de l’oreille interne, en montrant qu’il est possible d’obtenir la synthèse de la protéine thérapeutique entière après l’injection simultanée de deux vecteurs recombinants différents contenant chacun une moitié de la séquence codante du gène d’intérêt, grâce à la reconstitution « spontanée », dans les cellules co-infectées, de la séquence complète par fusion des deux séquences partielles (Figure 2) [10]. Ce résultat très encourageant, obtenu chez une souris dont le gène impliqué dans une forme assez fréquente de surdité humaine a été inactivé, ouvre la voie à des expériences similaires sur des modèles murins d’autres formes génétiques de surdité présentes dès la naissance, en prévision d’un possible essai clinique chez l’homme.
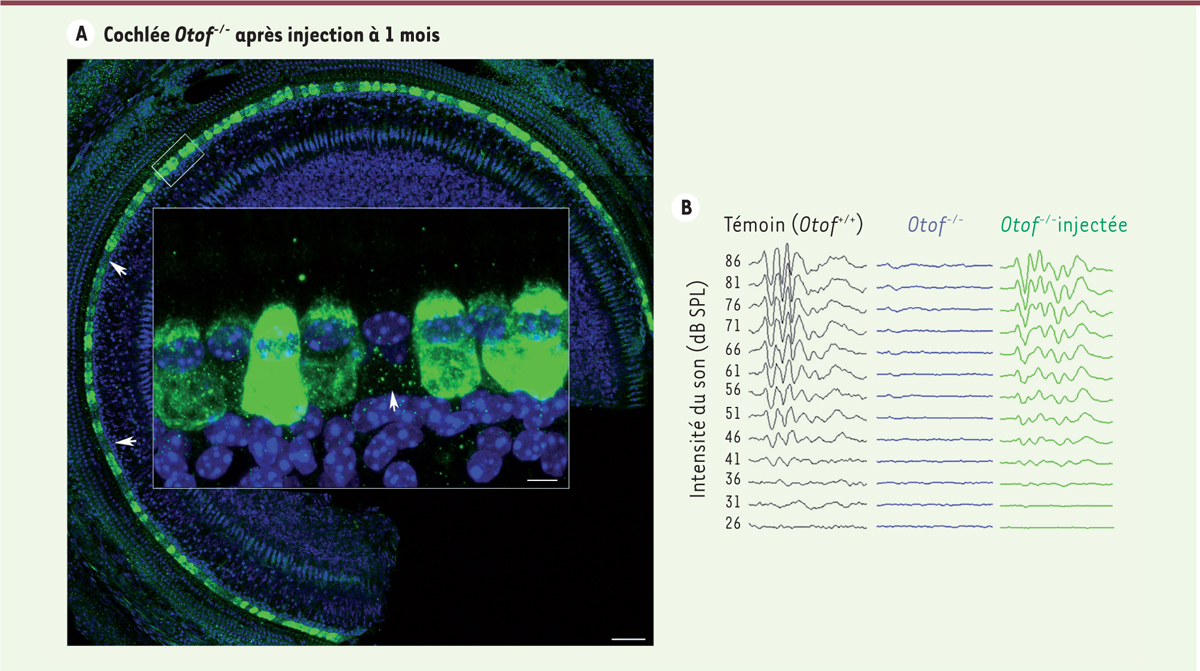
| Figure 1. Restauration durable de l’audition chez des souris mutantes
Otof-/- après injection intracochléaire, à l’âge de 1
mois, de l’ADNc Otof sous la forme de deux fragments complémentaires
insérés chacun dans un vecteur dérivé du virus AAV2.
A. Image de la cochlée (microscopie confocale) plusieurs
semaines après l’injection thérapeutique. La présence de l’otoferline dans
les cellules sensorielles auditives transduites par les virus recombinants
est révélée par un anticorps spécifique de cette protéine.
L’immunofluorescence verte de la plupart des cellules sensorielles indique
qu’elles produisent la protéine thérapeutique, mais quelques cellules,
probablement non-transduites, ne la produisent pas (les flèches indiquent
certaines de ces cellules). Barre d’échelle : 50 µm ou 10 µm (vignette
agrandie). B. Tracés de potentiels évoqués
auditifs enregistrés 7 semaines après la date de l’injection thérapeutique,
chez trois souris différentes (souris témoin Otof +/+ en noir,
souris mutante Otof-/- non-injectée en bleu, et souris mutante
Otof -/- injectée en vert), pour des sons brefs d’intensité
croissante (26 à 86 dB SPL, de bas en haut). On voit la présence des ondes
caractéristiques de la transmission nerveuse du signal auditif dès 41 dB SPL
chez la souris mutante injectée, comme chez la souris témoin. dB SPL :
décibels sound pressure level |
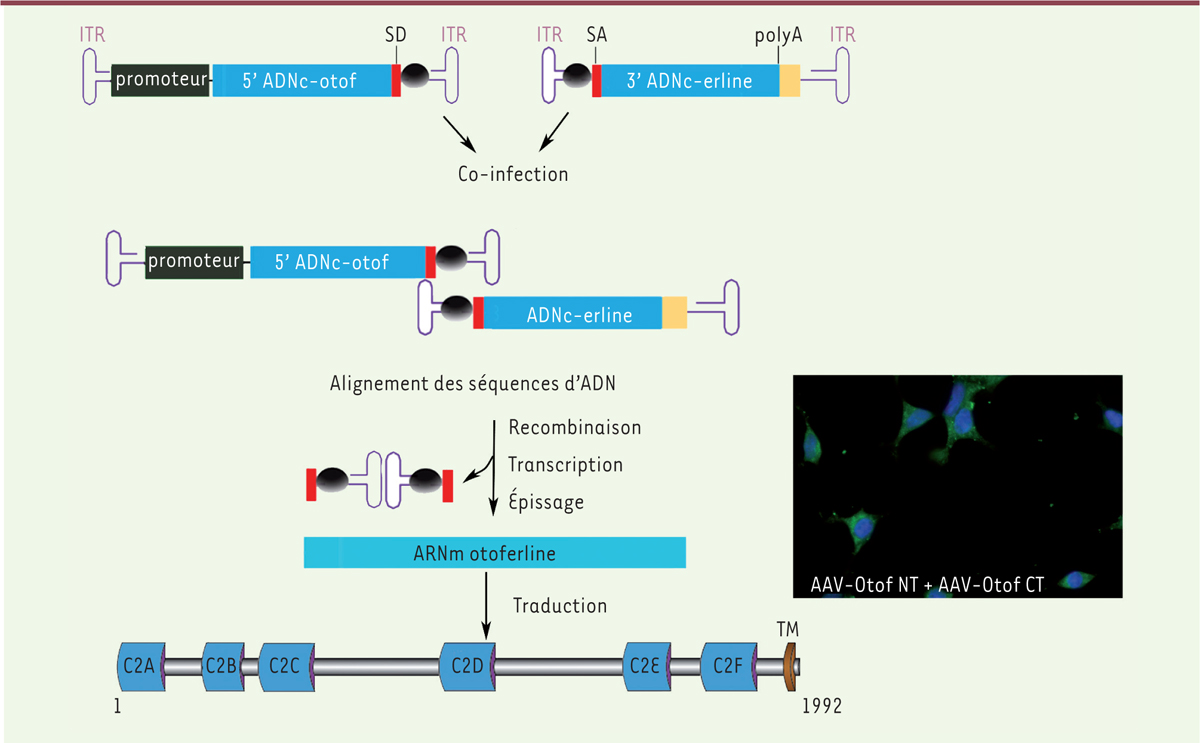
| Figure 2. Expression de l’otoferline entière dans des cellules HEK293 en
culture après co-infection par une paire de virus AAV recombinants
contenant chacun une moitié de la séquence codante.
À gauche: représentation schématique des deux vecteurs contenant la partie
5’ (5’ ADNc-otof) ou la partie 3’ (3’ ADNc-erline) de l’ADN complémentaire
(ADNc), qui codent respectivement la moitié N-terminale ou C-terminale de
cette grande protéine de 1 992 acides aminés. La succession des évènements
conduisant à la synthèse de la protéine entière est indiquée: co-infection
de la cellule, recombinaison entre les deux vecteurs reconstituant la
séquence codant la protéine entière, transcription de cette séquence
recombinante en ARNm, épissage de ce transcrit primaire permettant
d’éliminer la séquence non-codante intermédiaire ayant servi à la
recombinaison, traduction en protéine. À droite: l’otoferline synthétisée
par les cellules co-infectées est révélée par une fluorescence verte, grâce
à un anticorps spécifique dirigé contre l’extrémité C-terminale de la
protéine. Les noyaux des cellules sont révélés par une fluorescence bleue.
ITR: inverted terminal repeat ; SD et SA: sites d’épissage
donneur (SD) et accepteur (SA) ; polyA: site de polyadénylation du transcrit
; C2A-C2F: six domaines C2 de l’otoferline ; TM: domaine
transmembranaire. |