| |
| Med Sci (Paris). 2009 August; 25(8-9): 713–718. Published online 2009 August 15. doi: 10.1051/medsci/2009258-9713.Voie de signalisation Sonic Hedgehog et impact des glucocorticoïdes sur le cerveau en développement Olivier Baud1,2,3,4* and Pierre Gressens3,4,5,6 1AP-HP, service de Réanimation et pédiatrie néonatales, hôpital Robert Debré, 48, boulevard Sérurier, 75019 Paris, France 2Inserm Avenir R05230HS, Paris, France 3Université Paris 7, Faculté de médecine Denis Diderot, IFR02 et IFR25, Paris, France 4PremUP, Paris, France 5Inserm, U676, Paris, France 6AP HP, service de Neurologie, Hôpital Robert Debré, 48, boulevard Sérurier 75019 Paris, France |
Les glucocorticoïdes font partie des hormones stéroïdes et sont sécrétées par la glande surrénale. Elles produisent des effets biologiques très variés en se fixant le plus souvent sur des récepteurs intracellulaires (effets génomiques) et parfois membranaires (effets non génomiques) [
1]. Ces récepteurs sont capables de fixer les glucocorticoïdes endogènes et synthétiques administrés dans de très nombreuses pathologies humaines. Les glucocorticoïdes peuvent modifier considérablement le développement et la maturation de nombreux organes, notamment ceux du poumon et du cerveau. C’est ainsi que l’administration de glucocorticoïdes pendant la période anténatale a permis une réduction considérable des pathologies liées à la prématurité en accélérant la maturation des pneumocytes de type II de l’épithélium alvéolaire. Concernant le cerveau, les récepteurs aux glucocorticoïdes (GR) sont exprimés par les neurones fœtaux et dans de nombreuses régions cérébrales, notamment au niveau de l’hippocampe et du cortex cérébelleux, et ce jusqu’à l’âge adulte [
2]. Dès la période embryonnaire, l’administration de concentrations supraphysiologiques de glucocorticoïdes peut donc entraîner une altération de la prolifération et de la différenciation neuronales et de la croissance cérébrale. Expérimentalement, les glucocorticoïdes administrés en période périnatale vont inhiber la division des neurones, réduire la taille du cerveau et du cervelet et induire une mort neuronale dans l’hippocampe [
3]. Les effets néfastes d’une concentration trop élevée de glucocorticoïdes ne se limitent pas à la période fœtale ou périnatale : chez l’adulte, un excès de glucocorticoïdes peut supprimer la neurogenèse dans la couche sous-granulaire du gyrus dentelé ; à l’inverse, l’insuffisance corticosurrénalienne induite par une surrénalectomie l’augmente [
4,
5]. Cependant, les effets des glucocorticoïdes ne sont pas toujours délétères, et des effets neuroprotecteurs ont été observés, notamment en cas d’atteinte cellulaire sévère. |
Effets cérébraux délétères des glucocorticoïdes synthétiques en période périnatale Depuis plus de 20 ans, il est habituel d’utiliser les glucocorticoïdes dans les pathologies liées à la grande prématurité. Leur administration prophylactique à la mère en cas de menace d’accouchement prématuré permet de réduire considérablement l’incidence des détresses respiratoires néonatales, des hémorragies intraventriculaires et diminue globalement de 50 % la mortalité néonatale [
6]. Le traitement post-natal a également été promu dans les années 1990 afin de limiter le risque de dysplasie bronchopulmonaire, principale séquelle respiratoire observée chez le grand prématuré. Aux États-Unis dans les années 1995-1996, 19 à 28 % des prématurés étaient traités par glucocorticoïdes [
7,
8]. En 1999, 67 % des centres de néonatologie européens utilisaient des glucocorticoïdes pour traiter la dysplasie bronchopulmonaire [
9]. Il a été montré que la dexaméthasone facilite l’extubation, a un effet bénéfique sur la ventilation et diminue l’incidence des dysplasies bronchopulmonaires [
10]. Toutefois, les effets indésirables précoces (digestifs, hyperglycémie, hypertension artérielle) et à long terme (retard de la croissance staturo-pondérale et du développement neuropsychologique) suggèrent un rapport bénéfice/risque insuffisant [
11–
14]. Ces observations ont probablement conduit à substituer la bétaméthasone à la dexaméthasone, sans toutefois qu’il y ait de preuve clinique rapportée dans la littérature. Cette attitude était confortée par la moindre fréquence de leucomalacies périventriculaires chez les enfants exposés in utero à la bétaméthasone par rapport à ceux exposés à la dexaméthasone [6,
15,
16]. Ainsi, l’utilisation des glucocorticoïdes en période néonatale se perpétue, en grande partie parce que très peu de données fondamentales permettent d’expliquer comment précisément ils peuvent être délétères sur le cerveau en développement. À l’inverse, de nombreuses études ont montré une augmentation de l’incidence des lésions de la substance blanche et de l’infirmité motrice cérébrale en cas d’administration précoce de dexaméthasone chez le nouveau-né prématuré. Le suivi d’une cohorte d’enfants traités précocement pendant 4 semaines par dexaméthasone montre une réduction de la taille et du périmètre crânien et une limitation des performances motrices et du quotient de développement à l’âge scolaire [
17]. En utilisant les techniques d’IRM (imagerie par résonance magnétique) volumétrique, Murphy et al. ont quantifié à l’âge théorique du terme l’influence d’une administration parentérale postnatale de dexaméthasone sur la croissance cérébrale et le développement cortical chez les enfants ne présentant pas de lésions de la substance blanche ou d’hémorragie intra-ventriculaire [
18]. Les auteurs ont montré que l’administration de glucocorticoïdes induit une diminution de la croissance cérébrale touchant à la fois le cortex et les noyaux gris centraux. Expérimentalement, de multiples arguments montrent que les stéroïdes, lorsqu’ils sont administrés au cours du développement, peuvent perturber la maturation cérébrale mais sans que le mécanisme en cause ne soit jamais précisé. On a ainsi décrit chez le rat une augmentation de l’apoptose spontanée qui intervient au cours du développement, la perturbation de l’équilibre de la différenciation neuronale en faveur des neurones utilisant une neurotransmission GABAergique ou encore l’atteinte des fonctions neuroendocrines à l’âge adulte [
19]. L’impact des facteurs de risque impliqués dans la genèse des lésions de la substance blanche, première cause de handicap ultérieur chez le prématuré, peut aussi être aggravé par les glucocorticoïdes. C’est le cas de l’hypoxie-ischémie, de l’hypoglycémie et de l’accumulation de glutamate aboutissant à la cascade excitotoxique. De nombreuses interactions pourraient être impliquées dans la toxicité de la dexaméthasone, l’un des principaux glucocorticoïdes synthétiques utilisés chez le nouveau-né : inhibition des facteurs de croissance et augmentation de l’apoptose, influence sur la perméabilité de la barrière hémato-encéphalique en période périnatale, altération de la myélinisation et/ou modification de l’affinité du récepteur de type NMDA au glutamate, principal acide aminé excitateur responsable de la cascade excitotoxique [
20]. Indépendamment de la molécule active, on ne peut pas exclure le rôle néfaste des sulfites utilisés comme excipients dans la préparation de la dexaméthasone : ils pourraient reproduire in vivo l’effet neurotoxique qu’on leur connaît in vitro [
21]. L’ensemble de ces données a amené en 2002 les académies canadienne et américaine de pédiatrie à préciser [
22] que la dexaméthasone n’est plus recommandée pour prévenir ou traiter la dysplasie broncho-pulmonaire, que son utilisation ne devait s’envisager que dans le cadre d’essais randomisés avec comme critère de jugement principal la survie sans troubles du développement à long terme. |
Rôle de la voie de signalisation Sonic Hedgehog (Shh) dans les atteintes neurodéveloppementales induites par les glucocorticoïdes Le mécanisme moléculaire des effets délétères d’un excès de glucocorticoïdes sur le système nerveux central au cours du développement vient d’être récemment éclairci par Heine et Rowitch [
23]. Ces auteurs viennent de démontrer l’antagonisme entre l’action de Shh (sonic hedgehog) et des glucocorticoïdes sur la prolifération des précurseurs des neurones granulaires cérébelleux (PNGC) chez la souris en période néonatale [23]. La voie de signalisation Shh est cruciale pour la régulation de différentes étapes du développement. Elle est activée par la fixation de l’une des trois protéines : Shh (sonic hedgehog), Dhh (desert hedgehog) et Ihh (indian hedgehog) sur un récepteur transmembranaire appelé Ptch (patched). Cette interaction est capable d’abolir l’effet inhibiteur d’une protéine secondaire Smo (smoothened) impliquée dans la régulation de nombreux gènes contrôlant la prolifération et la différenciation cellulaires via la famille de facteurs de transcription Gli [
24]. La voie de signalisation Shh joue un rôle fondamental dans le développement du cervelet au cours duquel Shh induit l’expansion des PNGC. Shh joue également un rôle plus large dans la morphogenèse cérébrale. Parmi les nouvelles fonctions de Shh récemment découvertes figurent le renouvellement et le maintien de certaines populations de cellules souches et progéniteurs situées dans diverses régions cérébrales et mobilisables au cours du développement et de processus de réparation [
25]. En utilisant des modèles murins, Heine et Rowitch montrent que l’exposition chronique aux glucocorticoïdes pendant la première semaine de vie inhibe la croissance cérébelleuse et la prolifération des PNGC en favorisant la sortie du cycle cellulaire et donc la différenciation de ces progéniteurs [23]. L’administration aiguë de glucocorticoïdes à P7 provoque l’apoptose transitoire des PNGC. L’effet antiprolifératif des glucocorticoïdes s’explique par la modulation de la concentration de la plupart des protéines intervenant dans la voie de signalisation Shh. Ainsi, les glucocorticoïdes sont capables d’induire in vitro une réduction de la concentration des protéines N-myc et Cycline D, dont l’expression des gènes est contrôlée par Gli1. Bien que le mécanisme d’action précis des glucocorticoïdes reste inconnu, ceux-ci ne semblent pas agir au niveau transcriptionnel. II semble raisonnable de faire l’hypothèse que la migration dans le noyau ou la stabilité de Gli1 soient nécessaires à ce phénomène, même si un effet direct des glucocorticoïdes sur N-myc ou la Cycline D n’est pas exclu. L’implication de la voie de signalisation Shh est clairement démontrée par les auteurs in vitro (cultures de PNGC) et in vivo par l’effet de la surexpression de la forme activée de Smo : dans ces deux conditions expérimentales, Smo abolit l’effet anti-prolifératif des glucocorticoïdes [23]. Comment Shh interagit-elle avec les glucocorticoïdes ? En contrôlant l’enzyme qui inactive ou active les glucocorticoïdes endogènes. Shh est capable d’induire fortement l’expression de l’isoforme 11bêtaHSD2 qui transforme les glucocorticoïdes endogènes et certains glucocorticoïdes synthétiques comme la prednisone (mais pas la dexaméthasone) en cortisone inactive. Shh est donc capable de réduire ainsi l’action des glucocorticoïdes sur les PNGC. À l’inverse, l’utilisation d’inhibiteurs de la 11bêtaHSD2 potentialise la toxicité des glucocorticoïdes sur les PNGC (Figure 1). L’isoforme 11bêtaHSD1, quant à elle, transforme la cortisone en glucocorticoïdes actifs [
26].Ainsi, Heine et Rowitch ont découvert comment les glucocorticoïdes peuvent avoir un effet antiprolifératif sur certains progéniteurs neuronaux, via la voie de signalisation Shh. L’intérêt de ces observations, par l’identification d’une interaction entre les hormones stéroïdes et le développement et la morphogenèse, dépasse le cadre du développement cérébral ou cérébelleux et pourrait s’appliquer à d’autres organes.  | Figure1.
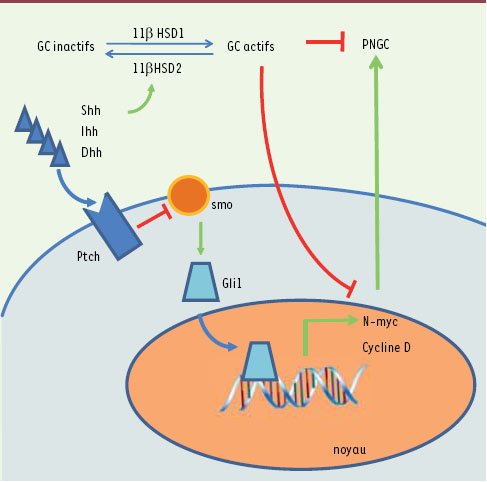
Représentation schématique du mécanisme d’action des glucocorticoïdes (GC) sur la prolifération des PNGC (précurseurs des neurones granulaires cérébelleux) et de l’implication de la voie de signalisation Shh. Shh : sonic hedgehog ; Ihh : Indian hedgehog ; Dhh : desert hedgehog ; Ptch : patched ; Smo : smoothened. |
On connaît déjà l’interaction étroite entre Shh et certaines hormones stéroïdes ou leur voie de synthèse (les intermédiaires de la vitamines D3 et leurs dérivés oxystérols notamment), et l’importance de la fixation covalente entre le cholestérol et la partie carboxy-terminale des protéines Hedgehog pour leur diffusion extracellulaire. Dans ce dernier exemple, une anomalie dans la voie de synthèse du cholestérol a été impliquée dans certaines malformations cérébrales comme l’holoprosencéphalie [
27]. Les oxystérols, dérivés du cholestérol, régulent eux-mêmes la voie de signalisation Shh [
28]. Autre exemple d’interaction, celui de la progestérone, capable de moduler la production d’Ihh lors de l’implantation embryonnaire [
29]. À l’inverse, les œstrogènes diminuent l’expression de Ihh et Dhh dans l’utérus [
30]. Les androgènes et les œstrogènes sont antagonistes : ils induisent et inhibent respectivement l’expression de Shh au cours du développement prostatique [
31,
32]. Ainsi, les hormones stéroïdes jouent des rôles variables sur la voie de signalisation Shh selon le type d’organe et le type d’hormone considéré. À l’inverse, la régulation de la fonction des hormones stéroides par Shh reste très peu étudiée. Cependant, COUP-TFII, un membre de la superfamille des récepteurs nucléaires orphelins, pourrait être impliqué à la fois dans ce contrôle et dans le développement du système nerveux central et du cervelet [
33]. |
L’interaction entre la voie de signalisation Shh et l’action des glucocorticoïdes sur le développement du système nerveux central découverte par Heine et Rowitch, outre son intérêt fondamental, aura des conséquences cliniques. Elle permettra d’orienter la conception de nouvelles molécules de glucocorticoïdes à la fois plus efficaces et moins toxiques sur le cerveau ; le rôle de la 11bêtaHSD doit contribuer à mieux sélectionner les glucocorticoïdes sensibles à cette enzyme afin d’en limiter les effets secondaires, notamment chez le prématuré. L’utilisation clinique de molécules agonistes de la voie Shh reste encore assez éloignée notamment en raison des risques de tumorigenèse neuronale. En revanche, la découverte de molécules régulatrices à la fois de la fonction glucocorticoïde et de la voie Shh au cours de la neurogenèse adulte pourrait permettre des avancées significatives dans le domaine des maladies neurodégénératives. |
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
|
1. Stahn C, Buttgereit F. Genomic and nongenomic effects of glucocorticoids. Nat Clin Pract Rheumatol 2008; 4 : 525–33. 2. McEwen BS. Steroid hormones and brain development: some guidelines for understanding actions of pseudohormones and other toxic agents. Environ Health Perspect 1987; 74 : 177–84. 3. Ozawa H. Steroid hormones, their receptors and neuroendocrine system.J Nippon Med Sch 2005; 72 : 316–25. 4. McEwen BS. Glucocorticoids, depression, and mood disorders: structural remodeling in the brain. Metabolism 2005; 54 : 20–3. 5. Nichols NR, Agolley D, Zieba M, Bye N. Glucocorticoid regulation of glial responses during hippocampal neurodegeneration and regeneration. Brain Res Rev 2005; 48 : 287–301. 6. Crowley P. Prophylactic corticosteroids for preterm birth. Cochrane database Syst Rev 2000; 2 : CD000065. 7. Lee SK. Variations in practice and outcomes in the canadian NICU Network 1996-1997. Pediatrics 2000; 106 : 1070–9. 8. Lemons JA. Very low birth weight outcomes of the National Institutes of Child Health and Human Development Neonatal Research Network, January 1995 through December 1996. Pediatrics 2001; 107 : E1. 9. Desnoulez L, Empana J, Anceschi M, Breart G, Truffert P. Prise en charge de l’immaturité pulmonaire en néonatologie : enquête sur les pratiques européennes. Arch Pediatr 2005; 12 : 4–9. 10. Halliday HL. Early postnatal (< 96 hours) corticosteroids for preventing chronic lung disease in preterm infants. Cochrane Database Syst Rev 2003; 1 : CD001146. 11. Yeh TF, Lin YJ, Hsieh WS, et al. Early postnatal dexamethasone therapy for the prevention of chronic lung disease in preterm infants with respiratory distress syndrome: a multicenter clinical trial. Pediatrics 1997; 100 : E3. 12. Lin YJ. The effects of early postnatal dexamethasone therapy on pulmonary outcome in premature infants with respiratory distress syndrome: a two year follow-up study. Acta Paediatr 2005; 94 : 310–6. 13. Shinwell ES. Early postnatal dexamethasone treatment and increased incidence of cerebral palsy. Arch Dis Child Fetal Neonatal Ed 2000;83 : F177-F181. 14. Stark AR, Carlo WA, Tyson JE, et al. Adverse effects of early dexamethasone in extremely-low-birth-weight infants. National Institute of Child Health and Human Development Neonatal Research Network. N Engl J Med 2001; 344 : 95–101. 15. Baud O, Foix-L’Helias L, Kaminski M, et al. Antenatal glucocorticoid treatment and cystic periventricular leukomalacia in very premature infants. N Engl J Med 1999; 341 : 1190–6. 16. Spinillo A, Viazzo F, Colleoni R, et al. Two-year infant neurodevelopmental outcome after single or multiple antenatal courses of corticosteroids to prevent complications of prematurity. Am J Obstet Gynecol 2004;191 : 217–24. 17. Yeh TF, Lin YJ, Lin HC, et al. Outcomes at school age after postnatal dexamethasone therapy for lung disease of prematurity. N Engl J Med 2004; 350 : 1304–13. 18. Murphy BP, Inder TE, Huppi PS, et al. Impaired cerebral cortical gray matter growth after treatment with dexamethasone for neonatal chronic lung disease. Pediatrics 2001; 107 : 217–21. 19. Baud O, Verney C, Evrard P, Gressens P. Injectable dexamethasone administration enhances cortical GABAergic neuronal differentiation in a novel model of postnatal steroid therapy in mice. Pediatr Res 2005;57 : 149–56. 20. Baud O. Antenatal corticosteroid therapy: benefits and risks. Acta Paediatr Suppl 2004; 93 : 6–10. 21. Baud O, Laudenbach V, Evrard P, Gressens P. Neurotoxic effects of fluorinated glucocorticoid preparations on the developing mouse brain: role of preservatives. Pediatr Res 2001; 50 : 706–11. 22. American Academy of Pediatrics and Canadian Paediatric Society. Postnatal corticosteroids to treat or prevent chronic lung disease in preterm infants. Pediatrics 2002; 109 : 330–8. 23. Heine VM, Rowitch DH. Hedgehog signaling has a protective effect in glucocorticoid-induced mouse neonatal brain injury through an 11[beta]HSD2-dependent mechanism. J Clin Invest 2009; 119 : 267–77. 24. Varjosalo M, Taipale J. Hedgehog: functions and mechanisms. Genes Dev 2008; 22 : 2454–72. 25. Ruiz i Altaba A. Hedgehog-Gli signaling in human disease. Georgetown, Texas, USA : Landes Bioscience, 2006 : 228 p. 26. Holmes MC, Seckl JR. The role of 11beta-hydroxysteroid dehydrogenases in the brain. Mol Cell Endocrinol 2006; 248 : 9–14. 27. Lewis PM, Dunn MP, McMahon JA, et al. Cholesterol modification of sonic hedgehog is required for long-range signaling activity and effective modulation of signaling by Ptc1. Cell 2001; 105 : 599–612. 28. Dwyer JR, Sever N, Carlson M, et al. Oxysterols are novel activators of the hedgehog signaling pathway in pluripotent mesenchymal cells. J Biol Chem 2007; 282 : 8959–68. 29. Lee K, Jeong J, Tsai MJ, et al. Molecular mechanisms involved in progesterone receptor regulation of uterine function. J Steroid Biochem Mol Biol 2006; 102 : 41–50. 30. Katayama S, Ashizawa K, Gohma H, et al. The expression of Hedgehog genes (Ihh, Dhh) and Hedgehog target genes (Ptc1, Gli1, Coup-TfII) is affected by estrogenic stimuli in the uterus of immature female rats. Toxicol Appl Pharmacol 2006; 217 : 375–83. 31. Prins GS, Huang L, Birch L, Pu Y. The role of estrogens in normal and abnormal development of the prostate gland. Ann NY Acad Sci 2006; 1089 : 1–13. 32. Pu Y, Huang L, Birch L, Prins GS. Androgen regulation of prostate morphoregulatory gene expression: Fgf10-dependent and -independent pathways. Endocrinology 2007;148 : 1697–706. 33. Kim BJ, Takamoto N, Yan J, et al. Chicken ovalbumin upstream promoter-transcription factor II (COUP-TFII) regulates growth and patterning of the postnatal mouse cerebellum. Dev Biol 2009; 15 : 378–91. |