La néovascularisation choroïdienne ou prérétinienne constitue une complication de différentes pathologies ophtalmologiques fréquentes. La néovascularisation choroïdienne est principalement observée dans la forme exsudative de la dégénérescence maculaire liée à l’âge (DMLA) [ 1] ainsi qu’au cours de la myopie forte. Cette forme de néovascularisation est la principale cause de la baisse visuelle observée dans ces deux pathologies car elle induit la formation d’un œdème intrarétinien ou une accumulation de fluide sous-rétinien, voire une hémorragie intra- ou sous-rétinienne le plus souvent localisée dans la région maculaire. La néovascularisation prérétinienne complique la rétinopathie diabétique ainsi que la rétinopathie drépanocytaire, deux grandes causes de malvoyance chez le sujet jeune. Dans toutes ces pathologies, le développement d’une néovascularisation est en partie la conséquence d’une augmentation de la concentration locale de VEGF (vascular endothelial growth factor) synthétisé par les cellules de l’épithélium pigmentaire en réponse aux phénomènes ischémiques locaux [ 2]. La Figure 1 illustre les observations faites au fond d’œil dans les principales pathologies néovasculaires rencontrées en ophtalmologie.
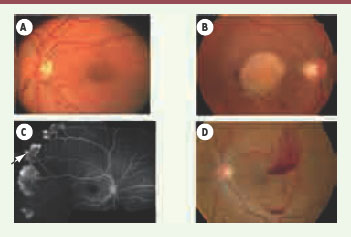
| Figure 1.
Principales pathologies néovasculaires rencontrées en ophtalmologie.
Images d’un fond d’œil normal (A) ou montrant une forme exsudative évoluée de dégénérescence maculaire liée à l’âge (B). (C) Cliché d’angiographie à la fluorescéine (mosaïque) montrant une rétinopathie drépanocytaire compliquée de néovaisseaux prérétiniens périphériques (flèche blanche). (D) Image d’un fond d’œil montrant une rétinopathie diabétique proliférante compliquée d’une hémorragie rétro-hyaloïdienne de faible abondance. |
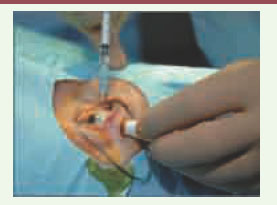
L’utilisation d’anticorps anti-VEGF, injectés par voie intravitréenne (Figure 2), constitue une avancée thérapeutique majeure en ophtalmologie dans certaines maladies se compliquant d’une néovascularisation. Actuellement, la seule indication reconnue des anti-VEGF en ophtalmologie est la forme exsudative de la dégénérescence maculaire liée à l’âge (DMLA) [1]. Pour d’autres maladies dont l’évolution peut être émaillée par l’apparition de néovaisseaux prérétiniens ou choroïdiens, leur utilisation semble intéressante, parfois bénéfique, mais reste à évaluer dans le cadre d’essais cliniques randomisés multicentriques en double insu dont certains sont actuellement en cours.
La dégénérescence maculaire liée à l’âge est la principale cause de malvoyance chez le sujet âgé de plus de 60 ans dans les pays développés [1]. À titre d’exemple, plus d’un million de personnes sont atteintes par la maladie en France selon l’association DMLA. Si les causes de la maladie restent obscures, des facteurs environnementaux et des facteurs de susceptibilité génétiques ont été clairement mis en évidence [1, 3]. La forme exsudative de cette maladie (qui représente environ 70 à 80 % des formes cliniques) se traduit par l’apparition de néovaisseaux choroïdiens dans la région maculaire, dont les conséquences fonctionnelles sont une baisse de l’acuité visuelle, une impression de vision déformée (métamorphopsies) et des amputations du champ visuel central (scotomes). Cette forme clinique de la maladie est la plus sévère car elle est rapidement progressive et peut se compliquer d’hémorragies rétiniennes ou sous-rétiniennes.