L’activation des lymphocytes T consécutive à l’engagement du TCR (T cell receptor) est sous le contrôle de co-récepteurs, dont les ligands respectifs sont multiples, et qui interviennent pour modifier qualitativement et quantitativement la réponse cellulaire. On connaissait les récepteurs membranaires CTLA-4, BTLA (B and T lymphocyte attenuator) et PD-1 comme atténuateurs de l’activation des lymphocytes T. Il faut à présent ajouter à cette liste le récepteur CD160 qui est ancré à la surface cellulaire par une liaison phosphatidylinositol- glycane [ 1]. CD160 a été initialement décrit à la surface des lymphocytes NK (natural killer) cytotoxiques et d’une sous-population de lymphocytes T CD8+ et de lymphocytes TCRγδ [ 2]. Par la suite, il a été montré que CD160 liait les molécules du CMH de classe I avec une faible affinité, son engagement ayant pour conséquence d’induire l’activation des lymphocytes NK [ 3]. Les résultats de l’équipe de G.J. Freeman, publiés dans la revue Nature Immunology [ 4], révèlent qu’après engagement à l’aide d’un anticorps monoclonal spécifique, le récepteur CD160, bien que très faiblement exprimé à la surface des lymphocytes CD4+ activés, est capable d’inhiber totalement l’activation lymphocytaire induite lors du recrutement de CD3 seul ou en association avec CD28. Les auteurs démontrent que CD160, qui se lie aux molécules du CMH de classe I avec une faible affinité, interagit avec une plus grande affinité avec le récepteur HVEM (herpes virus entry mediator). Ce dernier sert de voie d’entrée pour le virus de l’herpès, mais peut aussi interagir avec les protéines BTLA, LIGHT et la lymphotoxine α (Figure 1). Le récepteur CD160, tout comme BTLA, interagit spécifiquement avec le CRD1 (cystein rich domain 1) d’HVEM, alors que LIGHT se lie aux CRD2-CRD3 de HVEM. De façon très élégante, en utilisant des molécules chimériques, cette équipe établit la conséquence fonctionnelle de l’ensemble de ces interactions moléculaires au cours de la réponse spécifique d’un lymphocyte T CD4+ mis en présence d’une cellule présentatrice de l’antigène portant HVEM : la résultante est la dominance du co-signal inhibiteur délivré par BTLA et CD160 sur le puissant co-signal activateur dépendant de LIGHT. Néanmoins, plusieurs questions se posent à la lecture de ce travail. Les mécanismes moléculaires du signal inhibiteur consécutif à l’engagement de CD160 sont peu explorés. Notamment, il est important de savoir s’il est différent de celui qui implique le récepteur BTLA. Concernant l’inte raction de CD160 avec HVEM, CD160 qui est exprimé sous une forme multimérique à la surface cellulaire va-t-il interagir avec la forme monomérique de HVEM comme le fait BTLA, ou avec la forme trimérique qui est induite lors de son interaction avec LIGHT ? Par ailleurs, ces résultats soulèvent le problème du seuil de détection de récepteurs fonctionnels à la surface cellulaire en cytométrie en flux. Au dire des auteurs CD160, bien qu’il ne soit pas détecté en cytométrie en flux, est exprimé à la surface de l’ensemble des lymphocytes T CD4+ activés et surtout, il est capable de se lier au récepteur HVEM et d’induire une inhibition presque totale de l’activation cellulaire. Enfin, il reste à expliquer comment l’engagement de CD160 à la surface des lymphocytes NK induit une activation cellulaire [3].
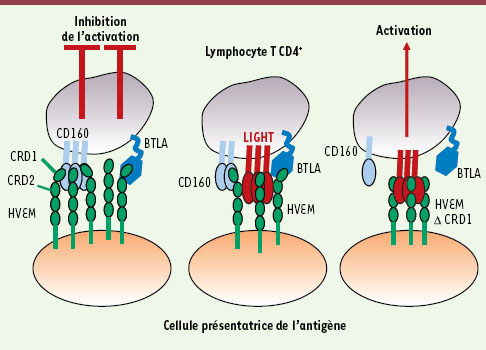
| Figure 1.
Co-récepteurs de la réponse lymphocytaire. Après engagement à l’aide d’un anticorps monoclonal spécifique, le récepteur CD160, bien que très faiblement exprimé à la surface des lymphocytes CD4+ activés, est capable d’inhiber totalement l’activation lymphocytaire induite lors du recrutement de CD3 seul ou en association avec CD28. CD160, qui se lie aux molécules du CMH de classe I avec une faible affinité, interagit avec une plus grande affinité avec le récepteur HVEM (herpes virus entry mediator). Ce dernier sert de voie d’entrée pour le virus de l’herpès, mais peut aussi interagir avec les protéines BTLA, LIGHT et la lymphotoxine α. |