Après la découverte du virus de l’hépatite C (VHC) en 1989, il a fallu attendre 16 ans pour disposer d’un système permettant la propagation du virus et la production de particules virales in vitro. La première étape fut la génération de réplicons subgénomiques. Cependant, ce système n’aboutissait pas à la production de virions infectieux et permettait uniquement l’étude de la phase intracellulaire du cycle réplicatif. L’identification d’une souche particulière qui, pour des raisons encore inconnues, se répliquait à un niveau élevé dans des lignées hépatocytaires humaines a constitué une avancée décisive. Ce nouveau système permet à présent l’étude du cycle cellulaire du VHC, élément essentiel pour le développement de nouveaux antiviraux.
Le VHC infecte 170 millions d’individus dans le monde et représente l’un des agents principaux de maladie chronique du foie. Six génotypes et de nombreux sous-types ont été décrits. Cette variabilité a des conséquences thérapeutiques puisque les différents génotypes ne présentent pas la même sensibilité au traitement [ 1]. Comme les autres Flaviviridae, le VHC est un virus enveloppé et est constitué d’un génome à ARN simple brin de polarité positive (Figure 1A). Sa biologie restait mal connue car le chimpanzé était le seul modèle animal et aucun modèle de culture cellulaire ne permettait un cycle réplicatif complet.
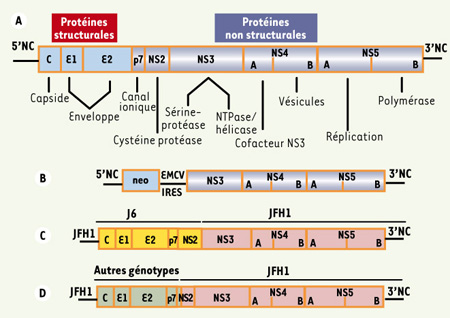
| Figure 1.
Organisation du génome du virus de l’hépatite C et structure des réplicons ou des génomes infectieux. A. Représentation schématique du génome viral. La fonction des protéines clivées est indiquée. C est la protéine de capside, E1 et E2 sont les glycoprotéines d’enveloppe, p7 forme un canal ionique impliqué dans la réplication du virus, NS2 est une cystéine protéase, NS3 forme un complexe stable avec NS4A créant une sérine protéase alors que son domaine carboxy-terminal contient une activité de phosphatase des nucléotides et une activité hélicase. NS4B peut induire la formation de vésicules intracellulaires servant de support à la réplication du virus. La phosphoprotéine NS5A est un co-facteur de réplication. NS5B est l’ARN polymérase dépendante de l’ARN. B. Structure des réplicons subgénomiques. La traduction du gène neo (conférant la résistance à G418) est sous la dépendance de l’IRES du HCV alors que les autres protéines sont sous la dépendance du site d’entrée dans le ribosome (internal ribosomal entry site, IRES) du virus de l’encéphalomyocardite (EMCV). C. Représentation schématique du virus chimère construit par Lindenbach et al. La région comprise entre le gène de capside et NS2 est dérivée de la souche J6 (génotype 2a), les autres régions du génome appartiennent à la souche JFH1 (génotype 2a). D. Représentation schématique des virus chimères construits par Pietschmann et al. Les fragments génomiques ont été fusionnés immédiatement après le premier domaine transmembranaire de NS2. |
Différentes stratégies ont été successivement développées. Par analogie aux travaux réalisés sur le poliovirus, des constructions subgénomiques composées seulement des gènes non structuraux du VHC ont été réalisées (Figure 1B) et leur transfection dans la lignée d’hépatome humain Huh-7 a permis une réplication autonome [ 2]. D’autres travaux ont confirmé ces résultats et ont montré qu’un niveau élevé de réplication était lié d’une part à des mutations adaptatives localisées dans les régions NS3 et NS5A, et d’autre part à l’existence de clones cellulaires hautement permissifs : Huh-7.5 et Huh-7 Lunet [ 3]. Ces éléments ont permis la construction de réplicons du VHC comportant le génome entier, mais aucun réplicon génomique ne permettait la production de particules virales infectieuses. De plus, il a été montré que les mutations adaptatives favorisant la multiplication in vitro étaient en fait délétères pour l’infectiosité in vivo chez le chimpanzé [ 4].
L’année 2005 aura été déterminante pour la mise au point d’un système cellulaire permettant de reproduire un cycle infectieux complet du VHC in vitro. Une étape essentielle fut la construction d’un clone consensus de génotype 2a, isolé d’un patient japonais présentant une hépatite fulminante, forme clinique exceptionnelle dans les hépatites C. Ce clone fut appelé JFH1. Un réplicon subgénomique de JFH1 présentait des niveaux de réplication plus élevés que les précédents, sans mutation adaptative [ 5]. Point crucial, la transfection du génome complet de JFH1 dans les cellules Huh-7 a permis la production de particules virales infectieuses dont l’infectiosité a été démontrée à la fois sur des lignées hépatocytaires et chez le chimpanzé [ 6]. Une autre innovation de ce système fut la possibilité d’accroître les titres du virus JFH1 en utilisant des cellules traitées par de l’interféron-γ [ 7]. Les cellules Huh7.5 semblent constituer le système le plus favorable à la production virale in vitro. Ces cellules présentent une mutation dans le gène RIG-I, conduisant à l’inactivation des réponses immunes innées antivirale [ 8]. La culture d’un virus de génotype 1a a pu être réalisée mais la production de virus infectieux était inférieure à celle de la souche JFH1 [ 9].
La production de particules virales infectieuses à partir d’un génome VHC chimère résultant du remplacement des gènes C, E1, E2 et NS2 de JFH1 par la séquence correspondante du virus J6 (génotype 2a) a été également décrite (Figure 1C) [ 10]. Ce virus chimère est infectieux chez le chimpanzé et après passage chez cet animal le virus reste infectieux en culture cellulaire [ 11]. De plus, la réplication est inhibée par l’interféron-α et les titres viraux obtenus avec ce virus chimère sont plus élevés qu’avec JFH1. Les gènes structuraux de JFH1 semblent donc présenter une plus faible capacité intrinsèque d’assemblage et/ou de libération du virus. Cette hypothèse est étayée par une étude récente où la production en culture de virus chimères intergénotypiques et intragénotypiques a été comparée à celle de JFH1 (Figure 1D) [ 12]. Les titres les plus élevés ont été obtenus avec le recombinant J6-JFH1. L’étude de ces virus chimères a permis récemment l’identification de déterminants essentiels à la production de virus in vitro [ 13]. Afin de produire en culture des virus de différents génotypes, d’autres constructions comportant l’ADN complémentaire du VHC flanqué par des structures ribozymes ont été réalisées mais les niveaux de réplication restent cependant faibles [ 14]. Il est intéressant de noter que les rares virus recombinants décrits in vivo chez des patients chroniquement infectés présentent un point de cassure localisé à la jonction NS2-NS3 et sont constitués des gènes structuraux de génotype 2 [ 15– 17].
Le modèle de culture cellulaire du VHC avec la souche JFH1 constitue donc un événement majeur permettant l’étude in vitro du cycle viral dans son ensemble et la confirmation des données établies précédemment à partir d’autres modèles. Ce système a récemment contribué à la caractérisation d’un nouveau récepteur impliqué dans l’entrée du VHC : la claudine-1 [ 18]. Cependant, malgré tout l’intérêt de la culture conventionnelle pour l’analyse détaillée de la biologie du VHC, les études concernent principalement le génotype 2a ou des constructions dérivées de ce génotype. Le développement de génomes chimériques, comportant les éléments structuraux et non structuraux de l’ensemble des génotypes, reste un enjeu essentiel.