| |
| Med Sci (Paris). 2006 August; 22(8-9): 755–760. Published online 2006 August 15. doi: 10.1051/medsci/20062289755.Immunothérapie du cancer : espoirs et réalités Salem Chouaib,* Faten El Hage, Houssem Benlalam, and Fathia Mami-Chouaib Laboratoire d’Immunologie des tumeurs humaines, Inserm U753, IFR-54, Institut Gustave-Roussy, 39, rue Camille Desmoulins, 94805 Villejuif Cedex, France |
Le concept de surveillance immunologique, qui stipule que le système immunitaire (inné et adaptatif) pourrait intervenir pour prévenir l’apparition des tumeurs et limiter leur croissance, est aujourd’hui soutenu par de nombreuses preuves expérimentales et données cliniques, telles que la corrélation entre l’immunodépression congénitale ou acquise et l’incidence des cancers [
1–
3]. |
De l’immunothérapie non spécifique à la vaccination antitumorale Cytokines et immunothérapie non spécifique La stimulation non spécifique du système immunitaire a débuté en 1890 avec William Coley, un chirurgien new yorkais utilisant des toxines bactériennes pour traiter des patients atteints de sarcomes. Plus tard, en 1922, l’efficacité du BCG à stimuler la réponse immune a été démontrée. Grâce à la disponibilité de cytokines recombinantes, l’immuno-intervention a connu un réel regain d’intérêt en thérapeutique oncologique, notamment dans la manipulation fine de l’hématopoïèse et des réponses immunitaires. Ainsi, certaines cytokines sont devenues des standards thérapeutiques, comme les facteurs de croissance (G-CSF 1, GM-CSF) dans la reconstitution hématopoïétique pour compenser la myélotoxicité, ou l’interleukine 2 et l’interféron a, utilisés dans le traitement des adénocarcinomes du rein métastatique, des mélanomes malins à haut risque de rechute et de la leucémie myéloïde chronique. D’autres cytokines ont montré une efficacité thérapeutique quand elles sont utilisées en association avec des substances antitumorales comme le TNF, lors du traitement des sarcomes des membres [
4]. Les effets secondaires des cytokines, leur action en cascade et leur grand pléiotropisme ont laissé la place à une immunothérapie antitumorale plus spécifique et mieux ciblée, visant l’optimisation de la réponse antitumorale locale. Antigènes de rejet tumoral et cellules dendritiques L’approche immunologique en thérapeutique oncologique est devenue un enjeu important, notamment grâce à sa capacité d’atteindre des cibles spécifiques [
5]. Cependant, le succès d’une telle immunothérapie anticancéreuse repose à la fois sur l’expression d’antigènes spécifiques à la surface des cellules tumorales, leur présentation et l’induction d’effecteurs cytotoxiques (CTL) capables de reconnaître ces antigènes et de lyser les cellules cibles [ 5]. L’identification des antigènes tumoraux et la compréhension du rôle des cellules dendritiques dans leur présentation aux cellules effectrices constituent deux avancées majeures dans les approches d’immunothérapie des cancers. Antigènes tumoraux Il est clairement établi que les nombreuses altérations génétiques et épigénétiques caractérisant les cellules tumorales entraînent une modification de leur profil d’expression génique, aboutissant à l’expression d’antigènes associés aux tumeurs (TAA) [
6]. L’existence d’une réponse immunitaire spécifique dirigée contre ces antigènes a pu être mise en évidence dans plusieurs modèles tumoraux humains. La majorité des TAA identifiés à ce jour sont des antigènes tumoraux reconnus par des CTL CD8 +. C’est surtout dans le modèle du mélanome que les antigènes spécifiques de tumeurs humaines ont été identifiés [
7]. Globalement, les antigènes associés aux tumeurs peuvent être classés en cinq catégories, en fonction de leur profil d’expression et de leur origine [
8]. Il s’agit des antigènes d’activation (ou antigènes de type cancer-testis), des antigènes de différenciation (Melan-A/MART-1, tyrosinase, gp100, gp75 et TRP-1 pour le mélanome), des antigènes surexprimés (HER-2/neu, p53 et télomérase), des antigènes codés par des gènes mutés (β-caténine, CDK4, caspase 8, α-actinine 4 et CDC27) [
9] et, enfin, de certains antigènes viraux (EBV, HBV, HCV et HPV). Cellules dendritiques Les cellules dendritiques (DC) sont des cellules présentatrices d’antigènes (APC) professionnelles, se caractérisant par leur grande hétérogénéité phénotypique et fonctionnelle. Elles ont la capacité d’activer efficacement des lymphocytes T naïfs, CD4 + auxiliaires ou CD8 + cytotoxiques, et de déclencher une réponse adaptative spécifique de l’antigène. Plusieurs arguments expérimentaux indiquent que les précurseurs naïfs des lymphocytes T ont un profil de migration restreint aux compartiments lymphoïdes secondaires, comme les ganglions lymphatiques et la rate, entre lesquels ils circulent continuellement : par conséquent, ils n’ont pas la capacité d’interagir avec les cellules tumorales au sein des tissus périphériques. La voie d’activation des CTL CD8+ spécifiques des antigènes tumoraux est probablement celle de la présentation croisée (cross-priming), propre aux cellules dendritiques, qui consiste à apprêter et présenter, par la voie des molécules du complexe majeur d’histocompatibilité (CMH), des antigènes captés de manière exogène [
10]. Selon le modèle généralement décrit, les effecteurs de la réponse innée et les facteurs de stress cellulaire du micro-environnement tumoral induisent des dommages cellulaires aboutissant à la libération de différentes sources d’antigènes exogènes (corps apoptotiques), qui sont l’objet d’une présentation croisée par les DC. Par ailleurs, des signaux de « danger » (protéines de choc thermique, HSP), libérés en réponse aux dommages cellulaires, induisent la maturation des DC, qui acquièrent alors la capacité d’exprimer fortement les molécules de costimulation et de migrer vers les ganglions lymphatiques drainants. L’ensemble de ces événements se traduit par l’activation des lymphocytes T CD8 naïfs spécifiques. Plusieurs travaux ont pu mettre en évidence une présentation croisée des TAA in vivo, déclenchée par des APC dérivées de la moelle osseuse, qui semble dépendre du niveau d’expression des antigènes tumoraux [
11–
13]. D’autres travaux ont suggéré un modèle de reconnaissance des TAA fondé sur la migration des cellules tumorales au niveau des ganglions lymphatiques drainants et leur activation directe des cellules T CD8. Immunothérapie active des cancers Avant l’identification des TAA, les approches vaccinales consistaient à immuniser les patients avec des cellules tumorales entières irradiées (autologues ou allogéniques), des cellules tumorales génétiquement modifiées (capable d’exprimer certaines molécules de costimulation ou de secréter certaines cytokines), des fusions de cellules tumorales et d’APC [
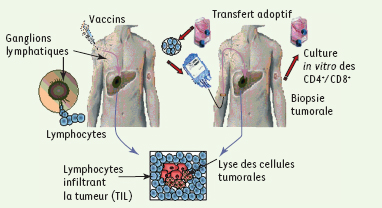
14] ou des extraits de cellules tumorales (lysats, membranes, HSP…) administrés en présence ou non d’adjuvants et de cytokines (Figure 1).
 | Figure 1.
Approches d’immunothérapie active et adoptive [
20]. |
L’identification de différents TAA a rendu les stratégies d’immunisation active contre les tumeurs de plus en plus spécifiques. De telles stratégies vaccinales ont pour objectif la stimulation active du système immunitaire du patient, réfractaire aux traitements classiques, afin d’activer spécifiquement ses défenses contre la tumeur primaire et ses métastases. Ainsi, différents types de vaccins ont été développés pour immuniser les patients, tels que des antigènes de tumeurs purifiés (naturels ou recombinants), des peptides synthétiques, de l’ADN nu (plasmides…) [
15], des virus recombinants (adénovirus,…) [
16,
17] ou, encore, des bactéries recombinantes (BCG, listéria). La plupart des essais ont été fondés sur l’administration, au patient, de cellules dendritiques chargées avec des TAA recombinants ou des peptides issus de la tumeur, ou infectées par des virus recombinants ou de l’ARN. L’un des aspects, inhabituels, de la vaccination antitumorale est qu’elle est thérapeutique, puisqu’elle s’adresse à des patients porteurs de tumeur. Même si des résultats encourageants ont été obtenus dans les modèles murins, les modèles créés par l’induction expérimentale de tumeurs n’ont pas, ou peu, de valeur prédictive chez l’homme. Chez les patients soumis à un tel traitement vaccinal, les réponses immunologiques induites par la vaccination, bien que détectables, ne s’accompagnent pas nécessairement d’une réponse clinique. À cet égard, il convient de signaler que le statut immunitaire du malade est souvent altéré par des traitements cytotoxiques, et que les patients bénéficiant d’une vaccination sont souvent sélectionnés à un stade relativement avancé de la maladie (stades III et IV). L’enjeu majeur du développement des vaccins antitumoraux est donc de les explorer chez des patients à un stade précoce du cancer. Immunothérapie cellulaire passive L’immunothérapie adoptive a fait son entrée dans la panoplie des approches thérapeutiques contre certains types de cancer. Elle consiste à injecter aux patients soit une population polyclonale TIL, fortement enrichie en lymphocytes de spécificité connue, soit une population clonale de lymphocytes T spécifiques (Figure 1). Ces dernières sont obtenues par clonage de la population de TIL, par tri des clones en utilisant des tétramères HLA/peptide ou, enfin, par sensibilisation des cellules périphériques du sang avec des APC chargées en peptides. Le groupe de Rosenberg a introduit une approche fondée sur l’immunodéplétion avec cyclophosphamide et fludarabine : ce traitement permet l’élimination spécifique des lymphocytes T régulateurs, qui jouent un rôle potentiel dans l’inhibition des effecteurs antitumoraux. Le transfert de ces cellules, aux potentiels lytique et sécrétoire importants, chez un hôte lymphodéplété, induirait un pourcentage de cellules T CD8 + spécifiques circulant allant de 5 % à 75 % [
18]. Rétrospectivement, les différentes études réalisées indiquent que l’association des TIL avec de l’IL-2 favoriserait les réponses cliniques, que l’immunodéplétion accroît la survie des patients et l’efficacité des TIL injectés et, enfin, que les patients ayant un ganglion envahi survivent plus longtemps. Ces informations sont à prendre en considération pour de prochains protocoles de thérapie adoptive, qui devraient notamment cibler des patients ayant un ganglion envahi et soumis au cyclophosphamide avant le transfert des TIL. Une des limites de cette approche réside dans le fait que les cellules injectées ne migrent pas vers le site tumoral, mais sont souvent détectées dans le foie ou la rate des patients. Ce défaut de migration intratumorale (défaut de homing) est souvent associé à un dysfonctionnement des systèmes intégrines/chimokines et de leurs ligands respectifs. Par ailleurs, le phénomène d’AICD constitue un autre facteur limitant l’efficacité du transfert de lymphocytes activés spécifiques d’antigènes : les lymphocytes T activés après stimulation antigénique et dopage cytokinique peuvent rentrer dans un processus de suicide fratricide, limitant ainsi le « pool » de ces cellules in situ [
19]. Malgré les quelques résultats indiquant une meilleure survie des patients, le transfert adoptif reste expérimentalement lourd, et sa difficulté majeure reste de réussir à produire un grand nombre de cellules T spécifiques d’un antigène déterminé, possédant des facultés fonctionnelles adéquates et des propriétés de survie appropriées. |
Approches vaccinales : quelques leçons En dépit des résultats modestes, mais réels, obtenus dans le cadre des essais cliniques, ces derniers ont le mérite d’avoir validé le concept de la vaccination et démontré la faisabilité de l’approche. Ils ont également mis en évidence l’absence d’effets secondaires et montré l’efficacité de la vaccination en termes d’induction des réponses T cytotoxiques, même si celles-ci sont rarement accompagnées d’une réponse clinique objective. Bien que les essais cliniques n’aient pas abouti aux résultats escomptés, ils pourraient inéluctablement conduire à poursuivre le suivi immunologique des patients. Un tel suivi devrait permettre d’améliorer la compréhension de l’échec thérapeutique et de revisiter les approches de vaccination sous leur forme actuelle. Ainsi, les travaux récents de Pagès et de ses collaborateurs suggèrent fortement que la nature de l’infiltration lymphocytaire est corrélée à l’évolution de la maladie [
21], et que les tumeurs fortement infiltrées par des lymphocytes T CD8 sont de meilleur pronostic. Plusieurs données expérimentales soulignent que les tumeurs solides n’expriment pas, ou peu, de molécules de costimulation et ne présentent pas de micro-environnement inflammatoire suffisant pour transformer les précurseurs lymphocytaires naïfs en lymphocytes activés, possédant les fonctions effectrices nécessaires pour l’éradication de la tumeur. De ce fait, les méthodes innovantes devraient avoir pour objectifs la production de cellules mémoires, mais également l’activation de ces cellules antitumorales : pour cela, il conviendrait probablement d’améliorer les techniques de stimulation des APC in vivo, avec de nouveaux adjuvants ou en créant un environnement inflammatoire au niveau du site tumoral pouvant attirer les lymphocytes effecteurs dans la tumeur. D’autres études soulignent la nécessité d’élaborer des approches plus intégratives visant à manipuler simultanément le système immunitaire et le système tumoral en tenant compte, notamment, de la grande plasticité du micro-environnement de la tumeur. Le développement des vaccins antitumoraux à venir devrait donc considérer le choix de l’antigène, en tenant compte de la mosaïque antigénique tumorale et la façon de le délivrer, ainsi que le type de réponse des CTL susceptibles d’aboutir à un effet antitumoral local. Par ailleurs, une meilleure sélection des patients sur la base de leur statut immunologique, des caractéristiques moléculaires de leur tumeur, mais aussi de leur charge tumorale minime, pourrait permettre de proposer des vaccins plus efficaces. |
Dualité fonctionnelle des effecteurs cytotoxiques antitumoraux Les principaux protocoles d’immunothérapie antitumorale (active ou passive) développés à l’heure actuelle ont pour ultime objectif l’induction de CTL possédant une activité antitumorale. Si l’induction de cette réponse cytotoxique forte et prolongée est un déterminant clé de la régression tumorale, des données récentes suggèrent que les effecteurs cytotoxiques antitumoraux jouent également un rôle dans la dynamique de « l’éditing tumoral ». Ces cellules cytotoxiques possèdent en effet une dualité fonctionnelle, en détruisant des cellules tumorales sensibles ainsi qu’en sélectionnant des variants résistants, ayant perdu l’antigène tumoral ou ayant acquis une résistance à la lyse en dépit de leur immunogénicité [
22]. Cette sélection est fortement facilitée par l’instabilité génétique, une caractéristique majeure de la plupart des tumeurs humaines. L’analyse de la réponse de ces variants résistants aux traitements cytotoxiques classiques suscite à l’heure actuelle un intérêt majeur. |
Complexité du système tumoral et de son micro-environnement Outre l’instabilité génétique tumorale et l’influence des phénomènes épigénétiques dans l’oncogenèse, plusieurs arguments indiquent que la tumeur entretient une relation très complexe avec son micro-environnement stromal, ainsi qu’avec le système immunitaire lui-même [
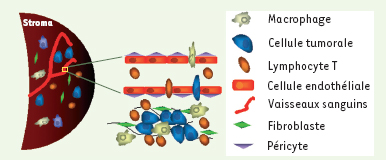
23]. Il est clairement établi que la tumeur est constituée de cellules néoplasiques et d’un micro-environnement constitué de capillaires, de cellules de soutien (péricytes, cellules musculaires lisses, fibroblastes) et de cellules inflammatoires (macrophages, polynucléaires, neutrophiles et mastocytes) (Figure 2). De ce fait, l’infiltrat inflammatoire d’une tumeur joue un rôle essentiel dans son développement, à travers la production de facteurs mitogéniques, angiogéniques et destructeurs de la matrice cellulaire [
24–
26]. Une tumeur ne peut en effet croître au sein de l’hôte que jusqu’à un certain seuil, au-delà duquel elle est menacée d’asphyxie et de nécrose. Pour exécuter leur programme invasif, les tumeurs développent des stratégies complexes et efficaces pour modifier, à leur profit, les tissus sains de l’hôte dans lesquels elles se nichent. Il se forme ainsi autour d’elles un cocon interactif et protecteur, le stroma. Dans ce contexte, les approches d’immunothérapie doivent cibler les cellules tumorales dans le contexte d’un micro-environnement hostile au système immunitaire et favorable à l’invasion tumorale [
27]. Ainsi, l’analyse du rôle de certains éléments immunologiques, inflammatoires et vasculaires du micro-environnement d’une tumeur dans le contrôle du dialogue entre les systèmes tumoral et immunitaire, ainsi que dans l’échec ou l’efficacité du système effecteur et l’invasivité tumorale, est cruciale pour l’élaboration de stratégies innovantes en immunothérapie.
 | Figure 2.
Le stroma, micro-environnement tumoral.
|
|
Les essais cliniques pour le traitement du cancer se sont multipliés grâce à l’arsenal immunologique, même si les résultats restent à ce jour relativement limités. Tous les progrès accomplis et à venir dans le domaine de l’immunologie des cancers laissent présager que l’immunothérapie prendra une place croissante dans les thérapeutiques du cancer. Bien que les approches utilisées soient efficaces en termes d’induction d’une réponse immune chez les patients, la propostion de patients développant une réponse clinique objective reste insignifiante, variant de 3 % à 4 % [5]. Il est devenu clair, à la lumière des résultats obtenus, que la vaccination antitumorale n’en est qu’à ses débuts et pourrait constituer à terme une révolution, mais de nombreuses étapes restent à franchir avant qu’elle ne prenne une vraie place dans l’abord thérapeutique du cancer. Les résultats cliniques encore décevants obtenus chez l’homme confirment la complexité du système tumoral. L’analyse dynamique et fonctionnelle du micro-environnement tumoral, dont notre connaissance aujourd’hui n’est que très hypothétique et fragmentaire, demeure un enjeu majeur pour les développements de l’immunothérapie. C’est dans ce contexte que, grâce à une approche multidisciplinaire, s’orientent les efforts visant un décryptage fin de l’interaction fonctionnelle entre deux systèmes mutuellement antagonistes, le système immunitaire de l’hôte et le système tumoral, et une meilleure intégration de la biologie tumorale dans l’élaboration de nouvelles stratégies d’immunothérapie, seules ou en association avec les thérapeutiques conventionnelles.

|
Footnotes |
1. Boshoff C, Weiss R. AIDS-related malignancies. Nat Rev Cancer 2002; 2 : 373–82. 2. Gatti RA, Good RA. Occurrence of malignancy in immunodeficiency diseases. A literature review. Cancer 1971; 28 : 89–98. 3. Penn I, Starzl TE. Malignant lymphomas in transplantation patients : a review of the world experience. Int Z Klin Pharmakol Ther Toxikol 1970; 3 : 49–54. 4. Lejeune FJ. High dose recombinant tumour necrosis factor (rTNF alpha) administered by isolation perfusion for advanced tumours of the limbs : a model for biochemotherapy of cancer. Eur J Cancer1995; 31A : 1009–16. 5. Rosenberg SA, Yang JC, Restifo NP. Cancer immunotherapy : moving beyond current vaccines. Nat Med 2004; 10 : 909–15. 6. Pardoll D. Does the immune system see tumors as foreign or self ? Annu Rev Immunol 2003; 21 : 807–39. 7. Van der Bruggen P, Traversari C, Chomez P, et al. A gene encoding an antigen recognized by cytolytic T lymphocytes on a human melanoma. Science 1991; 254 : 1643–7. 8. Boon T, Coulie PG, Van den Eynde B. Tumor antigens recognized by T cells. Immunol Today 1997; 18 : 267–8. 9. Echchakir H, Mami-Chouaib F, Vergnon I, et al. A point mutation in the alpha-actinin-4 gene generates an antigenic peptide recognized by autologous cytolytic T lymphocytes on a human lung carcinoma. Cancer Res 2001; 61 : 4078–83. 10. Heath WR, Carbone FR. Cross-presentation, dendritic cells, tolerance and immunity. Annu Rev Immunol 2001; 19 : 47–64. 11. Spiotto MT, Yu P, Rowley DA, et al. Increasing tumor antigen expression overcomes « ignorance » to solid tumors via crosspresentation by bone marrow-derived stromal cells. Immunity 2002; 17 : 737–47. 12. Huang AY, Golumbek P, Ahmadzadeh M, et al. Bone marrow-derived cells present MHC class I-restricted tumour antigens in priming of antitumour immune responses. Ciba Found Symp 1994; 187 : 229–44. 13. Huang AY, Bruce AT, Pardoll DM, et al.
In vivo cross-priming of MHC class I-restricted antigens requires the TAP transporter. Immunity 1996; 4 : 349–55. 14. Gong J, Apostolopoulos V, Chen D, et al. Selection and characterization of MUC1-specific CD8+ T cells from MUC1 transgenic mice immunized with dendritic-carcinoma fusion cells. Immunology 2000; 101 : 316–24. 15. Restifo NP, Ying H, Hwang L, et al. The promise of nucleic acid vaccines. Gene Ther 2000;7 : 89–92. 16. Marshall JL, Hoyer RJ, Toomey MA, et al. Phase I study in advanced cancer patients of a diversified prime-and-boost vaccination protocol using recombinant vaccinia virus and recombinant nonreplicating avipox virus to elicit anti-carcinoembryonic antigen immune responses. J Clin Oncol 2000; 18 : 3964–73. 17. Rosenberg SA, Zhai Y, Yang JC, et al. Immunizing patients with metastatic melanoma using recombinant adenoviruses encoding MART-1 or gp100 melanoma antigens. J Natl Cancer Inst 1998; 90 : 1894–900. 18. Dudley ME, Wunderlich JR, Robbins PF, et al. Cancer regression and autoimmunity in patients after clonal repopulation with antitumor lymphocytes. Science 2002; 298 : 850–4. 19. Russell JH, White CL, Loh DY, et al. Receptor-stimulated death pathway is opened by antigen in mature T cells. Proc Natl Acad Sci USA 1991; 88 : 2151–5. 20. Rosenberg SA. Shedding light on immunotherapy for cancer. N Engl J Med 2004; 350 : 1461–3. 21. Pages F, Berger A, Camus M, et al. Effector memory T cells, early metastasis, and survival in colorectal cancer. N Engl J Med 2005; 353 : 2654–66. 22. Abouzahr S, Bismuth G, Gaudin, C, et al. Identification of target actin content and polymerization status as a mechanism of tumor resistance after cytolytic T lymphocyte pressure. Proc Natl Acad Sci USA 2006; 103 : 1428–33. 23. Chouaib S. Integrating the quality of the cytotoxic response and tumor susceptibility into the design of protective vaccines in tumor immunotherapy. J Clin Invest 2003; 111 : 595–7. 24. Dong J, Grunstein J, Tejada M, et al. VEGF-null cells require PDGFR alpha signaling-mediated stromal fibroblast recruitment for tumorigenesis. EMBO J 2004; 23 : 2800–10. 25. Polverini PJ, Leibovich SJ. Induction of neovascularization in vivo and endothelial proliferation in vitro by tumor-associated macrophages. Lab Invest 1984; 51 : 635–42. 26. Silzle T, Randolph GJ, Kreutz M, et al. The fibroblast : sentinel cell and local immune modulator in tumor tissue. Int J Cancer 2004; 108 : 173–80. 27. Perdrizet GA, Kaneko H, Buckley TM, et al. Heat shock protects pig kidneys against warm ischemic injury. Transplant Proc 1990; 22 : 460–1. |