Au cours du développement, les précurseurs neuronaux engendrés par les épithélia germinatifs migrent vers leur destination cible où ils se différencient et s’intègrent dans le réseau neuronal [ 1]. Une migration anormale ou l’établissement de contacts inadéquats avec les cellules avoisinantes peut conduire à l’élimination des neurones via l’activation d’un programme de mort cellulaire [ 2]. Le neuropeptide PACAP (pituitary adenylate cyclase-activating polypeptide) est connu pour exercer des effets pro-différenciateurs et anti-apoptotiques sur divers types cellulaires notamment sur les neurones en grain du cervelet [ 3, 4]. Dans le cortex cérébelleux, les cellules en grain immatures, qui sont engendrées au niveau de la couche granulaire externe, expriment de fortes concentrations de récepteurs du PACAP. Ces précurseurs migrent au travers de la couche moléculaire pour former la couche granulaire interne (Figure 1). Le PACAP pourrait donc contrôler la migration et/ou la différenciation des neurones en grain du cervelet. Comparativement aux facteurs neurotrophiques, peu d’études ont été consacrées à l’action de molécules inductrices de la mort cellulaire programmée, un processus pourtant indispensable au développement harmonieux du système nerveux [ 5]. Les céramides constituent une classe de messagers intracellulaires produits soit par synthèse de novo, soit à partir de l’hydrolyse des sphingolipides sous l’effet de sphingomyélinases activées par des cytokines pro-inflammatoires telles que le TNFα ou FasL [ 6]. Il a été montré que les céramides peuvent induire des effets pro-apoptotiques au cours du neurodéveloppement suggérant une interaction avec le neuropeptide PACAP lors de la corticogenèse du cervelet [ 7, 8].
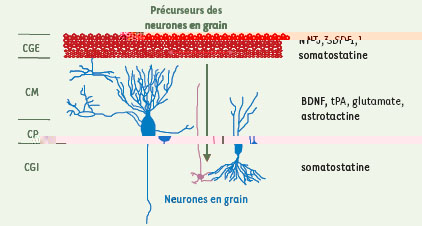
| Figure 1.
Trajet migratoire des cellules en grain dans le cortex cérébelleux immature. Différents facteurs décrits comme impliqués dans le contrôle de la migration des neurones en grain sont indiqués sur la droite du schéma. CGE : couche granulaire externe ; CGI : couche granulaire interne ; CM : couche moléculaire ; CP : couche des cellules de Purkinje. |
L’analyse de la motilité des cellules en grain en culture révèle que ces neurones se déplacent régulièrement par nucleokinesis [ 9]. La distance au point d’origine parcourue par les neurones pendant les 12 premières heures de culture est de l’ordre de 15 µm, soit une vitesse moyenne de 20 nm par minute environ (Figure 2). L’ajout de PACAP dans le milieu d’incubation ne modifie pas le déplacement des neurones pendant les 6 premières heures mais provoque ensuite leur immobilisation. Il en résulte une diminution de la distance au point d’origine dont la valeur moyenne tombe à 8 µm (Figure 2). À l’inverse, le C2-céramide, un analogue des céramides naturels, induit une activation précoce et rapide de la motilité cellulaire. Toutefois, tel le lièvre de la fable qui « part comme un trait, broute, se repose et s’amuse » [ 10], les neurones exposés au C2-céramide rayonnent autour de leur position initiale, de sorte que la distance à l’origine finalement parcourue reste faible comparativement à celle des cellules non traitées (Figure 2). Cette hypermotilité cellulaire s’apparente à la « danse de la mort » qu’effectuent les neurones de la rétine en cours de dégénérescence [ 11]. Les effets du C2-céramide et du PACAP sur la motilité des neurones en grain sont associés à des régulations différentes de la croissance neuritique. Le C2-céramide réduit fortement la neuritogenèse en agissant à la fois sur l’initiation et sur l’élongation des prolongements cellulaires alors que le PACAP abolit l’effet inhibiteur du C2-céramide sur la croissance des neurites sans modifier l’initiation, suggérant que ces deux processus sont régulés par des mécanismes distincts. Les effets du C2-céramide et du PACAP sur la morphogenèse du neurone en grain ne résultent pas de modifications d’expression de l’actine ni de la tubuline [9]. En revanche, la distribution cellulaire de ces deux protéines du cytosquelette est fortement modifiée. Ainsi, le C2-céramide induit une diffusion de l’actine dans le cytoplasme et une forte dépolymérisation de la tubuline alors que le PACAP renforce nettement l’association de l’actine avec le cône d’émergence du prolongement neuritique et prévient très clairement la dépolymérisation de la tubuline. Les actions du C2-céramide et du PACAP sur la tubuline sont associées à des modifications de la protéine Tau : le C2-céramide diminue à la fois la quantité totale de Tau et son degré de phosphorylation au niveau de la sérine 195 alors que le PACAP accroît très fortement les taux de Ser195pTau. Par ailleurs, le PACAP atténue l’effet du C2-céramide sur la phosphorylation de Tau et cette action est mimée par l’acide okadaïque, un inhibiteur de la phosphatase PP2A, et le Z-VAD-FMK, un inhibiteur des caspases.
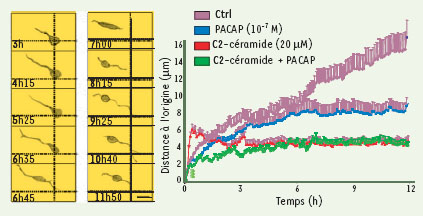
| Figure 2.
Effets du PACAP et du C2-céramide sur la motilité des neurones en grain immatures du cervelet. A. Microphotographies issues d’un enregistrement vidéomicroscopique illustrant la motilité et la croissance neuritique d’un neurone traité au PACAP pendant 12 heures. La barre d’échelle représente 5 µm. B. Courbes moyennes de distance à l’origine pour des neurones traités par le PACAP et/ou le C2-céramide. |
Un certain nombre de facteurs tels que la somatostatine, diverses neurotrophines, ou encore le tPA (tissue plasminogen activator) sont connus pour contrôler la migration des neurones en grain à différents stades du développement du cervelet (Figure 1). Le PACAP est exprimé in situ dans les cellules de Purkinje et l’administration de PACAP à la surface du cortex cérébelleux immature induit une augmentation significative du nombre de neurones en grain dans la couche granulaire interne [ 12], suggérant un rôle du peptide endogène dans les processus de survie neuronale. Pour la première fois, les effets du C2-céramide et du PACAP sur la motilité des neurones en grain ont pu être visualisés et caractérisés par vidéomicroscopie [9]. Ces effets sont associés à des modifications morphologiques particulièrement marquées en ce qui concerne la croissance neuritique et à des régulations différentes des protéines du cytosquelette.
En conclusion, ces données indiquent que des facteurs bien caractérisés pour leurs effets anti- et pro-apoptotiques tels que le PACAP ou FasL (qui induit la production de céramides) pourraient participer au contrôle de la migration neuronale. Ils accréditent l’hypothèse selon laquelle migration et mort cellulaire programmée sont deux processus étroitement liés au cours du neurodéveloppement et probablement lors de pathologies.